في سوق الأدوية الأوروبية شديدة التنظيم، وثائق إجراءات التشغيل القياسية الخاصة بغرف الأبحاث المتوافقة مع ملحق GMP للاتحاد الأوروبي إنه أكثر من مجرد صندوق تنظيمي، فهو أساس سلامة المرضى واستمرارية السوق. بالنسبة لمسؤولي الامتثال في جميع أنحاء الاتحاد الأوروبي - من مراكز الإنتاج في ألمانيا إلى مجموعات التكنولوجيا الحيوية في إسبانيا - يعد إتقان بنية التوثيق هذه أمرًا ضروريًا للاستعداد لشهر يناير 2026.
من يجب أن يستخدم هذا الدليل
- مسؤولو الامتثال: - مسؤول عن الالتزام بمتطلبات EMA.
- أخصائيو الشؤون التنظيمية: إدارة ملفات ترخيص السوق في الاتحاد الأوروبي.
- مدراء الجودة: الإشراف على التوثيق في المرافق المعقمة في الاتحاد الأوروبي.
- متخصصو التحقق من الصحة: التأكد من أن التحقق من صحة غرف الأبحاث يلبي معايير الملحق 1.
نظرة عامة على الملحق 1 لبرنامج الرصد العالمي للاتحاد الأوروبي والجدول الزمني للتنفيذ
المراجعة المنشورة
تحديثات هامة لمكافحة التلوث والرصد البيئي.
تبدأ الفترة الانتقالية
مرحلة الإعداد للامتثال الكامل.
التنفيذ الكامل
الامتثال الإلزامي في جميع الدول الأعضاء في الاتحاد الأوروبي.
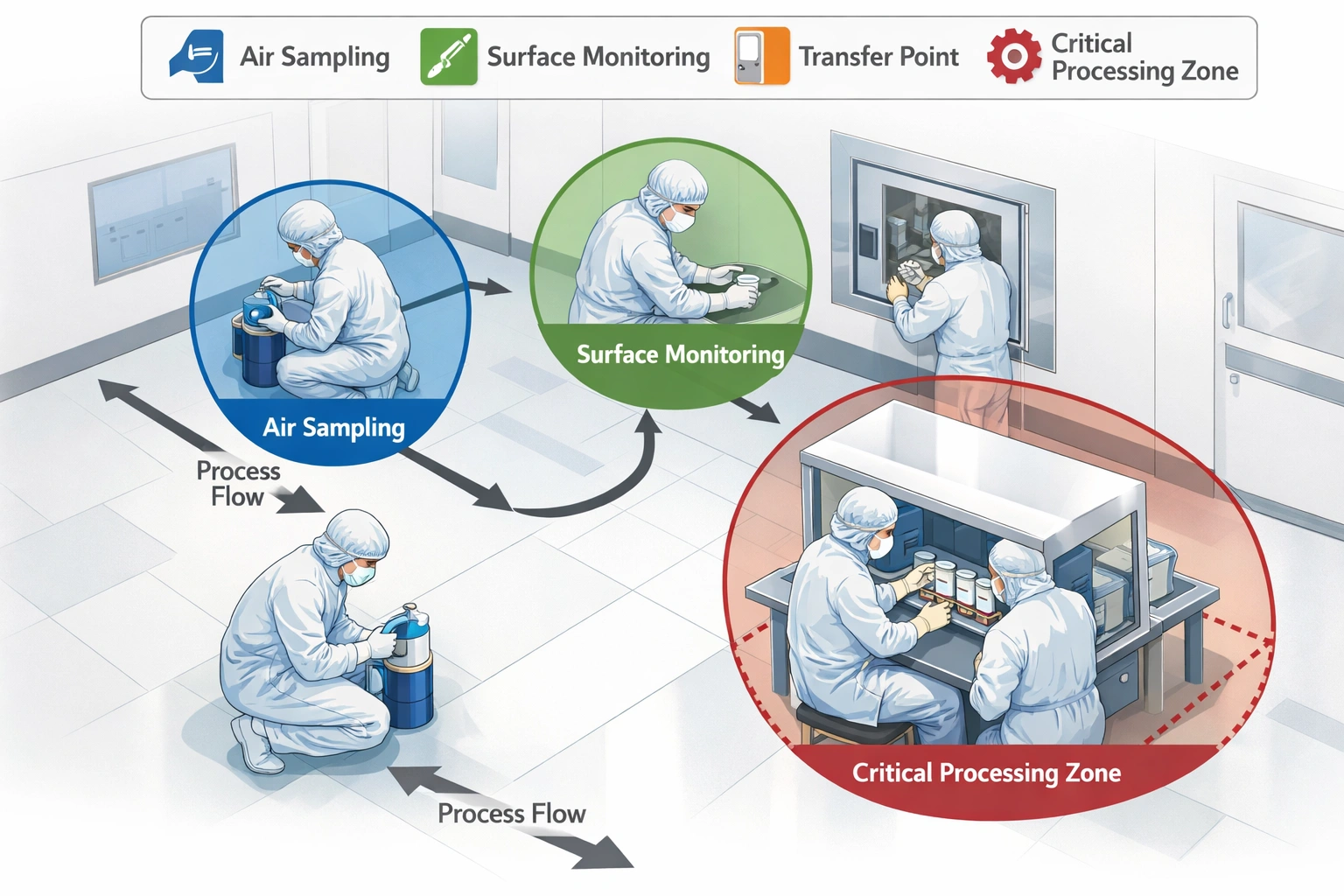
التحديثات الرئيسية التي تؤثر على التوثيق
| منطقة | المتطلبات المنقحة | تأثير التوثيق |
|---|---|---|
| م | على أساس المخاطر مع تتجه | بروتوكولات جديدة لتقييم المخاطر. |
| تلوث | استراتيجية مستمرة | إجراءات التشغيل القياسية الخاصة بالتنظيف. |
| دورة الحياة | إدارة دورة الحياة الكاملة | إجراءات الرقابة الشاملة. |
متطلبات بنية التوثيق في الاتحاد الأوروبي
European regulators expect a hierarchical approach that ensures "clear and unambiguous" instructions throughout the facility.
المستوى 1 & 2: الجودة & إجراءات التشغيل الموحدة للنظام
يتضمن أدلة الجودة وأنظمة مراقبة الوثائق.

المستوى 3 & 4: معالجة إجراءات التشغيل القياسية والسجلات
إجراءات التشغيل القياسية الحاسمة في غرف الأبحاث، بما في ذلك ارتداء الملابس والتطهير وسجلات إنتاج الدُفعات.
متطلبات الاتحاد الأوروبي المحددة: يجب أن تكون الوثائق باللغة الرسمية للاتحاد الأوروبي للدولة العضو التي تقع فيها المنشأة. النظر في الإصدارات ثنائية اللغة من أجل الوضوح الدولي.
احتياجات التوثيق الخاصة بغرف الأبحاث
أوجه القصور الشائعة في التفتيش: يعد عدم كفاية التحكم في التغيير والافتقار إلى وثائق تقييم المخاطر من أهم الأسباب وراء نتائج التفتيش الخاص بالاتحاد الأوروبي.

| نوع SOP | متطلبات الاتحاد الأوروبي المحددة | الأدلة المطلوبة |
|---|---|---|
| التطهير | اختبار الفعالية | بروتوكولات التحقق من الصحة & التقارير. |
| تغيير التحكم | مخاطرة & تقييم الأثر | التقييمات الرسمية. |
| تصديق | التحقق من دورة الحياة | VMP & تقارير موجزة. |
اعتبارات محددة للدول الأعضاء في الاتحاد الأوروبي
في حين تمت مواءمة الملحق 1، توجد فروق دقيقة محلية في مراكز التصنيع الرئيسية:
- ألمانيا: وثائق السلامة الإضافية والترجمات الألمانية.
- فرنسا: متطلبات التتبع الموسعة لسجلات الدُفعات.
- إيطاليا & إسبانيا: إخطارات التدريب المحددة وسجلات تقييم الكفاءة.

تحقيق الامتثال للملحق 1 من GMP الخاص بالاتحاد الأوروبي
يوفر فريق الخبراء لدينا أنظمة توثيق مركزية ومرنة مصممة لتحقيق النجاح التنظيمي للاتحاد الأوروبي لعام 2026. تأكد من أن سلسلة التوريد وإجراءات التشغيل القياسية الخاصة بك تلبي أعلى المعايير.






تعليق الخبراء: تنفيذ المرفق الأول لبرنامج الرصد العالمي (GMP) الخاص بالاتحاد الأوروبي
"The revised Annex 1 represents the most significant update to sterile manufacturing in decades. Regulators expect a demonstrable quality culture embedded in every document—comprehensive risk assessments are the new standard."