Batchsporbarhed for renrumsforbrugsvarer er ikke kun en dokumentationsøvelse. Det er den operationelle rygrad, der gør det muligt for producenter, sterile behandlingshold og regulerede faciliteter at forbinde råmaterialer, produktion, sterilisering, distribution og slutbrug i én verificerbar kæde af beviser.
I miljøer med farmaceutiske, bioteknologiske, halvledere og medicinsk udstyr skaber ufuldstændig sporbarhed risiko langt ud over huller i papirarbejdet. Det forsinker undersøgelser, svækker tilbagekaldelsesrespons, komplicerer revisioner og underminerer tilliden til programmer til forureningskontrol. Et robust system skal hjælpe kvalitetshold med at bevæge sig fra reaktiv registreringsindsamling til proaktiv kontrol.
Batchsporbarhed for renrumsforbrugsvarer betyder at opretholde en komplet, genfindelig registrering af hver batch fra indgående materiale gennem fremstilling, sterilisering, distribution og endelig brug. I praksis bør et effektivt system identificere, hvad der blev lavet, af hvilke kildematerialer, under hvilke procesforhold, hvor det blev afsendt, og hvilke kunder eller interne brugere, der blev berørt, hvis der sker en afvigelse eller tilbagekaldelse.
For regulerede faciliteter er de bedste systemer ikke kun kompatible på papiret. De er hurtige at søge, nemme at verificere, audit-klare og i stand til at understøtte en målrettet tilbagekaldelse inden for få timer i stedet for dage.
Stærk batchsporbarhed forbinder råmaterialepartier, produktionsbatcher, steriliseringsoptegnelser, forsendelsesdata og slutbrugerforbrug i en enkelt kæde af beviser.
Audit-klare systemer skal understøtte hurtig efterforskning og målrettet tilbagekaldelse, ikke kun passiv lagring af frakoblede poster.
En klar batchnummereringslogik reducerer operatørforvirring og forbedrer downstream-rapportering, mærkning, frigivelse og klagehåndtering.
Sporbarhed fremad, baglæns sporbarhed og tilbagekaldelsessimulering bør testes med jævne mellemrum for at bevise, at systemet faktisk fungerer under pres.
Mange faciliteter registrerer allerede batchnumre på kartoner, etiketter eller steriliseringsdokumenter. Problemet er, at disse optegnelser ofte er fragmenteret på tværs af indkøb, lager, produktion, sterilisering, logistik og slutbrugerlogfiler. Når en klage, kontamineringshændelse eller revisionsanmodning opstår, skal teamet derefter rekonstruere historikken manuelt.
Den tilgang er langsom, fejltilbøjelig og dyr. Et modent sporbarhedsprogram reducerer undersøgelsestiden, forbedrer frigivelsestilliden og begrænser omfanget af tilbagekaldelseshandlinger. Det understøtter også trendanalyse, leverandørstyring, CAPA og kundekommunikation.

Et sporbarhedssystem for renrumsforbrugsvarer bør designes omkring, hvordan regulerede organisationer undersøger afvigelser og beviser kontrol. For mange brugere omfatter de mest relevante referencer EU GMP Annex 1, FDAs cGMP-registreringsforventninger og ISO 13485 sporbarhedskrav for medicinsk udstyrsrelaterede kvalitetssystemer.
| Regulering / Standard | Fokusområde | Operationel betydning |
|---|---|---|
| EU GMP bilag 1 | Sporbarhed, batch-registreringer, tilbagekaldelsesevne | Faciliteter bør være i stand til hurtigt at identificere berørte materialer og færdigvarer under undersøgelser eller markedshandlinger. |
| FDA 21 CFR 211.180 / 211.198 | Distributionsregistre, klagefiler, opbevaring | Optegnelser skal understøtte klageevaluering, gennemgang af partipåvirkninger og kontrolleret tilbagekaldelsesudførelse. |
| ISO 13485 Afsnit 7.5.8 | Unik identifikation og genfinding | Organisationen bør opretholde dokumenterede sporbarhedsprocedurer og være i stand til at hente tilknyttede optegnelser, når det er nødvendigt. |
For købere og QA-teams betyder det, at sporbarhed ikke bør behandles som en funktion, der kun er på lager. Det er et tværgående kvalitetskrav, der berører leverandørkontrol, produktionsdokumentation, steriliseringsfrigivelse, forsendelseshistorik og slutbrugeransvarlighed.
En nyttig måde at strukturere batchsporbarhed på er at opdele systemet i fem forbundne lag: råmaterialer, fremstilling, sterilisering, distribution og forbrug. Denne ramme hjælper teams med at definere ejerskab, datafelter og verifikationskontrolpunkter uden at miste synlighed fra ende til ende.
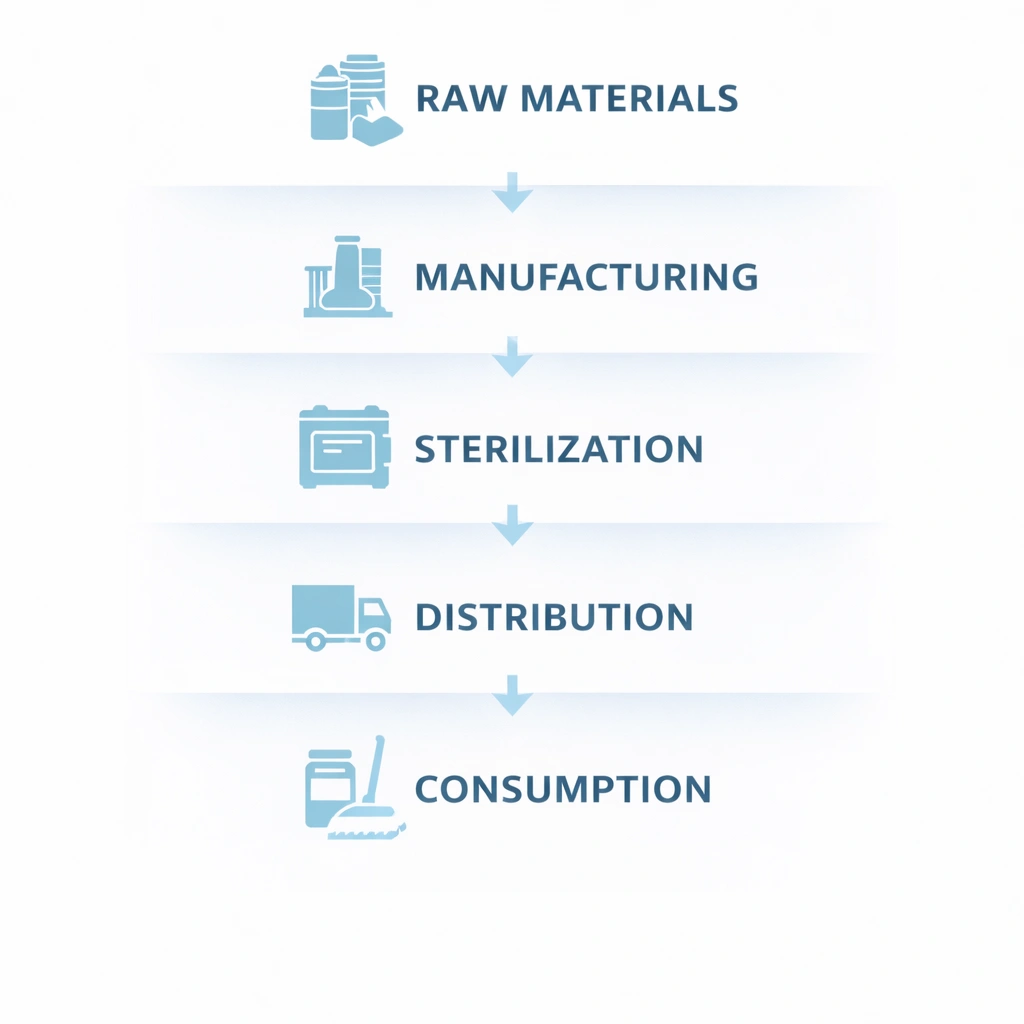
Registrer leverandøridentitet, leverandørlotnummer, modtagelsesdato, indgående inspektionsstatus og relevante certifikater såsom COA eller CoC. Dette er udgangspunktet for opstrømskontrol.
Registrer, hvilke materialer der blev brugt, hvilken linje der producerede partiet, hvem der drev eller frigav processen, og hvilke i-proces eller afsluttende QC-tjek der blev udført.
For sterile forbrugsvarer skal du knytte produktionsbatchen til steriliseringsbatchen, cyklusparametre, steriliseringsmetode, frigivelsesstatus og eventuelt valideringsbevis.
Link batchnumre til kunder, forsendelsesmængder, forsendelsesdatoer, transportøroplysninger og destinationsoplysninger. Dette er afgørende for klagebehandling og indeslutning af tilbagekaldelse.
Hvor brugsmodellen kræver det, skal du vedligeholde brugersiden fortegnelser over batchnummer, brugt dato, placering og bortskaffelsesrute. Dette er især værdifuldt i højrisiko GMP-miljøer.
Batchnummeret skal være mere end et seriestempel. Det bør understøtte hurtig fortolkning, nøjagtig opbevaring, ren etiketpræsentation og manuel håndtering med lav fejl. Et struktureret format gør også digital søgning og rapportering mere pålidelig.

| Batch element | Eksempel | Hvorfor det betyder noget |
|---|---|---|
| Leverandør-/producentkode | MIDDELPOSI | Identificerer produktionens oprindelse og adskiller mærker, websteder eller forsyningsstrømme. |
| Dato segment | 2026-04-06 | Hjælper operatører med hurtigt at identificere produktionskronologi og opbevaringslogik. |
| Serienummer | 001 | Differentierer flere batcher produceret inden for samme dag eller cyklusvindue. |
| Suffiks / Procesmarkør | A/B/C | Nyttig til produktion, sterilisering, gensterilisering eller kvalitetskontrol af arbejdsgange. |
Selv stærk fysisk mærkning er ikke nok, hvis understøttende optegnelser er ufuldstændige. En forsvarlig sporbarhedsfil bør give en korrekturlæser mulighed for at flytte fra en færdig batch tilbage til kildemateriale og fra et kildemateriale frem til hver berørt færdig batch og kundeforsendelse.
Leverandørparti, modtaget mængde, kontrolresultat, dokumentkontrol, frigivelsesstatus.
Batchnummer, operatør, linje, procesdato, materialeforbrug, QC-kontrolpunkter, afvigelser.
Steriliseringsparti, cyklusdata, frigivelsesbeslutning, kunde afsendt mængde, destination, klageforbindelse.
Dokumentationssættet skal også være nemt at hente under leverandøraudits, kundekvalificering, klagebehandling og CAPA-gennemgange. Hvis det tager for lang tid at finde den rigtige fil, er systemet funktionelt svagere, end det ser ud på papiret.
Et sporbarhedssystem bør testes, ikke antages. Den mest praktiske tilgang er at køre tre typer øvelser: fremadsporbarhed, bagudsporbarhed og genkaldelsessimulering. Disse test afslører, om datafelter virkelig er forbundet, om teams ved, hvor de skal lede, og om responstiden lever op til de interne forventninger.
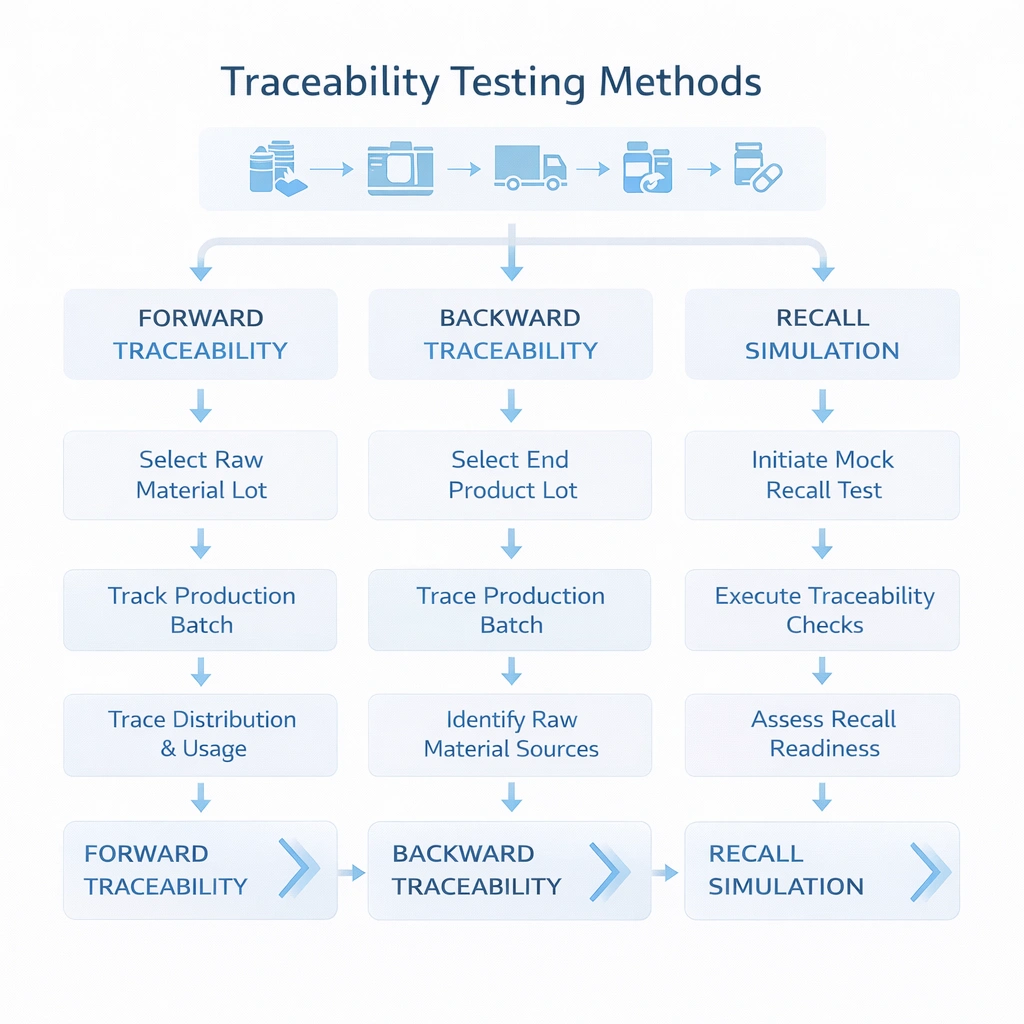
Start med et indgående materialeparti og afgør, hvilke produktionsbatcher, steriliseringscyklusser og kundeforsendelser, der blev påvirket.
Start med en klage eller kundebrugt batch og spor tilbage til kildemateriale, procesregistreringer og udgivelsesstatus.
Vælg en batch og simuler en målrettet tilbagekaldelse: Identificer hver berørt kunde, mængde, forsendelsesrute og kontakt ejeren. Registrer den samlede nødvendige tid og de fundne datahuller. I miljøer med høj kontrol er denne øvelse en af de hurtigste måder at vurdere, om systemet virkelig er klar til genkaldelse.
| Testtype | Hovedspørgsmål | Forventet output |
|---|---|---|
| Sporbarhed fremad | Hvor blev dette input af? | Berørte produktions-, steriliserings- og forsendelsesregistre |
| Sporbarhed bagud | Hvad skabte dette resultat? | Kildemateriale, proceshistorik, frigivelsesbeviser |
| Genkald simulering | Kan vi handle hurtigt og præcist? | Kundeliste, mængdekort, responstiming, datagab-log |
En tilbagekaldelsesarbejdsgang bør være forudbestemt snarere end improviseret. Når et kvalitetsproblem dukker op, bør teams allerede vide, hvordan de klassificerer problemet, identificerer berørte batches, underretter interessenter, stopper yderligere distribution og dokumenterer den grundlæggende årsag og korrigerende handlinger.
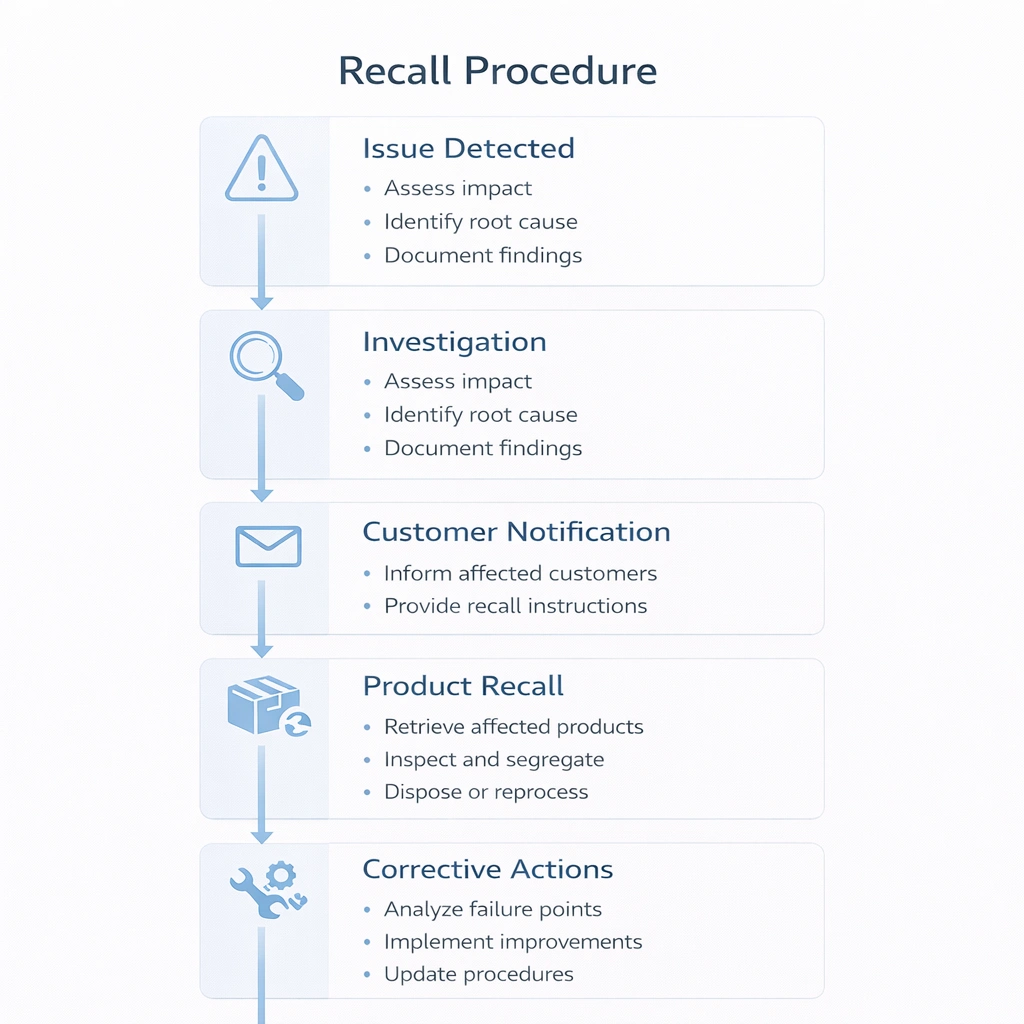
Regnearksbaserede systemer kan arbejde med lav kompleksitet, men efterhånden som produktsortiment, kundevolumen og sterilitetsarbejdsgange udvides, bliver elektronisk sporbarhed normalt mere praktisk. Stregkode- eller RFID-understøttede systemer reducerer risikoen for manuel adgang og gør tilbagekaldelsessimulering hurtigere og mere gentagelig.

Definer datafelter, ejerskab, batchkodelogik, opbevaringsregler og sporbarhedsomfang for sterile og ikke-sterile linjer.
Standardiser formularer, leverandørpartiregistrering, produktionsregistreringer, steriliseringsforbindelser og forsendelsesregistre.
Kør fremadsporing, bagudsporbarhed, og genkald simuleringstests og dokumenter de fundne huller.
Systemet bør som minimum forbinde indgående materialepartier, produktionsbatcher, frigivelses- eller steriliseringsregistre, hvor det er relevant, forsendelseshistorik og evnen til at identificere berørte kunder eller brugere under en undersøgelse.
Batchmærkning identificerer en produktgruppe. Fuld sporbarhedslinks, der mærker til upstream-materialer, procesregistreringer, frigivelsesbeslutninger og downstream-distributions- eller brugsposter.
Mange kvalitetsteams udfører det mindst årligt, mens højere risiko eller mere komplekse operationer kan teste oftere, især efter systemændringer, leverandørskift eller større CAPA-handlinger.
Ja, til lavt volumen operationer. Men når produktvariation, sterilitetskontrol eller kundekompleksitet øges, giver digitale systemer normalt bedre genfindingshastighed, fejlreduktion og revisionskontrol.
Fordi sterile produkter kræver strammere kontrol af batchhistorik, steriliseringsforbindelse, frigivelsesbeviser og nedstrømssynlighed, hvis der opstår en klage, sterilitetsbekymring eller tilbagekaldelsesbeslutning.
Midposi understøtter regulerede købere med renrumsforbrugsvarer designet til kontrollerede miljøer, herunder dokumentationsorienteret kommunikation til kvalificering, sterilitetsstatusgennemgang og diskussioner om batchsporbarhed.


Vi kontakter dig inden for 1 arbejdsdag, vær venligst opmærksom på e-mailen med suffikset “*@midposi.com”.