En teknisk reference for QA-ledere og valideringsingeniører om integrationen af sporbarhed af forbrugsvarer i webstedets Contamination Control Strategy (CCS).

I et GMP-reguleret miljø ses renrumsmoppen ikke længere som et generisk hjælpemiddel, men som et kritisk kontrolleret input. Batchsporbar renrumsmoppe Systemer har tre primære funktioner:
Product-level traceability identifies a SKU; batch-level traceability identifies the specific manufacturing event. For cleanroom mops, this requires a "genealogy" that links the finished product back to the specific lot of polyester yarn or microfiber fabric used, the cleanroom laundry shift, and the specific sterilization cycle.
Når mopper behandles som kontrollerede input, er hver enkelt pakke et datapunkt. Disse data giver QA-teams mulighed for at verificere, at produktet i deres hånd er identisk med hensyn til ydeevne og renhed med det produkt, der blev valideret under den første opstart af faciliteten eller PQ (Performance Qualification).
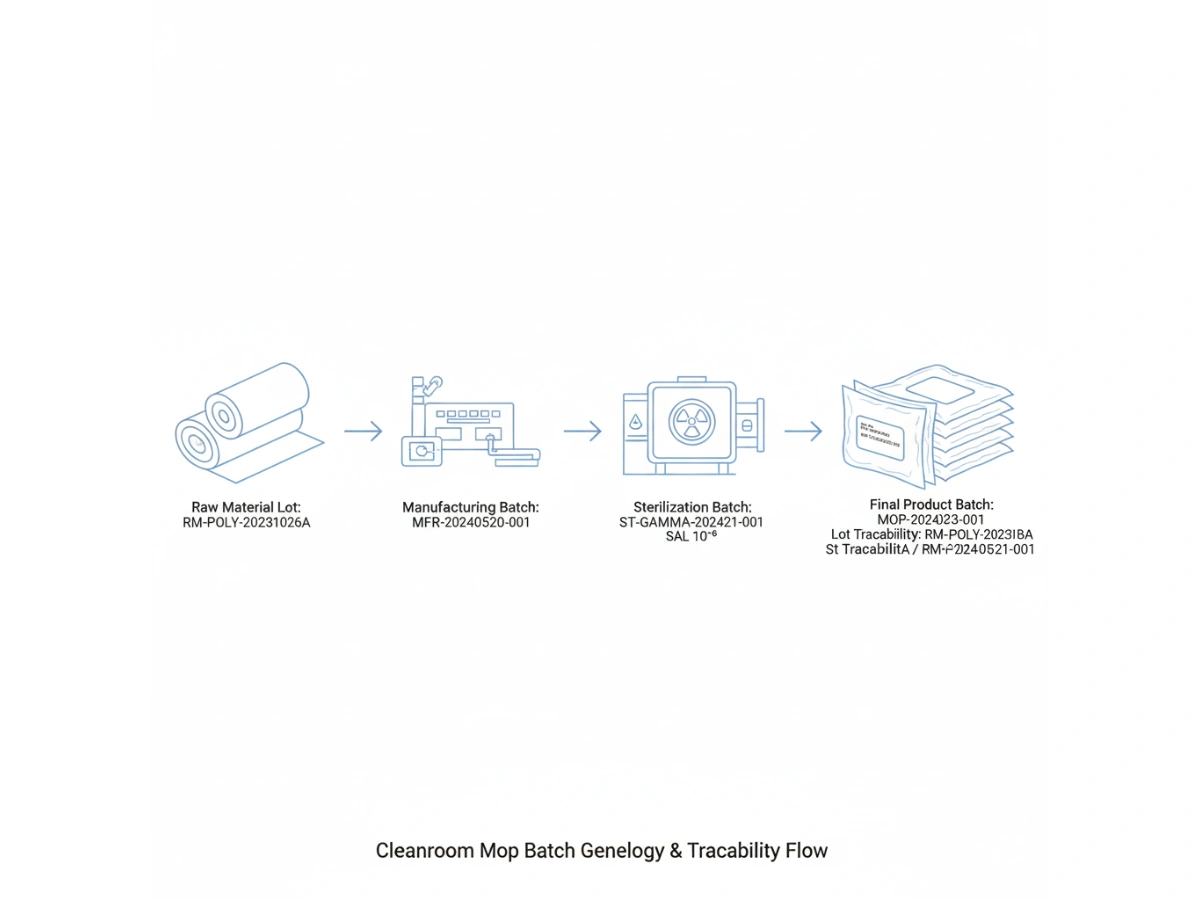
Moderne GMP-principper kræver, at der tages fuldt hensyn til alle materialer, der kommer i kontakt med følsomme overflader. Under en inspektion kan en revisor vælge en produktionsdato og bede om parti sporbarhed af de rengøringsmidler, der blev brugt den dag.
Expectations focus on the "Linkage of Records." An auditor will look for a seamless transition from the facility's cleaning logs to the dokumentation på batchniveau leveret af leverandøren. Hvis en moppebatch ikke kan knyttes til et analysecertifikat (COA) eller en steriliseringsjournal, kan steriliteten og renheden af hele renrumssuiten blive sat i tvivl.

Et robust sporbarhedssystem til renrumsforbrugsvarer GMP overholdelse skal omfatte:
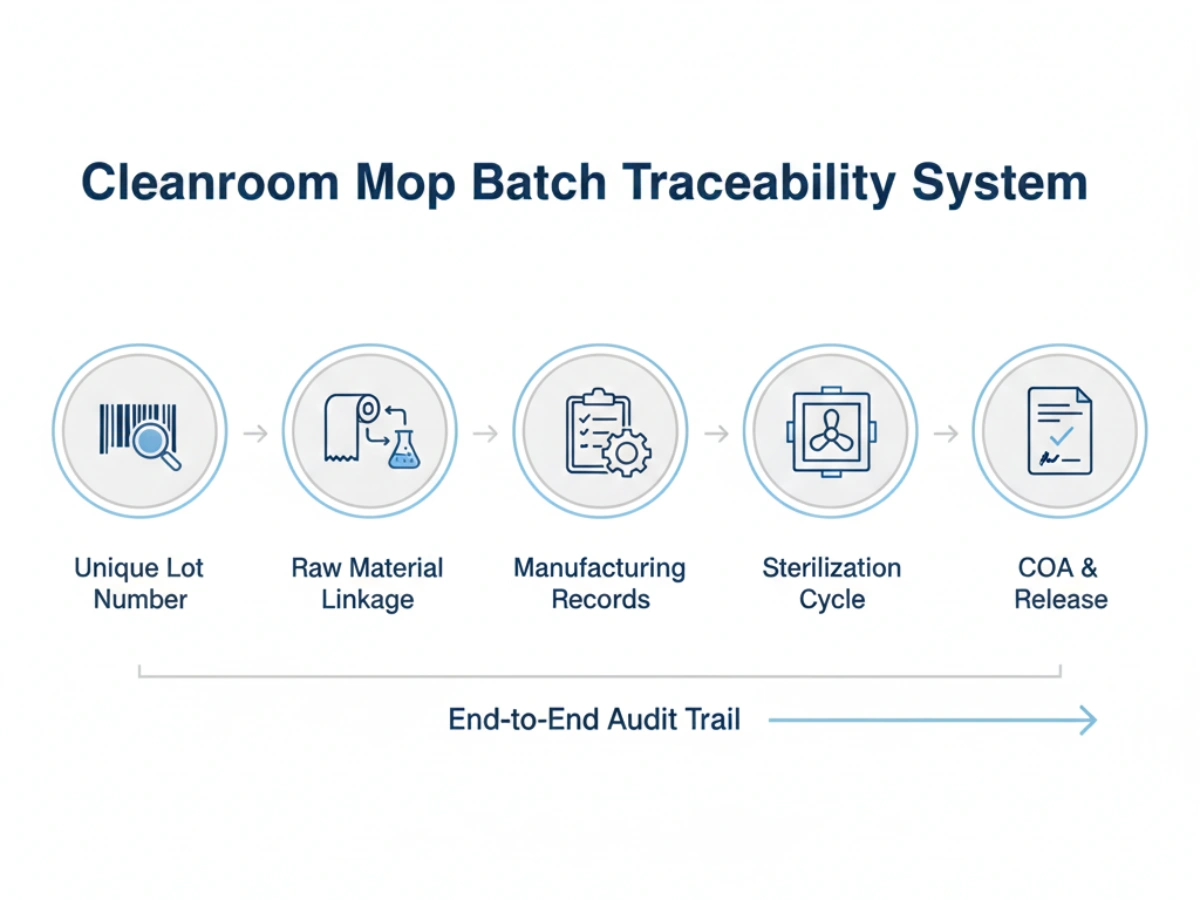
Supply stability is often threatened by "drift"—small, undocumented changes in manufacturing that accumulate over years. Batch traceability prevents this by establishing a baseline for konsistens fra parti til parti.
I tilfælde af en CAPA (Corrective and Preventive Action), der involverer stigninger i miljøovervågning (EM), giver sporbarhed QA mulighed for at afgøre, om et specifikt parti mopper bidrog til begivenheden. Uden dette kan anlægget blive tvunget til at kassere alt lager og standse produktionen, hvilket udgør en massiv operationel risiko. Sporbarhed forvandler en potentiel krise på hele faciliteten til en lokaliseret materialekarantæne.

EN farmaceutisk moppe producent / OEM fungerer som en forlængelse af pharma-sidens kvalitetssystem. Deres ansvar omfatter:
For en kvalificeret producent, evnen til at producere disse poster på efterspørgsel er kendetegnende for GMP-modenhed.
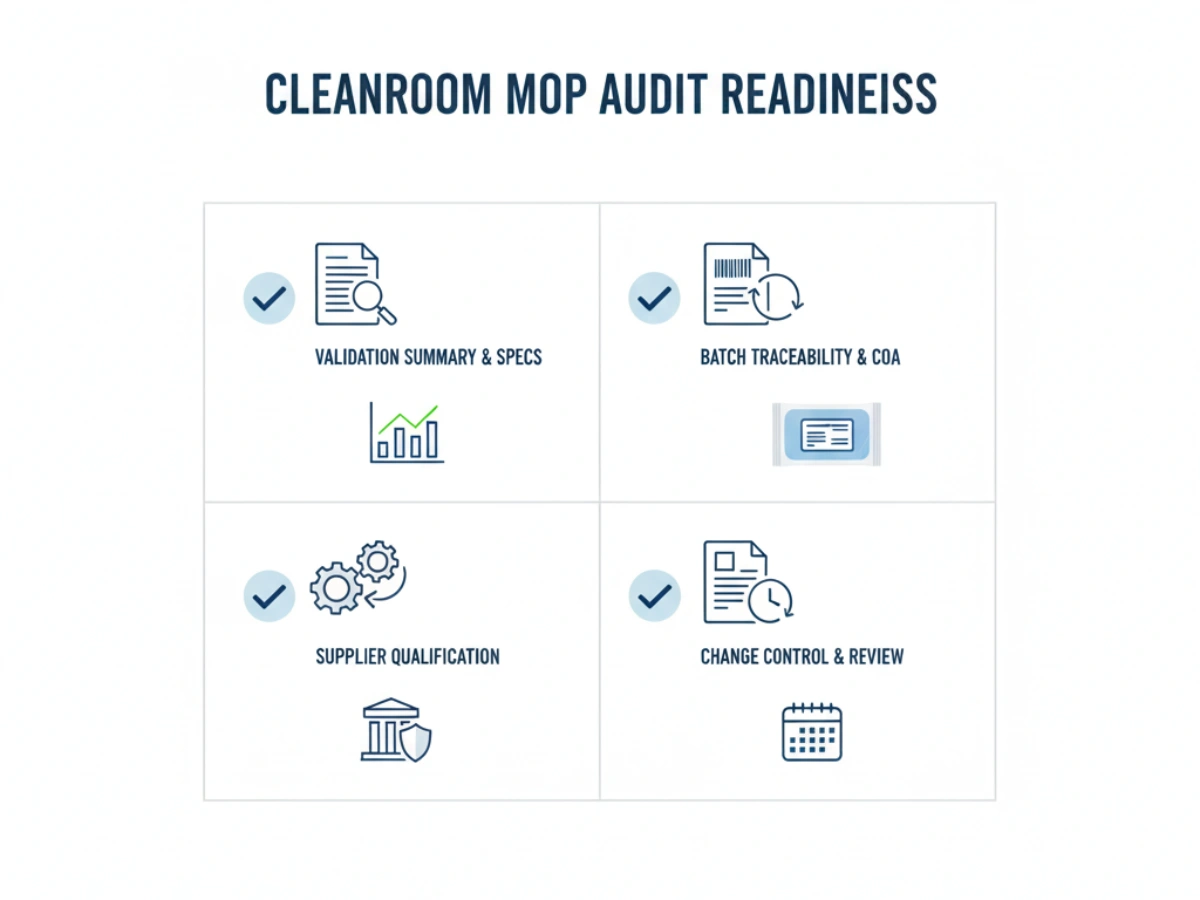
Under OEM leverandør kvalifikation, QA-teams bør bruge følgende tjekliste:
| Kontrolpunkt | Krav |
|---|---|
| Batch definition | Er batchstørrelsen klart defineret og overskuelig? |
| Prøveopbevaring | Beholder leverandøren prøver for hvert parti? |
| Revisionsadgang | Kan leverandøren levere fuldstændige råvarelogfiler inden for 48 timer? |
| Fysisk mærkning | Er batchnummeret modstandsdygtigt over for renrumsdesinfektionsmidler (IPA)? |
Batchsporbarhed er ikke blot en dokumentationsøvelse; det er rygraden i et forsvarligt kvalitetssystem. I forbindelse med klasse A og B-miljøer sikrer evnen til at spore hver fiber- og steriliseringscyklus, at rengøringsprocessen forbliver en kontrolleret variabel snarere end en ukendt risiko.
Modne farmaceutiske QA-teams prioriterer leverandører, der viser total gennemsigtighed i deres batch-registreringer, og ser dem som langsigtede partnere i patientsikkerhed og overholdelse af lovgivning.
Bed om parti-slægtsforskning, batch-specifikke COA'er, steriliseringskobling og ændringskontrolberedskab for at styrke din revisionsfortælling.
Anmod om dokumentationspakke

Vi kontakter dig inden for 1 arbejdsdag, vær venligst opmærksom på e-mailen med suffikset “*@midposi.com”.