På det stærkt regulerede europæiske lægemiddelmarked, EU GMP Annex 1-kompatibel SOP-dokumentation for renrum er mere end en reguleringsboks – det er grundlaget for patientsikkerhed og markedets levetid. For overholdelsesansvarlige i hele EU – fra produktionscentrene i Tyskland til biotekklyngerne i Spanien – er det afgørende at beherske denne dokumentationsarkitektur for klarhed i januar 2026.
Hvem skal bruge denne vejledning
- Overholdelsesansvarlige: Ansvarlig for overholdelse af EMA krav.
- Regulatory Affairs Professionals: Håndtering af EU-markedsgodkendelsesdossierer.
- Kvalitetschefer: Overvåge dokumentation i EU-baserede sterilanlæg.
- Valideringsspecialister: Sikring af renrumsvalidering opfylder bilag 1-standarder.
EU GMP Annex 1 Oversigt og implementeringstidslinje
Revision udgivet
Væsentlige opdateringer af forureningskontrol og miljøovervågning.
Overgangsperioden begynder
Forberedelsesfase til fuld overholdelse.
Fuld implementering
Obligatorisk overholdelse på tværs af alle EU-medlemslande.
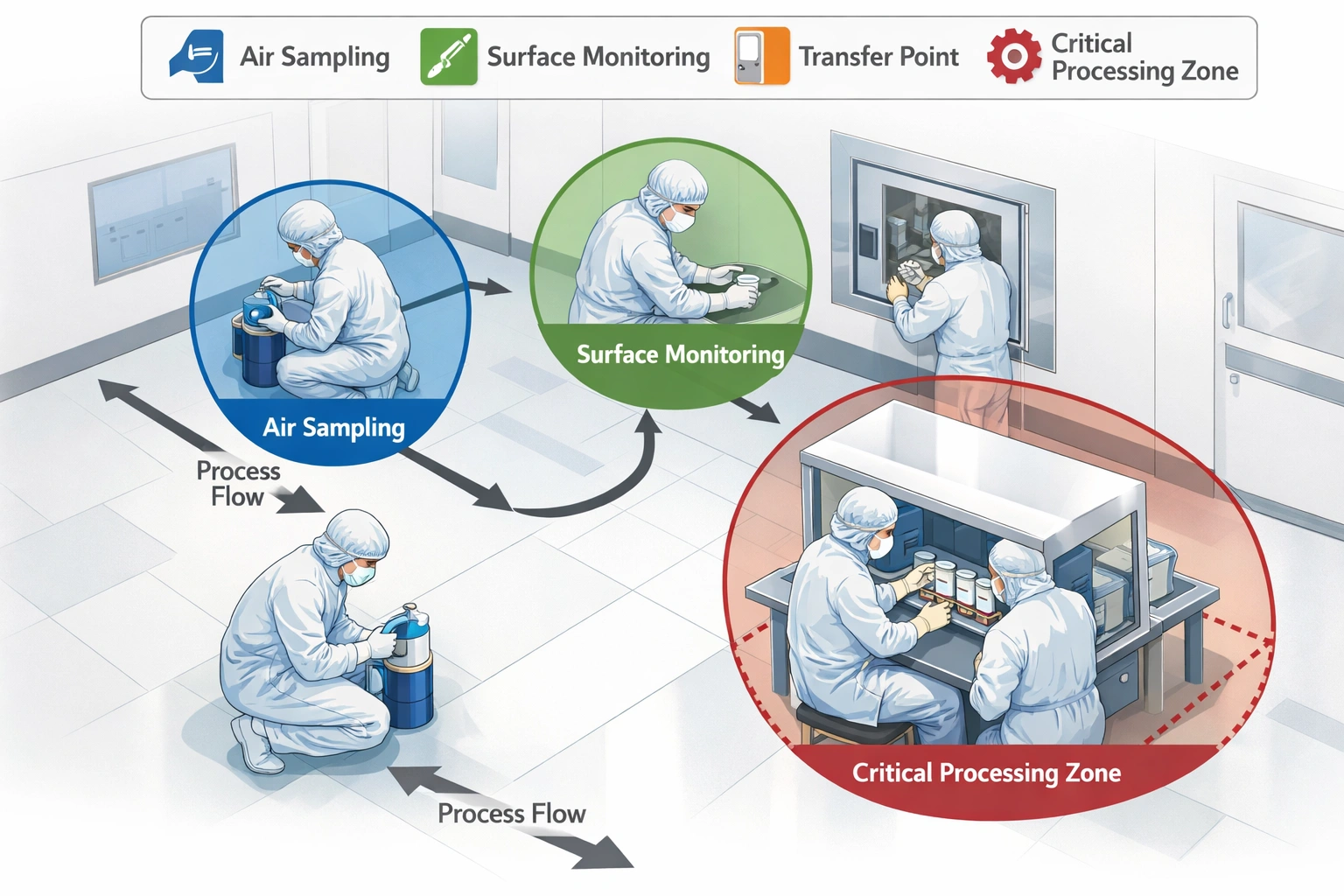
Større opdateringer, der påvirker dokumentation
| Areal | Revideret krav | Dokumentationspåvirkning |
|---|---|---|
| EM | Risikobaseret med trending | Nye risikovurderingsprotokoller. |
| Forurening | Vedvarende strategi | Forbedrede rengørings-SOP'er. |
| Livscyklus | Fuld livscyklusstyring | Omfattende kontrolprocedurer. |
EU-dokumentationsarkitekturkrav
European regulators expect a hierarchical approach that ensures "clear and unambiguous" instructions throughout the facility.
Niveau 1 & 2: Kvalitet & System SOP'er
Indeholder kvalitetsmanualer og dokumentkontrolsystemer.

Niveau 3 & 4: Behandle SOP'er og registreringer
Vigtige SOP'er for renrum, herunder beklædnings-, desinfektions- og batchproduktionsregistreringer.
EU-specifikke krav: Dokumentationen skal være på det officielle EU-sprog i den medlemsstat, hvor anlægget er placeret. Overvej tosprogede versioner for international klarhed.
Renrumsspecifikke dokumentationsbehov
Almindelige inspektionsmangler: Utilstrækkelig ændringskontrol og mangel på risikovurderingsdokumentation er hovedårsagerne til EU-inspektionsresultater.

| SOP type | Specifikt EU-krav | Bevis påkrævet |
|---|---|---|
| Desinfektion | Effektivitetstest | Valideringsprotokoller & rapporter. |
| Skift kontrol | Risiko & Effektevaluering | Formelle vurderinger. |
| Validering | Livscyklus verifikation | VMP & Sammenfattende rapporter. |
EU-medlemsstatsspecifikke overvejelser
Mens bilag 1 er harmoniseret, findes der lokale nuancer i store produktionscentre:
- Tyskland: Yderligere sikkerhedsdokumentation og tyske oversættelser.
- Frankrig: Udvidede krav til sporbarhed for batch records.
- Italien & Spanien: Specifikke uddannelsesnotifikationer og kompetencevurderingsposter.

Opnå overholdelse af EU GMP Annex 1
Vores ekspertteam leverer centraliserede, fleksible dokumentationssystemer designet til EU-lovgivningssucces i 2026. Sørg for, at din forsyningskæde og SOP'er opfylder de højeste standarder.






Ekspertkommentar: EU GMP Bilag 1 Implementering
"The revised Annex 1 represents the most significant update to sterile manufacturing in decades. Regulators expect a demonstrable quality culture embedded in every document—comprehensive risk assessments are the new standard."