En teknisk evaluering af gammabestråling versus autoklavesterilisering for Annex 1-kompatible renrumsmiljøer.

Under EU GMP Annex 1 udgør moppesystemer en kritisk del af Forureningskontrolstrategi (CCS). The selected sterilization method directly affects audit exposure, validation workload, and transfer risk for pharmaceutical facilities.
Som forklaret i vores vejledning til valg af leverandør af farmaceutisk renrumsmoppe , sterility alone is not sufficient — material stability, packaging integrity, and documentation traceability must also be demonstrated.
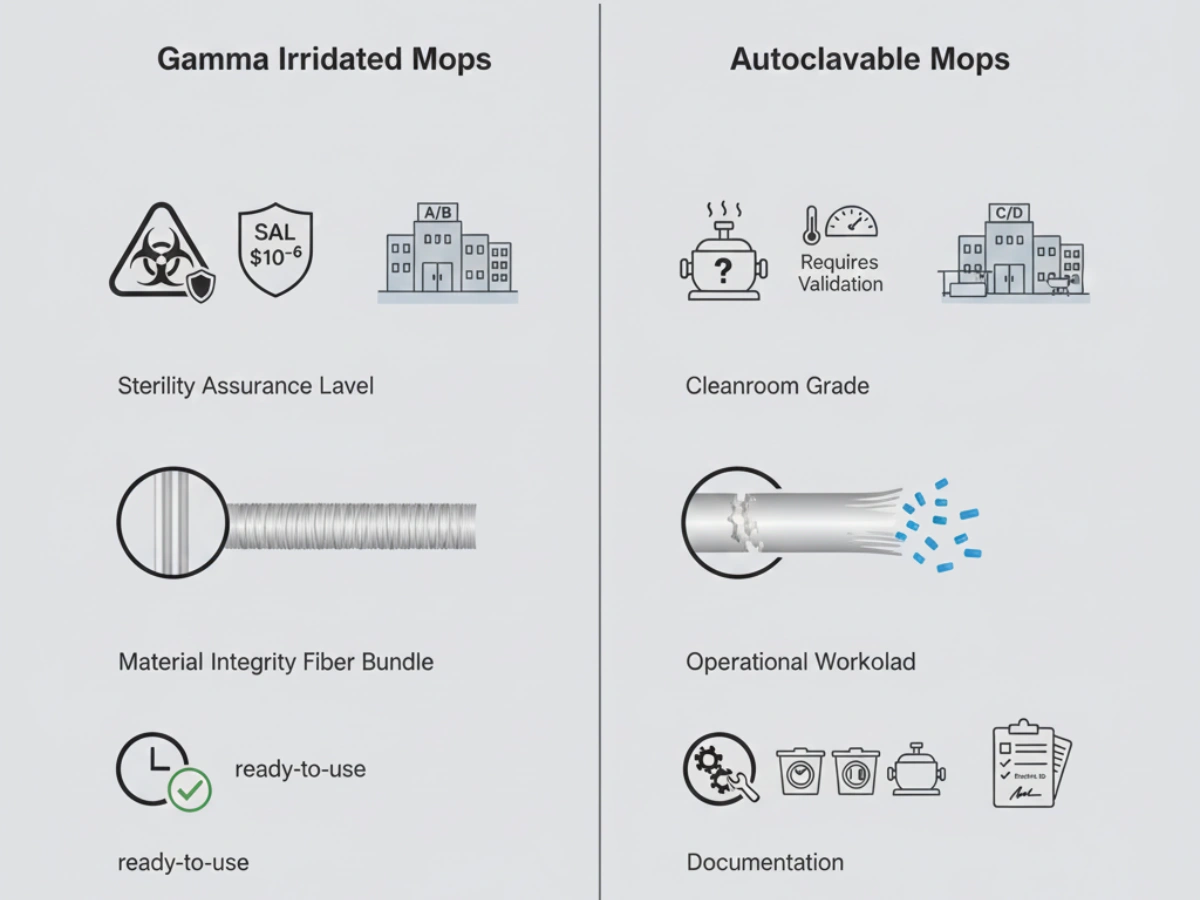
Gamma irradiation is a terminal "cold" sterilization process. Its penetrative nature ensures uniform sterilization throughout dense mop structures. Each batch is validated to SAL 10⁻⁶ and supplied with a batch-specific COI.

Autoklavesterilisering er afhængig af mættet damp (121 °C). Effektiv autoklavering kræver tætte moppehoveder for at gennemgå validerede vakuumcyklusser for at eliminere indespærret luft og forhindre kolde pletter.

Faciliteter skal validere de maksimalt tilladte cyklusser, før partikeludskillelsen overskrider GMP-grænserne.
| Feature | Gamma-bestrålet moppe | Autoklaverbar moppe |
|---|---|---|
| Sterilitetssikring | Valideret SAL 10⁻⁶ pr. batch | Cyklusafhængig; Intern validering |
| Karakter Egnethed | Optimeret til klasse A/B | Typisk klasse C/D |
| Materiel integritet | Høj (engangsbrug, ingen slid) | Nedbrydes med hver cyklus |
This risk is most visible during material transfer into Grade A/B areas. For a detailed explanation, refer to our dedicated guide on dobbeltpose steril renrumsmoppeemballage og overførselslogik .
From a QA and operations perspective, sterilization method selection should align with cleanroom grade, internal validation capability, and supplier documentation maturity.
For validation-driven facilities, we support technical review with batch documentation, sterilization summaries, and evaluation samples.
Anmod om tekniske data eller prøver

Vi kontakter dig inden for 1 arbejdsdag, vær venligst opmærksom på e-mailen med suffikset “*@midposi.com”.