Supportartikel · GMP / Bilag 1
A technical supplement for QA, validation, and operations teams—focused on GMP expectations, Annex 1 interpretation, and practical supplier qualification checkpoints for cleanroom mops.

This article serves as a technical supplement to the primary pharmaceutical cleanroom mop supplier guide, focusing specifically on GMP and Annex 1 interpretation.
In pharmaceutical manufacturing, mop selection directly affects the robustness of the cleaning validation program. Under the revised EU GMP Annex 1, regulators place increased scrutiny on how disinfectants are applied and how residues are removed as part of routine and sporicidal cleaning.
Hvis substrater binder/neutraliserer desinfektionsaktive stoffer, kan overfladekoncentrationen falde under validerede log-reduktionsmål.
Fiberafgivelse øger ikke-levedygtige partikler, hvilket øger risikoen for EM-ekskursion og undersøgelsesbyrden.
Manglende sporbarhed eller steriliseringsdokumentation for mopper er en tilbagevendende kilde til revisionsresultater.
Although “mops” are not explicitly referenced in every clause, Annex 1 cleanroom cleaning requirements are inherently linked to the tools used to execute validated cleaning processes.
Annex 1 emphasizes that cleanroom design and equipment must facilitate effective cleaning. From a regulatory interpretation standpoint, this extends to tools that can access all relevant surfaces and are constructed from materials that do not harbor or generate contamination. In Grade A/B areas, contamination control principles require sterile tools introduced via a validated transfer process (e.g., double-bagged entry through an airlock). This places mop mechanical performance within the scope of cleaning process validation—not product selection alone.
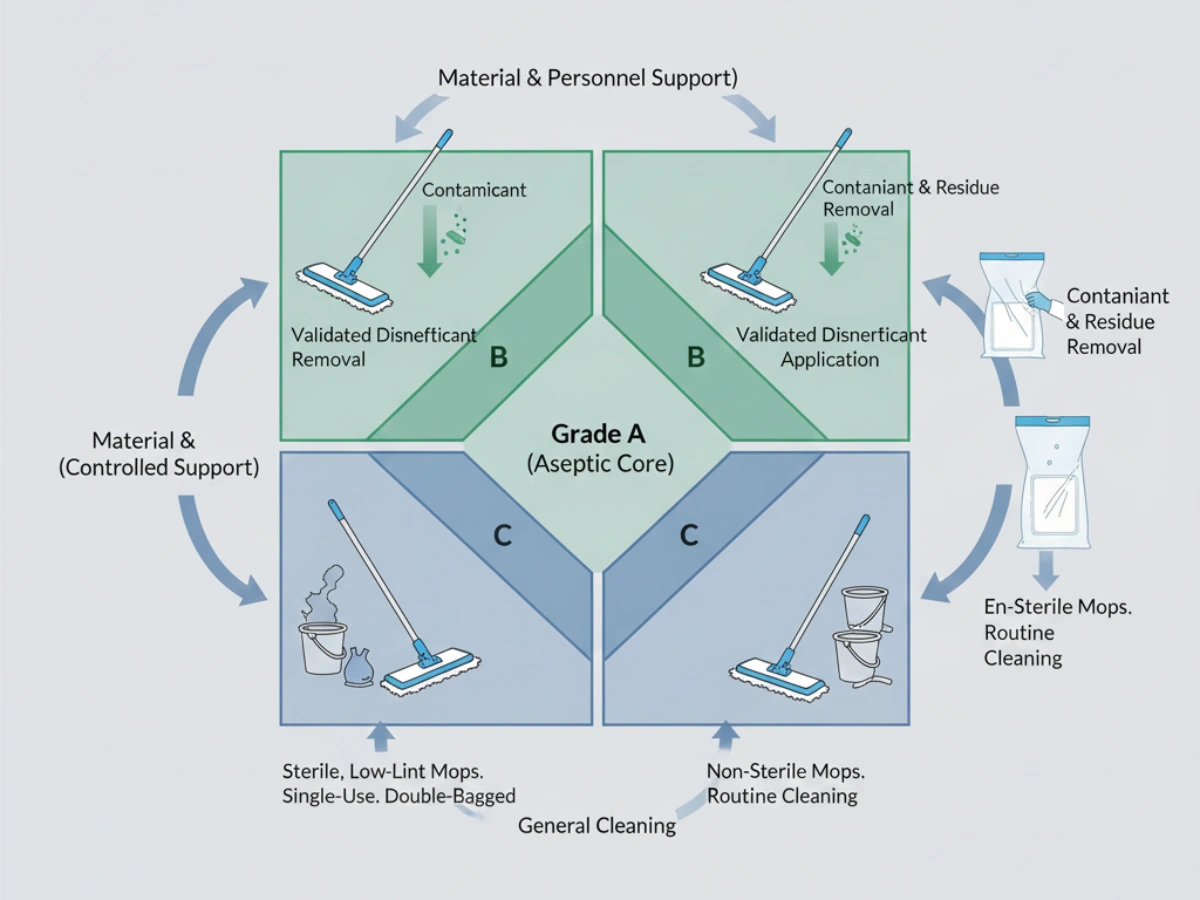
Under GMP expectations, pharmaceutical cleaning tools must be manufactured from chemically inert materials. Natural fibers/foams/cellulose may degrade or interact with aggressive sporicides and high-concentration alcohols. GMP-compliant mop systems typically use knitted polyester for chemical resistance and low particle generation.
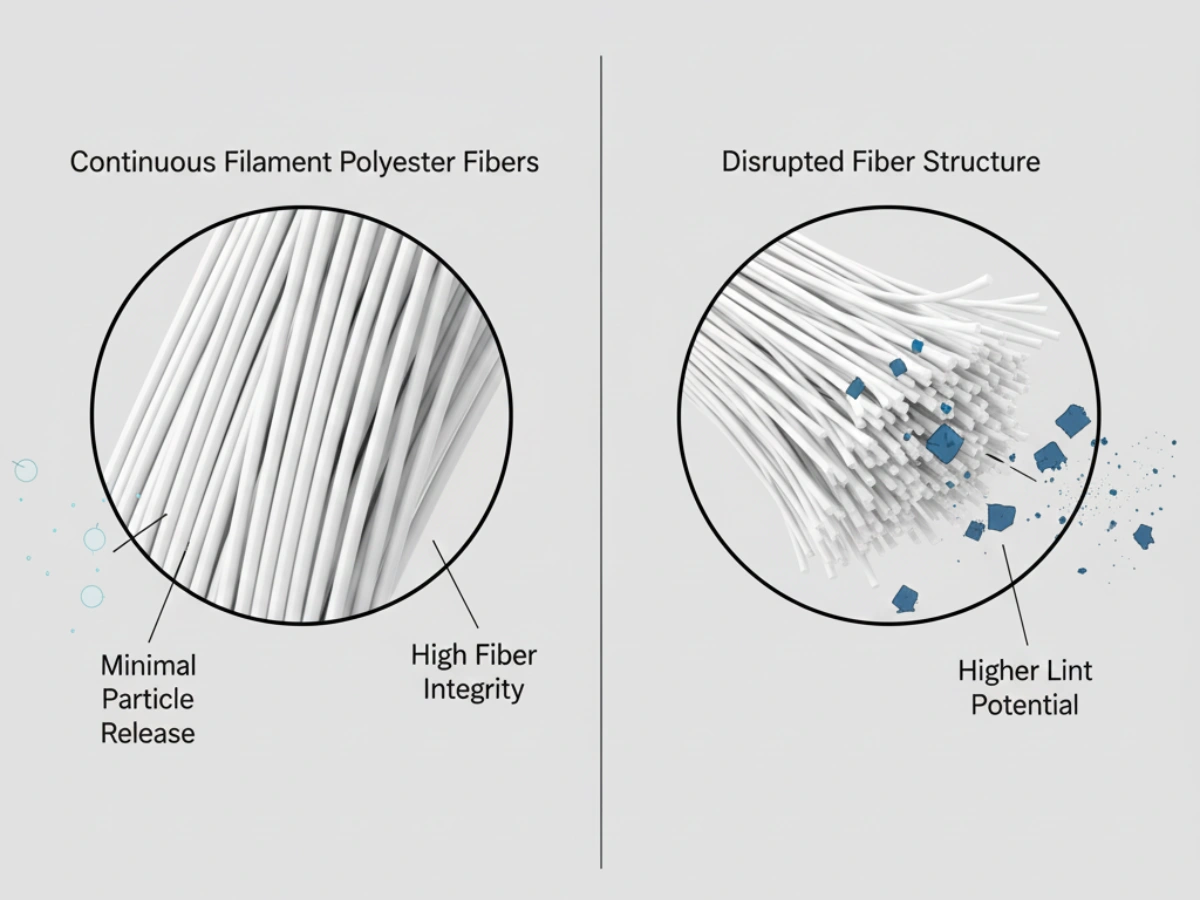
In Grade A/B cleanrooms, mops are expected to be sterile at the point of use. In Grade C/D, non-sterile but low-particulate mops may be acceptable when justified by risk assessment. For sterile applications, suppliers should provide sterilization validation—commonly gamma irradiation—demonstrating SAL 10⁻⁶ and batch-specific Certificates of Irradiation.
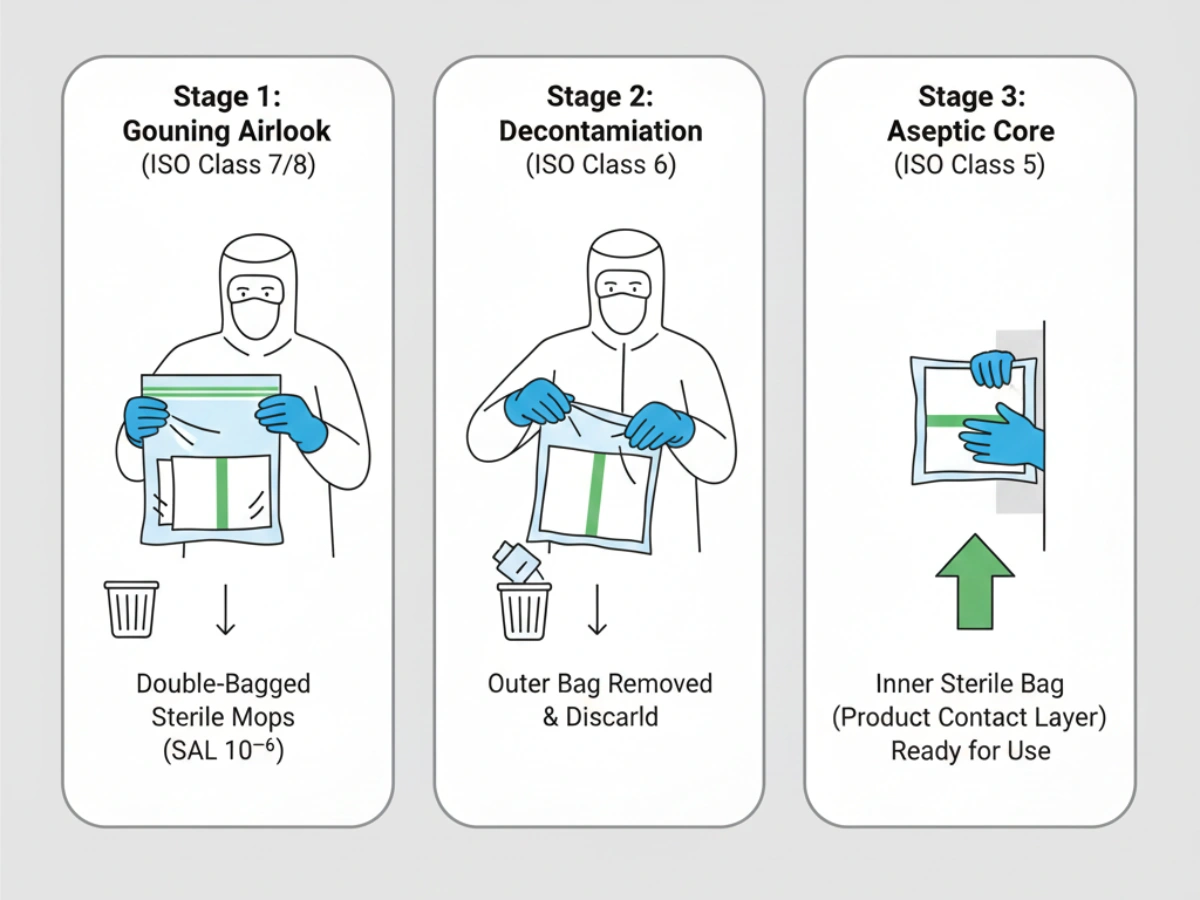
Double/triple bagging enables staged peel-and-transfer procedures; outer packaging is removed in lower grade areas and inner sterile bag opened only within Grade A/B. GMP also requires maintaining a defined “state of control”: mop heads delivered today must remain equivalent to those qualified during cleaning validation. Material/process/packaging changes should be governed under formal change control with advance notification.
For en bredere ramme om leverandørevaluering henvises til hovedvejledningen vedr valg af leverandør af farmaceutisk renrumsmoppe.
For revisionsfokuserede dokumentationskrav, se valideringsdokumenter for renrumsmoppe og COA-standarder.
Supplier qualification under GMP and Annex 1 typically requires access to technical documentation and evaluation samples. You may request:
Bemærk: Angiv din renrumskvalitet (A/B/C/D), rotation af desinfektionsmiddel, krav om sterilitet og emballage/overførsel SOP-begrænsninger for en præcis dokumentationspakke.


Vi kontakter dig inden for 1 arbejdsdag, vær venligst opmærksom på e-mailen med suffikset “*@midposi.com”.