I det udviklende farmaceutiske landskab står kvalitetssikrings- og overholdelsesansvarlige over for et stigende pres for at udvikle sofistikerede risikobaseret renrums miljøovervågning SOP'er der stemmer overens med 2026-regulatoriske forventninger. Denne vejledning letter skiftet i retning af at bruge data og risikovurdering til at fokusere ressourcer der, hvor de giver størst beskyttelse. Integrering af høj ydeevne renrumsmopper i din forureningskontrolstrategi er et basiskrav for disse dynamiske miljøer.
Hvem skal bruge denne vejledning
- Kvalitetssikringsspecialister: Ansvarlig for EM program design og tilsyn.
- Overholdelsesansvarlige: Sikring af overholdelse af FDA- og EMA-krav.
- Valideringsingeniører: Førende renrumskvalificeringsaktiviteter.
- Facility Managers: Implementering af overvågningsprogrammer.
- Regulatoriske anliggender: Navigering i skiftende overholdelseskrav.
2026 Reguleringslandskab

FDA's risikobaserede tilgangsudvikling
- Enhanced Quality Risk Management (QRM): Integration af ICH Q9 principper.
- Dataintegritet 2.0: Dataindsamling i realtid og automatiseret trendanalyse.
- Kontinuerlig overvågning: Krav om kontinuerlig miljøovervågning (CEM) på kritiske områder.
- Forudsigende analyse: Implementering af tidlige varslingssystemer for forureningsrisici.
- Supply Chain Integration: Risikovurdering inklusive forsyningskædepåvirkninger.
EMA GMP Annex 1 (2026 Implementation)
- Risikobaseret klassificering: Dynamisk renrumsklassificering baseret på risikovurdering.
- Forureningskontrolstrategi (CCS): Omfattende tilgang til vedvarende forurening.
- EM-program: Risikojusterede overvågningsfrekvenser og -steder.
- Undersøgelsesprotokoller: Struktureret tilgang til overvågning af udflugter.
- Kontinuerlig forbedring: Påbudt krav om løbende programoptimering.
Overgangstidslinje for overholdelse
| Tidslinje | Krav | Handlinger påkrævet |
|---|---|---|
| Q1 2024 - Q2 2024 | Gab analyse og risikovurdering udvikling | Udvikle rammer for risikovurdering; identificere højrisikoområder. |
| Q3 2024 - Q1 2025 | SOP revision og validering | Opdater EM-procedurer; validere nye overvågningsmetoder. |
| Q2 2025 - Q4 2025 | Implementering og pilottest | Udrul risikobaseret program; indsamle præstationsdata. |
| Q1 2026 - Fuld overholdelse | Fuldstændig implementering og optimering | Afslut program; etablere løbende forbedringer. |
Udvikling af Risk Assessment Framework
Trin 1: Definer risikovurderingskriterier
Etabler omfattende kriterier for evaluering af renrumsområder og processer.
- Produktrisiko: Sterilt vs. ikke-sterilt, terapeutisk område, indgivelsesvej.
- Procesrisiko: Proceskompleksitet, automatiseringsniveau, interventionsfrekvens.
- Facilitetsrisiko: Luftskift, trykforskelle, persontrafik.
- Historiske data: Tidligere overvågningsresultater og forureningstendenser.
- Ændringspåvirkning: Seneste ændringer, afvigelseshistorik, CAPA-effektivitet.
Trin 2: Udvikl risikomatrix
Kategoriser områder og processer baseret på foruddefinerede kriterier i en struktureret matrix.
Kontinuerlig overvågning
Øjeblikkelig undersøgelse
Øget frekvens
Rettidig undersøgelse
Standard frekvens
Rutinemæssig undersøgelse
Implementeringstip: Brug et scoringssystem (1-5) for hver risikofaktor. Områder, der scorer ≥15, kræver højrisikoovervågningsstrategier.
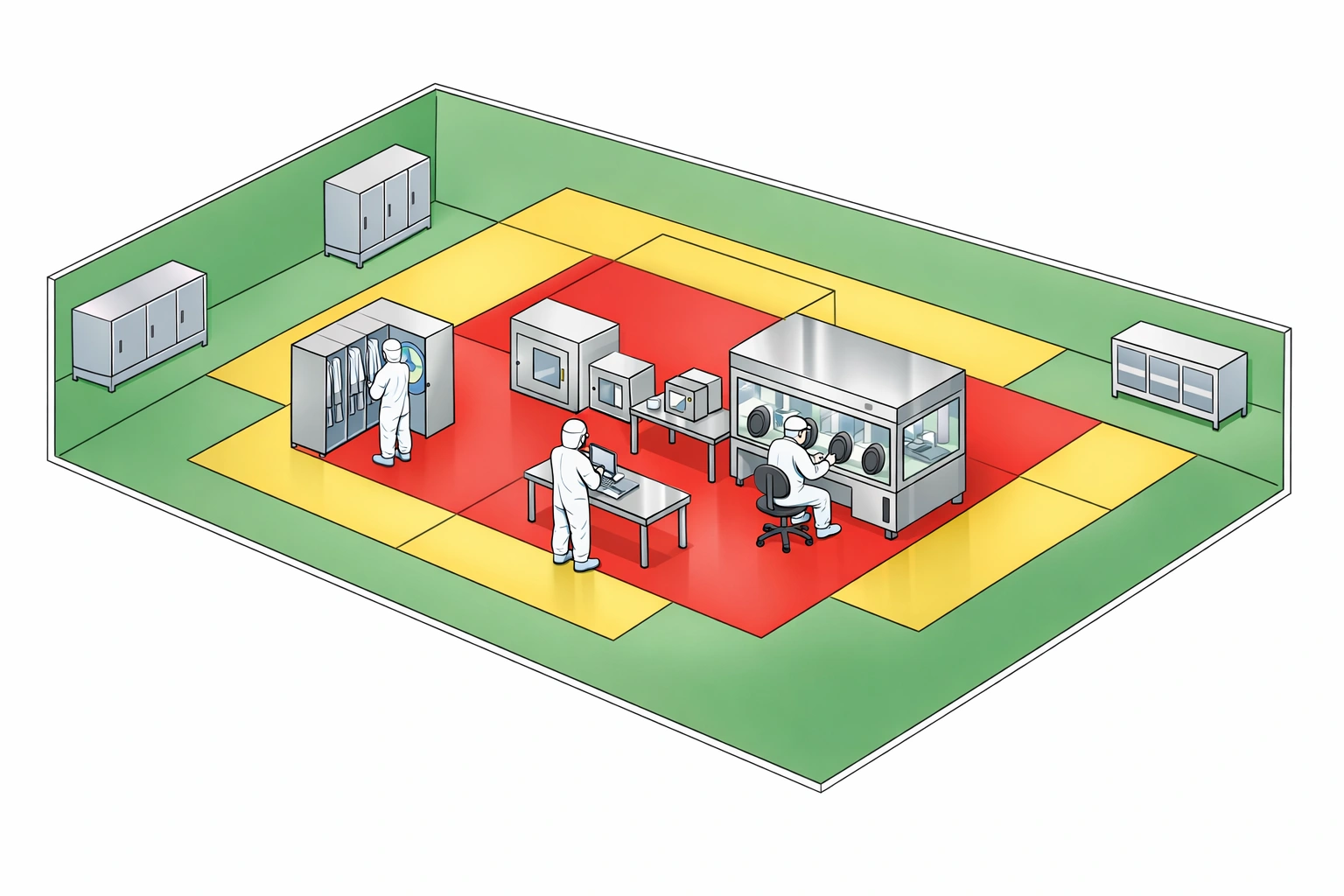
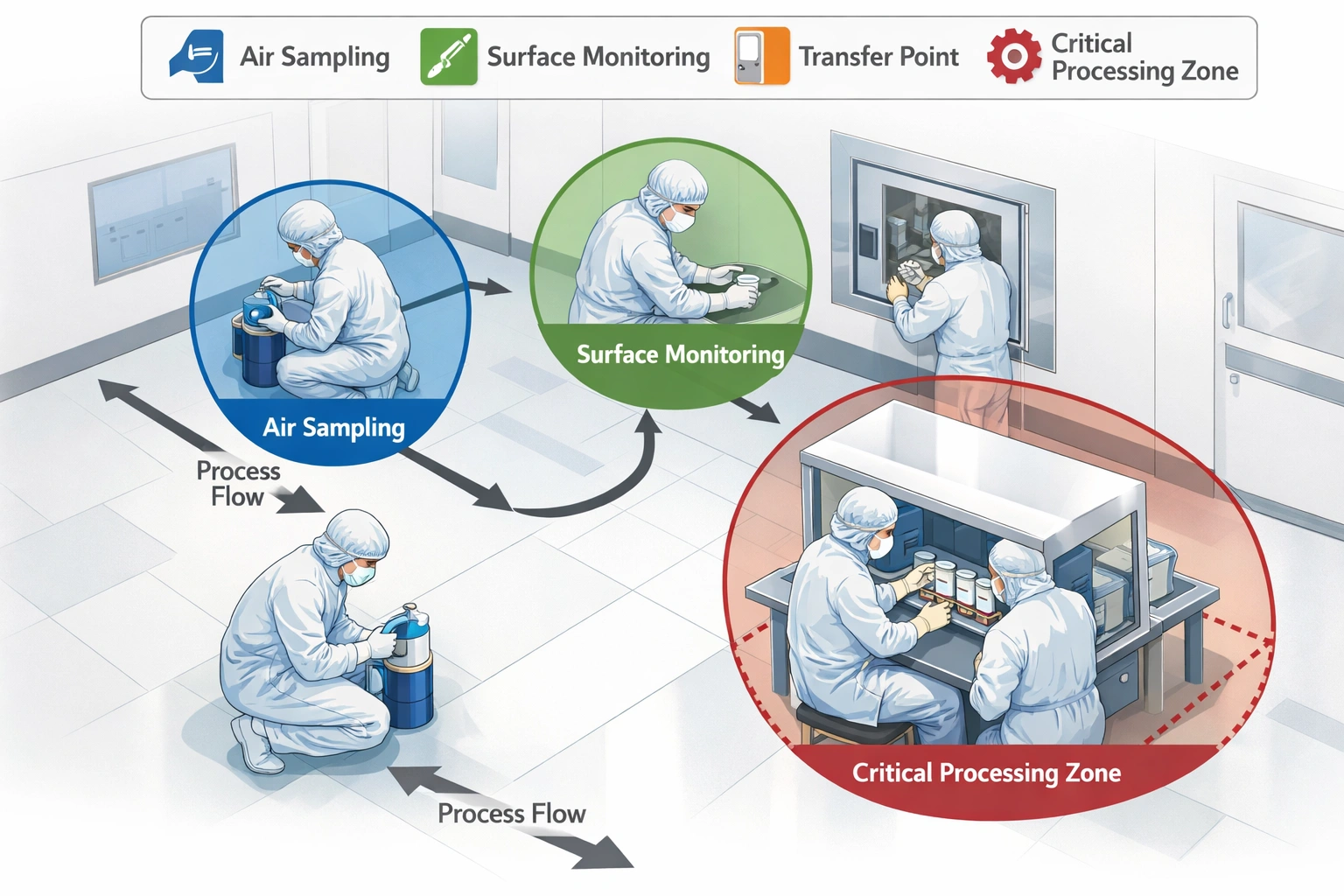
Trin 3: Etabler overvågningssteder
Strategisk placering af udstyr er afgørende. Bruge renrumsvalidering indsigt til at lokalisere kritiske steder.
- Aseptisk behandling: Kritiske zoner, fyld-finish-grænseflader.
- Overførselspoint: Luftsluser, beklædningsrum.
- Områder med høj trafik: Hovedkorridorer, indgrebspunkter.
Trin 4: Definer overvågningsfrekvenser
| Risikoniveau | Levedygtig | Ikke-levedygtig | Overflade |
|---|---|---|---|
| Høj | Kontinuerlig + Ugentligt | Sammenhængende | Daglig. |
| Medium | 2-3 gange om ugen | 2 gange om ugen | 2-3 gange om ugen. |
| Lav | 1-2 gange om ugen | 1 gang/uge | 1 gang/uge. |
Trin 5: Indstil alarm- og handlingsniveauer
Etabler videnskabeligt begrundede niveauer baseret på historiske data og processårbarhed. Anvend statistiske proceskontrolmetoder for præcision.
SOP udviklingsstruktur
Skabelon: ENV-MON-001 (version 2.0)
1.0 Formål: Etabler et risikobaseret EM-program, der sikrer produktkvalitet, samtidig med at ressourcer optimeres.
4.0 Procedure: Risikovurderingsprotokol, overvågningslokationsstrategi, frekvensbestemmelse, styring af alarm-/handlingsniveau.
| SOP element | Traditionel tilgang | Risikobaseret 2026 |
|---|---|---|
| Overvågningssteder | Fast gittermønster | Risikobaseret strategisk placering. |
| Frekvens | Standardiseret tidsplan | Risikojusteret med dynamisk gennemgang. |
| Alarmniveauer | Statiske numeriske værdier | Statistisk + kontekstuel analyse. |
Implementering bedste praksis
Effektiv administration af farmaceutiske faciliteter involverer at gå fra statiske til dynamiske procedurer.
Teknologianbefaling: Implementer CEM-systemer med dataanalyse i realtid. Disse giver væsentlige forudsigelsesmuligheder for 2026-overholdelse.
Trænings- og kompetencematrix
| Publikum | Træningsemner | Vurdering |
|---|---|---|
| QA personale | Risikometodologi, Dataanalyse | Simulering af risikovurdering. |
| Mikrobiologi | Mikrobiel risiko, Trendanalyse | Casestudie analyse. |
| Operationer | Alarmsvar, Dokumentation | Praktisk demonstration. |
Casestudie: Global implementering
Global Farmaceutisk Succeshistorie
- 35 % reduktion i overvågningsomkostninger.
- 40 % hurtigere registrering af kontaminering.
- 50 % reduktion af falske positive alarmer.
- Forbedret operatørforståelse af risikokoncepter.
"The risk-based approach transformed our environmental monitoring program from a compliance burden to a valuable quality assurance tool".
Performance Metrics og KPI'er
| Metrisk kategori | Specifikke KPI | Mål |
|---|---|---|
| Effektivitet | Detektionstid for kontaminering | < 2 timer. |
| Effektivitet | Overvågningsomkostninger pr. enhed | ↓ 30 % baseline. |
| Overholdelse | Lovpligtig inspektionsscore | ≥ 95 %. |
| Kvalitet | Alarm nøjagtighedshastighed | ≥ 90 %. |
Klar til at transformere dit EM-program?
Vent ikke på, at 2026-mandater handler. Kontakt vores ekspertteam for en omfattende vurdering og skræddersyet implementeringsplan skræddersyet til dit anlæg.
Yderligere væsentlige ressourcer
- FDA-vejledning for industrien: Sterile lægemiddelprodukter (2021).
- EU GMP Annex 1: Fremstilling af sterile lægemidler (2026).
- ISPE Baseline Guide: Environmental Monitoring (2024).
- ICH Q9 Kvalitetsrisikostyring.
- ISO 14644-serien: Renrum og tilhørende miljøer.
Ansvarsfraskrivelse: Denne vejledning er kun til informationsformål. Rådfør dig med regulatoriske eksperter og kvalificerede fagfolk for dine specifikke facilitetskrav.





Ekspertkommentar: Overvågningens udvikling
"The shift from traditional to risk-based environmental monitoring represents the most significant evolution in cleanroom management in decades. It's about using data and risk assessment to focus resources where they matter most".
"By 2026, regulatory agencies will mandate risk-based approaches. Companies that proactively implement these strategies will gain competitive advantages through improved efficiency and better contamination control".