En el mercado farmacéutico europeo, altamente regulado, Documentación SOP para salas blancas que cumple con el Anexo 1 de GMP de la UE es más que un marco regulatorio: es la base de la seguridad del paciente y la longevidad del mercado. Para los responsables de cumplimiento de toda la UE, desde los centros de producción en Alemania hasta los clusters de biotecnología en España, dominar esta arquitectura de documentación es esencial para estar preparados para enero de 2026.
¿Quién debería utilizar esta guía?
- Oficiales de cumplimiento: Responsable del cumplimiento de los requisitos de la EMA.
- Profesionales de Asuntos Regulatorios: Gestión de expedientes de autorización de comercialización en la UE.
- Responsables de Calidad: Supervisión de la documentación en instalaciones estériles con sede en la UE.
- Especialistas en Validación: Garantizar que la validación de la sala limpia cumpla con los estándares del Anexo 1.
Anexo 1 de GMP de la UE: descripción general y cronograma de implementación
Revisión publicada
Actualizaciones significativas para el control de la contaminación y el monitoreo ambiental.
Comienza el período de transición
Fase de preparación para su pleno cumplimiento.
Implementación completa
Cumplimiento obligatorio en todos los estados miembros de la UE.
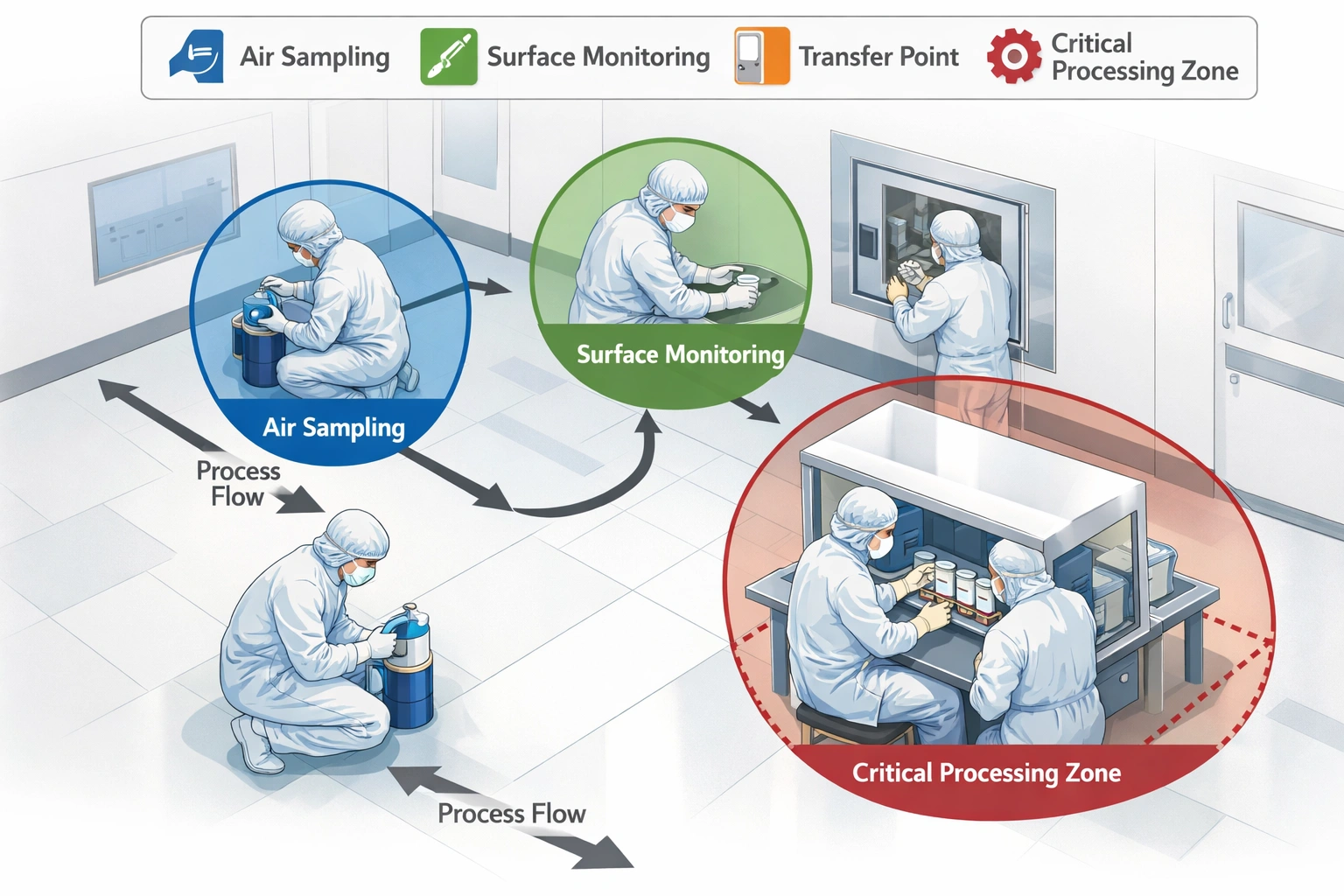
Actualizaciones importantes que afectan la documentación
| Área | Requisito revisado | Impacto de la documentación |
|---|---|---|
| EM | Basado en riesgos con tendencias | Nuevos protocolos de evaluación de riesgos. |
| Contaminación | Estrategia persistente | POE de limpieza mejorados. |
| Ciclo vital | Gestión completa del ciclo de vida | Procedimientos de control integral. |
Requisitos de arquitectura de documentación de la UE
European regulators expect a hierarchical approach that ensures "clear and unambiguous" instructions throughout the facility.
Nivel 1 & 2: calidad & POE del sistema
Incluye Manuales de Calidad y sistemas de Control Documental.

Nivel 3 & 4: Procesar SOP y registros
Procedimientos operativos estándar para salas limpias, incluidos registros de batas, desinfección y producción de lotes.
Requisito específico de la UE: La documentación debe estar en el idioma oficial de la UE del estado miembro donde está ubicada la instalación. Considere versiones bilingües para mayor claridad internacional.
Necesidades de documentación específicas para salas limpias
Deficiencias comunes de inspección: El control de cambios inadecuado y la falta de documentación de evaluación de riesgos son las principales razones de los hallazgos de las inspecciones de la UE.

| Tipo de POE | Requisito específico de la UE | Evidencia requerida |
|---|---|---|
| Desinfección | Pruebas de eficacia | Protocolos de validación & informes. |
| Control de cambios | Riesgo & Evaluación de impacto | Evaluaciones formales. |
| Validación | Verificación del ciclo de vida | VMP & Informes resumidos. |
Consideraciones específicas de los Estados miembros de la UE
Si bien el Anexo 1 está armonizado, existen matices locales en los principales centros manufactureros:
- Alemania: Documentación de seguridad adicional y traducciones al alemán.
- Francia: Requisitos de trazabilidad ampliados para registros de lotes.
- Italia & España: Registros de notificación de formación específica y evaluación de competencias.

Lograr el cumplimiento del Anexo 1 de las GMP de la UE
Nuestro equipo de expertos proporciona sistemas de documentación centralizados y flexibles diseñados para el éxito regulatorio de la UE en 2026. Asegúrese de que su cadena de suministro y sus SOP cumplan con los más altos estándares.






Comentario de expertos: Implementación del Anexo 1 de GMP de la UE
"The revised Annex 1 represents the most significant update to sterile manufacturing in decades. Regulators expect a demonstrable quality culture embedded in every document—comprehensive risk assessments are the new standard."