Gestion du cycle de vie de la validation des salles blanches : un guide complet
Understand the full cleanroom validation lifecycle from DQ, IQ, OQ, and PQ through ongoing verification, requalification, and change control for GMP and ISO environments.

Réponse à l'extrait en vedette
Cleanroom validation lifecycle management covers the complete control framework from design qualification through ongoing performance verification. It helps manufacturers maintain GMP and ISO compliance, reduce contamination risk, and keep cleanroom performance documented throughout the facility’s operational life.
Points clés à retenir
- La validation en salle blanche est un processus de cycle de vie et non un événement de qualification ponctuel.
- DQ, IQ, OQ et PQ vérifient chacun différents aspects de la préparation et du contrôle des salles blanches.
- Une vérification continue et une analyse des tendances sont essentielles au maintien de l’état validé.
- La requalification doit être déclenchée par le calendrier, les événements et la dérive des performances.
- Un contrôle rigoureux des modifications protège l’intégrité de la validation et la qualité du produit.
Introduction
Cleanroom validation is a continuous lifecycle that extends beyond initial IQ, OQ, and PQ certification. Ongoing performance verification and periodic requalification are essential to maintain compliance and ensure product quality throughout the cleanroom’s operational life.
Many regulatory findings stem from weak lifecycle control, including inadequate requalification, incomplete documentation, poor trend analysis, and ineffective change control. A lifecycle-based validation approach helps close these gaps and strengthen GMP inspection readiness.
Présentation du cycle de vie de la validation
The cleanroom validation lifecycle includes initial validation, ongoing verification, and long-term maintenance of the validated state. In practical terms, this means building a system that not only qualifies the room at the beginning, but also keeps it under control over time.
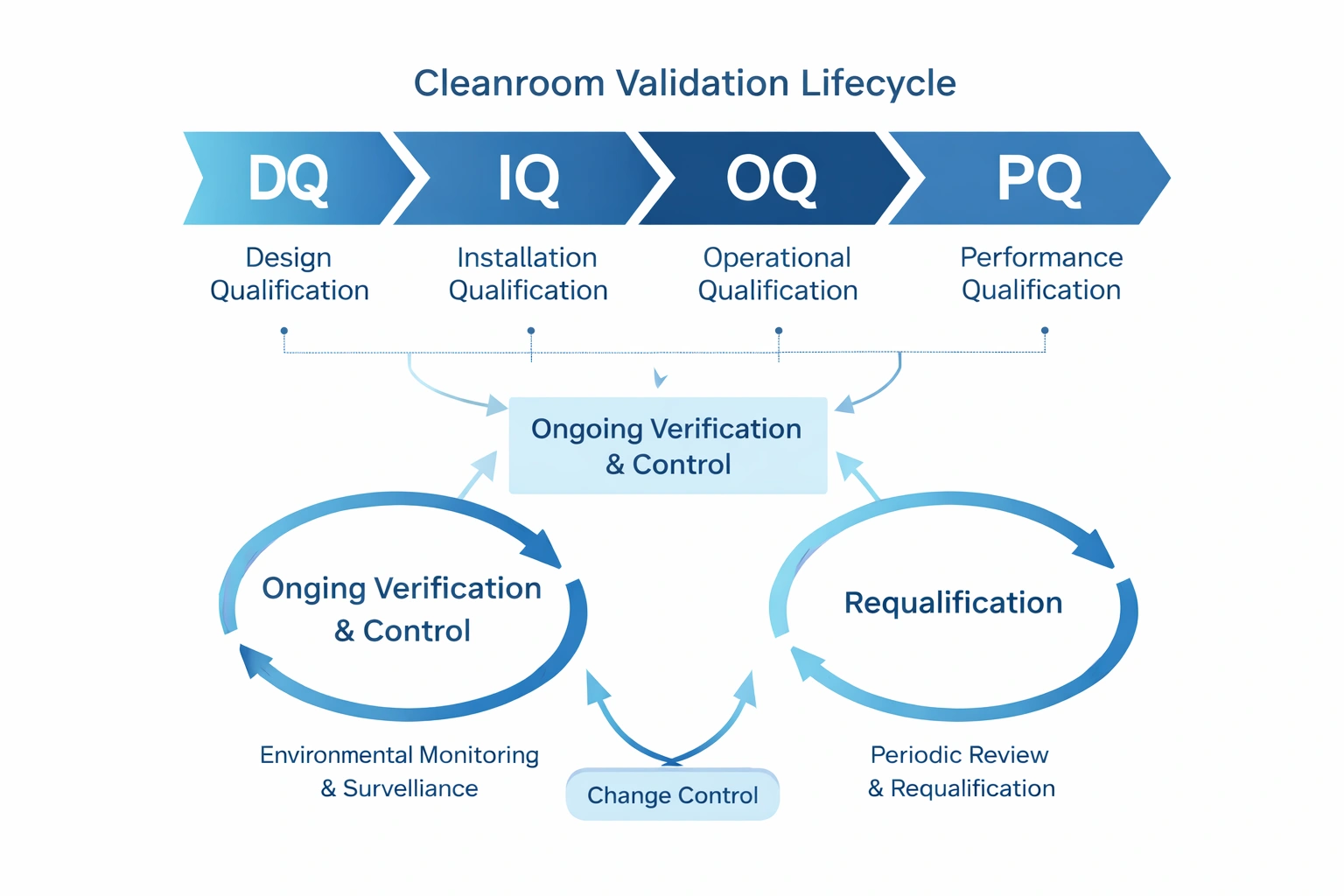
Validation initiale
DQ, IQ, OQ, PQ et version initiale à utiliser.
Vérification continue
Surveillance environnementale, analyse des tendances, examen et contrôle.
Requalification & Changement
La requalification et l’évaluation des changements préservent l’intégrité du cycle de vie.
| Phase | Durée typique | Déclenchement | Propriétaire |
|---|---|---|---|
| QD | 2 à 4 semaines | Lancement d'un nouveau projet | Ingénierie |
| QI | 2 à 4 semaines | Chantier terminé | Installations |
| QO | 4 à 8 semaines | QI complet | Validation |
| PQ | 3 à 6 mois | QO terminé | Validation |
| Vérification continue | En cours | Certification initiale terminée | Assurance qualité |
| Requalification | 2 à 4 semaines | Événement annuel ou déclencheur | Validation |
Qualification de conception (DQ)
Design Qualification verifies that the cleanroom design meets user requirements and is suitable for the intended process, cleanliness class, and contamination control strategy.

Focus DQ
- Spécification des exigences de l'utilisateur (URS)
- Spécification de conception fonctionnelle (FDS)
- Évaluation des risques et examen de la contamination
- Examen de la conception par les parties prenantes
- Approbation DQ documentée
Questions clés
- La conception répond-elle aux besoins de l'utilisateur prévu ?
- Le système peut-il atteindre le niveau de propreté cible ?
- Les risques majeurs de contamination sont-ils identifiés et atténués ?
- La documentation de conception est-elle complète et consultable ?
Qualification d'installation (QI)
IQ provides documented verification that the cleanroom and its supporting systems have been installed according to design specifications, approved drawings, and utility requirements.
Paquet de documentation IQ
- Protocole de QI
- Dessins d'exécution
- Dossiers d'installation
- Enregistrements de connexion aux services publics
- Certificats d'étalonnage
- Rapport récapitulatif sur le QI
Focus sur l'acceptation du QI
- Installé selon les spécifications approuvées
- Utilitaires connectés et fonctionnels
- Instrumentation critique calibrée
- Documentation complète et traçable
- Tous les contrôles d'installation requis ont été réussis
Qualification Opérationnelle (QO)
OQ demonstrates that the cleanroom operates within predetermined limits under anticipated operating conditions. Typical OQ activities include airflow, pressure, particle, temperature, humidity, alarm, and interlock verification.
| Critère | Exigence typique | Objectif d'acceptation |
|---|---|---|
| Vitesse du flux d'air | Dans la plage spécifiée | Tous les emplacements critiques à portée |
| Uniformité du flux d'air | ±20% de la moyenne | Profil stable et reproductible |
| Différentiel de pression | Dans la cascade cible | Toutes les relations de pression sont maintenues |
| Nombre de particules | Conforme à la classe ISO | Classement au repos atteint |
| Température / HR | Dans la bande de consigne | L’environnement reste contrôlable |
Qualification de performance (QP)
PQ verifies that the cleanroom performs effectively and reproducibly under normal operating conditions with actual personnel activity, process simulation, and product-related contamination risk.

Période 1
Vérification de base dans des conditions contrôlées de faible activité.
Période 2
Simulation de processus de routine avec suivi aligné sur le plan EM.
Période 3
Vérification des performances étendue ou dans le pire des cas pour garantir la cohérence.
Vérification continue
Ongoing verification is what keeps the validated state alive after release. It typically includes environmental monitoring, continuous parameter monitoring, periodic trend analysis, deviation review, and assessment of whether requalification is needed.
Activités typiques
- Surveillance environnementale selon le plan approuvé
- Examen de la pression, de la température et de l'humidité
- Analyse des tendances trimestrielles ou périodiques
- Examen de l'état de préparation à l'audit
- Suivi de requalification
Pourquoi c'est important
- Détecte précocement les dérives de performances
- Prend en charge CAPA et la réduction des risques
- Renforce la préparation à l’inspection BPF
- Fournit la preuve d’un contrôle continu
Stratégie de requalification
Requalification should be based not only on a schedule, but also on change events and performance signals. A robust strategy combines annual review with event-based and trend-based triggers.
Déclencheurs programmés
Cycle d’examen annuel et intervalles de qualification définis par les SOP.
Déclencheurs d'événements
Entretien majeur, remplacement HEPA, modifications CVC, changements de processus.
Déclencheurs de performances
Excursions répétées, taux d’alerte en hausse, dégradation inexpliquée, dérive.
Contrôle des modifications
Change control protects validation integrity by ensuring each relevant modification is assessed before implementation. The goal is to determine whether the change has no validation impact, requires partial requalification, or requires expanded requalification.
Enregistrements de contrôle des modifications requis
- Demande de changement
- Analyse d'impact
- Examen des risques
- Requalification plan
- Preuve d’approbation et de mise en œuvre
- Dossiers de validation mis à jour
Résultats typiques
- Aucun impact — aucune requalification nécessaire
- Impact mineur – qualification ciblée requise
- Impact majeur — requalification complète ou élargie requise
Questions fréquemment posées
À quelle fréquence la requalification des salles blanches doit-elle être effectuée ?
Annual review is common, but requalification should also be triggered by significant maintenance, process changes, major modifications, repeated excursions, or evidence of performance degradation.
Quelle est la différence entre la validation initiale et la requalification ?
Initial validation establishes the original validated state through DQ, IQ, OQ, and PQ. Requalification confirms that the validated state remains acceptable after time, use, or change.
Comment puis-je déterminer si un changement nécessite une requalification ?
Review whether the change affects airflow, pressure cascade, filtration, environmental control, process conditions, contamination risk, or documentation status. The higher the impact, the broader the scope.
Quelle documentation est requise pour la gestion du cycle de vie de validation ?
Typical records include DQ, IQ, OQ, and PQ protocols and reports, environmental monitoring records, trend analyses, requalification files, change control records, and approval evidence.
Pourquoi la gestion du cycle de vie de la validation est-elle importante pour la qualité des produits ?
Because cleanroom control is not static. Lifecycle management helps maintain the validated state, detect drift early, reduce contamination risk, and support consistent product quality.



