La tracciabilità dei lotti di materiali di consumo per camere bianche non è solo un esercizio di documentazione. È la spina dorsale operativa che consente ai produttori, ai team di lavorazione sterile e agli impianti regolamentati di collegare materie prime, produzione, sterilizzazione, distribuzione e utilizzo finale in un'unica catena di prove verificabili.
Negli ambienti farmaceutici, biotecnologici, dei semiconduttori e dei dispositivi medici, la tracciabilità incompleta crea rischi che vanno ben oltre le lacune burocratiche. Ritarda le indagini, indebolisce la risposta al ritiro, complica gli audit e mina la fiducia nei programmi di controllo della contaminazione. Un sistema robusto dovrebbe aiutare i team di qualità a passare dalla raccolta reattiva dei record al controllo proattivo.
Tracciabilità dei lotti per i materiali di consumo per camere bianche significa mantenere una registrazione completa e recuperabile di ciascun lotto, dal materiale in entrata fino alla produzione, sterilizzazione, distribuzione e utilizzo finale. In pratica, un sistema efficace dovrebbe identificare cosa è stato prodotto, da quali materiali di origine, in quali condizioni di processo, dove è stato spedito e quali clienti o utenti interni sono stati interessati in caso di deviazione o richiamo.
Per le strutture regolamentate, i sistemi migliori non sono conformi solo sulla carta. Sono veloci da ricercare, facili da verificare, pronti per l'audit e in grado di supportare un richiamo mirato in poche ore invece che in giorni.
Una solida tracciabilità dei lotti collega i lotti di materie prime, i lotti di produzione, i registri di sterilizzazione, i dati di spedizione e il consumo da parte dell'utente finale in un'unica catena di prove.
I sistemi predisposti per l’audit devono supportare indagini rapide e richiami mirati, non solo l’archiviazione passiva di record disconnessi.
Una chiara logica di numerazione dei lotti riduce la confusione dell'operatore e migliora la reportistica, l'etichettatura, il rilascio e la gestione dei reclami a valle.
La tracciabilità in avanti, la tracciabilità all'indietro e la simulazione del ritiro dovrebbero essere periodicamente testate per dimostrare che il sistema funziona effettivamente sotto pressione.
Molte strutture registrano già i numeri di lotto su cartoni, etichette o documenti di sterilizzazione. Il problema è che questi registri sono spesso frammentati tra registri di acquisto, magazzino, produzione, sterilizzazione, logistica e utente finale. Quando si verifica un reclamo, un evento di contaminazione o una richiesta di audit, il team deve ricostruire manualmente la cronologia.
Questo approccio è lento, soggetto a errori e costoso. Un programma di tracciabilità maturo riduce i tempi di indagine, migliora la sicurezza del rilascio e limita la portata delle azioni di richiamo. Supporta inoltre l'analisi delle tendenze, la gestione dei fornitori, il CAPA e la comunicazione con i clienti.

Un sistema di tracciabilità dei materiali di consumo per camere bianche dovrebbe essere progettato in base al modo in cui le organizzazioni regolamentate indagano sulle deviazioni e dimostrano il controllo. Per molti utenti, i riferimenti più rilevanti includono l’Allegato 1 GMP dell’UE, le aspettative di tenuta dei registri cGMP della FDA e i requisiti di tracciabilità ISO 13485 per i sistemi di qualità relativi ai dispositivi medici.
| Regolamento/Normativa | Area di messa a fuoco | Significato operativo |
|---|---|---|
| Allegato 1 delle GMP dell'UE | Tracciabilità, record dei lotti, capacità di richiamo | Le strutture dovrebbero essere in grado di identificare rapidamente i materiali e i prodotti finiti interessati durante le indagini o le azioni di mercato. |
| FDA 21 CFR 211.180 / 211.198 | Registri di distribuzione, file di reclamo, conservazione | Le registrazioni dovrebbero supportare la valutazione dei reclami, la revisione dell'impatto del lotto e l'esecuzione controllata del ritiro. |
| ISO 13485 Sezione 7.5.8 | Identificazione e recupero univoci | L'organizzazione dovrebbe mantenere procedure di tracciabilità documentate ed essere in grado di recuperare i record collegati quando necessario. |
Per gli acquirenti e i team di QA, ciò significa che la tracciabilità non dovrebbe essere trattata come una funzione esclusivamente di magazzino. Si tratta di un requisito di qualità interfunzionale che riguarda il controllo dei fornitori, la documentazione di produzione, il rilascio della sterilizzazione, lo storico delle spedizioni e la responsabilità dell'utente finale.
Un modo utile per strutturare la tracciabilità dei lotti è dividere il sistema in cinque livelli collegati: materie prime, produzione, sterilizzazione, distribuzione e consumo. Questo framework aiuta i team a definire proprietà, campi dati e checkpoint di verifica senza perdere la visibilità end-to-end.
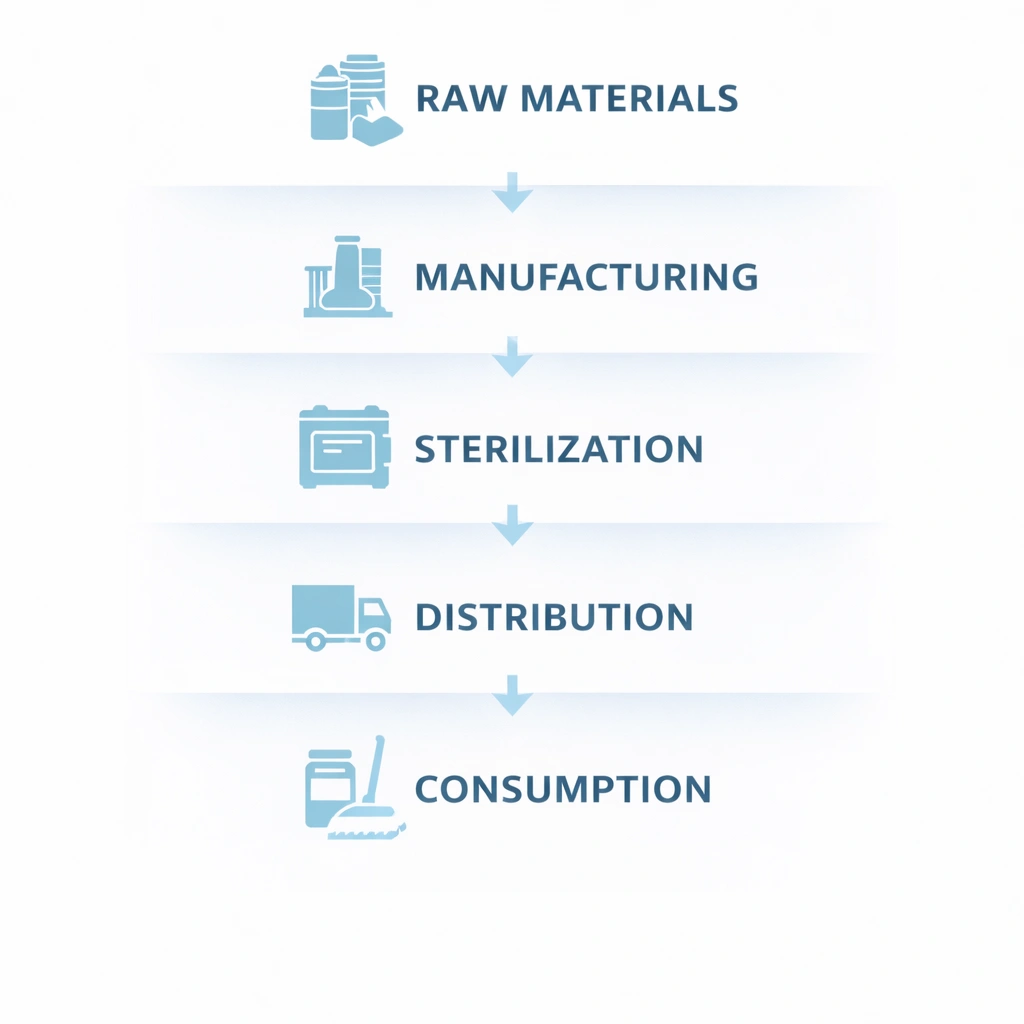
Acquisisci l'identità del fornitore, il numero di lotto del fornitore, la data di ricevimento, lo stato dell'ispezione in entrata e i certificati pertinenti come COA o CoC. Questo è il punto di partenza per il controllo a monte.
Registrare quali materiali sono stati utilizzati, quale linea ha prodotto il lotto, chi ha gestito o rilasciato il processo e quali controlli QC in corso o finali sono stati eseguiti.
Per i materiali di consumo sterili, collegare il lotto di produzione al lotto di sterilizzazione, ai parametri del ciclo, al metodo di sterilizzazione, allo stato di rilascio e a qualsiasi prova di convalida.
Collega i numeri di lotto ai clienti, alle quantità di spedizione, alle date di spedizione, alle informazioni sul corriere e ai dettagli della destinazione. Ciò è essenziale per la valutazione dei reclami e il contenimento dei richiami.
Laddove il modello d'uso lo richieda, conservare i record lato utente relativi al numero di lotto, alla data di utilizzo, all'ubicazione e al percorso di smaltimento. Ciò è particolarmente utile negli ambienti GMP ad alto rischio.
Il numero di lotto dovrebbe essere più di un timbro seriale. Dovrebbe supportare un'interpretazione rapida, un'archiviazione accurata, una presentazione pulita delle etichette e una gestione manuale a basso errore. Un formato strutturato rende inoltre più affidabili la ricerca e il reporting digitale.

| Elemento batch | Esempio | Perché è importante |
|---|---|---|
| Codice Fornitore/Produttore | MIDPOSI | Identifica l'origine della produzione e separa marchi, siti o flussi di fornitura. |
| Segmento data | 2026-04-06 | Aiuta gli operatori a identificare rapidamente la cronologia di produzione e la logica di conservazione. |
| Numero di serie | 001 | Differenzia più lotti prodotti nello stesso giorno o finestra del ciclo. |
| Suffisso/Marcatore di processo | A/B/C | Utile per le distinzioni del flusso di lavoro di produzione, sterilizzazione, risterilizzazione o QA. |
Anche una forte etichettatura fisica non è sufficiente se i documenti di supporto sono incompleti. Un file di tracciabilità difendibile dovrebbe consentire a un revisore di passare da un lotto finito ai materiali di origine e da un materiale di origine a ogni lotto finito interessato e spedizione al cliente.
Lotto fornitore, quantità ricevuta, esito ispezione, controllo documenti, stato rilascio.
Numero di lotto, operatore, linea, data del processo, utilizzo del materiale, punti di controllo QC, deviazioni.
Lotto di sterilizzazione, dati del ciclo, decisione di rilascio, quantità spedita dal cliente, destinazione, collegamento del reclamo.
Il set di documentazione dovrebbe anche essere facile da recuperare durante gli audit dei fornitori, la qualificazione dei clienti, la gestione dei reclami e le revisioni del CAPA. Se l’individuazione del file giusto richiede troppo tempo, il sistema è funzionalmente più debole di quanto appaia sulla carta.
Un sistema di tracciabilità dovrebbe essere testato, non dato per scontato. L'approccio più pratico consiste nell'eseguire tre tipi di esercizi: tracciabilità in avanti, tracciabilità all'indietro e simulazione del richiamo. Questi test rivelano se i campi dati sono realmente collegati, se i team sanno dove cercare e se il tempo di risposta soddisfa le aspettative interne.
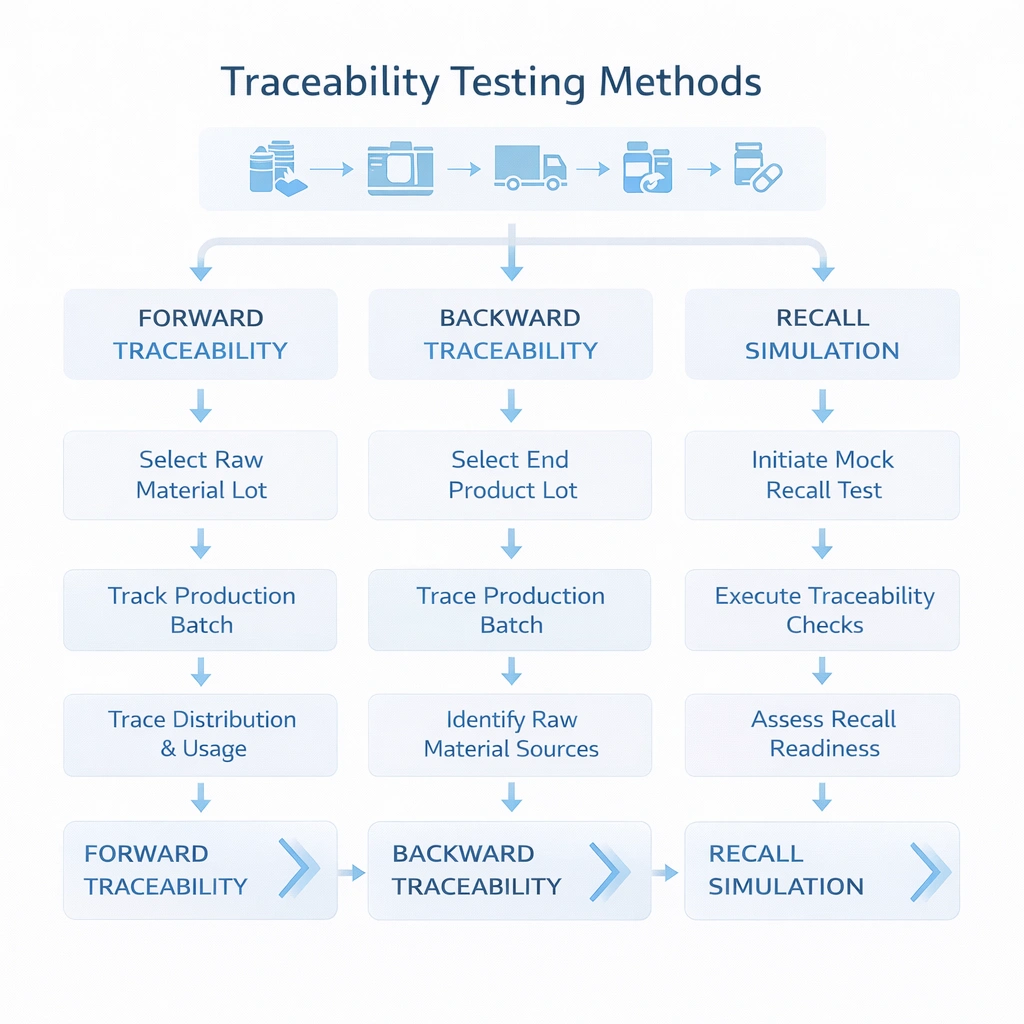
Inizia con un lotto di materiale in entrata e determina quali lotti di produzione, cicli di sterilizzazione e spedizioni ai clienti sono stati interessati.
Inizia con un reclamo o un lotto utilizzato dal cliente e risali ai materiali di origine, ai record di processo e allo stato di rilascio.
Seleziona un lotto e simula un richiamo mirato: identifica ogni cliente interessato, quantità, percorso di spedizione e proprietario del contatto. Registrare il tempo totale necessario e le lacune nei dati rilevate. Negli ambienti ad alto controllo, questo esercizio è uno dei modi più rapidi per valutare se il sistema è realmente pronto per il ritiro.
| Tipo di prova | Domanda principale | Risultato previsto |
|---|---|---|
| Tracciabilità in avanti | Dove è finito questo input? | Registri di produzione, sterilizzazione e spedizione interessati |
| Tracciabilità a ritroso | Cosa ha creato questo risultato? | Materiale originale, cronologia del processo, prove rilasciate |
| Richiama la simulazione | Possiamo agire in modo rapido e accurato? | Elenco clienti, mappa quantità, tempi di risposta, registro gap dati |
Un flusso di lavoro di richiamo dovrebbe essere predeterminato piuttosto che improvvisato. Quando si verifica un problema di qualità, i team dovrebbero già sapere come classificare il problema, identificare i lotti interessati, informare le parti interessate, interrompere l'ulteriore distribuzione e documentare la causa principale e le azioni correttive.
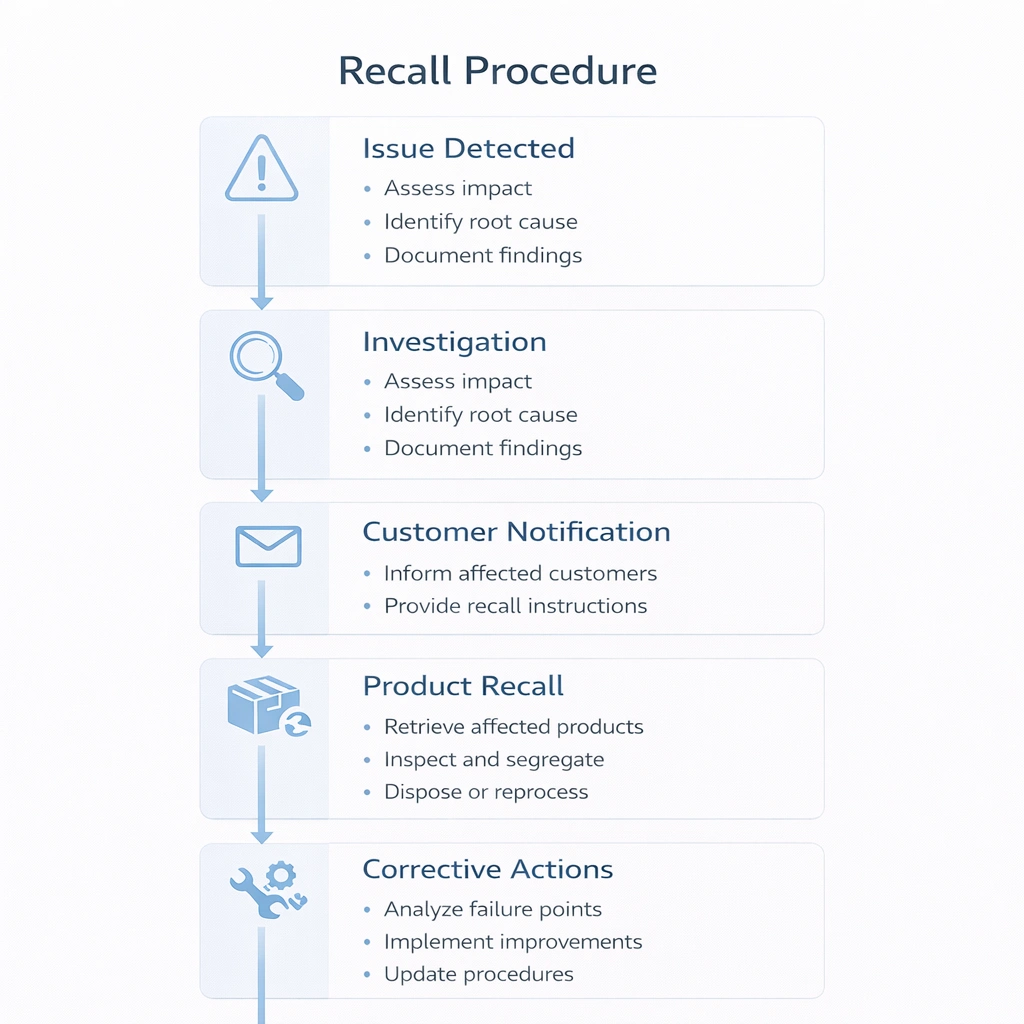
I sistemi basati su fogli di calcolo possono funzionare a bassa complessità, ma con l’espansione della gamma di prodotti, del volume dei clienti e dei flussi di lavoro legati alla sterilità, la tracciabilità elettronica diventa solitamente più pratica. I sistemi supportati da codici a barre o RFID riducono il rischio di immissione manuale e rendono la simulazione del richiamo più rapida e ripetibile.

Definire campi dati, proprietà, logica del codice batch, regole di conservazione e ambito di tracciabilità per linee sterili e non sterili.
Standardizzare i moduli, l'acquisizione dei lotti dei fornitori, i registri di produzione, il collegamento alla sterilizzazione e i registri di spedizione.
Esegui la tracciabilità in avanti e all'indietro, richiama i test di simulazione e documenta le lacune rilevate.
Come minimo, il sistema dovrebbe collegare i lotti di materiale in entrata, i lotti di produzione, i registri di rilascio o sterilizzazione, ove applicabile, la cronologia delle spedizioni e la capacità di identificare i clienti o gli utenti interessati durante un'indagine.
L'etichettatura dei lotti identifica un gruppo di prodotti. La tracciabilità completa collega l'etichetta ai materiali a monte, ai record di processo, alle decisioni di rilascio e ai record di distribuzione o utilizzo a valle.
Molti team di qualità lo eseguono almeno una volta all'anno, mentre le operazioni ad alto rischio o più complesse possono essere testate più spesso, soprattutto dopo cambiamenti di sistema, spostamenti di fornitori o importanti azioni CAPA.
Sì, per operazioni a basso volume. Ma una volta che la variazione del prodotto, il controllo della sterilità o la complessità del cliente aumentano, i sistemi digitali solitamente forniscono una migliore velocità di recupero, riduzione degli errori e controllo di audit.
Perché i prodotti sterili richiedono un controllo più rigoroso della cronologia dei lotti, dei collegamenti alla sterilizzazione, delle prove di rilascio e della visibilità a valle in caso di reclamo, preoccupazione per la sterilità o decisione di richiamo.
Midposi supporta gli acquirenti regolamentati con materiali di consumo per camere bianche progettati per ambienti controllati, compresa la comunicazione orientata alla documentazione per la qualificazione, la revisione dello stato di sterilità e le discussioni sulla tracciabilità dei lotti.


Ti contatteremo entro 1 giorno lavorativo, fai attenzione all'email con il suffisso “*@midposi.com”.