Un riferimento tecnico per i responsabili del controllo qualità e gli ingegneri di validazione sull'integrazione della tracciabilità dei materiali di consumo nella strategia di controllo della contaminazione (CCS) del sito.

In un ambiente regolamentato dalle GMP, lo spazzolone per camere bianche non è più visto come un'utilità generica ma come un input controllato critico. Mop per camere bianche con tracciabilità dei lotti i sistemi svolgono tre funzioni principali:
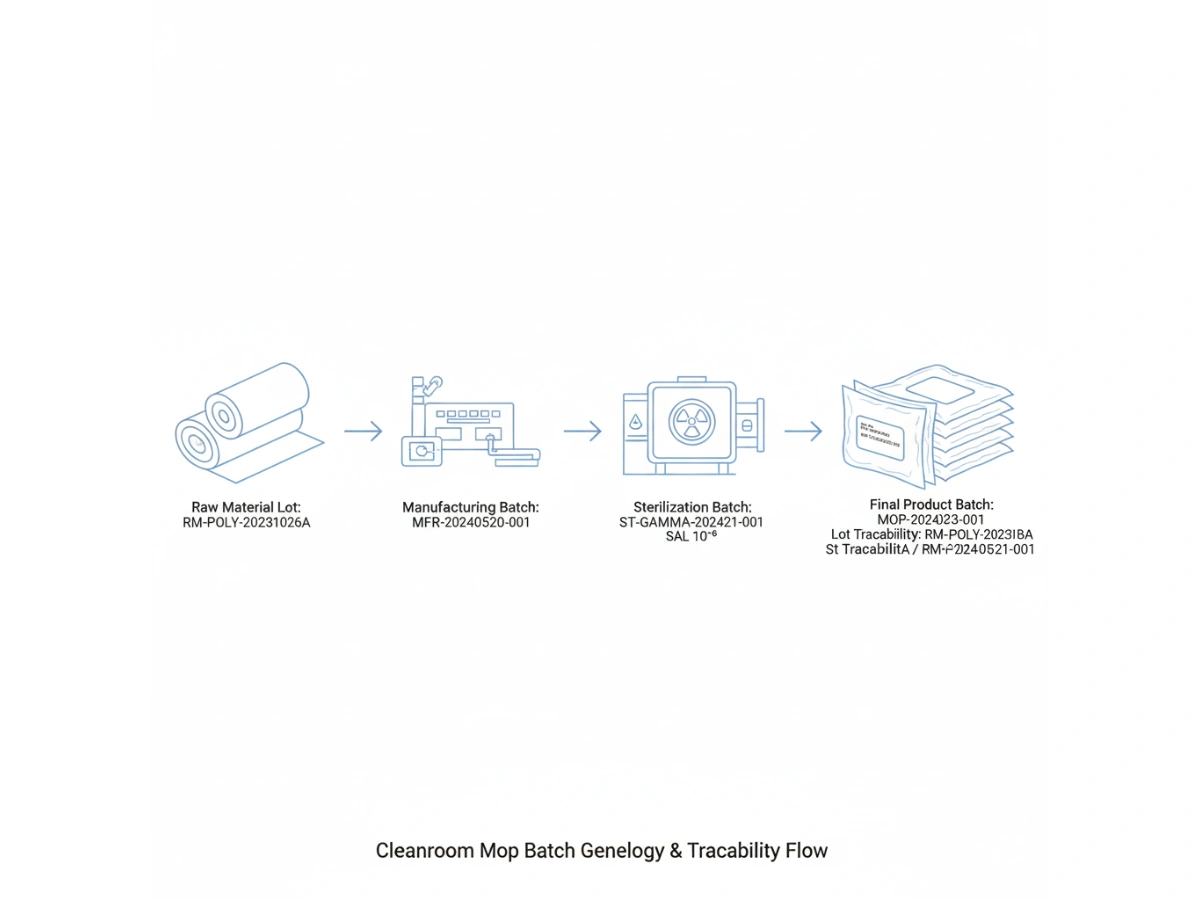
Product-level traceability identifies a SKU; batch-level traceability identifies the specific manufacturing event. For cleanroom mops, this requires a "genealogy" that links the finished product back to the specific lot of polyester yarn or microfiber fabric used, the cleanroom laundry shift, and the specific sterilization cycle.
Quando i panni vengono trattati come input controllati, ogni singolo pacchetto è un punto dati. Questi dati consentono ai team QA di verificare che il prodotto che hanno in mano sia identico in termini di prestazioni e purezza al prodotto convalidato durante l'avvio iniziale della struttura o PQ (Performance Qualification).
I moderni principi GMP richiedono che tutti i materiali che entrano in contatto con superfici sensibili siano pienamente presi in considerazione. Durante un'ispezione, un auditor può selezionare una data di produzione e richiederne la data tracciabilità del lotto dei materiali per la pulizia utilizzati quel giorno.
Expectations focus on the "Linkage of Records." An auditor will look for a seamless transition from the facility's cleaning logs to the documentazione a livello di batch forniti dal fornitore. Se un lotto di mop non può essere collegato a un certificato di analisi (COA) o a un registro di sterilizzazione, la sterilità e la pulizia dell'intera camera bianca potrebbero essere messe in discussione.

Un robusto sistema di tracciabilità per materiali di consumo per camere bianche GMP la conformità deve includere:
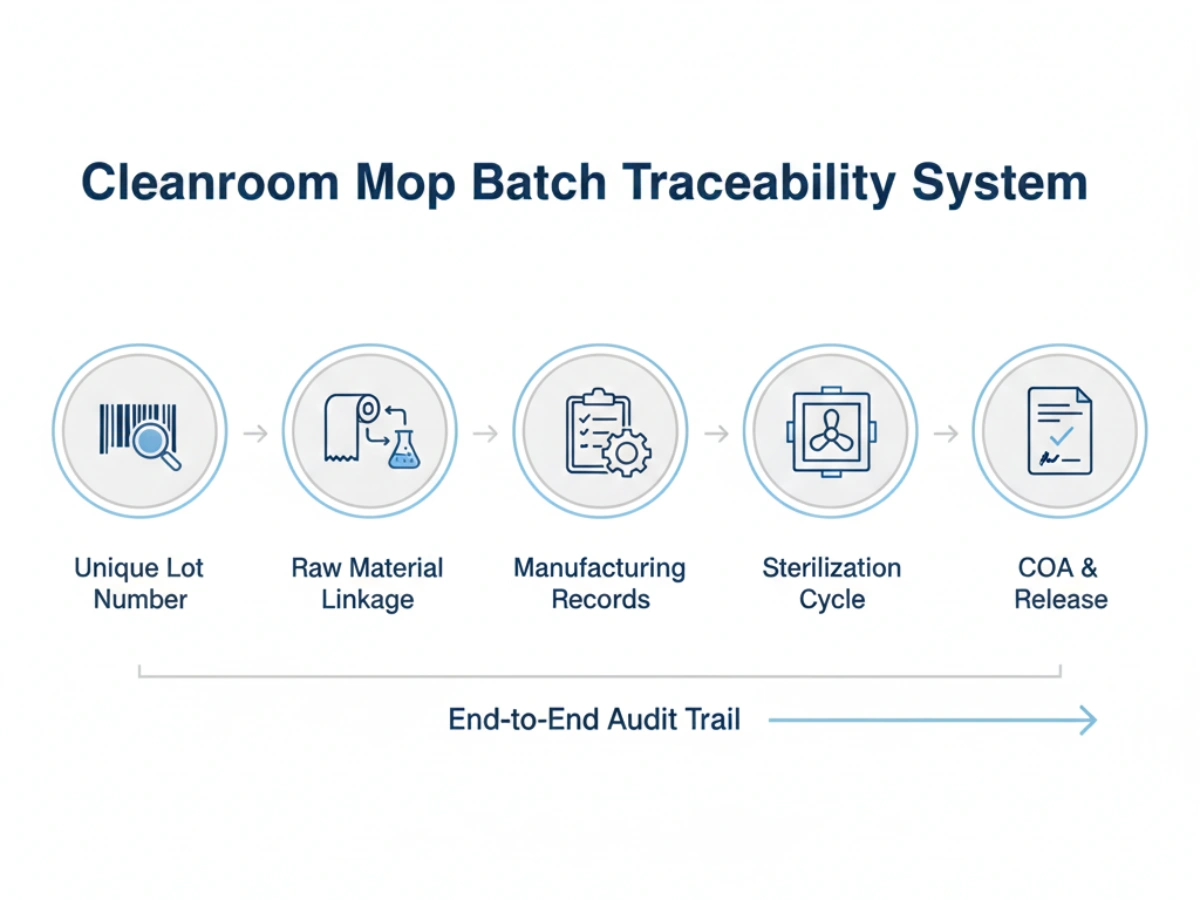
Supply stability is often threatened by "drift"—small, undocumented changes in manufacturing that accumulate over years. Batch traceability prevents this by establishing a baseline for coerenza tra lotti.
Nel caso di un CAPA (azione correttiva e preventiva) che coinvolga picchi di monitoraggio ambientale (EM), la tracciabilità consente al QA di determinare se un lotto specifico di mop ha contribuito all'evento. Senza questo, la struttura potrebbe essere costretta a eliminare tutto l’inventario e a interrompere la produzione, ponendo un enorme rischio operativo. La tracciabilità trasforma una potenziale crisi a livello di struttura in una quarantena materiale localizzata.

UN produttore/OEM di mop farmaceutici funge da estensione del sistema di qualità del sito farmaceutico. Le loro responsabilità includono:
Per un produttore qualificato, la capacità di produrre questi documenti su richiesta è il segno distintivo della maturità del GMP.
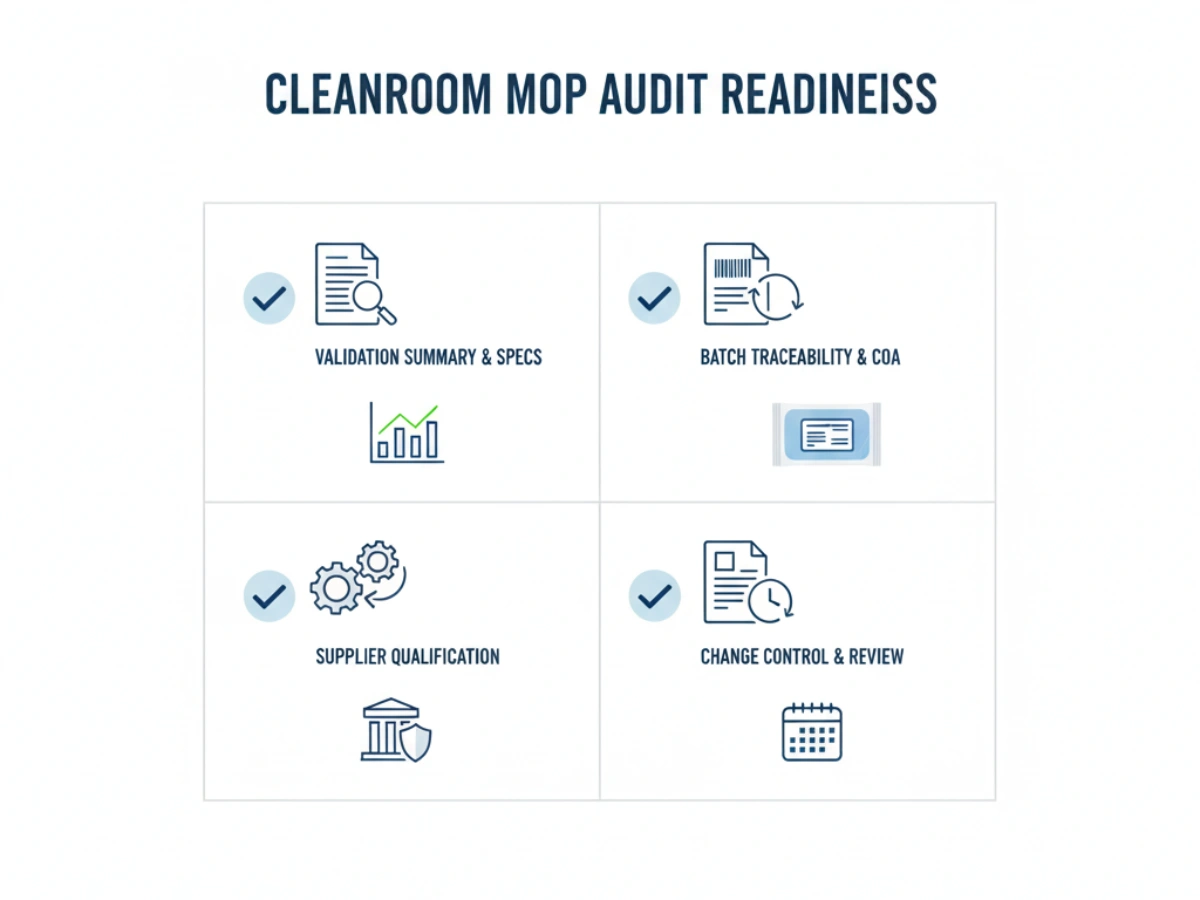
Durante Qualificazione dei fornitori OEM, i team di QA dovrebbero utilizzare il seguente elenco di controllo:
| Punto di controllo | Requisito |
|---|---|
| Definizione batch | La dimensione del lotto è chiaramente definita e gestibile? |
| Conservazione del campione | Il fornitore conserva campioni per ogni lotto? |
| Accesso al controllo | Il fornitore può fornire i registri completi delle materie prime entro 48 ore? |
| Etichettatura fisica | Il numero di lotto è resistente ai disinfettanti per camere bianche (IPA)? |
La tracciabilità dei lotti non è semplicemente un esercizio di documentazione; è la spina dorsale di un sistema di qualità difendibile. Nel contesto degli ambienti di grado A e B, la capacità di monitorare ogni fibra e ogni ciclo di sterilizzazione garantisce che il processo di pulizia rimanga una variabile controllata anziché un rischio sconosciuto.
I team di QA farmaceutici maturi danno priorità ai fornitori che dimostrano totale trasparenza nei loro registri dei lotti, considerandoli come partner a lungo termine nella sicurezza dei pazienti e nella conformità normativa.
Richiedi la genealogia dei lotti, i COA specifici del lotto, il collegamento alla sterilizzazione e la disponibilità al controllo delle modifiche per rafforzare la narrativa dell'audit.
Richiedi pacchetto di documentazione

Ti contatteremo entro 1 giorno lavorativo, fai attenzione all'email con il suffisso “*@midposi.com”.