Nella produzione farmaceutica, i fallimenti nel controllo della contaminazione riconducibili agli strumenti di pulizia rappresentano una delle fonti più prevenibili di escursioni di monitoraggio ambientale e osservazioni normative. Una lettera di avvertimento della FDA del 2025 citava specificamente “salviette non sterili all’interno dell’area di lavorazione asettica ISO 5” e “l’incapacità di stabilire un sistema adeguato per la pulizia e la disinfezione” come violazioni CGMP che mettevano a repentaglio la sterilità dei lotti. La causa principale: strumenti di pulizia riutilizzabili che trasportano carica batterica e contaminazione da particelle derivanti dall’uso precedente, lavati in modo inadeguato e introdotti in zone asettiche senza un ritrattamento convalidato.
I panni monouso per camere bianche eliminano completamente questo percorso di contaminazione. Ogni ciclo di pulizia inizia con un panno nuovo e convalidato: nessun rischio di contaminazione incrociata dalle stanze precedenti, nessun residuo di bucato, nessun onere di convalida del ritrattamento. Per le strutture che operano secondo la norma ISO 14644-1 e l'allegato 1 GMP dell'UE rivisto (in vigore da agosto 2023), i panni usa e getta offrono zero contaminazioni incrociate, prestazioni prevedibili delle particelle e una documentazione di convalida della pulizia notevolmente semplificata. Il panorama normativo e l’economia dei costi totali favoriscono sempre più gli strumenti di pulizia monouso nella produzione asettica, nelle linee di riempimento e finitura e nelle aree di produzione farmaceutica ad alto rischio.
Questo non significa “i prodotti usa e getta sono sempre migliori”. I sistemi di scopa riutilizzabili rimangono convenienti nelle aree di supporto ISO 8, nella produzione su larga scala con riciclaggio interno convalidato e nelle strutture con una solida infrastruttura di ritrattamento. Ma quando il controllo della contaminazione è rigoroso (nuclei asettici ISO 5-7), gli errori di monitoraggio ambientale sono frequenti o le risorse di validazione sono limitate, i panni monouso per camere bianche offrono un controllo superiore della contaminazione e un costo totale di proprietà inferiore nonostante il prezzo unitario più elevato.
Questa guida esamina i fattori normativi alla base dell'adozione dei mop usa e getta, quantifica i principali vantaggi (contaminazione incrociata zero, prestazioni prevedibili, oneri di convalida ridotti), confronta il costo totale di proprietà con i sistemi riutilizzabili, mappa i casi d'uso in base alla classificazione ISO e consiglia i prodotti mop usa e getta MIDPOSI abbinati ai requisiti della struttura. Alla fine, avrai un quadro decisionale chiaro su quando i panni usa e getta per camere bianche giustificheranno il loro costo attraverso la riduzione del rischio di contaminazione, la conformità semplificata e l’eliminazione dei cicli di indagine EM.

Perché i panni usa e getta stanno crescendo nel settore farmaceutico
Lo spostamento verso i panni usa e getta per camere bianche non è una tendenza guidata dal marketing dei fornitori: riflette cambiamenti fondamentali nelle aspettative normative, fallimenti misurabili nel controllo della contaminazione riconducibili a strumenti riutilizzabili e gli aspetti economici del monitoraggio ambientale nella moderna produzione farmaceutica.
Vantaggi principali dei panni monouso per camere bianche (contaminazione incrociata zero)
I panni monouso per camere bianche offrono quattro vantaggi misurabili rispetto ai sistemi riutilizzabili: contaminazione incrociata garantita pari a zero, prestazioni microbiche e di particelle prevedibili, minore onere di convalida e documentazione e migliore efficienza della manodopera. Questi vantaggi si sommano nelle applicazioni farmaceutiche ad alto rischio in cui i margini di controllo della contaminazione sono ristretti e il controllo normativo è intenso.
Contaminazione incrociata zero garantita
La contaminazione incrociata, ovvero il trasferimento di contaminanti da un luogo, un prodotto o un'operazione a un altro, è il rischio fondamentale introdotto dagli strumenti di pulizia riutilizzabili. Ogni panno riutilizzabile accumula carica batterica, particelle e residui chimici durante l'uso. Il lavaggio riduce questi contaminanti ma raramente raggiunge la sterilità o la completa rimozione dei residui. Quando lo spazzolone rientra in un'area classificata, trasporta la contaminazione degli ambienti precedenti.
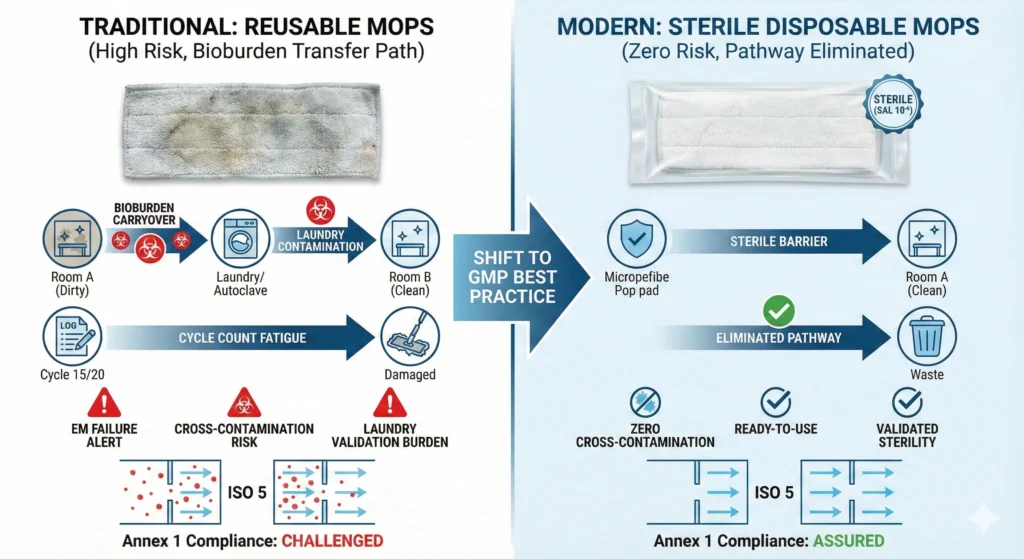
I panni monouso per camere bianche eliminano questo percorso:
- Mocio fresco ad ogni ciclo: Ogni operazione di pulizia inizia con un nuovo tampone rimosso direttamente dalla confezione sterile convalidata (per i prodotti monouso irradiati con raggi gamma) o dalla confezione sigillata che lascia pochi pelucchi (per i prodotti monouso non sterili). Nessun residuo di carica batterica dalle stanze precedenti, nessun accumulo di particelle da precedenti passaggi di pulizia, nessun residuo di detersivo per il bucato.
- Nessun trasferimento di contaminazione da una stanza all'altra: Le strutture che utilizzano mop riutilizzabili in genere mantengono un inventario separato per i diversi gradi ISO (i mop ISO 5 non vengono mai utilizzati nelle aree ISO 8). Anche con protocolli di segregazione perfetti, gli errori di etichettatura e le carenze di inventario creano rischi di assegnazioni incrociate. I sistemi monouso eliminano questa modalità di guasto: i panni non possono essere riutilizzati, quindi la contaminazione trasversale è impossibile.
- Nessuna contaminazione legata al bucato: I panni riutilizzabili passano attraverso le lavanderie dove abbondano le opportunità di contaminazione incrociata: lavaggio a carico misto, cicli di risciacquo inadeguati, attrezzature condivise per la movimentazione sia dei camici per camere bianche che della biancheria generale delle strutture. I panni usa e getta bypassano l'intero sistema di lavanderia, eliminando un percorso di contaminazione in più fasi.
Semplificazione della convalida attraverso l'eliminazione delle variabili di rielaborazione
I protocolli di convalida della pulizia per gli strumenti riutilizzabili devono tenere conto degli scenari di ritrattamento peggiori: numero massimo di cicli (fine vita qualificata), massimo rischio di carica batterica, minima efficacia di riciclaggio. Ciascuna variabile introduce incertezza nelle prestazioni del controllo della contaminazione.
I panni usa e getta non presentano variabili di ritrattamento. I test di qualificazione dei materiali (generazione di particelle, compatibilità chimica, livello di carica batterica) convalidano il panno nel suo stato come ricevuto, mai utilizzato, lo stesso stato presentato durante l'uso effettivo. Ciò elimina la complessità della convalida:
- Nessuno studio sulla degradazione del conteggio dei cicli: La convalida del mop riutilizzabile richiede test in più punti del ciclo di vita (nuovo, 25 cicli, 50 cicli, 100 cicli) per dimostrare che la generazione di particelle rimane entro i criteri di accettazione. La validazione monouso testa solo la singola condizione “nuova”.
- Nessuna convalida dell'efficacia del riciclaggio: Le strutture che utilizzano mop riutilizzabili devono convalidare i cicli di bucato, le concentrazioni di detersivo, la riduzione della carica batterica e la rimozione dei residui. I sistemi monouso non hanno fasi di lavaggio da convalidare.
- Nessuna modalità di errore di rielaborazione: Contaminazione incrociata durante il bucato, errori di sterilizzazione in autoclave, errori di tracciamento nell'assegnazione dei panni alle aree sbagliate: nessuna di queste modalità di errore esiste quando gli strumenti sono monouso.
Particella prevedibile & Prestazioni microbiche
I programmi di monitoraggio ambientale dipendono da fonti di contaminazione stabili e prevedibili per rilevare eventi di contaminazione reali. Quando gli strumenti di pulizia perdono conteggi variabili di particelle e carica batterica durante il loro ciclo di vita, introducono rumore nei dati EM che oscura i reali segnali di contaminazione.
Generazione di particelle stabili (<100 Particelle/m²)
I panni monouso in poliestere con bordi sigillati generano un numero di particelle costante in tutte le unità:
- Prestazione tipica: <50-100 particelle ≥ 0,5 µm per metro quadrato pulite per materiali monouso convalidati di grado farmaceutico
- Nessun degrado nel tempo: Ogni mop usa e getta offre prestazioni identiche: nessuna separazione dei bordi, nessuna rottura delle fibre, nessuna variazione dimensionale indotta dall'autoclave. La generazione di particelle sul mocio n. 1 corrisponde al mocio n. 1.000.
- Trend dei mercati emergenti semplificato: Quando il conteggio delle particelle rimane stabile durante le operazioni di pulizia, i team di monitoraggio ambientale possono attribuire con sicurezza i picchi di particelle a eventi di contaminazione (guasti degli indumenti del personale, contaminazione del trasferimento di materiale, malfunzionamenti delle apparecchiature) piuttosto che al degrado degli strumenti di pulizia.
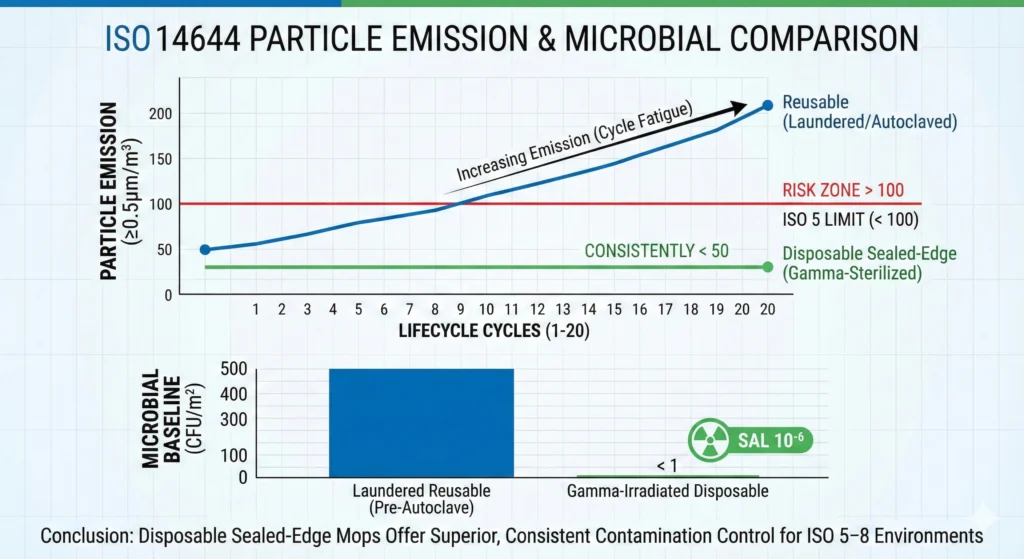
I panni riutilizzabili, al contrario, aumentano la generazione di particelle nel corso della loro vita utile. Un panno riutilizzabile in poliestere con bordi sigillati potrebbe iniziare con 50 particelle/m² quando è nuovo, aumentare a 100 particelle/m² entro il ciclo 50 e raggiungere 200-300 particelle/m² verso la fine della vita qualificata (ciclo 100-150). Questo aumento della generazione di particelle da 4× a 6× crea un contributo di contaminazione dipendente dal tempo che complica l’interpretazione dei dati EM.
Valore di riferimento prevedibile della carica batterica (prodotti monouso gamma-sterili)
I panni monouso irradiati con raggi gamma offrono un livello di garanzia di sterilità (SAL) 10⁻⁶, una probabilità su un milione di unità non sterili. Questo metodo di sterilizzazione terminale consente di eliminare completamente la carica batterica:
- Zero microrganismi vitali: L'irradiazione gamma (tipicamente una dose di 25–50 kGy) inattiva tutte le cellule vegetative batteriche, le spore, i funghi e i virus attraverso il danno al DNA. A differenza dell’autoclavaggio (che può lasciare vitali le spore resistenti al calore se i parametri del ciclo variano) o della disinfezione chimica (che lascia residui disinfettanti e potrebbe non raggiungere l’efficacia sporicida), l’irradiazione gamma fornisce sterilità assoluta senza residui.
- Certificati di sterilità convalidati: I prodotti monouso sterilizzati a raggi gamma vengono forniti con certificati di sterilizzazione che documentano la dose erogata, i risultati dell'indicatore biologico (BI) e il raggiungimento del SAL. Le strutture possono accettare questi certificati previa qualificazione del fornitore (secondo l'Allegato 1 Sezione 4.34), evitando test di sterilità interni.
- Performance prevedibile dei mercati emergenti: Le aree di grado A/B che utilizzano spazzoloni monouso gamma-sterili stabiliscono linee di base stabili per la carica batterica. Qualsiasi rilevamento microbico durante il monitoraggio ambientale post-pulizia rappresenta una contaminazione da altre fonti (personale, trattamento dell'aria, trasferimento di materiale), non il residuo di carica batterica degli strumenti di pulizia.
I panni monouso non sterili (per applicazioni ISO Classe 7–8) continuano a fornire prestazioni prevedibili in termini di carica batterica attraverso controlli di produzione convalidati. I materiali monouso di grado farmaceutico mantengono la carica batterica <10 CFU/tampone per panno grazie alla produzione in camera bianca, ai materiali di imballaggio sterilizzati e allo stoccaggio convalidato. Questo valore di riferimento rimane costante in tutte le unità, a differenza dei panni riutilizzabili in cui la variabilità dell’efficacia del bucato introduce fluttuazioni della carica batterica.
Convalida inferiore & Aumento della documentazione
Il carico di lavoro di convalida è un costo nascosto nei programmi di strumenti di pulizia riutilizzabili. Le strutture devono sviluppare protocolli, eseguire studi, analizzare dati e conservare la documentazione per molteplici elementi di convalida, ciascuno dei quali richiede tempo da parte di specialisti del controllo qualità, risorse del laboratorio di microbiologia e ore di qualificazione delle apparecchiature.

Cosa richiedono i mop riutilizzabili:
- Qualificazione delle attrezzature per lavanderia (IQ/OQ/PQ): Qualificazione dell'installazione che verifica le specifiche dell'apparecchiatura, qualifica operativa che convalida i parametri del ciclo (distribuzione della temperatura, concentrazione del detergente, efficacia del risciacquo), qualifica delle prestazioni che dimostra la riduzione della carica batterica in condizioni di carico peggiore
- Qualificazione dei materiali degli strumenti di pulizia: Test di generazione delle particelle a nuova condizione e a fine vita (conteggio massimo di cicli); convalida della compatibilità chimica tra tutti i disinfettanti per strutture; test di stabilità dimensionale mediante cicli in autoclave
- Convalida del sistema di tracciamento del conteggio dei cicli: Convalida dei sistemi di tracciamento con codici a barre o RFID, test degli avvisi di pensionamento, dimostrazione della tracciabilità durante tutto il ciclo di vita del mop
- Verifica della sterilità o della carica batterica (se autoclavato): Studi sul posizionamento degli indicatori biologici, validazione del ciclo di sterilizzazione, dimostrazione del livello di garanzia della sterilità (SAL).
- Rivalidazione periodica: riconvalida annuale o biennale dopo modifiche dell'attrezzatura, modifiche dei parametri del ciclo o aggiornamenti della formula del detersivo
Cosa richiedono i mop usa e getta:
- Solo qualificazione materiale: test sulla generazione di particelle (generalmente condotti dal fornitore con rapporto di convalida fornito), verifica della compatibilità chimica con disinfettanti specifici della struttura
- Ricevere l'ispezione: Ispezione visiva dell'integrità della confezione, verifica dei certificati di sterilità (per unità gamma-sterili), documentazione del numero di lotto
- Qualificazione del venditore: Verifica dei controlli delle camere bianche del produttore, convalida del processo di sterilizzazione, sistema di gestione della qualità, generalmente soddisfatti attraverso la revisione del pacchetto di convalida fornito dal fornitore
Riduzione delle ore di convalida
Una struttura farmaceutica rappresentativa che passa dai panni riutilizzabili a quelli usa e getta in un'area di supporto asettico ISO Classe 7 di 500 m² potrebbe ridurre il carico di lavoro di convalida:
- Convalida iniziale: 120–160 ore (convalida della biancheria riutilizzabile + configurazione del sistema di tracciabilità) rispetto a 20–30 ore (qualificazione del materiale monouso + procedura di ricezione)
- Rinnovo annuale: 40–60 ore (riconvalida della lavanderia + verifica del sistema di conteggio dei cicli) rispetto a 0 ore (non è richiesta alcuna riconvalida; il ricevimento dell'ispezione fa parte delle operazioni di routine)
- Supporto investigativo: 8–12 ore per escursione EM (revisione forense della cronologia di assegnazione dei panni, registri della lavanderia, conteggi dei cicli) rispetto a 2–3 ore (semplice verifica del numero di lotto monouso e revisione del certificato)
Per i team QA che operano con un numero limitato di dipendenti, cosa comune nelle startup biotecnologiche, nelle organizzazioni di produzione a contratto e nelle strutture che eseguono operazioni snelle, questa riduzione dell'onere di convalida si traduce direttamente in larghezza di banda per attività di valore più elevato: convalida della pulizia per nuovi prodotti, miglioramenti del programma di monitoraggio ambientale, indagini sulle deviazioni.
Lavoro & Efficienza temporale
L'efficienza operativa aumenta grazie a centinaia o migliaia di cicli di lavaggio all'anno. Piccoli miglioramenti procedurali, come l'eliminazione della registrazione del conteggio dei cicli, l'eliminazione delle fasi di ispezione del panno e la semplificazione dello smaltimento, si accumulano in risparmi misurabili sulla manodopera.
Nessun monitoraggio del conteggio dei cicli
I programmi di pulizia riutilizzabili richiedono agli operatori di registrare ogni utilizzo della pulizia:
- Preuso: scansione del codice a barre o del tag RFID del panno, verifica del conteggio dei cicli entro l'intervallo qualificato, documentazione dell'assegnazione del panno a una stanza/area specifica
- Post-utilizzo: Riporta il panno nell'area dedicata alla biancheria sporca, esegue la scansione dell'inventario, attiva il ciclo di lavanderia/autoclave se si raggiunge la soglia di conteggio predeterminata
- Audit periodici: Il QA conduce controlli mensili o trimestrali dei registri di conteggio dei cicli per verificare la conformità, identificare le lacune nel monitoraggio e imporre il ritiro dei mop troppo invecchiati
Disposable systems eliminate this entire workflow. Operators remove mop from packaging, use once, discard into classified waste—no scanning, no logging, no cycle-count verification. For facilities mopping 200–500 m² daily across multiple shifts, this procedural simplification saves 10–15 minutes per shift (aggregate across all mopping operations)—roughly 60–75 hours per year of operator time recovered.
No Laundering, Drying, Re-Distribution
Reusable mop logistics create multi-step workflows:
- Soiled laundry collection: Operators transfer used mops from cleanroom areas to laundry staging, maintaining segregation by ISO grade
- Riciclaggio: Laundry staff load mops into washers (segregated by grade), execute validated wash cycles, transfer to dryers
- Sterilizzazione (se richiesta): Caricare i panni asciutti nell'autoclave, eseguire il ciclo validato, verificare gli indicatori biologici
- Ridistribuzione: Trasportare i panni puliti/sterili nelle aree delle camere bianche, rifornire l'inventario nei luoghi di stoccaggio designati
Ogni passaggio consuma ore di lavoro e introduce ritardi. Il tempo di consegna tipico di un mop riutilizzabile è di 24-48 ore (più lungo se è necessaria la sterilizzazione in autoclave o se la lavanderia viene esternalizzata). Le strutture devono mantenere un inventario compreso tra 2× e 3× per garantire un'adeguata disponibilità di scopa durante i cicli di lavanderia.
I panni usa e getta riducono questa catena logistica in due fasi:
- Ricezione e archiviazione: Accettare spedizioni di mop usa e getta, condurre ispezioni alla ricezione, conservare in aree di inventario designate per camere bianche
- Disposizione: Rimuovere i panni usati dalla camera bianca in contenitori per rifiuti classificati secondo i protocolli di gestione dei rifiuti della struttura
Nessun riciclaggio, nessuna sterilizzazione, nessuna ridistribuzione. I requisiti di inventario scendono a 1× (i panni necessari per le operazioni correnti) più le scorte di sicurezza (in genere una confezione aggiuntiva per SKU). Per le piccole strutture con infrastrutture di lavanderia limitate o startup biotecnologiche senza capacità di lavanderia interna, i sistemi usa e getta eliminano la necessità di costruire o esternalizzare completamente le operazioni di lavanderia.
Particolarmente prezioso per le strutture GMP di piccole dimensioni
Le startup biotecnologiche, i produttori specializzati e le organizzazioni di produzione a contratto che gestiscono team operativi snelli beneficiano in modo sproporzionato dai sistemi di pulizia usa e getta:
- Nessun personale di lavanderia dedicato: Servizi con <20 addetti alle camere bianche spesso non possono giustificare gli operatori di lavanderia a tempo pieno. I sistemi usa e getta eliminano questo requisito di personale.
- Formazione semplificata: La formazione degli operatori per i sistemi usa e getta richiede una SOP ("Rimuovere dalla confezione, utilizzare una volta, eliminare") rispetto a più SOP per i sistemi riutilizzabili (ispezione del panno, registrazione del conteggio dei cicli, separazione della biancheria, caricamento dell'autoclave).
- Carico di lavoro CAPA ridotto: Le indagini sugli errori di tracciamento del conteggio dei cicli, sugli errori di separazione della lavanderia e sulle deviazioni della sterilizzazione in autoclave scompaiono quando gli strumenti sono monouso.
Modifiche all’Allegato 1 delle GMP dell’UE (2023–2025)
L’allegato 1 GMP dell’UE rivisto (in vigore dal 25 agosto 2023) riposiziona sostanzialmente il controllo della contaminazione come quadro strategico a livello di sito. Le versioni precedenti trattavano la pulizia e la disinfezione come requisiti procedurali; la revisione del 2023 eleva la strategia di controllo della contaminazione (CCS) a un sistema obbligatorio e documentato che definisce i punti critici di controllo e valuta l'efficacia delle misure di progettazione, procedurali, tecniche e di monitoraggio in tutta la struttura.
Strumenti di pulizia come elementi CCS
L'Allegato 1, Sezione 2.5, elenca esplicitamente "pulizia e disinfezione" tra gli elementi fondamentali del CCS che richiedono la convalida, e la Sezione 4.33-4.35 impone che i disinfettanti e i detergenti utilizzati nelle aree di Grado A e Grado B "devono essere sterili prima dell'uso". Il regolamento richiede inoltre processi di disinfezione convalidati, con la pulizia che precede la disinfezione per garantire un'efficace rimozione dei residui. Questi requisiti si applicano non solo alle sostanze chimiche ma anche agli strumenti che le applicano: le testine, le salviette e gli strumenti per la pulizia devono mantenere la sterilità e le prestazioni convalidate all'interno delle zone asettiche.
La frase “strumenti sterili per manipolazioni” (Sezione 8.16) estende questa logica: se gli operatori manipolano materiali in aree di lavorazione asettiche utilizzando strumenti sterili, gli strumenti di pulizia che entrano in contatto con quelle stesse superfici classificate devono soddisfare standard di controllo di sterilità e contaminazione equivalenti.
Vettori di contaminazione nascosti e disinfezione del trasferimento
L'Allegato 1, Sezione 4.11–4.12, identifica il trasferimento di materiali e attrezzature come "una delle maggiori potenziali fonti di contaminazione", che richiede una disinfezione di trasferimento convalidata e programmi monitorati. Gli strumenti di pulizia riutilizzabili vengono trasferiti costantemente tra stanze e aree: uno spazzolone utilizzato un giorno in un corridoio di supporto di grado C può essere lavato e utilizzato in uno sfondo di grado B il turno successivo. Senza un ritrattamento convalidato (lavaggio, disinfezione, verifica della sterilità), il mocio diventa un “vettore di contaminazione nascosto” che trasporta carica batterica, residui di particelle e residui chimici tra ambienti classificati.
L’enfasi del regolamento sulle superfici lisce e impermeabili che riducono al minimo la perdita e tollerano la disinfezione ripetuta (Sezione 4.5–4.7) si applica anche alla scelta degli strumenti di pulizia. I panni usa e getta eliminano il percorso di degradazione: nessun tracciamento del conteggio dei cicli, nessuna separazione dei bordi indotta dall'autoclave, nessuna rottura delle fibre indotta dal bucato. Ogni panno inizia da zero, rispettando le specifiche di generazione di particelle e sterilità senza usura cumulativa.
Rischio di lavanderia e ricondizionamento
L'Allegato 1 Sezione 7.17 segnala esplicitamente il riciclaggio degli indumenti come un rischio di contaminazione e contaminazione incrociata, richiedendo processi di lavanderia qualificati, separazione dalle aree di produzione e limiti di ciclo definiti. Gli stessi percorsi di contaminazione interessano i sistemi di spazzolone riutilizzabili. Le strutture di lavanderia che trattano sia camici che strumenti per la pulizia introducono opportunità di contaminazione incrociata: cicli di risciacquo con detersivo inadeguati lasciano residui di tensioattivi, la riduzione incompleta della carica batterica trasferisce carichi microbici e la lavorazione a carico misto contamina gli strumenti di grado A/B con particelle provenienti da articoli di qualità inferiore.
Le strutture senza operazioni di lavanderia interne convalidate devono esternalizzare, aggiungendo complessità alla catena di fornitura, ritardi nei tempi di consegna e rischio di contaminazione da parte di terzi. I panni usa e getta bypassano l'intero sistema della lavanderia, riducendo la logistica del ritrattamento in un unico passaggio: rimuovere il panno dalla confezione sterile, utilizzarlo una volta, smaltirlo nei rifiuti classificati.
Causa principale: strumenti riutilizzabili che provocano guasti EM
I programmi di monitoraggio ambientale presso gli stabilimenti farmaceutici rilevano regolarmente picchi di contaminazione durante e immediatamente dopo la pulizia dei pavimenti. Quando le squadre investigative riconducono queste escursioni alla causa principale, gli strumenti di pulizia riutilizzabili emergono come recidivi.
Carico biologico residuo e carry-over incrociato
Reusable mop heads contact floor surfaces laden with microbial contamination, disinfectant residues, and particulate matter. Even after laundering, bioburden and chemical residues persist:
- Incomplete bioburden reduction: Standard laundry cycles (hot water wash, detergent, tumble dry) reduce microbial load but do not achieve sterility. Bacterial vegetative cells survive in fabric interstices, and spore-formers (Bacillus, Geobacillus) tolerate laundry conditions entirely. A reusable mop entering a Grade A/B area without terminal sterilization (autoclaving or gamma irradiation) introduces viable microorganisms directly onto surfaces subsequently contacted by sterile product or product-contact equipment.
- Cross-carryover between areas: I panni utilizzati nelle aree di supporto di Classe ISO 8 accumulano carica batterica e conteggi di particelle più elevati rispetto ai panni dedicati ai nuclei asettici di Classe ISO 5. Se la separazione della biancheria è inadeguata (lavaggio a carico misto, attrezzatura per lavanderia condivisa, tracciabilità impropria) i panni di grado A/B vengono contaminati con residui di grado C/D. Un singolo evento di assegnazione incrociata (utilizzo di uno spazzolone ISO 8 in una stanza ISO 5 a causa di errori di etichettatura o carenza di inventario) può seminare la carica batterica in ambienti asettici e innescare cicli di indagine di più settimane.
- Residui di detersivo per bucato: I tensioattivi e gli ammorbidenti rimasti sulle fibre del mocio creano superfici appiccicose che attraggono e trattengono le particelle. Questi residui interferiscono anche con l’efficacia del disinfettante: i tensioattivi cationici presenti negli ammorbidenti neutralizzano i disinfettanti anionici (composti di ammonio quaternario), riducendo i tassi di uccisione microbica durante il lavaggio e lasciando organismi vitali sulle superfici trattate.
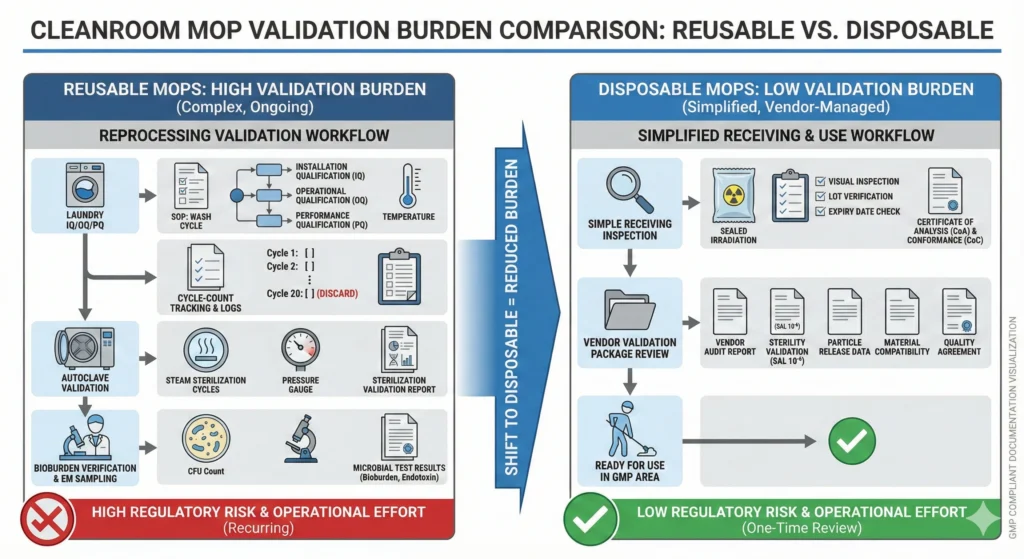
Rielaborazione della documentazione e oneri di convalida
I programmi di strumenti di pulizia riutilizzabili impongono requisiti estesi di convalida e documentazione:
- Convalida del riciclaggio (IQ/OQ/PQ): Le strutture devono qualificare le attrezzature per lavanderia (lavatrici, asciugatrici, autoclavi), convalidare i parametri del ciclo (tempo, temperatura, concentrazione di detersivo) e dimostrare la riduzione della carica batterica entro limiti accettabili. Ciò richiede studi di sfida microbiologica (inoculazione delle teste dei mop con organismi bersaglio, trattamento attraverso l'intero ciclo di lavanderia, recupero e quantificazione dei sopravvissuti) e riconvalida periodica quando i parametri del ciclo cambiano o l'attrezzatura viene sottoposta a manutenzione.
- Monitoraggio del conteggio dei cicli e criteri di pensionamento: Each reusable mop head has a qualified service life (e.g., 50 autoclave cycles for polyester sealed-edge mops). Facilities must implement tracking systems—barcoding, manual logs, or RFID tags—to record usage history and enforce retirement at end of qualified life. Tracking failures introduce risk: over-aged mops shed particles and bioburden, but premature retirement wastes inventory and increases cost.
- Sterility or bioburden verification: Se i panni riutilizzabili vengono sterilizzati in autoclave per l'uso in aree di grado A/B, il ciclo di sterilizzazione deve essere convalidato secondo ISO 11137 o equivalente, con indicatori di sterilità posizionati in configurazioni di carico rappresentative. Le strutture prive di capacità di autoclave devono inviare i panni a fornitori esterni di sterilizzazione (aggiungendo tempi e costi di consegna) o accettare un rischio elevato di carica batterica.
- Documentazione dell'indagine: Quando si verificano escursioni EM, le squadre investigative devono esaminare la cronologia degli strumenti di pulizia: quale scopa è stata utilizzata, quando è stata lavata l'ultima volta, qual è stato il conteggio dei cicli, in quali aree è stata utilizzata in precedenza. Questa analisi forense richiede registrazioni di tracciabilità complete. Le lacune nella documentazione (registri della lavanderia mancanti, assegnazioni di spazzoloni non registrati) prolungano le indagini e complicano la chiusura del CAPA.
I panni usa e getta eliminano la maggior parte di questa infrastruttura di convalida. Gli strumenti monouso richiedono solo l'ispezione (verifica dei certificati di sterilità, ispezione visiva dell'integrità dell'imballaggio) e la qualificazione del materiale (test sulla generazione di particelle, convalida della compatibilità chimica), nessuna convalida del bucato, nessun monitoraggio del conteggio dei cicli, nessuna documentazione di ricondizionamento.
Crescente adozione di Fill-Finish & Biotecnologia
I dati di mercato mostrano un’adozione accelerata di materiali di consumo per la pulizia monouso convalidati nella produzione farmaceutica e biotecnologica, spinta dalle pressioni sulla conformità normativa e dagli aspetti economici operativi.
Linee di riempimento-finitura e lavorazione asettica
Le operazioni di riempimento e finitura (riempimento sterile, caricamento della liofilizzazione, tappatura delle fiale) operano con un flusso d'aria unidirezionale di Classe ISO 5 (Grado A) con sfondi di Classe ISO 7 (Grado B). I limiti delle particelle sono estremi: 3.520 particelle ≥ 0,5 µm per metro cubo per ISO 5, contro 352.000 particelle/m³ per ISO 7. Qualsiasi strumento di pulizia che generi un contributo misurabile di particelle rischia di deviare dalla classificazione.
Mop monouso per camere bianche convalidati per la generazione di particelle (<50 particelle/m² per bordo sigillato in poliestere; <10 particelle/m² per design premium a filamento continuo) offrono prestazioni prevedibili e costanti in tutti gli usi. I panni riutilizzabili si degradano nel tempo (la sigillatura dei bordi si separa, le fibre si rompono, la generazione di particelle aumenta) creando un contributo di contaminazione variabile che complica l'analisi delle tendenze del monitoraggio ambientale.
Produzione di biotecnologie e terapie cellulari
La produzione di sostanze farmaceutiche biologiche e terapie cellulari opera in lotti più piccoli e paradigmi di potenza più elevata rispetto ai tradizionali prodotti farmaceutici a piccole molecole. Gli eventi di contaminazione che potrebbero essere tollerabili in un lotto di compresse da 10.000 dosi diventano catastrofici in un prodotto CAR-T personalizzato da 50 dosi. Le strutture biotecnologiche adottano strumenti di pulizia usa e getta come parte di più ampie strategie di sistema monouso:
- Bioreattori monouso e percorsi dei fluidi: I sistemi basati su sacche monouso eliminano la convalida della pulizia dei recipienti e riducono il rischio di contaminazione incrociata tra i lotti. L’estensione di questa logica alla pulizia dei pavimenti mantiene la filosofia di controllo della contaminazione monouso a livello di sistema.
- Produzione conto terzi e strutture multiprodotto: I CDMO che gestiscono più prodotti cliente nelle stesse camere bianche devono affrontare rigorosi requisiti di convalida della pulizia e di prevenzione della contaminazione tra prodotti. I panni usa e getta semplificano il cambio: ogni nuova campagna inizia con nuovi strumenti di pulizia, eliminando il rischio di residui dai prodotti precedenti senza studi approfonditi di convalida della pulizia.
- Modelli operativi snelli: Le startup biotecnologiche e i piccoli produttori spesso non dispongono di infrastrutture di lavanderia interne. L’esternalizzazione del riciclaggio dei panni riutilizzabili aumenta i costi, i tempi di consegna e il rischio di contaminazione da parte di terzi. I panni usa e getta riducono la catena di fornitura alla consegna diretta al fornitore di materiali di consumo pre-sterilizzati e pronti all'uso.
L’analisi del settore conferma che l’Allegato 1 delle GMP dell’UE “obbliga i produttori farmaceutici a passare ad indumenti e salviette monouso di grado sterile”, guidando l’adozione di materiali di consumo monouso convalidati in tutte le categorie di pulizia. Le salviette sterili presaturate conquistano già una quota di mercato sostanziale nelle suite asettiche; I sistemi di spazzoloni usa e getta seguono la stessa curva di adozione poiché le strutture estendono le strategie di controllo della contaminazione monouso alla pulizia dei pavimenti.

Confronto dei costi: usa e getta vs riutilizzabili
Il costo unitario più elevato dei panni usa e getta per camere bianche – in genere 8-25 dollari per panno contro i 15-40 dollari di un panno riutilizzabile con una durata di 50-100 cicli – crea uno shock iniziale per i team di approvvigionamento. Ma l’analisi del costo totale di proprietà (TCO) rivela che i sistemi usa e getta spesso offrono costi di vita inferiori in applicazioni farmaceutiche ad alto rischio una volta inclusi i costi di ritrattamento, convalida e mancata contaminazione.
Elementi di costo diretto
Sistemi di pulizia usa e getta
- Costo unitario del panno: 8–15 USD per tampone per materiali monouso in poliestere non sterili con bordi sigillati (applicazioni ISO 7–8); $ 15-25 per tampone per materiali monouso sterili irradiati con raggi gamma (aree ISO 5-6 grado A/B)
- Sistemi di movimentazione: $ 50–150 per manico riutilizzabile in alluminio o acciaio inossidabile (compatibile con i sistemi di fissaggio degli assorbenti monouso); le maniglie hanno una durata di servizio pluriennale
- Stoccaggio e inventario: Minimo: i prodotti monouso vengono spediti in imballaggi compatti, non richiedono la separazione in base al numero di cicli o allo stato di sterilizzazione
- Smaltimento dei rifiuti: gestione classificata dei rifiuti farmaceutici (tipicamente 0,50-2 dollari per libbra); i panni usa e getta pesano 50-150 grammi, aggiungendo $ 0,05-0,30 per panno in termini di costi di smaltimento dei rifiuti
Sistemi di pulizia riutilizzabili
- Costo iniziale della testa del mocio: $ 15-40 per testina riutilizzabile in poliestere o microfibra con bordi sigillati
- Costo del lavaggio per ciclo: $ 2–5 per mocio (lavorazione della lavanderia commerciale, detersivi, servizi pubblici); il riciclaggio interno riduce questo importo a 1-3 dollari per ciclo, ma richiede investimenti in beni strumentali
- Autoclave sterilization (if required): $3–8 per cycle including utilities, biological indicators, documentation, and equipment amortization
- Cycle-count tracking system: $5,000–20,000 for barcode or RFID infrastructure (scanners, software, label printing) plus $0.50–1 per mop per cycle in tracking labor
- Inventory carrying cost: 2× to 3× mop inventory required to maintain adequate availability during laundry turnaround cycles
Costi indiretti nascosti (spesso trascurati)
The decisive TCO factors often lie in hidden operational costs that procurement teams underestimate when evaluating unit price alone.
Validation and Documentation Burden
- Initial laundry validation: 120–160 hours of QA specialist time ($60–100/hour) for IQ/OQ/PQ = $7,200–16,000
- Mop material qualification through lifecycle: 40–60 ore per test sulle particelle in condizioni nuove e a fine vita, convalida della compatibilità chimica = $ 2.400–6.000
- Convalida della sterilizzazione in autoclave (se applicabile): 60–80 ore per lo sviluppo del ciclo, studi sugli indicatori biologici, dimostrazione SAL = $ 3.600–8.000
- Rinnovo annuale: 40–60 ore all'anno = $ 2.400–6.000 all'anno
- Convalida monouso per confronto: 20–30 ore per la qualificazione del materiale (spesso fornita dal fornitore) + sviluppo della procedura di ricezione = costo una tantum di $ 1.200–3.000, senza riconvalida annuale
Costi delle indagini sul monitoraggio ambientale
Le escursioni EM riconducibili alla contaminazione degli strumenti di pulizia attivano cicli di indagine di più settimane:
- Lavoro investigativo: 20–40 ore per escursione (tempo del microbiologo, documentazione QA, elaborazione delle deviazioni) = $ 1.200–4.000 per evento
- Analisi delle cause profonde: Revisione forense della cronologia delle assegnazioni dei panni, dei registri della lavanderia, dei conteggi dei cicli, dei registri di ritrattamento
- Implementazione del CAPA: Revisioni delle procedure, riqualificazione, monitoraggio migliorato: spesso 40-80 ore aggiuntive = $ 2.400-8.000
- Rischio impatto batch: Negli scenari peggiori, i guasti EM durante il riempimento asettico determinano la sospensione dei lotti, l'espansione dei test di sterilità o il rifiuto dei lotti: costi che vanno da $ 50.000 (mantenimento di piccoli lotti e indagini) a oltre $ 500.000 (rifiuto dei lotti e notifica normativa)
Le strutture che subiscono anche un solo guasto EM all’anno con un onere investigativo moderato (5.000-10.000 dollari in manodopera e documentazione) compensano costi significativi per i panni usa e getta.
Guadagni in efficienza del lavoro
- Eliminazione del tracciamento del conteggio dei cicli: 60–75 ore all'anno risparmiate in tutte le operazioni di pulizia = valore annuo di $ 1.800–3.000 (a tariffa operatore mista di $ 30/ora)
- Eliminazione della logistica della lavanderia: 100–200 ore all'anno risparmiate (raccolta dello sporco, caricamento del ciclo di lavaggio, sterilizzazione, ridistribuzione) = valore annuo di $ 3.000–6.000
- Semplificazione della formazione: La ridotta complessità della SOP consente di risparmiare 10-20 ore all'anno nell'erogazione della formazione e nella verifica delle competenze = valore annuo di $ 600-2.000
Confronto del costo totale di proprietà (esempio di area di supporto asettico ISO Classe 7)
Consideriamo un'area di supporto alla produzione farmaceutica ISO Classe 7 di 500 m² lavata quotidianamente (365 giorni all'anno), che richiede 2 panni per ciclo di pulizia:
Scenario A: Mop riutilizzabili
- Costi diretti: 730 usi del mop/anno ÷ durata di vita di 75 cicli del mop = 10 mop acquistati ogni anno a $ 30 ciascuno = $ 300
- Riciclaggio: 730 cicli × $ 3 per ciclo (elaborazione interna) = $ 2.190
- Sterilizzazione in autoclave: 730 cicli × $ 5 per ciclo = $ 3.650
- Monitoraggio del ciclo del travaglio: 730 cicli × $ 0,75 per ciclo = $ 548
- Convalida iniziale (ammortizzato in 5 anni): $ 12.000 ÷ 5 = $ 2.400 all'anno
- Rinnovo annuale: $ 4.000
- Onere delle indagini sui mercati emergenti (1 evento ogni 2 anni, prudenzialmente): $ 7.500 ÷ 2 = $ 3.750 media annua
- TCO annuo totale: $ 16.838
Scenario B: Mop monouso (Gamma-sterile)
- Costi diretti: 730 panni per scopa × $ 18 per tampone = $ 13.140
- Gestire l'ammortamento: $ 100 ÷ 5 anni di vita = $ 20 all'anno
- Smaltimento dei rifiuti: 730 tamponi × 0,15 USD per tampone = 110 USD
- Qualificazione iniziale del materiale (ammortizzato in 5 anni): $ 2.000 ÷ 5 = $ 400 all'anno
- Nessun costo di riconvalida, lavanderia, sterilizzazione o tracciabilità
- Riduzione degli oneri investigativi dei mercati emergenti: escursioni legate agli strumenti di pulizia prossime allo zero = $ 0
- Guadagni in efficienza del lavoro: $ 4.000 all'anno (tracciabilità, logistica della lavanderia, formazione)
- TCO annuo totale: $ 13.670 – $ 4.000 (aumento di efficienza) = Costo netto di $ 9.670
Risultato: Consegna dei panni usa e getta TCO inferiore del 42%. (9.670 dollari contro 16.838 dollari) nonostante il costo unitario più elevato, determinato dall’eliminazione dell’infrastruttura di ritrattamento, dalla riduzione degli oneri di convalida e dall’elusione delle indagini EM.
Soglie decisionali: quando i prodotti usa e getta giustificano i costi
I panni monouso per camere bianche offrono un TCO favorevole in queste condizioni:
- Classificazioni ISO ad alto rischio (ISO 5–7): i limiti delle particelle e i margini di controllo della contaminazione sono stretti; Il rischio di fallimento dei mercati emergenti e l’onere delle indagini sono elevati
- Strutture con storia di guasti EM: Anche una sola escursione di contaminazione all’anno riconducibile agli strumenti di pulizia (costo di indagine di $ 5.000-10.000) compensa sostanziali spese per i panni usa e getta
- Operazioni di piccola e media scala (<1.000 m² di camera bianca): i sistemi riutilizzabili richiedono una convalida fissa e costi infrastrutturali che non diminuiscono; i costi usa e getta scalano linearmente con l’utilizzo
- Strutture senza lavanderia interna: la lavanderia in outsourcing aggiunge 5-10 dollari per mocio per ciclo più ritardi di consegna; i prodotti usa e getta eliminano la dipendenza da terze parti
- Team operativi snelli: Le startup biotecnologiche e i CMO con un numero limitato di dipendenti QA/lavanderia traggono vantaggio dalla riduzione degli oneri di convalida e dall’aumento dell’efficienza del lavoro
- Strutture multiprodotto (CDMO): La convalida della pulizia per il cambio prodotto è semplificata quando gli strumenti di pulizia sono monouso; nessun rischio di riporto tra le campagne
I panni riutilizzabili rimangono convenienti quando:
- Produzione su larga scala (>2.000 m² di pulizia giornaliera): l'elevato volume di consumo di panni (oltre 1.000 panni all'anno) fa aumentare i costi dei prodotti usa e getta al di sopra del TCO dei panni riutilizzabili, anche con l'onere del ritrattamento incluso
- Aree di supporto ISO 8 con basso rischio EM: I minori requisiti di controllo della contaminazione riducono il carico delle indagini; l'economia riutilizzabile migliora negli ambienti di livello inferiore
- Esiste già un’infrastruttura di lavanderia interna convalidata: Strutture con attività di lavanderia mature e qualificate e un solido monitoraggio del conteggio dei cicli riducono la differenza nei costi di ritrattamento
- Priorità alla sostenibilità: Alcune organizzazioni danno priorità alla riduzione degli sprechi rispetto all'ottimizzazione del TCO; i sistemi riutilizzabili convalidati con controllo documentato della contaminazione forniscono profili di rischio accettabili
I migliori casi d'uso dei panni usa e getta negli ambienti GMP
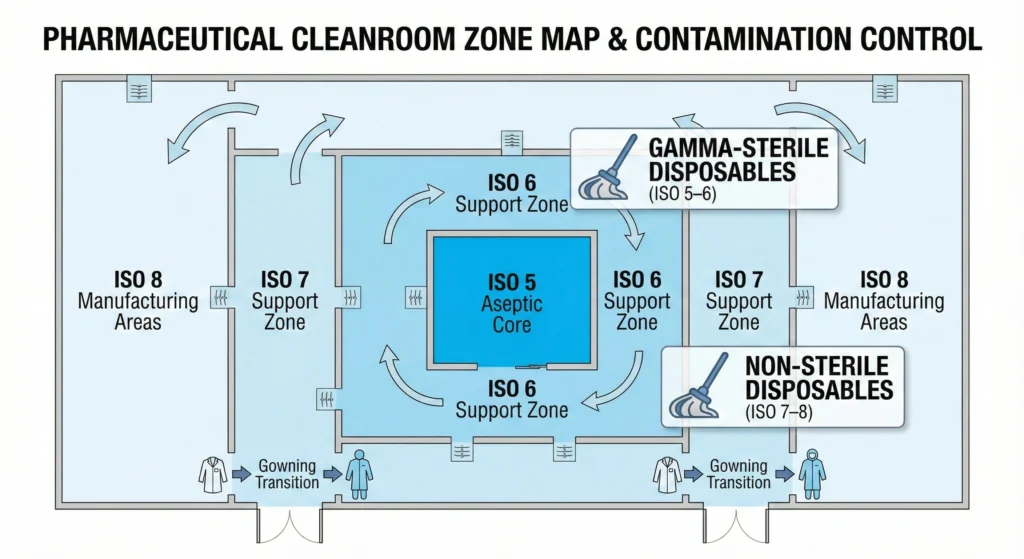
I panni monouso per camere bianche offrono il massimo valore quando i requisiti di controllo della contaminazione, i vincoli operativi e i profili di rischio si allineano con i loro punti di forza. Questa sezione illustra tipi specifici di strutture, classificazioni ISO e scenari operativi in cui i sistemi monouso giustificano il loro costo attraverso un controllo superiore della contaminazione e un costo totale di proprietà ridotto.
Nuclei asettici ISO Classe 5 (Grado A).
Requisiti: Flusso d'aria unidirezionale, limite di particelle 3.520 particelle ≥0,5 µm/m³, sterilizzazione terminale o lavorazione asettica, tolleranza zero alla carica batterica
Perché i prodotti usa e getta Excel:
- I materiali monouso gamma-sterili forniscono SAL 10⁻⁶: I panni riutilizzabili richiedono il trattamento in autoclave per la sterilità, introducendo oneri di convalida del ciclo di sterilizzazione, requisiti di indicatori biologici e potenziali errori di sterilizzazione. I prodotti monouso irradiati con raggi gamma arrivano pre-sterilizzati con certificati, eliminando i requisiti di sterilizzazione interna.
- Zero rischio di contaminazione incrociata: Le aree di Grado A richiedono un controllo assoluto della contaminazione. Un'assegnazione incrociata di un singolo panno (utilizzando un panno ISO 7 di Grado A a causa della carenza di scorte) introduce carica batterica nelle zone asettiche. I prodotti usa e getta eliminano questa modalità di fallimento.
- Prestazioni prevedibili delle particelle: I limiti delle particelle sono estremi (3.520/m³). I panni riutilizzabili perdono sempre più particelle man mano che invecchiano; I panni monouso in poliestere con bordi sigillati mantengono <50 particelle/m² per tutti gli usi.
- Convalida semplificata: Le strutture evitano la validazione dell'autoclavaggio, la validazione del monitoraggio del conteggio dei cicli e gli studi sulla riduzione della carica batterica nelle lavanderie, aspetti fondamentali per le piccole strutture biotecnologiche con risorse limitate di QA.
Applicazioni tipiche:
- Linee di riempimento asettico (riempimento flaconi, riempimento siringhe, caricamento liofilizzazione)
- Sale di preparazione sterili (farmacie ospedaliere, strutture di preparazione)
- Produzione di terapie cellulari (elaborazione CAR-T, produzione di medicinali personalizzati)
- Cabine di sicurezza biologica e pulizia isolatori
Raccomandazione MIDPOSI: Panni monouso in poliestere con bordi sigillati irradiati gamma con convalida <Prestazione 50 particelle/m² e certificati di sterilità SAL 10⁻⁶
Aree di supporto asettico di classe ISO 6–7 (grado B/C).
Requisiti: Limiti di particelle da 35.200/m³ (ISO 6) a 352.000/m³ (ISO 7), carica batterica controllata, controllo della contaminazione da trasferimento di materiale
Perché i prodotti usa e getta Excel:
- Prevenzione della contaminazione da trasferimento di materiale: Le aree di grado B/C fungono da camere di equilibrio e zone di trasferimento di materiale tra le aree di grado inferiore e i nuclei di grado A. I panni riutilizzabili utilizzati in più zone diventano vettori di contaminazione. I prodotti monouso garantiscono che ogni ciclo di pulizia inizi con uno strumento convalidato e privo di contaminazioni.
- Riduzione degli oneri investigativi dei mercati emergenti: Le aree di grado B/C sono sottoposte ad un elevato controllo EM: qualsiasi escursione di particelle o carica batterica attiva l'indagine. I panni usa e getta con prestazioni prevedibili semplificano l'andamento degli EM e riducono le escursioni legate agli strumenti di pulizia.
- Efficienza della manodopera in strutture multi-room: Le suite asettiche spesso includono 5-10 stanze di supporto di Grado B/C interconnesse. I sistemi usa e getta eliminano il tracciamento del panno nelle stanze, la verifica del conteggio dei cicli ad ogni utilizzo e la logistica di separazione della lavanderia.
Fattori decisionali:
- Le strutture con frequenti escursioni EM ne traggono i maggiori benefici: anche una sola indagine all’anno (costo di $ 5.000-10.000) compensa sostanziali spese per i panni usa e getta
- Operazioni di piccola e media scala (<500 m² di superficie totale di Grado B/C) vedere TCO usa e getta favorevole
- Le strutture senza lavanderia interna convalidata eliminano la dipendenza dalla lavanderia di terzi
Applicazioni tipiche:
- Riempi gli sfondi del traguardo e i corridoi di supporto
- Camere di equilibrio per il trasferimento del materiale tra le aree di Grado C e Grado A
- Spogliatoi che servono nuclei asettici
- Aree di pulizia e allestimento attrezzature
Raccomandazione MIDPOSI: Materiali monouso irradiati con raggi gamma per aree critiche di grado B adiacenti alle zone di grado A; Materiali monouso in poliestere con bordi sigillati non sterili accettabili per aree di supporto di Grado C con convalida <Prestazione di 100 particelle/m²
Produzione di classe ISO 8 (grado D). & Aree di supporto: uso selettivo
Requisiti: Limite di particelle 3.520.000/m³, monitoraggio di routine della carica batterica, minor rischio di controllo della contaminazione
Quando l'usa e getta ha senso:
- Strutture multiprodotto (CMO/CDMO): La pulizia del cambio prodotto richiede l'eliminazione convalidata della contaminazione incrociata del prodotto. I panni usa e getta semplificano il cambio: nessun rischio di residui di prodotto precedenti dai panni riutilizzabili.
- Produzione di farmaci ad alta potenza: I composti altamente potenti (citotossici, ormoni) richiedono una rigorosa convalida della pulizia per prevenire l'esposizione dell'operatore e la contaminazione incrociata. Gli strumenti di pulizia usa e getta eliminano il rischio di trascinamento senza studi approfonditi di convalida della pulizia.
- Strutture con infrastrutture di lavanderia limitate: Le startup biotecnologiche e i piccoli produttori senza lavanderia interna evitano di costruire o esternalizzare le attività di lavanderia utilizzando prodotti usa e getta di tutti i gradi ISO.
- Risposta agli eventi di contaminazione: Dopo le escursioni EM o gli eventi di contaminazione, le strutture possono passare temporaneamente ai prodotti monouso nelle aree interessate durante l'indagine sulle cause profonde e l'implementazione del CAPA, garantendo che gli strumenti di pulizia non contribuiscano alla contaminazione continua.
Quando i materiali riutilizzabili rimangono ottimali:
- Aree di supporto ISO 8 su larga scala (>1.000 m² di magazzino, sistemi di corridoi, produzione generale) dove il rischio di contaminazione è basso e il volume di consumo di panni è elevato
- Strutture con lavanderia interna convalidata e robusti sistemi di monitoraggio del conteggio dei cicli già operativi
- Organizzazioni che danno priorità alla riduzione dei rifiuti e alla sostenibilità laddove il profilo di rischio di contaminazione è accettabile
Applicazioni tipiche dei prodotti monouso:
- Suite di produzione API multiprodotto (scenari di cambio CMO)
- Aree di produzione di sostanze farmaceutiche ad alta potenza
- Aree di sosta per la pulizia delle attrezzature che servono zone di livello superiore
- Zone di isolamento per le indagini sulla contaminazione
Raccomandazione MIDPOSI: Materiali monouso in poliestere con bordi sigillati non sterili con validazione <prestazione di 100 particelle/m²; economicamente vantaggioso per l’implementazione selettiva pur mantenendo sistemi riutilizzabili per le aree di supporto a basso rischio
Startup biotecnologiche & Impianti GMP su piccola scala
Profilo operativo: <20 addetti alle camere bianche, risorse limitate per QA/convalida, nessuna infrastruttura di lavanderia interna, modello operativo snello, produzione agile (piccoli lotti, frequenti cambi di prodotto)
Perché i prodotti usa e getta sono strategici:
- Nessun investimento nelle infrastrutture della lavanderia: Elimina investimenti di capitale di 50.000-200.000 dollari in lavatrici, asciugatrici, autoclavi e costruzioni di lavanderie industriali
- Riduzione degli oneri di convalida: I team QA concentrati su molteplici attività di convalida (qualificazione delle apparecchiature, convalida della pulizia, convalida dei processi) traggono vantaggio dall'eliminazione della convalida della lavanderia, della convalida del monitoraggio del conteggio dei cicli e della convalida della sterilizzazione
- Formazione semplificata degli operatori: L'unica SOP ("Rimuovere dalla confezione, utilizzare una volta, eliminare") riduce i tempi di formazione e l'onere di verifica delle competenze
- Costi scalabili: I costi usa e getta si adattano linearmente al volume di produzione: ideale per le startup nella fase iniziale della produzione con frequenza di batch variabile
- Avvio rapido della struttura: Le nuove suite GMP diventano operative più rapidamente senza la qualificazione delle apparecchiature per lavanderia, lo sviluppo di procedure di ricondizionamento e la convalida del sistema di tracciamento
Profili tipici:
- Startup biotecnologiche nella produzione clinica di Fase I/II (1-5 lotti al mese)
- Produttori di terapia cellulare e genica (medicina personalizzata, lotti di piccole dimensioni)
- Centri medici accademici con suite di compounding GMP
- Produttori di API specializzati con <Superficie totale della camera bianca di 500 m²
Raccomandazione MIDPOSI: Programma completo di mop monouso per tutti i gradi ISO: materiali monouso gamma-sterili per nuclei asettici di grado A/B, materiali monouso non sterili per aree di supporto di grado C/D, abbinato a un pacchetto di convalida (dati sulle particelle, certificati di sterilità, rapporti sulla compatibilità dei materiali) per accelerare la preparazione normativa
Organizzazioni di produzione a contratto (CMO/CDMO)
Sfida operativa: Prodotti client multipli fabbricati in suite di camere bianche condivise; rigorosi requisiti di convalida della pulizia e di prevenzione della contaminazione incrociata dei prodotti; frequenti cambi di prodotto
Perché i prodotti monouso semplificano le operazioni:
- Nessun rischio di carryover del prodotto: Gli studi di validazione della pulizia devono dimostrarlo <Residuo di 10 ppm del prodotto precedente. Gli strumenti di pulizia usa e getta eliminano completamente un percorso di trascinamento: nessun rischio di residui di prodotto precedenti incorporati nelle fibre del mocio riutilizzabili.
- Documentazione di cambio semplificata: Le liste di controllo per il cambio prodotto includono la verifica degli strumenti di pulizia. I prodotti usa e getta eliminano il tracciamento forense ("Questo mocio è stato utilizzato nella campagna precedente? Qual è stato il numero dei cicli? Quando è stato lavato l'ultima volta?"): gli operatori utilizzano semplicemente prodotti usa e getta nuovi.
- Fiducia del cliente: I clienti farmaceutici che effettuano audit e due diligence valutano i controlli della contaminazione incrociata. I sistemi di pulizia monouso dimostrano una prevenzione proattiva della contaminazione e una ridotta complessità di convalida.
- Capacità flessibile: I CMO sperimentano programmi di produzione variabili. I costi usa e getta si adattano all'attività produttiva effettiva, evitando i costi operativi fissi della lavanderia durante i periodi di basso utilizzo.
Applicazioni tipiche:
- CMO sterili di riempimento e finitura che gestiscono più prodotti cliente
- CMO che producono API con suite multiprodotto
- CDMO a piccole molecole e sostanze farmaceutiche biologiche
- Produzione specializzata (API ad alta potenza, sostanze controllate)
Raccomandazione MIDPOSI: Programmi di panni usa e getta per nuclei asettici (aree ISO 5–7) in cui avviene il cambio di prodotto; implementazione riutilizzabile selettiva in aree di supporto ISO 8 dedicate al servizio di campagne per singoli prodotti

Linea di mop monouso per camere bianche MIDPOSI (Selettore prodotti)
MIDPOSI produce panni monouso per camere bianche di grado farmaceutico progettati specificatamente per applicazioni di controllo della contaminazione GMP. Tutti i prodotti vengono forniti con pacchetti completi di documentazione di convalida: dati sui test di generazione delle particelle, certificati di sterilità (per prodotti irradiati con raggi gamma), rapporti sulla compatibilità dei materiali e certificati di analisi, consentendo una rapida qualificazione normativa e l'avvio della struttura.
MDCR-GS100 Mop gamma sterile monouso (ISO 5–6 grado A/B)
Specifiche chiave:
- Materiale: 100% poliestere con bordo sigillato, maglia a filamento continuo, prodotto in camera bianca per uso farmaceutico
- Sterilizzazione: Irradiazione gamma (dose da 25–50 kGy) che raggiunge il livello di garanzia di sterilità (SAL) 10⁻⁶
- Generazione di particelle: <50 particelle ≥0,5 µm per metro quadrato pulite (convalidato secondo i metodi di test ISO 14644-1)
- Riferimento alla carica batterica: Zero microrganismi vitali (sterilizzazione terminale)
- Dimensioni: Testa del mop da 40 cm × 15 cm (compatibile con i sistemi con manico in alluminio/acciaio inossidabile MIDPOSI)
- Confezione: Confezione sterile in doppia busta con sigilli peel-open; sacca interna idonea al trasferimento in zone di Grado A/B
- Documentazione: Certificato di sterilizzazione (dose erogata, risultati indicatori biologici, validazione SAL), dati test particelle, rapporto compatibilità materiali (IPA, perossido di idrogeno, disinfettanti all'ammonio quaternario)
Applicazioni convalidate:
- Linee di riempimento asettico (riempimento flaconi, assemblaggio siringhe, liofilizzazione)
- Sale di preparazione sterile (farmacie ospedaliere, strutture 503B)
- Camere bianche per la produzione di terapie cellulari e geniche
- Cabine di sicurezza biologica, isolatori e sistemi di barriere ad accesso limitato (RABS)
Costo: $ 18-22 per panno (prezzo in base al volume disponibile per le strutture che utilizzano >500 assorbenti all'anno)
Supporto per la convalida: Pacchetto di validazione completo incluso con l'ordine iniziale: rapporto sul test sulla generazione di particelle secondo ISO 14644-1, certificato di sterilizzazione con mappatura della dose e risultati degli indicatori biologici, studio sugli estraibili dimostrativi <10 ppm di sostanze rilasciabili dopo il contatto con il disinfettante
MDCR-NS200 Mop monouso non sterile (ISO 7–8 grado C/D)
Specifiche chiave:
- Materiale: Miscela di microfibra di poliestere con bordi sigillati, prodotta in camera bianca con prestazioni comprovate di basso rilascio di pelucchi
- Riferimento alla carica batterica: <10 CFU per panno (controlli di produzione convalidati, test di routine sulla carica batterica)
- Generazione di particelle: <100 particelle ≥0,5 µm per metro quadrato pulite
- Compatibilità chimica: Convalidato per isopropanolo, perossido di idrogeno (3–6%), composti di ammonio quaternario, biossido di cloro e disinfettanti fenolici
- Dimensioni: Testa del mop da 40 cm × 15 cm (sistema di fissaggio universale compatibile con la maggior parte dei manici dei mop per camere bianche)
- Confezione: Confezione sigillata a basso rilascio di pelucchi con chiusura richiudibile (50 panni per sacchetto)
- Documentazione: dati sui test sulle particelle, rapporto di riferimento sulla carica batterica, rapporto di convalida della compatibilità dei materiali
Applicazioni convalidate:
- Aree di supporto asettiche di classe ISO 7 (sfondi di riempimento, stanze per vestizione)
- Aree di produzione farmaceutica ISO Classe 8 (produzione di API, produzione di compresse, suite di confezionamento)
- Impianti multiprodotto che richiedono la pulizia del cambio (operazioni CMO/CDMO)
- Zone di isolamento per le indagini sulla contaminazione
Costo: $ 8–12 per panno (sconti per quantità per >1.000 assorbenti all'anno)
Supporto per la convalida: Pacchetto di convalida del fornitore fornito: rapporto sul test di generazione delle particelle, documentazione di riferimento della carica batterica (CFU media e valori del 95° percentile), matrice di compatibilità chimica che mostra la compatibilità con i principali disinfettanti farmaceutici
Mop monouso pre-saturato MDCR-PSAT (pronto all'uso con alcool isopropilico o disinfettante)
Specifiche chiave:
- Materiale: Poliestere con bordi sigillati con potere assorbente e ritenzione disinfettante convalidati
- Opzioni di saturazione: 70% isopropanolo/30% acqua (grado USP); perossido di idrogeno al 3%; o disinfettante specificato dalla struttura (saturazione personalizzata disponibile)
- Sterilizzazione: Irradiazione gamma post-saturazione con raggiungimento di SAL 10⁻⁶ (disinfettante sterile e panno sterile)
- Generazione di particelle: <50 particelle/m² (paragonabile a MDCR-GS100)
- Scadenza: Durata di conservazione di 24 mesi (l'imballaggio in alluminio sigillato impedisce l'evaporazione)
- Confezione: Buste singole in alluminio (pronte per il trasferimento in aree di Grado A/B) o confezioni da 25 panni per l'uso di Grado C/D
Applicazioni convalidate:
- Pulizia spot e risposta alle fuoriuscite in aree asettiche
- Lavaggio di piccole aree (<locali di 50 m²) dove la preparazione del disinfettante risulta scomoda
- Pulizia di emergenza durante la produzione (nessuna interruzione per la miscelazione del disinfettante)
- Strutture che cercano di eliminare la preparazione dei disinfettanti e l'esposizione al contatto con gli operatori
Costo: $ 22-28 per panno (costo maggiore dovuto alla saturazione del disinfettante e alla sterilizzazione post-saturazione)
Supporto per la convalida: Pacchetto di validazione completo che comprende test di efficacia disinfettante (riduzione del registro contro gli organismi bersaglio), dati sulla generazione di particelle dopo la saturazione, certificato di sterilità e test di compatibilità che dimostrano l'assenza di residui superficiali o degradazione del materiale
Sistemi di maniglie MIDPOSI (riutilizzabili, compatibili con tutti i panni usa e getta)
MDH-AL100 Maniglia in alluminio (Applicazioni ISO 7–8):
- Costruzione leggera in alluminio anodizzato (150 grammi)
- Autoclavabile a 134°C (validato per 100 cicli di sterilizzazione)
- Clip di fissaggio universale compatibile con i panni per mop MDCR-GS100, MDCR-NS200 e MDCR-PSAT
- Costo: $ 85 per maniglia
Maniglia in acciaio inossidabile MDH-SS200 (Applicazioni ISO 5–6 Grado A/B):
- Costruzione in acciaio inossidabile 316L (resistente alla corrosione, generazione zero di particelle)
- Autoclavabile a 134°C (convalidato per oltre 200 cicli di sterilizzazione)
- Finitura superficiale liscia senza fessure (facile disinfezione, nessun deposito di carica batterica)
- Sistema di fissaggio universale
- Costo: $ 140 per maniglia
Come ordinare e richiedere pacchetti di convalida
MIDPOSI fornisce supporto tecnico e normativo completo per le strutture che valutano o implementano programmi di pulizia usa e getta per camere bianche:
Kit di campioni per test pilota:
- Richiedi 10-20 campioni di panni per scopa (MDCR-GS100 o MDCR-NS200) per una valutazione interna
- Include: pacchetto di validazione (dati sulle particelle, report di sterilità/carico batterico, matrice di compatibilità), istruzioni per l'utente e scheda delle specifiche tecniche
- I test pilota consentono alle strutture di convalidare le prestazioni nelle condizioni operative effettive prima dell’approvvigionamento completo
Contenuto del pacchetto di convalida (Fornito con tutti gli ordini):
- Rapporto sul test di generazione delle particelle: Test conformi alla norma ISO 14644-1 che documentano particelle ≥ 0,5 µm per m² pulito
- Certificato di sterilità (per prodotti irradiati con raggi gamma): dose erogata, risultati indicatori biologici, convalida SAL 10⁻⁶
- Rapporto di riferimento sulla carica batterica (per prodotti non sterili): unità formanti colonie (CFU) per panno, testate secondo USP <61> E <62>
- Convalida della compatibilità dei materiali: Matrice di compatibilità che non mostra degradazione o aumento della generazione di particelle dopo il contatto con disinfettanti specifici della struttura (IPA, perossido di idrogeno, composti di ammonio quaternario, biossido di cloro)
- Studio degli estraibili e dei leachables: Dimostrazione <10 ppm di sostanze rilasciabili dopo il contatto con il disinfettante (analisi GC-MS secondo ICH Q3C)
- Certificato di conformità: Verifica della conformità specifica del lotto alle specifiche relative a particelle, carica batterica e sterilità
Technical Consultation:
- MIDPOSI contamination control specialists provide facility-specific recommendations based on ISO classification, EM failure history, operational scale, and TCO optimization
- Support for regulatory submissions: Validation summaries formatted for FDA, EMA, or PMDA regulatory filings
- Custom validation studies available (contact resistance testing, specific disinfectant compatibility, extended particle generation studies)
Contact for Pricing, Samples, and Technical Support:
- E-mail: [email protected]
- Response time: Pricing quotes and validation packages delivered within 12 hours of request
- Lead time: Stock items ship within 48 hours; custom configurations (specific dimensions, custom disinfectant saturation) ship within 2 weeks









