A QA-focused technical guide for GMP material entry into Grade A/B zones—covering peel-and-pass logic, packaging integrity risks, and audit-defensible controls aligned with EU GMP Annex 1 expectations.

La sterilità viene raggiunta durante la produzione, ma la maggior parte degli eventi di contaminazione si verificano durante trasferimento asettico—when materials move from uncontrolled areas to Grade C, then B, and finally A. Without redundant barriers, the mop packaging surface can act as a carrier for particulates and bioburden.
In pratica, confezione di mop sterile functions as a controlled boundary: the outer bag is stripped at the interface, while the inner bag remains sterile until the point of use. This is the operational basis of stacca e passa.
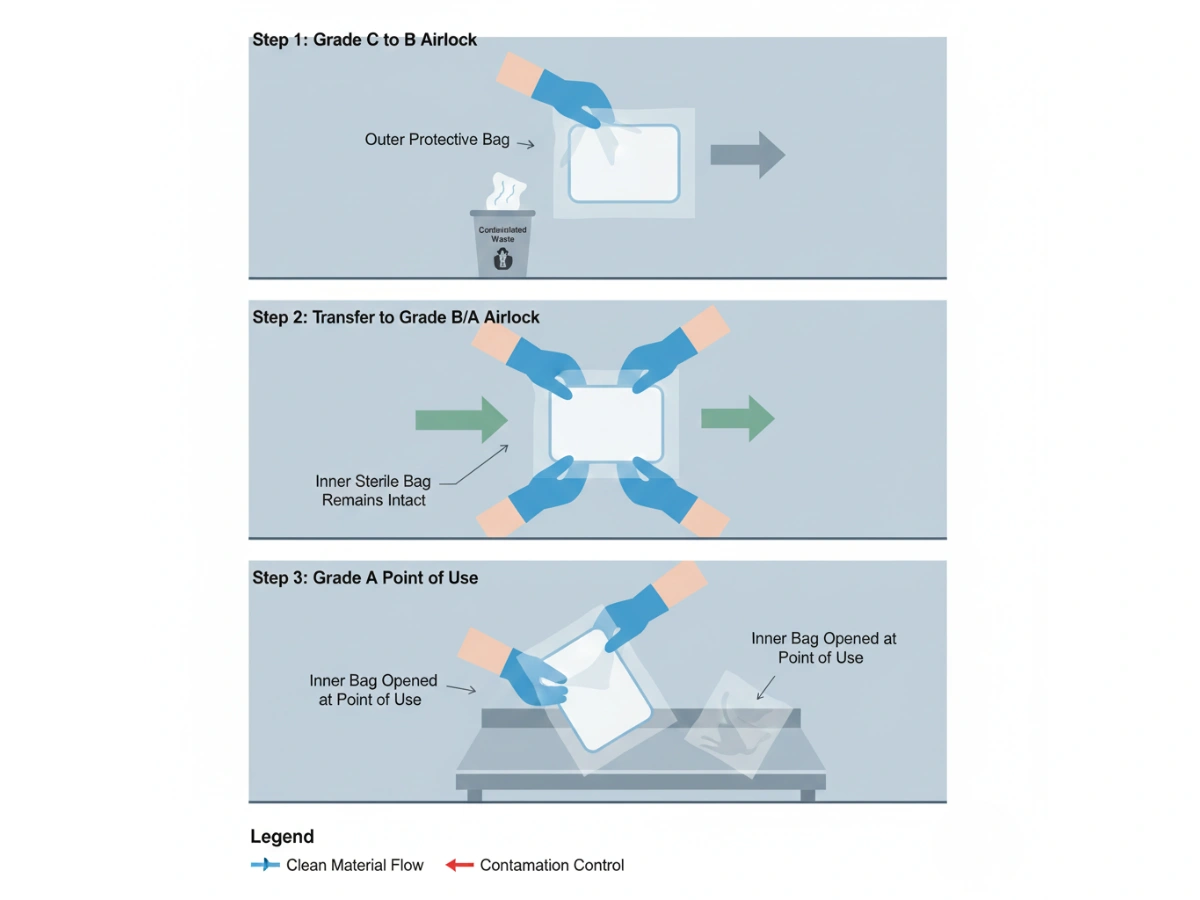

For Grade A/B operations, the core question is not “sterile at release,” but “sterile at point-of-use.” Double-bagging reduces transfer variability by removing the external surface at the boundary rather than relying on wipe-down success every time.

Use this simplified logic to align packaging selection with grade, transfer method, and validation burden. For Grade A/B, an engineered barrier is typically preferred over manual disinfection dependence.
| Fattore decisionale | Confezione in sacchetto singolo | Confezione in doppio sacchetto |
|---|---|---|
| Controllo del trasferimento | Richiede pulizia e disciplina convalidate | Il peel-and-pass rimuove la contaminazione al confine |
| Modalità di fallimento | Singolo punto di guasto | Strati barriera sterili ridondanti |
| Difendibilità dell'audit | Fortemente dipendente dalle prove di esecuzione della SOP | Narrazione di controllo ingegnerizzato più forte per CCS |
| Carico di lavoro operativo | Superiore (disinfezione, monitoraggio, deviazioni) | Inferiore (processo strip-at-bound standardizzato) |



Ti contatteremo entro 1 giorno lavorativo, fai attenzione all'email con il suffisso “*@midposi.com”.