In the highly regulated European pharmaceutical market, EU GMP Annex 1 compliant cleanroom SOP documentation is more than a regulatory box—it is the foundation of patient safety and market longevity. For compliance officers across the EU—from the production hubs in Germany to the biotech clusters in Spain—mastering this documentation architecture is essential for January 2026 readiness.
Quem deve usar este guia
- Diretores de Conformidade: Responsible for adherence to EMA requirements.
- Regulatory Affairs Professionals: Managing EU market authorization dossiers.
- Gerentes de Qualidade: Overseeing documentation in EU-based sterile facilities.
- Validation Specialists: Ensuring cleanroom validation meets Annex 1 standards.
EU GMP Annex 1 Overview and Implementation Timeline
Revision Published
Significant updates to contamination control and environmental monitoring.
Transition Period Begins
Preparation phase for full compliance.
Full Implementation
Mandatory compliance across all EU member states.
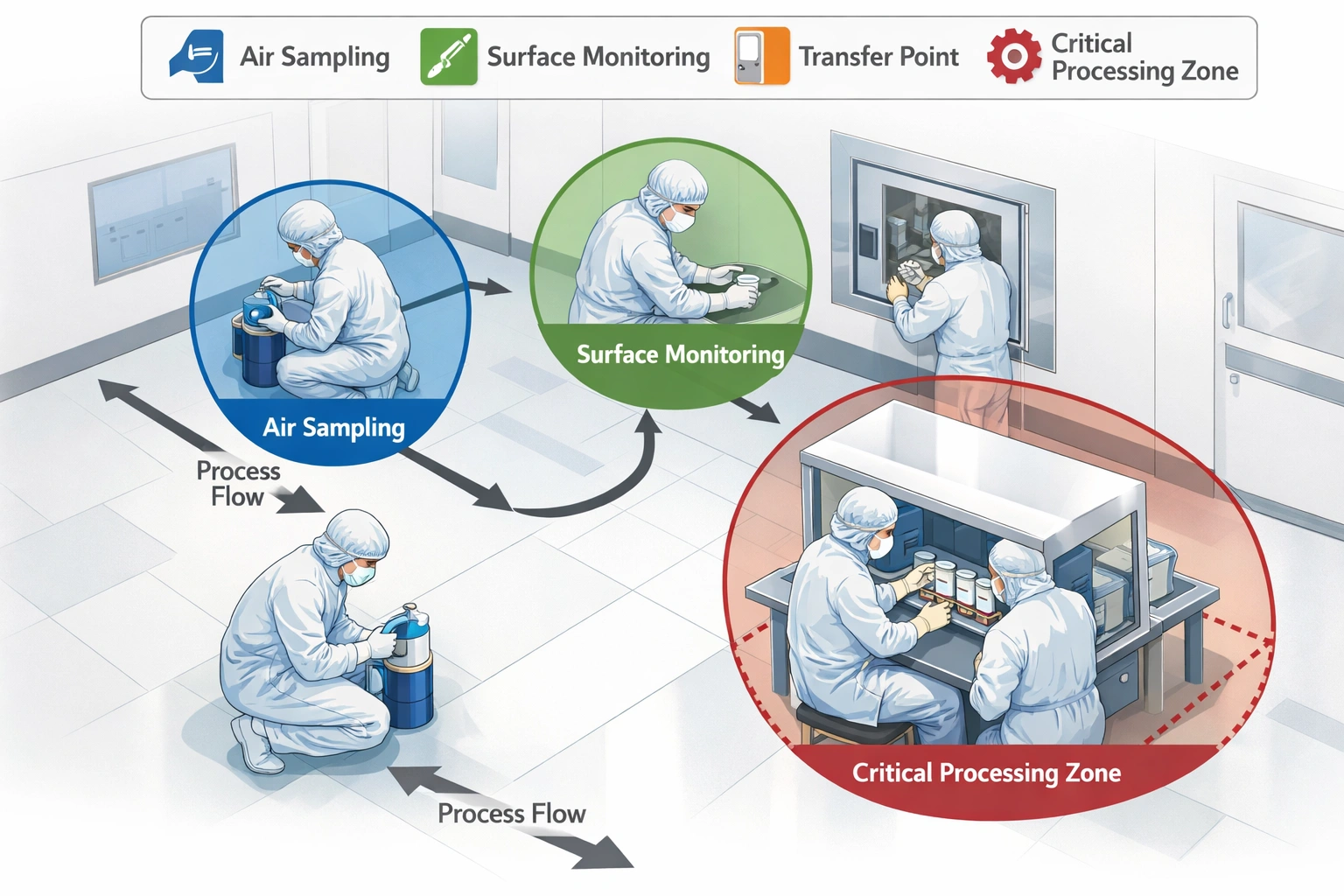
Major Updates Impacting Documentation
| Área | Revised Requirement | Impacto da Documentação |
|---|---|---|
| EM | Risk-based with trending | New risk assessment protocols. |
| Contamination | Persistent strategy | Enhanced cleaning SOPs. |
| Lifecycle | Full lifecycle management | Procedimentos de controle abrangentes. |
Requisitos de arquitetura de documentação da UE
European regulators expect a hierarchical approach that ensures "clear and unambiguous" instructions throughout the facility.
Nível 1 & 2: Qualidade & POPs do sistema
Inclui Manuais de Qualidade e Sistemas de Controle de Documentos.

Nível 3 & 4: Processar POPs e Registros
POPs cruciais para salas limpas, incluindo registros de vestimentas, desinfecção e produção em lote.
Requisito específico da UE: A documentação deve estar no idioma oficial da UE do estado membro onde a instalação está localizada. Considere versões bilíngues para maior clareza internacional.
Necessidades de documentação específica para salas limpas
Deficiências comuns de inspeção: O controlo inadequado das alterações e a falta de documentação de avaliação dos riscos são as principais razões para as conclusões das inspeções da UE.

| SOP Type | Specific EU Requirement | Evidência necessária |
|---|---|---|
| Desinfecção | Efficacy testing | Protocolos de validação & reports. |
| Change Control | Risco & Impact evaluation | Formal assessments. |
| Validação | Lifecycle verification | VMP & Summary reports. |
EU Member State Specific Considerations
While Annex 1 is harmonized, local nuances exist in major manufacturing hubs:
- Germany: Additional safety documentation and German translations.
- France: Extended traceability requirements for batch records.
- Italy & Spain: Specific training notification and competency assessment records.

Achieve EU GMP Annex 1 Compliance
Nossa equipe de especialistas fornece sistemas de documentação centralizados e flexíveis projetados para o sucesso regulatório da UE em 2026. Garanta que sua cadeia de suprimentos e POPs atendam aos mais altos padrões.






Expert Commentary: EU GMP Annex 1 Implementation
"The revised Annex 1 represents the most significant update to sterile manufacturing in decades. Regulators expect a demonstrable quality culture embedded in every document—comprehensive risk assessments are the new standard."