No cenário farmacêutico em evolução, os responsáveis pela garantia da qualidade e pela conformidade enfrentam uma pressão crescente para desenvolver soluções sofisticadas. POPs de monitoramento ambiental de salas limpas com base em riscos que se alinham com as expectativas regulatórias para 2026. Este guia facilita a mudança para a utilização de dados e avaliação de riscos para concentrar os recursos onde eles proporcionam maior proteção. Integrando alto desempenho esfregões para salas limpas em sua estratégia de controle de contaminação é um requisito básico para esses ambientes dinâmicos.
Quem deve usar este guia
- Especialistas em garantia de qualidade: Responsável pelo design e supervisão do programa EM.
- Diretores de Conformidade: Garantir a adesão aos requisitos da FDA e EMA.
- Engenheiros de validação: Liderando atividades de qualificação de salas limpas.
- Gerentes de instalações: Implementação de programas de monitoramento.
- Assuntos Regulatórios: Navegando pelos requisitos de conformidade em evolução.
Cenário Regulatório de 2026

Evolução da abordagem baseada em risco da FDA
- Gerenciamento aprimorado de risco de qualidade (QRM): Integração dos princípios ICH Q9.
- Integridade de dados 2.0: Coleta de dados em tempo real e análise automatizada de tendências.
- Monitoramento Contínuo: Exigência de monitoramento ambiental contínuo (CEM) em áreas críticas.
- Análise Preditiva: Implementação de sistemas de alerta precoce para riscos de contaminação.
- Integração da cadeia de suprimentos: Avaliação de riscos, incluindo impactos na cadeia de abastecimento.
Anexo 1 das BPF da EMA (implementação em 2026)
- Classificação Baseada em Risco: Classificação dinâmica de salas limpas com base na avaliação de riscos.
- Estratégia de Controle de Contaminação (CCS): Abordagem abrangente para contaminação persistente.
- EM Program: Frequências e locais de monitoramento ajustados ao risco.
- Protocolos de Investigação: Abordagem estruturada para monitoramento de excursões.
- Melhoria Contínua: Requisito obrigatório para otimização contínua do programa.
Cronograma de transição para conformidade
| Linha do tempo | Requisitos | Ações necessárias |
|---|---|---|
| 1º trimestre de 2024 - 2º trimestre de 2024 | Análise de lacunas e desenvolvimento de avaliação de risco | Desenvolver um quadro de avaliação de riscos; identificar áreas de alto risco. |
| 3º trimestre de 2024 - 1º trimestre de 2025 | Revisão e validação do POP | Atualizar procedimentos EM; validar novas abordagens de monitoramento. |
| 2º trimestre de 2025 - 4º trimestre de 2025 | Implementação e teste piloto | Implementar programa baseado em risco; coletar dados de desempenho. |
| 1º trimestre de 2026 – Conformidade total | Implementação e otimização completas | Finalizar programa; estabelecer melhoria contínua. |
Desenvolvimento da Estrutura de Avaliação de Risco
Passo 1: Definir Critérios de Avaliação de Risco
Estabeleça critérios abrangentes para avaliar áreas e processos de salas limpas.
- Risco do produto: Estéril vs. não estéril, área terapêutica, via de administração.
- Risco de Processo: Complexidade do processo, nível de automação, frequência de intervenção.
- Risco de instalação: Mudanças de ar, diferenciais de pressão, tráfego de pessoal.
- Dados históricos: Resultados de monitoramento anteriores e tendências de contaminação.
- Impacto da mudança: Mudanças recentes, histórico de desvios, eficácia do CAPA.
Passo 2: Desenvolver Matriz de Risco
Categorize áreas e processos com base em critérios predefinidos em uma matriz estruturada.
Monitoramento Contínuo
Investigação Imediata
Maior frequência
Investigação oportuna
Frequência Padrão
Investigação de Rotina
Dica de implementação: Use um sistema de pontuação (1-5) para cada fator de risco. As áreas com pontuação ≥15 requerem estratégias de monitorização de alto risco.
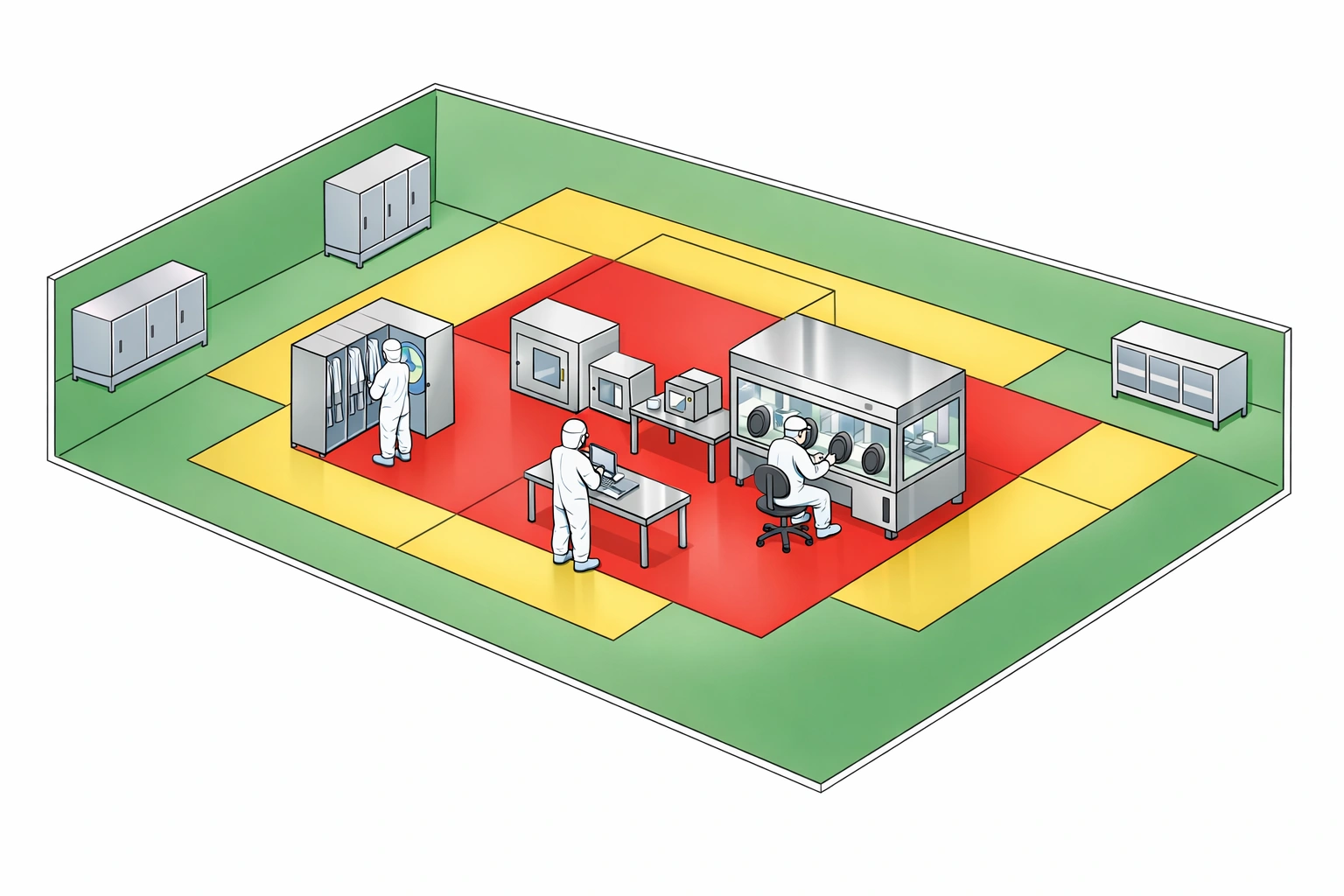
Passo 3: Estabelecer Locais de Monitoramento
A colocação estratégica de equipamentos é vital. Usar validação de sala limpa insights para identificar locais críticos.
- Processamento Asséptico: Zonas críticas, interfaces de preenchimento e acabamento.
- Pontos de transferência: Câmaras de ar, vestiários.
- Áreas de alto tráfego: Corredores principais, pontos de intervenção.
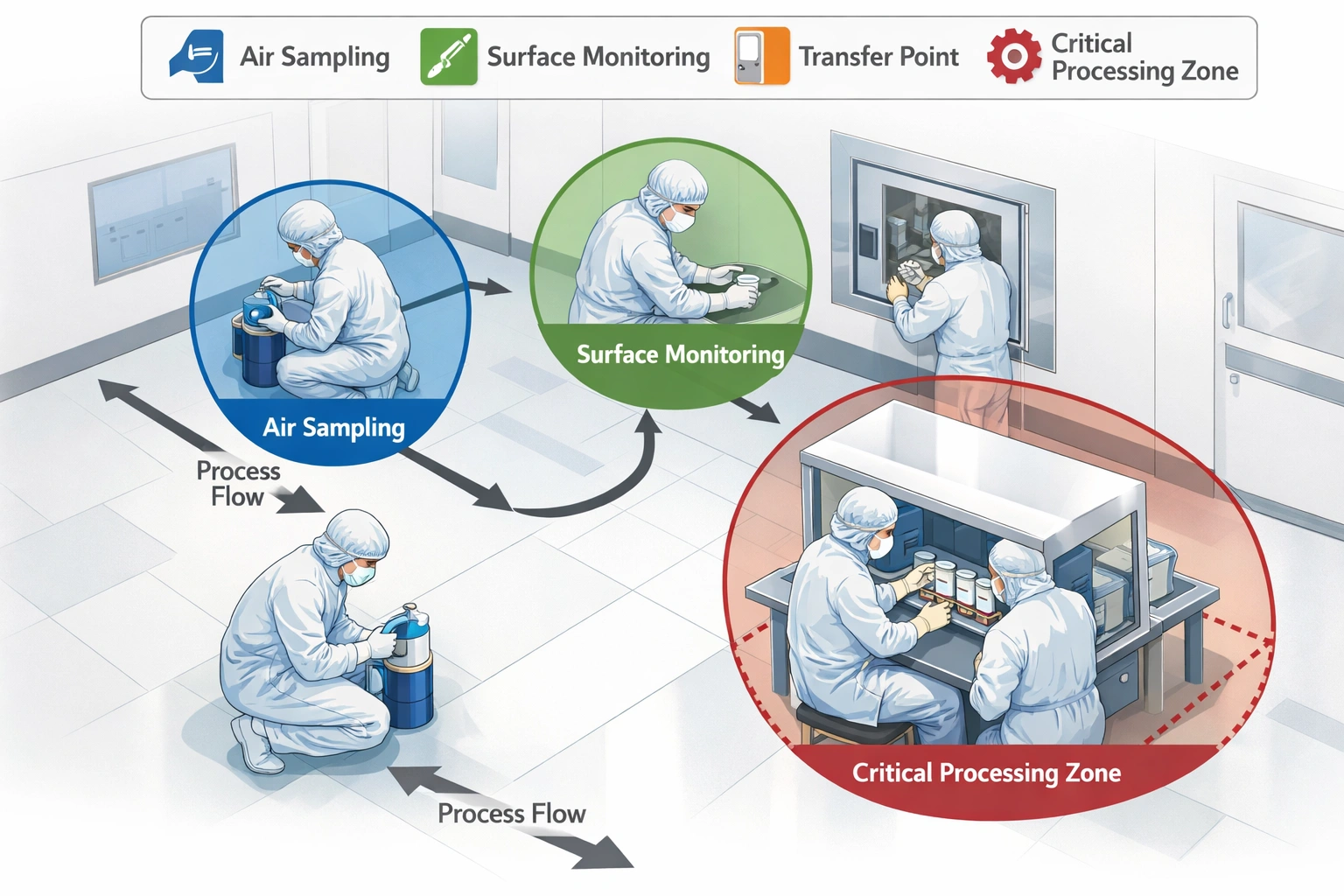
Passo 4: Definir Frequências de Monitoramento
| Nível de risco | Viável | Inviável | Superfície |
|---|---|---|---|
| Alto | Contínuo + Semanal | Contínuo | Diário. |
| Médio | 2-3 vezes/semana | 2 vezes/semana | 2-3 vezes/semana. |
| Baixo | 1-2 vezes/semana | 1 vez/semana | 1 vez/semana. |
Etapa 5: definir níveis de alerta e ação
Estabeleça níveis cientificamente justificados com base em dados históricos e vulnerabilidade do processo. Aplique métodos estatísticos de controle de processo para obter precisão.
Estrutura de Desenvolvimento do POP
Modelo: ENV-MON-001 (versão 2.0)
1.0 Objetivo: Estabeleça um programa EM baseado em risco que garanta a qualidade do produto enquanto otimiza os recursos.
4.0 Procedimento: Protocolo de avaliação de risco, monitoramento de estratégia de localização, determinação de frequência, gerenciamento de nível de alerta/ação.
| Elemento POP | Abordagem Tradicional | Baseado em Risco 2026 |
|---|---|---|
| Locais de monitoramento | Padrão de grade fixo | Posicionamento estratégico baseado em risco. |
| Freqüência | Cronograma padronizado | Ajustado ao risco com revisão dinâmica. |
| Níveis de alerta | Valores numéricos estáticos | Análise estatística + contextual. |
Melhores práticas de implementação
Eficaz gerenciamento de instalações farmacêuticas envolve passar de procedimentos estáticos para procedimentos dinâmicos.
Recomendação de tecnologia: Implemente sistemas CEM com análise de dados em tempo real. Eles fornecem recursos preditivos essenciais para conformidade com 2026.
Matriz de Treinamento e Competências
| Público | Tópicos de treinamento | Avaliação |
|---|---|---|
| Equipe de controle de qualidade | Metodologia de risco, análise de dados | Simulação de avaliação de risco. |
| Microbiologia | Risco microbiano, análise de tendências | Análise de estudo de caso. |
| Operações | Resposta de alerta, Documentação | Demonstração prática. |
Estudo de caso: implementação global
História global de sucesso farmacêutico
- Redução de 35% nos custos de monitoramento.
- Detecção de contaminação 40% mais rápida.
- Redução de 50% em alertas falsos positivos.
- Melhor compreensão do operador sobre conceitos de risco.
"The risk-based approach transformed our environmental monitoring program from a compliance burden to a valuable quality assurance tool".
Métricas de desempenho e KPIs
| Categoria de métrica | KPI específico | Alvo |
|---|---|---|
| Eficácia | Tempo de detecção de contaminação | < 2 horas. |
| Eficiência | Custo de monitoramento por unidade | ↓ 30% da linha de base. |
| Conformidade | Pontuação de inspeção regulatória | ≥ 95%. |
| Qualidade | Taxa de precisão do alerta | ≥ 90%. |
Pronto para transformar seu programa EM?
Não espere pelos mandatos de 2026 para agir. Entre em contato com nossa equipe de especialistas para obter uma avaliação abrangente e um plano de implementação personalizado adaptado às suas instalações.
Recursos essenciais adicionais
- Orientação da FDA para a Indústria: Medicamentos Estéreis (2021).
- Anexo 1 das BPF da UE: Fabricação de medicamentos estéreis (2026).
- Guia de Base ISPE: Monitoramento Ambiental (2024).
- Gestão de Risco de Qualidade ICH Q9.
- Série ISO 14644: Salas limpas e ambientes associados.
Isenção de responsabilidade: Este guia é apenas para fins informativos. Consulte especialistas regulatórios e profissionais qualificados para os requisitos específicos de suas instalações.





Comentário de Especialista: A Evolução do Monitoramento
"The shift from traditional to risk-based environmental monitoring represents the most significant evolution in cleanroom management in decades. It's about using data and risk assessment to focus resources where they matter most".
"By 2026, regulatory agencies will mandate risk-based approaches. Companies that proactively implement these strategies will gain competitive advantages through improved efficiency and better contamination control".