En teknisk referens för QA-chefer och valideringsingenjörer om integrationen av spårbarhet av förbrukningsvaror i webbplatsens Contamination Control Strategy (CCS).

I en GMP-reglerad miljö ses renrumsmoppen inte längre som ett generiskt verktyg utan som en kritisk kontrollerad ingång. Renrumsmopp med spårbarhet för batch system fyller tre primära funktioner:
Product-level traceability identifies a SKU; batch-level traceability identifies the specific manufacturing event. For cleanroom mops, this requires a "genealogy" that links the finished product back to the specific lot of polyester yarn or microfiber fabric used, the cleanroom laundry shift, and the specific sterilization cycle.
När moppar behandlas som kontrollerade ingångar är varje enskilt paket en datapunkt. Dessa data gör det möjligt för QA-team att verifiera att produkten i deras hand är identisk i prestanda och renhet med produkten som validerades under den första anläggningsstarten eller PQ (Performance Qualification).
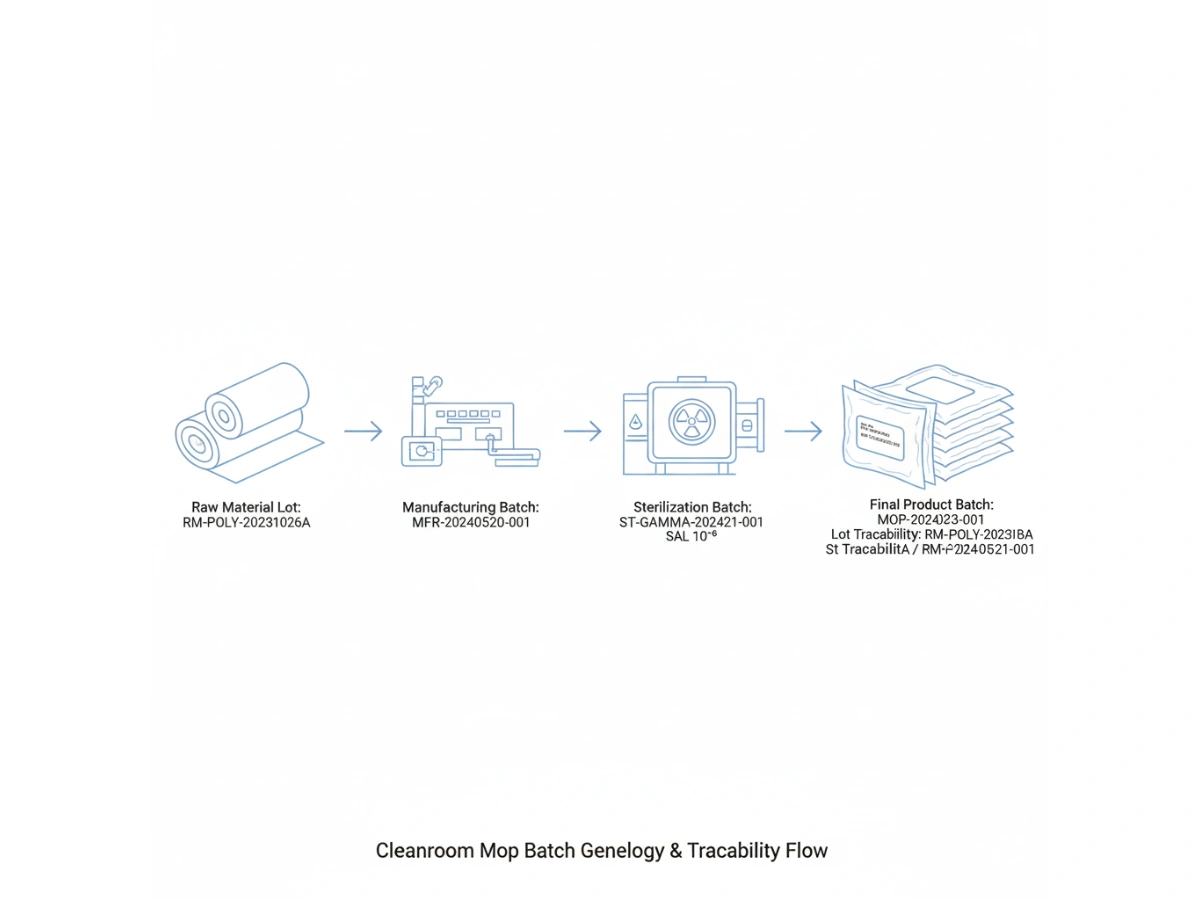
Moderna GMP-principer kräver att alla material som kommer i kontakt med känsliga ytor beaktas fullt ut. Under en inspektion kan en revisor välja ett produktionsdatum och fråga efter mycket spårbarhet av de rengöringsmaterial som användes den dagen.
Expectations focus on the "Linkage of Records." An auditor will look for a seamless transition from the facility's cleaning logs to the dokumentation på batchnivå tillhandahålls av leverantören. Om en moppsats inte kan kopplas till ett analyscertifikat (COA) eller en steriliseringsjournal, kan steriliteten och renheten i hela renrumssviten ifrågasättas.

Ett robust spårbarhetssystem för renrumsförbrukningsvaror GMP efterlevnaden måste inkludera:
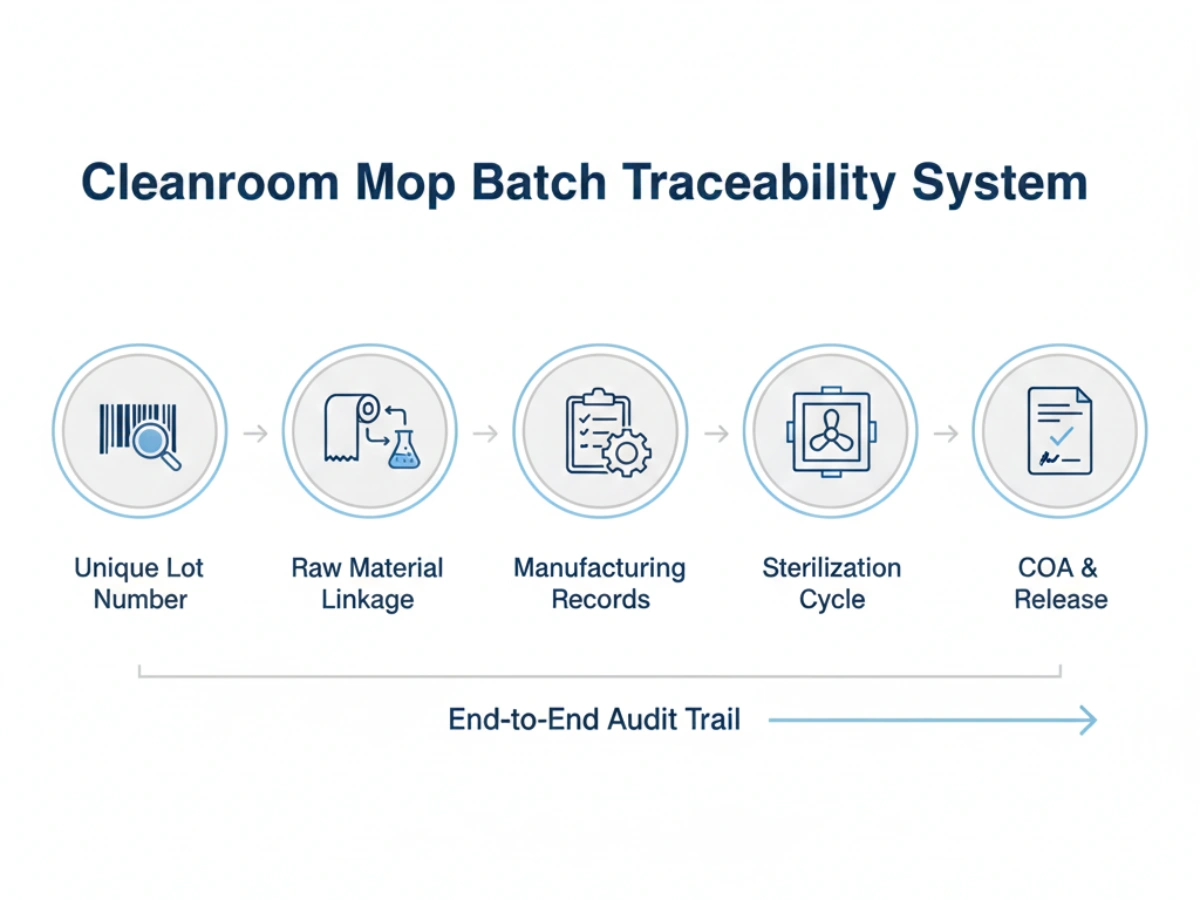
Supply stability is often threatened by "drift"—small, undocumented changes in manufacturing that accumulate over years. Batch traceability prevents this by establishing a baseline for konsistens från lott till parti.
I händelse av en CAPA (Corrective and Preventive Action) som involverar toppar för miljöövervakning (EM), tillåter spårbarhet QA att avgöra om en specifik sats moppar bidrog till händelsen. Utan detta kan anläggningen tvingas kassera allt lager och stoppa produktionen, vilket innebär en enorm operativ risk. Spårbarhet förvandlar en potentiell anläggningsomfattande kris till en lokal materialkarantän.

A läkemedelsmopptillverkare / OEM fungerar som en förlängning av läkemedelssidans kvalitetssystem. Deras ansvar inkluderar:
För en kvalificerad tillverkare, är förmågan att producera dessa poster på begäran kännetecknet för GMP-mognad.
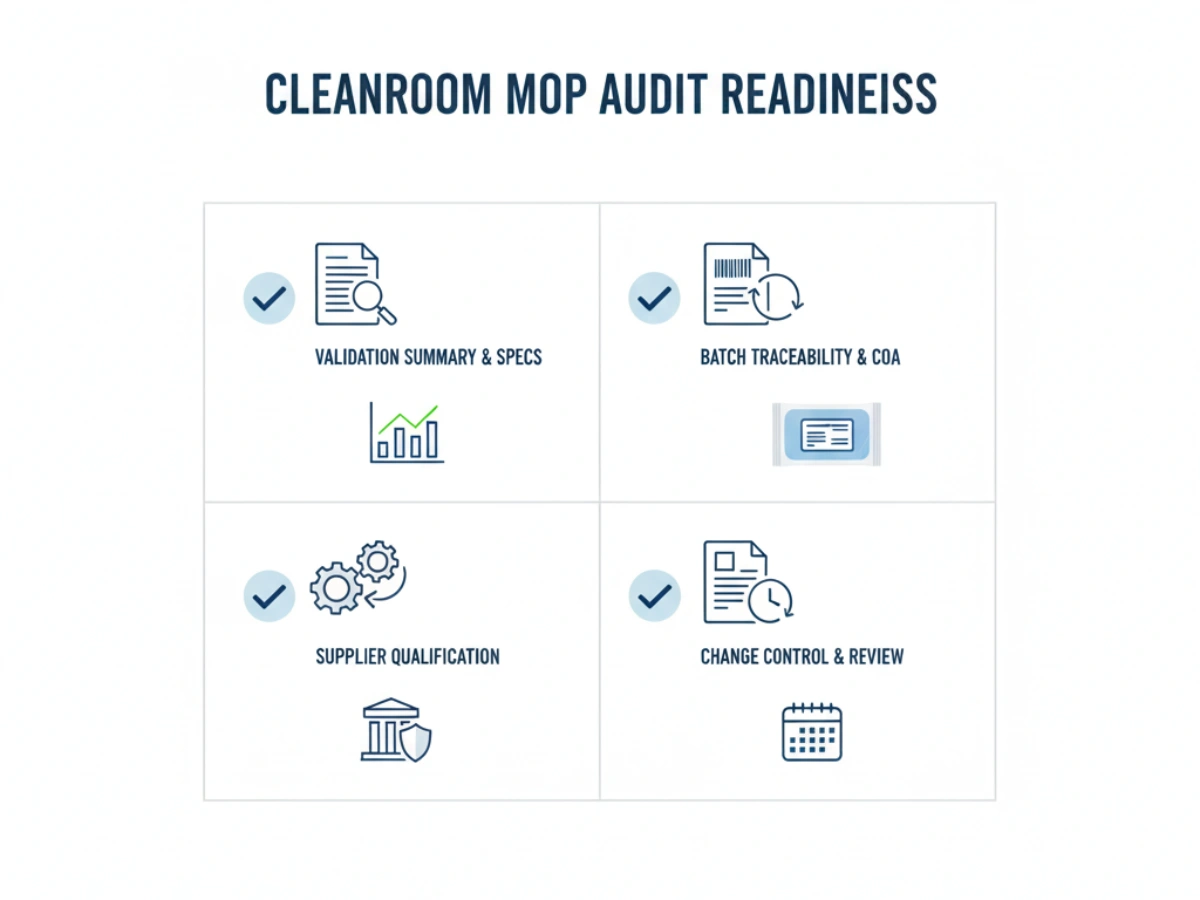
Under OEM-leverantörskvalifikation, QA-team bör använda följande checklista:
| Kontrollstation | Krav |
|---|---|
| Batch definition | Är batchstorleken tydligt definierad och hanterbar? |
| Provretention | Behåller leverantören prover för varje parti? |
| Revisionsåtkomst | Can the supplier provide full raw material logs within 48 hours? |
| Physical Labeling | Is the batch number resistant to cleanroom disinfectants (IPA)? |
Batch traceability is not merely a documentation exercise; it is the backbone of a defensible quality system. In the context of Grade A and B environments, the ability to track every fiber and sterilization cycle ensures that the cleaning process remains a controlled variable rather than an unknown risk.
Mature pharmaceutical QA teams prioritize suppliers who demonstrate total transparency in their batch records, viewing them as long-term partners in patient safety and regulatory compliance.
Ask for lot genealogy, batch-specific COAs, sterilization linkage, and change-control readiness to strengthen your audit narrative.
Request Documentation Package

Vi kommer att kontakta dig inom 1 arbetsdag, vänligen uppmärksamma mejlet med suffixet “*@midposi.com”.