Renrumsvalidering Lifecycle Management: En omfattande guide
Understand the full cleanroom validation lifecycle from DQ, IQ, OQ, and PQ through ongoing verification, requalification, and change control for GMP and ISO environments.

Utvalt Snippet Answer
Cleanroom validation lifecycle management covers the complete control framework from design qualification through ongoing performance verification. It helps manufacturers maintain GMP and ISO compliance, reduce contamination risk, and keep cleanroom performance documented throughout the facility’s operational life.
Nyckel takeaways
- Renrumsvalidering är en livscykelprocess, inte en engångskvalificeringshändelse.
- DQ, IQ, OQ och PQ verifierar var och en olika aspekter av renrumsberedskap och kontroll.
- Löpande verifiering och trendanalys är avgörande för att upprätthålla det validerade tillståndet.
- Omkvalificering bör utlösas av schema, händelser och prestationsavvikelse.
- Stark förändringskontroll skyddar valideringsintegritet och produktkvalitet.
Introduktion
Cleanroom validation is a continuous lifecycle that extends beyond initial IQ, OQ, and PQ certification. Ongoing performance verification and periodic requalification are essential to maintain compliance and ensure product quality throughout the cleanroom’s operational life.
Many regulatory findings stem from weak lifecycle control, including inadequate requalification, incomplete documentation, poor trend analysis, and ineffective change control. A lifecycle-based validation approach helps close these gaps and strengthen GMP inspection readiness.
Valideringslivscykelöversikt
The cleanroom validation lifecycle includes initial validation, ongoing verification, and long-term maintenance of the validated state. In practical terms, this means building a system that not only qualifies the room at the beginning, but also keeps it under control over time.
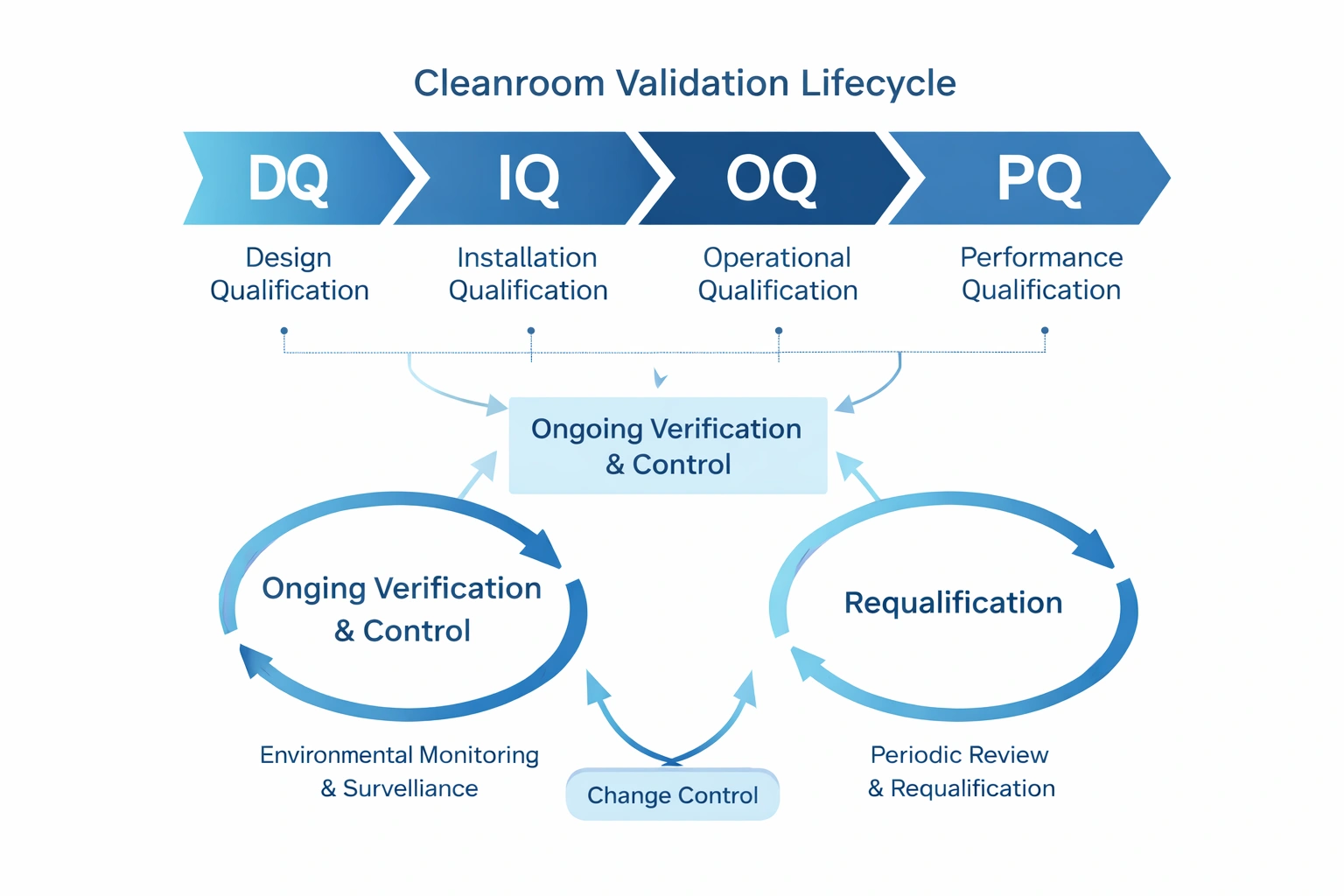
Initial validering
DQ, IQ, OQ, PQ och initial release för användning.
Pågående verifiering
Miljöövervakning, trendanalys, granskning och kontroll.
Omkvalificering & Ändra
Omkvalificering och förändringsbedömning upprätthåller livscykelintegriteten.
| Fas | Typisk varaktighet | Utlösare | Ägare |
|---|---|---|---|
| DQ | 2–4 veckor | Nytt projekt initieras | Teknik |
| IQ | 2–4 veckor | Bygget är klart | Faciliteter |
| OQ | 4–8 veckor | IQ komplett | Godkännande |
| PQ | 3–6 månader | OQ klar | Godkännande |
| Pågående verifiering | Pågående | Inledande certifiering klar | QA |
| Omkvalificering | 2–4 veckor | Årlig eller utlösande händelse | Godkännande |
Design Qualification (DQ)
Design Qualification verifies that the cleanroom design meets user requirements and is suitable for the intended process, cleanliness class, and contamination control strategy.

DQ Fokus
- Användarkravsspecifikation (URS)
- Funktionell designspecifikation (FDS)
- Riskbedömning och föroreningsgranskning
- Granskning av intressentdesign
- Dokumenterat DQ-godkännande
Nyckelfrågor
- Uppfyller designen det avsedda användarkravet?
- Kan systemet uppnå målet för renhetsgraden?
- Identifieras och mildras stora föroreningsrisker?
- Är designdokumentationen komplett och går att granska?
Installationskvalifikation (IQ)
IQ provides documented verification that the cleanroom and its supporting systems have been installed according to design specifications, approved drawings, and utility requirements.
IQ-dokumentationspaket
- IQ-protokoll
- Som-byggda ritningar
- Installationsprotokoll
- Utility anslutningsposter
- Kalibreringscertifikat
- IQ sammanfattande rapport
IQ Acceptans Fokus
- Installerad enligt godkänd specifikation
- Verktyg anslutna och funktionella
- Kritisk instrumentering kalibrerad
- Dokumentation komplett och spårbar
- Alla nödvändiga installationskontroller godkändes
Operationell kvalifikation (OQ)
OQ demonstrates that the cleanroom operates within predetermined limits under anticipated operating conditions. Typical OQ activities include airflow, pressure, particle, temperature, humidity, alarm, and interlock verification.
| Kriterium | Typiskt krav | Acceptansfokus |
|---|---|---|
| Luftflödeshastighet | Inom specificerat intervall | Alla kritiska platser inom räckhåll |
| Luftflödeslikformighet | ±20 % av medelvärdet | Stabil och repeterbar profil |
| Tryckskillnad | Inom målkaskad | Alla tryckförhållanden bibehölls |
| Partikelräkning | Uppfyller ISO-klass | Klassificering i vila uppnådd |
| Temperatur / RH | Inom börvärdesbandet | Miljön förblir kontrollerbar |
Performance Qualification (PQ)
PQ verifies that the cleanroom performs effectively and reproducibly under normal operating conditions with actual personnel activity, process simulation, and product-related contamination risk.

Period 1
Baslinjeverifiering under kontrollerade, lågaktivitetsförhållanden.
Period 2
Rutinmässig processsimulering med övervakning anpassad till EM-planen.
Period 3
Utökad eller värsta möjliga prestandaverifiering för konsekvens.
Pågående verifiering
Ongoing verification is what keeps the validated state alive after release. It typically includes environmental monitoring, continuous parameter monitoring, periodic trend analysis, deviation review, and assessment of whether requalification is needed.
Typiska aktiviteter
- Miljöövervakning per godkänd plan
- Granskning av tryck, temperatur och luftfuktighet
- Kvartalsvis eller periodisk trendanalys
- Granskning av revisionsberedskap
- Omkvalificeringsuppföljning
Varför det spelar roll
- Upptäcker prestandadrift tidigt
- Stöder CAPA och riskminskning
- Stärker GMP-inspektionsberedskapen
- Ger bevis på pågående kontroll
Omkvalificeringsstrategi
Requalification should be based not only on a schedule, but also on change events and performance signals. A robust strategy combines annual review with event-based and trend-based triggers.
Schemalagda utlösare
Årlig granskningscykel och SOP-definierade kvalificeringsintervall.
Händelseutlösare
Större underhåll, HEPA-byte, HVAC-modifieringar, processförändringar.
Prestandautlösare
Upprepade utflykter, stigande larmfrekvens, oförklarlig försämring, drift.
Ändra kontroll
Change control protects validation integrity by ensuring each relevant modification is assessed before implementation. The goal is to determine whether the change has no validation impact, requires partial requalification, or requires expanded requalification.
Obligatoriska ändringskontrollposter
- Ändra begäran
- Konsekvensanalys
- Risköversyn
- Planera omkvalificering
- Godkännande och genomförandebevis
- Uppdaterade valideringsposter
Typiska resultat
- Ingen påverkan – ingen omkvalificering behövs
- Mindre påverkan — fokuserad kvalifikation krävs
- Stor påverkan — fullständig eller utökad omkvalificering krävs
Vanliga frågor
Hur ofta ska omkvalificering av renrum utföras?
Annual review is common, but requalification should also be triggered by significant maintenance, process changes, major modifications, repeated excursions, or evidence of performance degradation.
Vad är skillnaden mellan initial validering och omkvalificering?
Initial validation establishes the original validated state through DQ, IQ, OQ, and PQ. Requalification confirms that the validated state remains acceptable after time, use, or change.
Hur avgör jag om en förändring kräver omkvalificering?
Review whether the change affects airflow, pressure cascade, filtration, environmental control, process conditions, contamination risk, or documentation status. The higher the impact, the broader the scope.
Vilken dokumentation krävs för valideringslivscykelhantering?
Typical records include DQ, IQ, OQ, and PQ protocols and reports, environmental monitoring records, trend analyses, requalification files, change control records, and approval evidence.
Varför är valideringslivscykelhantering viktig för produktkvaliteten?
Because cleanroom control is not static. Lifecycle management helps maintain the validated state, detect drift early, reduce contamination risk, and support consistent product quality.



