Temiz oda sarf malzemelerinin parti izlenebilirliği yalnızca bir dokümantasyon çalışması değildir. Üreticilerin, steril işleme ekiplerinin ve düzenlemeye tabi tesislerin ham maddeleri, üretimi, sterilizasyonu, dağıtımı ve son kullanımı tek bir doğrulanabilir kanıt zincirine bağlamasına olanak tanıyan operasyonel omurgadır.
Farmasötik, biyoteknoloji, yarı iletken ve tıbbi cihaz ortamlarında eksik izlenebilirlik, evrak boşluklarının çok ötesinde risk yaratır. Soruşturmaları geciktirir, geri çağırma yanıtını zayıflatır, denetimleri karmaşıklaştırır ve kontaminasyon kontrol programlarına olan güveni zayıflatır. Sağlam bir sistem, kalite ekiplerinin reaktif kayıt toplamadan proaktif kontrole geçmesine yardımcı olmalıdır.
Temiz oda sarf malzemeleri için seri izlenebilirliği, üretim, sterilizasyon, dağıtım ve son kullanıma kadar gelen malzemeden her partinin eksiksiz, geri alınabilir bir kaydının tutulması anlamına gelir. Uygulamada etkili bir sistem, neyin yapıldığını, hangi kaynak malzemelerden, hangi süreç koşulları altında, nereye nakledildiğini ve bir sapma veya geri çağırma meydana geldiğinde hangi müşterilerin veya dahili kullanıcıların etkileneceğini tanımlamalıdır.
Düzenlemelere tabi tesisler için en iyi sistemler yalnızca kağıt üzerinde uyumlu değildir. Aramaları hızlıdır, doğrulamaları kolaydır, denetime hazırdırlar ve hedeflenen geri çağırma işlemini günler yerine saatler içinde destekleyebilirler.
Güçlü parti izlenebilirliği, hammadde partilerini, üretim partilerini, sterilizasyon kayıtlarını, sevkiyat verilerini ve son kullanıcı tüketimini tek bir kanıt zincirine bağlar.
Denetime hazır sistemler, yalnızca bağlantısız kayıtların pasif olarak saklanmasını değil, hızlı araştırmayı ve hedefli geri çağırmayı da desteklemelidir.
Açık bir parti numaralandırma mantığı, operatörün kafa karışıklığını azaltır ve aşağı yönlü raporlamayı, etiketlemeyi, yayınlamayı ve şikayet yönetimini iyileştirir.
Sistemin gerçekten baskı altında çalıştığını kanıtlamak için ileri izlenebilirlik, geriye dönük izlenebilirlik ve geri çağırma simülasyonu periyodik olarak test edilmelidir.
Pek çok tesis parti numaralarını kartonlara, etiketlere veya sterilizasyon belgelerine zaten kaydetmektedir. Sorun, bu kayıtların genellikle satın alma, depo, üretim, sterilizasyon, lojistik ve son kullanıcı günlüklerine göre parçalanmış olmasıdır. Bir şikayet, kontaminasyon olayı veya denetim talebi oluştuğunda ekibin geçmişi manuel olarak yeniden yapılandırması gerekir.
Bu yaklaşım yavaş, hataya açık ve pahalıdır. Olgun bir izlenebilirlik programı, araştırma süresini kısaltır, serbest bırakma güvenini artırır ve geri çağırma eylemlerinin kapsamını sınırlandırır. Ayrıca trend analizini, tedarikçi yönetimini, CAPA'yı ve müşteri iletişimini de destekler.

Temiz oda sarf malzemeleri izlenebilirlik sistemi, düzenlemeye tabi kuruluşların sapmaları nasıl araştırdığı ve kontrolü nasıl kanıtladığı temel alınarak tasarlanmalıdır. Birçok kullanıcı için en alakalı referanslar arasında AB GMP Ek 1, FDA cGMP kayıt tutma beklentileri ve tıbbi cihazla ilgili kalite sistemleri için ISO 13485 izlenebilirlik gereksinimleri yer almaktadır.
| Yönetmelik / Standart | Odak Alanı | Operasyonel Anlam |
|---|---|---|
| Me GMP Ek 1 | İzlenebilirlik, toplu kayıtlar, geri çağırma yeteneği | Tesisler, soruşturmalar veya piyasa eylemleri sırasında etkilenen malzemeleri ve bitmiş ürünleri hızlı bir şekilde tanımlayabilmelidir. |
| FDA 21 CFR 211.180 / 211.198 | Dağıtım kayıtları, şikayet dosyaları, saklama | Kayıtlar şikayet değerlendirmesini, parti etkisi incelemesini ve kontrollü geri çağırma uygulamasını desteklemelidir. |
| ISO 13485 Bölüm 7.5.8 | Benzersiz tanımlama ve erişim | Kuruluş, belgelendirilmiş izlenebilirlik prosedürlerini sürdürmeli ve gerektiğinde bağlantılı kayıtları alabilmelidir. |
Alıcılar ve QA ekipleri için bu, izlenebilirliğin yalnızca depoya özgü bir işlev olarak ele alınmaması gerektiği anlamına gelir. Tedarikçi kontrolü, üretim dokümantasyonu, sterilizasyon onayı, sevkıyat geçmişi ve son kullanıcının hesap verebilirliği ile ilgili işlevler arası bir kalite gereksinimidir.
Parti izlenebilirliğini yapılandırmanın yararlı bir yolu, sistemi birbirine bağlı beş katmana bölmektir: hammaddeler, üretim, sterilizasyon, dağıtım ve tüketim. Bu çerçeve, ekiplerin uçtan uca görünürlüğü kaybetmeden sahipliği, veri alanlarını ve doğrulama kontrol noktalarını tanımlamasına yardımcı olur.
Tedarikçi kimliğini, tedarikçi parti numarasını, alındı tarihini, gelen denetim durumunu ve COA veya CoC gibi ilgili sertifikaları yakalayın. Bu, yukarı yönlü kontrolün başlangıç noktasıdır.
Hangi malzemelerin kullanıldığını, partiyi hangi hattın ürettiğini, prosesi kimin çalıştırdığını veya serbest bıraktığını ve hangi proses içi veya son kalite kontrol kontrollerinin gerçekleştirildiğini kaydedin.
Steril sarf malzemeleri için üretim partisini sterilizasyon partisine, döngü parametrelerine, sterilizasyon yöntemine, sürüm durumuna ve doğrulama kanıtlarına bağlayın.
Parti numaralarını müşterilere, gönderi miktarlarına, gönderi tarihlerine, taşıyıcı bilgilerine ve varış ayrıntılarına bağlayın. Bu, şikayet önceliklendirmesi ve geri çağırmanın kontrol altına alınması için gereklidir.
Kullanım modelinin gerektirdiği durumlarda parti numarası, kullanım tarihi, konum ve imha yoluna ilişkin kullanıcı tarafında kayıtlar tutun. Bu, özellikle yüksek riskli GMP ortamlarında değerlidir.
Parti numarası seri damgasından daha fazla olmalıdır. Hızlı yorumlamayı, doğru depolamayı, temiz etiket sunumunu ve düşük hatalı manuel kullanımı desteklemelidir. Yapılandırılmış bir format aynı zamanda dijital aramayı ve raporlamayı daha güvenilir hale getirir.

| Toplu Öğe | Örnek | Neden Önemlidir? |
|---|---|---|
| Tedarikçi / Üretici Kodu | MİDPOZİS | Üretim kaynağını tanımlar ve markaları, tesisleri veya tedarik akışlarını ayırır. |
| Tarih Segmenti | 2026-04-06 | Operatörlerin üretim kronolojisini ve saklama mantığını hızlı bir şekilde tanımlamasına yardımcı olur. |
| Seri numarası | 001 | Aynı gün veya döngü penceresi içerisinde üretilen birden fazla partiyi birbirinden ayırır. |
| Son Ek / Süreç İşaretleyicisi | A / B / C | Üretim, sterilizasyon, yeniden sterilizasyon veya QA iş akışı ayrımları için kullanışlıdır. |
Destekleyici kayıtlar eksikse, güçlü fiziksel etiketleme bile yeterli değildir. Savunulabilir bir izlenebilirlik dosyası, incelemecinin bitmiş bir partiden kaynak malzemelere geri dönmesine ve kaynak materyalden etkilenen her bitmiş partiye ve müşteri sevkiyatına ilerlemesine olanak sağlamalıdır.
Tedarikçi partisi, alınan miktar, inceleme sonucu, belge kontrolü, serbest bırakma durumu.
Parti numarası, operatör, hat, işlem tarihi, malzeme kullanımı, kalite kontrol kontrol noktaları, sapmalar.
Sterilizasyon partisi, döngü verileri, serbest bırakma kararı, müşteriye gönderilen miktar, varış yeri, şikayet bağlantısı.
Dokümantasyon setine tedarikçi denetimleri, müşteri yeterliliği, şikayetlerin ele alınması ve CAPA incelemeleri sırasında da kolayca erişilebilmelidir. Doğru dosyayı bulmak çok uzun sürüyorsa sistem işlevsel olarak kağıt üzerinde göründüğünden daha zayıf demektir.
Bir izlenebilirlik sistemi varsayılmamalı, test edilmelidir. En pratik yaklaşım üç tür alıştırma yürütmektir: ileri izlenebilirlik, geriye doğru izlenebilirlik ve geri çağırma simülasyonu. Bu testler, veri alanlarının gerçekten bağlantılı olup olmadığını, ekiplerin nereye bakacağını bilip bilmediğini ve yanıt süresinin şirket içi beklentileri karşılayıp karşılamadığını ortaya çıkarır.
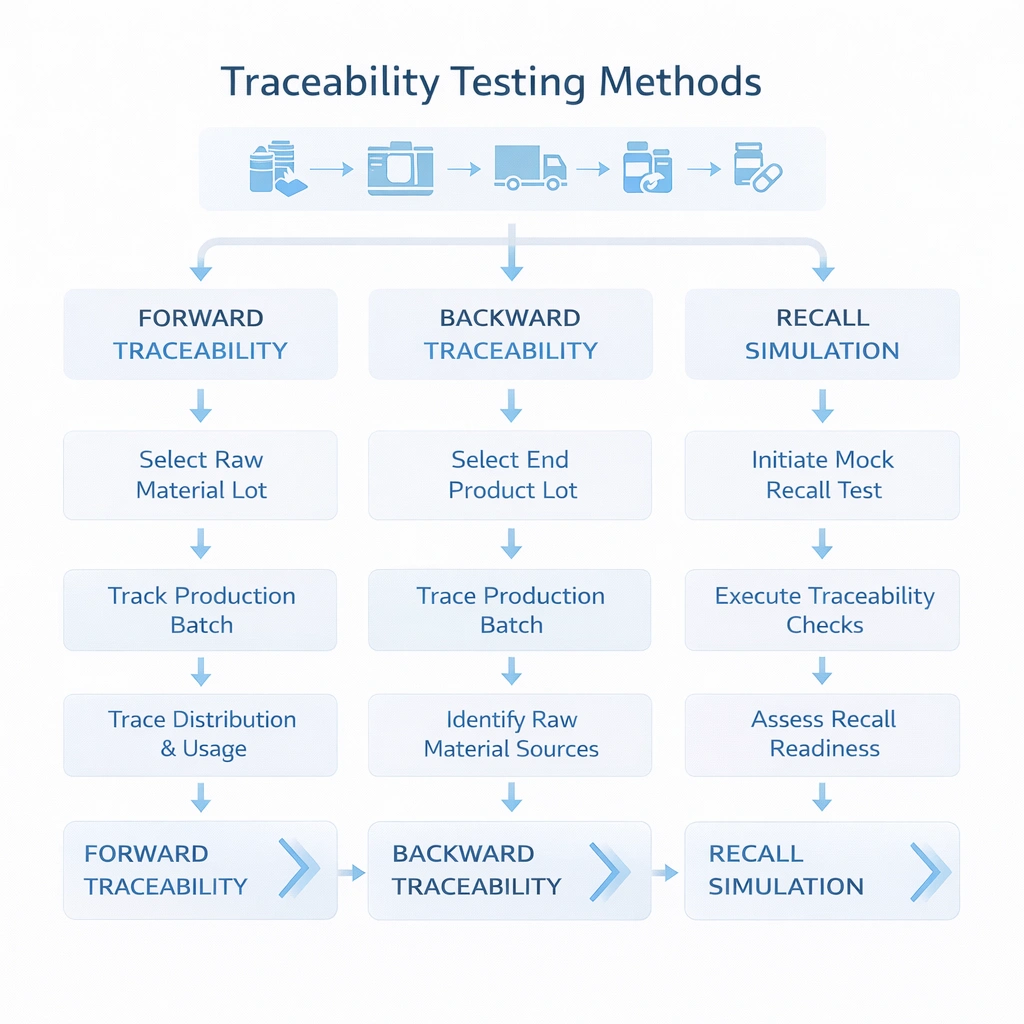
Gelen malzeme partisiyle başlayın ve hangi üretim partilerinin, sterilizasyon döngülerinin ve müşteri sevkiyatlarının etkilendiğini belirleyin.
Bir şikayetle veya müşteri tarafından kullanılan bir partiyle başlayın ve kaynak malzemelere, süreç kayıtlarına ve sürüm durumuna kadar geriye doğru izleyin.
Bir parti seçin ve hedeflenen geri çağırmayı simüle edin: etkilenen her müşteriyi, miktarı, gönderi rotasını belirleyin ve sahiple iletişime geçin. Gereken toplam süreyi ve bulunan veri boşluklarını kaydedin. Yüksek kontrollü ortamlarda bu alıştırma, sistemin gerçekten geri çağırmaya hazır olup olmadığını değerlendirmenin en hızlı yollarından biridir.
| Test Türü | Ana Soru | Beklenen Çıktı |
|---|---|---|
| İleriye Doğru İzlenebilirlik | Bu girdi nereye gitti? | Etkilenen üretim, sterilizasyon ve sevkiyat kayıtları |
| Geriye Doğru İzlenebilirlik | Bu sonucu ne yarattı? | Kaynak materyal, süreç geçmişi, yayın kanıtı |
| Simülasyonu Geri Çağırma | Hızlı ve doğru hareket edebilir miyiz? | Müşteri listesi, miktar haritası, yanıt zamanlaması, veri boşluğu günlüğü |
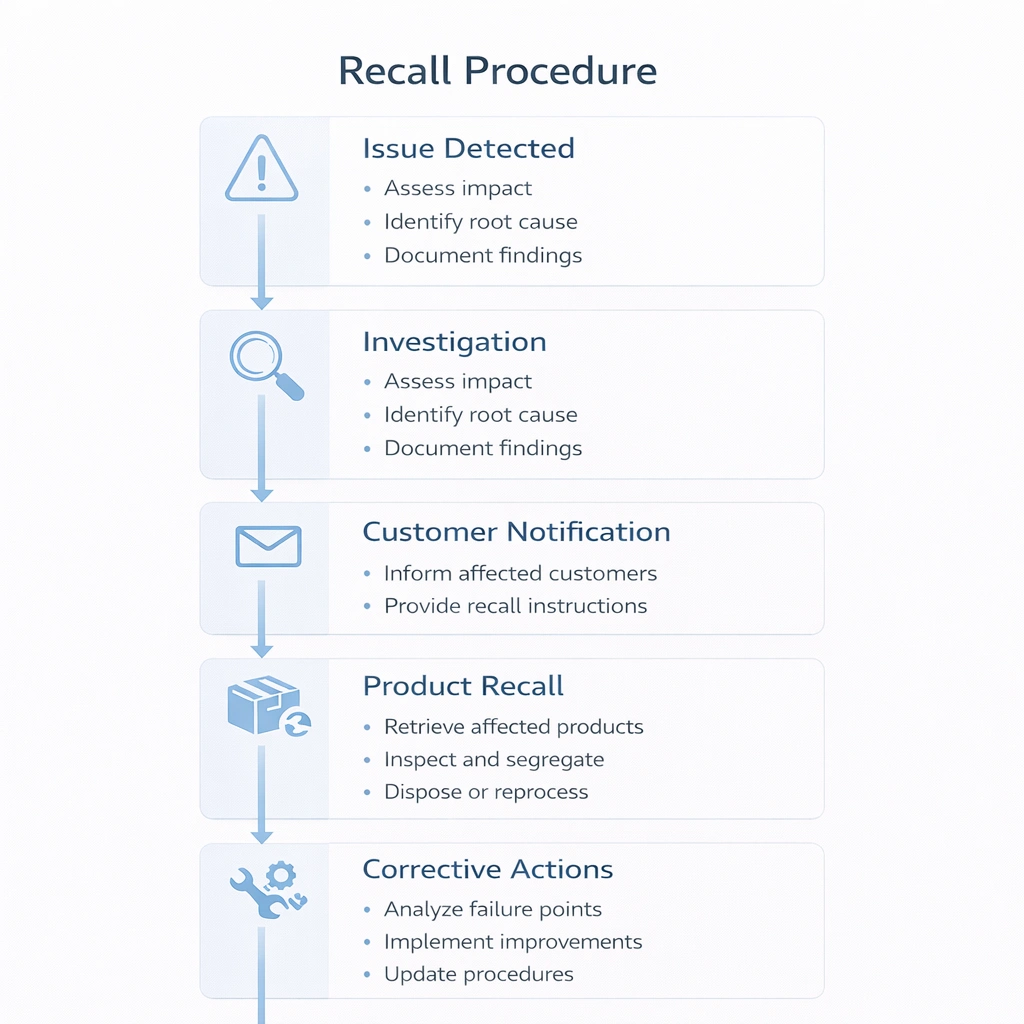
Geri çağırma iş akışı doğaçlama yerine önceden belirlenmelidir. Bir kalite sorunu ortaya çıktığında ekiplerin sorunu nasıl sınıflandıracaklarını, etkilenen partileri nasıl belirleyeceklerini, paydaşları nasıl bilgilendireceklerini, daha fazla dağıtımı nasıl durduracaklarını ve temel nedeni ve düzeltici eylemleri nasıl belgeleyeceklerini zaten bilmeleri gerekir.
Elektronik tablo tabanlı sistemler düşük karmaşıklıkta çalışabilir ancak ürün yelpazesi, müşteri hacmi ve sterilite iş akışları genişledikçe elektronik izlenebilirlik genellikle daha pratik hale gelir. Barkod veya RFID destekli sistemler manuel giriş riskini azaltır ve geri çağırma simülasyonunu daha hızlı ve tekrarlanabilir hale getirir.

Steril ve steril olmayan hatlar için veri alanlarını, sahipliği, parti kodu mantığını, saklama kurallarını ve izlenebilirlik kapsamını tanımlayın.
Formları, tedarikçi parti kayıtlarını, üretim kayıtlarını, sterilizasyon bağlantısını ve sevkiyat kayıtlarını standartlaştırın.
İleriye doğru izlenebilirlik, geriye doğru izlenebilirlik ve geri çağırma simülasyon testlerini çalıştırın ve bulunan boşlukları belgeleyin.
Sistem en azından gelen malzeme partilerini, üretim partilerini, uygun olduğu durumlarda serbest bırakma veya sterilizasyon kayıtlarını, nakliye geçmişini ve bir araştırma sırasında etkilenen müşteri veya kullanıcıları belirleme yeteneğini birbirine bağlamalıdır.
Toplu etiketleme bir ürün grubunu tanımlar. Tam izlenebilirlik, etiketlemeyi yukarı yöndeki materyallere, proses kayıtlarına, sürüm kararlarına ve alt yöndeki dağıtım veya kullanım kayıtlarına bağlar.
Birçok kalite ekibi bunu en az yılda bir kez gerçekleştirirken, daha yüksek riskli veya daha karmaşık operasyonlar, özellikle sistem değişiklikleri, tedarikçi değişimleri veya büyük CAPA eylemlerinden sonra daha sık test yapabilir.
Evet, düşük hacimli işlemler için. Ancak ürün çeşitliliği, sterilite kontrolü veya müşteri karmaşıklığı arttığında, dijital sistemler genellikle daha iyi erişim hızı, hata azaltma ve denetim kontrolü sağlar.
Çünkü steril ürünler, seri geçmişinin, sterilizasyon bağlantısının, sürüm kanıtlarının ve bir şikayet, sterilite endişesi veya geri çağırma kararının ortaya çıkması durumunda aşağı yönde görünürlük üzerinde daha sıkı kontrol gerektirir.
Midposi, kalifikasyon için dokümantasyon odaklı iletişim, sterilite durumu incelemesi ve seri izlenebilirlik tartışmaları dahil olmak üzere, kontrollü ortamlar için tasarlanmış temiz oda sarf malzemeleriyle düzenlemeye tabi alıcıları destekler.


1 iş günü içinde sizinle iletişime geçeceğiz, lütfen son eki olan e-postaya dikkat edin. “*@midposi.com”.