Sarf malzemesi izlenebilirliğinin tesis Kirlilik Kontrol Stratejisine (CCS) entegrasyonu konusunda QA yöneticileri ve doğrulama mühendisleri için teknik bir referans.

GMP düzenlemeli bir ortamda, temiz oda paspası artık genel bir yardımcı program olarak değil, kritik kontrollü bir girdi olarak görülüyor. Toplu izlenebilirlik temiz oda paspası sistemler üç temel işleve hizmet eder:
Product-level traceability identifies a SKU; batch-level traceability identifies the specific manufacturing event. For cleanroom mops, this requires a "genealogy" that links the finished product back to the specific lot of polyester yarn or microfiber fabric used, the cleanroom laundry shift, and the specific sterilization cycle.
Paspaslar kontrollü girdiler olarak ele alındığında her bir paket bir veri noktasıdır. Bu veriler, QA ekiplerinin ellerindeki ürünün performans ve saflık açısından ilk tesis başlatma veya PQ (Performans Yeterliliği) sırasında doğrulanan ürünle aynı olduğunu doğrulamasını sağlar.
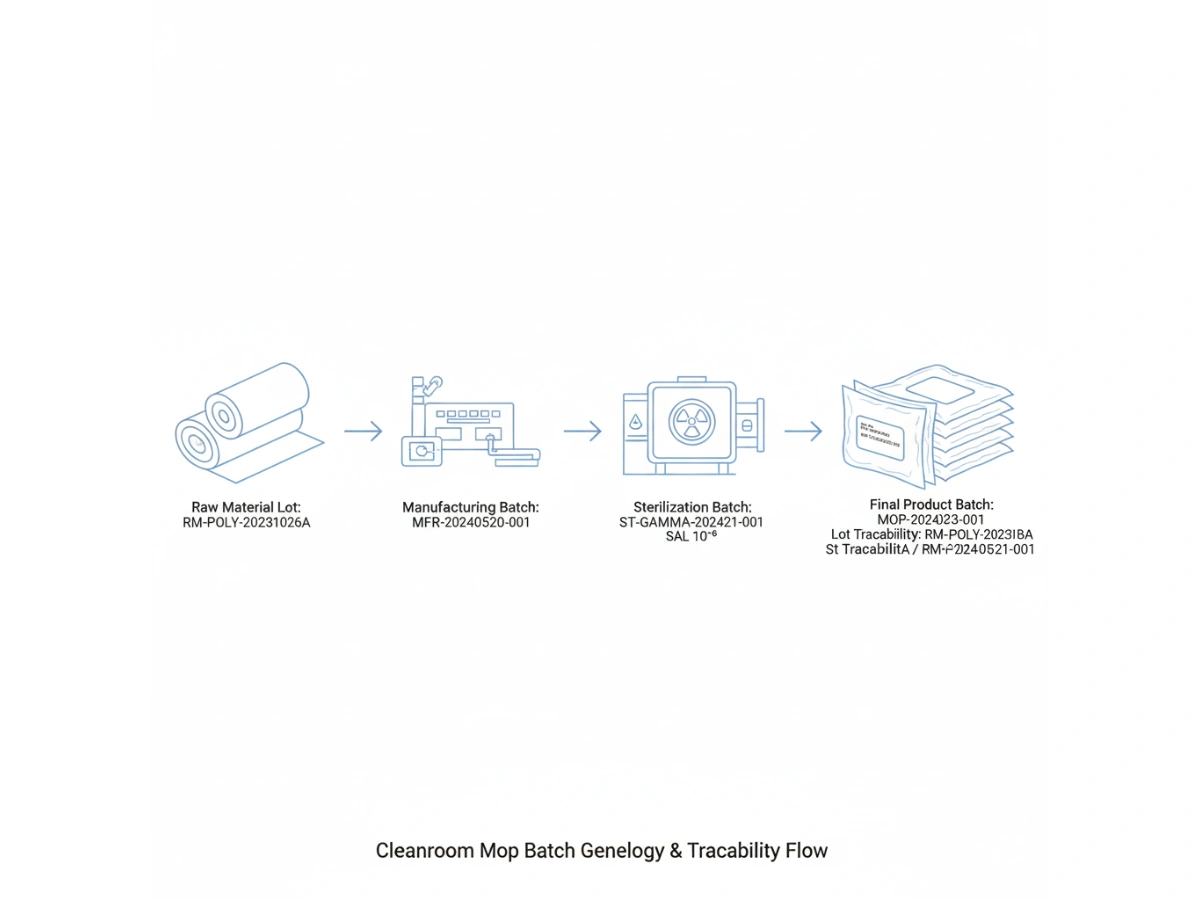
Modern GMP ilkeleri, hassas yüzeylerle temas eden tüm malzemelerin tam olarak hesaba katılmasını gerektirir. Denetim sırasında denetçi üretim tarihini seçebilir ve üretim tarihini isteyebilir. parti izlenebilirliği O gün kullanılan temizlik malzemeleri.
Expectations focus on the "Linkage of Records." An auditor will look for a seamless transition from the facility's cleaning logs to the toplu düzeyde belgeler tedarikçi tarafından sağlanır. Bir paspas partisi bir Analiz Sertifikasına (COA) veya bir sterilizasyon kaydına bağlanamazsa, tüm temiz oda takımının sterilliği ve temizliği sorgulanabilir.

için sağlam bir izlenebilirlik sistemi temiz oda sarf malzemeleri GMP uyumluluk şunları içermelidir:
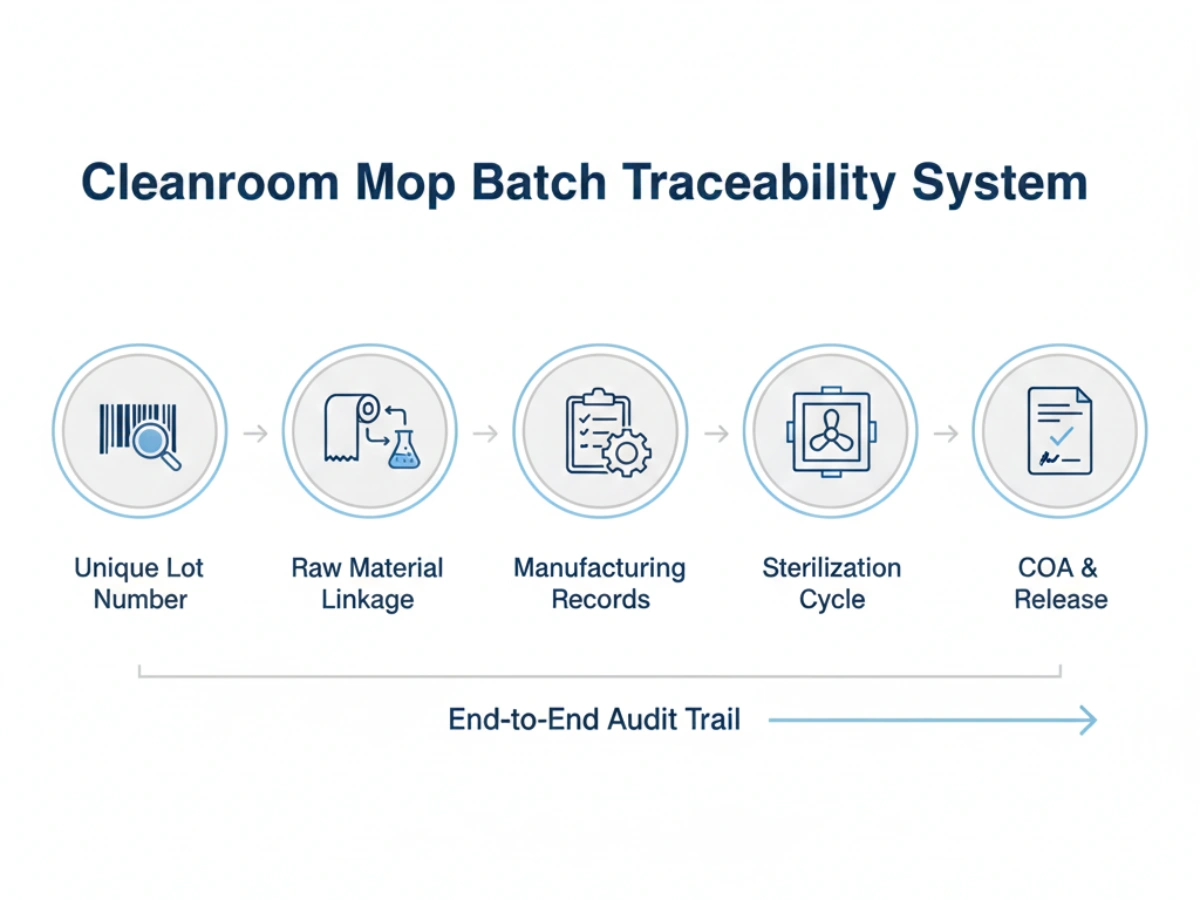
Supply stability is often threatened by "drift"—small, undocumented changes in manufacturing that accumulate over years. Batch traceability prevents this by establishing a baseline for lottan lota tutarlılık.
Çevresel izleme (EM) artışlarını içeren bir CAPA (Düzeltici ve Önleyici Faaliyet) durumunda izlenebilirlik, QA'nın belirli bir paspas grubunun olaya katkıda bulunup bulunmadığını belirlemesine olanak tanır. Bu olmazsa tesis, tüm envanteri atmaya ve üretimi durdurmaya zorlanabilir ve bu da büyük bir operasyonel risk oluşturur. İzlenebilirlik, tesis çapında olası bir krizi yerelleştirilmiş bir malzeme karantinasına dönüştürür.

A farmasötik paspas üreticisi / OEM ilaç tesisinin kalite sisteminin bir uzantısı olarak hareket eder. Sorumlulukları şunları içerir:
bir için nitelikli üreticiBu kayıtları talep üzerine üretme yeteneği, GMP olgunluğunun ayırt edici özelliğidir.
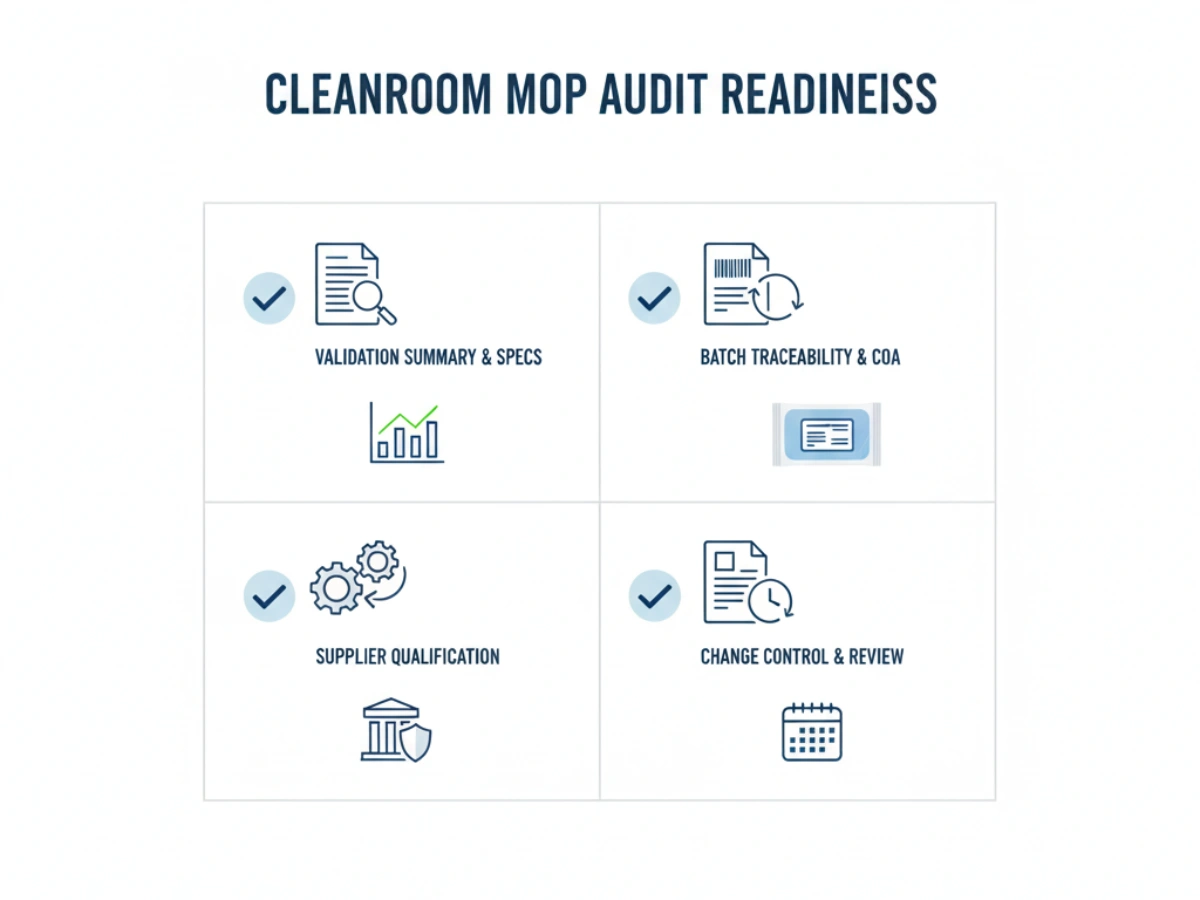
Sırasında OEM tedarikçi yeterliliği, QA ekipleri aşağıdaki kontrol listesini kullanmalıdır:
| Kontrol noktası | Gereklilik |
|---|---|
| Toplu Tanım | Parti büyüklüğü açıkça tanımlanmış ve yönetilebilir mi? |
| Örnek Saklama | Tedarikçi her parti için numuneleri saklıyor mu? |
| Denetim Erişimi | Tedarikçi 48 saat içinde tam hammadde kayıtlarını sağlayabilir mi? |
| Fiziksel Etiketleme | Parti numarası temiz oda dezenfektanlarına (IPA) dayanıklı mı? |
Seri izlenebilirliği yalnızca bir dokümantasyon çalışması değildir; savunulabilir bir kalite sisteminin omurgasıdır. A ve B Sınıfı ortamlar bağlamında, her elyafı ve sterilizasyon döngüsünü takip etme yeteneği, temizleme sürecinin bilinmeyen bir risk yerine kontrollü bir değişken olarak kalmasını sağlar.
Olgun farmasötik QA ekipleri, seri kayıtlarında tam şeffaflık sergileyen tedarikçilere öncelik vererek onları hasta güvenliği ve mevzuata uygunluk konusunda uzun vadeli ortaklar olarak görüyor.
Denetim anlatınızı güçlendirmek için parti şeceresini, partiye özel COA'ları, sterilizasyon bağlantısını ve değişiklik-kontrol hazırlığını isteyin.
Dokümantasyon Paketi İste

1 iş günü içinde sizinle iletişime geçeceğiz, lütfen son eki olan e-postaya dikkat edin. “*@midposi.com”.