
Abbildung 1: Pharmazeutischer Autoklav (Consolidated SR-24C) mit Edelstahlkammer, digitalem Bedienfeld mit mehreren Manometern und Doppelscharniertür. Autoklaven validieren die Reinraum-Moppsterilisation durch Platzierung biologischer Indikatoren, parametrische Überwachung (Temperatur, Druck, Zeit) und Qualifizierung der Ladungskonfiguration, um SAL 10⁻⁶ zu erreichen.
Was bedeutet „autoklavierbar“ bei Reinraum-Reinigungswerkzeugen?
Definition von Autoklavieren: Temperatur, Dampf, Druck
Beim Autoklavieren handelt es sich um eine Sterilisation mit feuchter Hitze unter Verwendung von gesättigtem Dampf unter Druck, um eine validierte mikrobielle Letalität zu erreichen. Standardpharmazeutische Zyklen arbeiten bei 121–134 °C (250–273 °F) und einem Überdruck von 15–30 psi (103–207 kPa über Atmosphäre). Bei 121 °C dringt Dampf in poröse Ladungen ein und kondensiert auf kühleren Oberflächen, wobei latente Wärme freigesetzt wird, die Proteine denaturiert und Zellstrukturen in vegetativen Bakterien, Sporen, Pilzen und Viren zerstört.
Das Zyklusdesign zielt auf einen Sterilitätssicherungsgrad (SAL) von 10⁻⁶ ab – eine Wahrscheinlichkeit von ≤1 zu 1.000.000, dass ein lebensfähiger Mikroorganismus den Prozess überlebt. Bei der Validierung werden biologische Indikatoren (BIs) verwendet, die Sporen von enthalten Geobacillus stearothermophilus (früher Bacillus stearothermophilus), ein hitzebeständiger Organismus mit einem dokumentierten D₁₂₁-Wert (dezimale Reduktionszeit bei 121 °C) von typischerweise ≥1 Minute. Ein Overkill-Ansatz liefert eine Reduzierung um ≥12 log (12-facher D-Wert), um die SAL-Anforderungen zu erfüllen; Produktspezifische Ansätze berechnen F₀ (äquivalente Minuten bei 121 °C) basierend auf der gemessenen Keimbelastung und den D-Werten.
Bei Reinraum-Mopps erfüllt das Autoklavieren zwei Funktionen: Endsterilisation (Erzielung eines SAL-Werts von 10⁻⁶ für die Verwendung der Klasse A/B) und Wiederaufbereitung zwischen den Anwendungen (Entfernung der während der Reinigung entstandenen Keimbelastung bei gleichzeitiger Beibehaltung der Materialleistung). „Autoklavierbar“ bedeutet, dass das Material wiederholter Einwirkung von gesättigtem Dampf bei 121 °C standhält, ohne dass es zu Funktionsstörungen kommt. In Marketingaussagen wird jedoch selten angegeben, wie viele Zyklen oder welche Leistungskennzahlen eingehalten werden.
Erforderlicher Sterilitätssicherungsgrad (SAL 10⁻⁶ für Aseptik)
EU-GMP-Anhang 1 Abschnitt 4.29 schreibt vor, dass „Desinfektionsmittel und Reinigungsmittel steril sein müssen“, wenn sie in Umgebungen der Klassen A und B verwendet werden. „Steril“ im Sinne der Vorschriften bedeutet einen nachgewiesenen SAL-Wert von 10⁻⁶ – keine visuelle Sauberkeit, keine Keimbelastung <10 KBE, aber probabilistische Sicherheit validiert durch Overkill-Zyklen oder Keimbelastungs-/D-Wert-Berechnungen.
Die SAL-Validierung für autoklavierbare Mopps erfordert:
Platzierung biologischer Indikatoren: BIs sind an den ungünstigsten kalten Stellen (identifiziert bei Wärmeverteilungsstudien) innerhalb von Wischbeladungen positioniert. Dicht gepackte Ladungen, geschichtete Stoffe und versiegelte Beutel stellen Probleme beim Eindringen von Dampf dar. Die Validierung bestätigt, dass alle BIs in aufeinanderfolgenden Läufen inaktiviert sind.
Zyklusparametrische Überwachung: Kontinuierliche Aufzeichnung von Kammertemperatur, Druck und Zeit. An jeder Stelle der Ladung muss eine Mindestexposition (typischerweise 15–30 Minuten bei 121 °C oder 3–10 Minuten bei 134 °C) erreicht werden, wobei die F₀-Berechnung eine kumulative Letalität von ≥8–12 Minuten Äquivalent bestätigt.
Konfigurationsqualifizierung laden: Worst-Case-Szenarien (maximale Mopanzahl, dichteste Packung, in der Praxis verwendete Behälter/Beutel) müssen validiert werden. Ein Zyklus, der 10 lose Moppköpfe sterilisiert, kann fehlschlagen, wenn 20 Köpfe eng gestapelt oder in Autoklavenbeutel eingewickelt sind.
Routinemäßige BI-Überwachung: Regelmäßige Läufe mit biologischen Indikatoren (Häufigkeit im Validierungsprotokoll festgelegt, häufig wöchentlich oder pro Charge) bestätigen die fortlaufende Wirksamkeit der Sterilisation. Die Umgebungsüberwachung der Qualität des Autoklavenwassers, der Dampfreinheit und der Keimbelastung in der Kammer ergänzt die parametrische Freigabe.
Grade C and D areas may accept disinfected (not sterilized) mops, but pharmaceutical best practice increasingly extends SAL 10⁻⁶ validation to reusable cleaning tools across all classified zones to prevent bioburden migration from lower to higher grades.
Unterschied zwischen „sauber“, „steril“ und „autoklavierbar“
These terms are often conflated in procurement specifications, creating qualification gaps that surface during audits:
Clean: Visibly free from soil, particulates, and gross contamination. Achieved through laundering with pharmaceutical-grade detergents, validated rinse cycles, and clean-room drying. “Clean” mops may still harbor 10³–10⁶ CFU bioburden and generate hundreds of particles per m². Acceptable for unclassified areas; insufficient for ISO-classified cleanrooms.
Sterile: Validiert auf SAL 10⁻⁶ durch abschließende Sterilisation (Autoklavieren, Gammabestrahlung, Ethylenoxid). Mikrobiologische Tests (USP <71> Sterilitätstest) und parametrische Überwachung bestätigen die Abwesenheit lebensfähiger Organismen. Für Bereiche der Klasse A/B sind gemäß Anhang 1 Abschnitt 4.29 sterile Wischmopps erforderlich. Die Sterilität lässt mit der Zeit nach (Verfallsdatum) und wird durch unsachgemäße Lagerung oder Verpackungsfehler beeinträchtigt.
Autoklavierbar: Das Material hält der Sterilisation mit feuchter Hitze ohne unzulässige Zersetzung stand. Dabei handelt es sich um eine Materialeigenschaft, nicht um einen Sterilitätszustand. Autoklavierbare Materialien steril gemacht werden kann durch validierte Zyklen, aber „autoklavierbar“ allein bedeutet nicht „derzeit steril“ oder „für die pharmazeutische Verwendung geeignet“. Ein Polyesterhandtuch in Verbraucherqualität übersteht zwar das Autoklavieren, erzeugt aber 10.000 Partikel/m² und verliert Fasern – technisch gesehen autoklavierbar, funktionsungeeignet.
Beschaffungsspezifikationen müssen die Materialfähigkeit („autoklavierbar bis 121 °C für 50 Zyklen pro Validierungsdaten“) von den Prozessergebnissen („sterilisiert bis SAL 10⁻⁶ pro validiertem Zyklus“) und der Leistungserhaltung („Partikelerzeugung“) trennen <100/m² erhalten durch qualifizierte Nutzungsdauer“).
Warum wiederverwendbare Werkzeuge wiederholten Zyklen standhalten müssen
Sterile Einmalmopps (gammabestrahlt, einzeln verpackt) erreichen durch die Validierung des Herstellers einen SAL von 10⁻⁶ und vermeiden das Problem der Zyklenzählung vollständig. Wiederverwendbare autoklavierbare Systeme müssen jedoch ihre Leistung über mehr als 50 bis 200 Zyklen aufrechterhalten, um Kapitalinvestitionen und betriebliche Komplexität zu rechtfertigen.
Wirtschaftsmotor: Reusable mops cost \$60–\$150 per head but deliver \$1–\$3 per use when amortized over 100–200 uses (including laundering and autoclave costs). Single-use mops cost \$15–\$30 per use. For a 1,000 m² Grade C area mopped 5× per week (260 uses/year), reusable systems save \$3,000–\$7,000 annually per mop. Facilities mopping large areas (pharmaceutical manufacturing suites, biologics production zones, device assembly cleanrooms) realize five-figure annual savings with reusable systems—but only if mops survive the full qualified cycle count without premature failure.
Betriebsfahrer: Einrichtungen mit hauseigenen Autoklaven und Wäschereien können wiederverwendbare Mopps über Nacht produzieren und so tägliche Reinigungspläne ohne große Lagerpuffer unterstützen. Gamma-sterilisierte Einwegmopps erfordern Vorlaufzeiten des Lieferanten von 2–4 Wochen und größere Sicherheitsbestände, was die Bestandsverwaltung bei Mehrschichtbetrieben erschwert.
Regulatorischer Treiber: Anhang 1 Abschnitt 4.20 definiert die Lebensdauer von Verbrauchsmaterialien als „den Zeitraum oder die Anzahl der Zyklen, für die ein Reinraum-Verbrauchsmaterial zur Verwendung geeignet ist.“ Die Qualitätssicherung muss Zyklusgrenzen, Degradationsüberwachung und Ausmusterungskriterien dokumentieren. Mopps, die für 50 Zyklen ausgelegt sind, aber 80 Zyklen lang ohne erneute Qualifizierung verwendet werden, führen zu Audit-Ergebnissen – auch wenn sie optisch „gut aussehen“.
Missverständnisse: „Autoklavierbar“ ≠ „Immer aseptisch geeignet“
Marketing materials tout “autoclavable” as a premium feature, implying suitability for aseptic manufacturing. Regulatory reality is more nuanced:
Misconception 1: All autoclavable materials are equivalent. Materials survive autoclaving through different mechanisms. Polyester relies on high glass transition temperature (Tg ~250°C) and hydrophobic structure resisting steam penetration. Polypropylene uses crystalline structure and heat-stabilizing additives. Microfiber polyester/polyamide blends depend on balanced copolymer ratios—slight formulation changes cause one material to last 100 cycles, another to fail after 20. “Autoclavable” without documented cycle validation is meaningless.
Misconception 2: If it doesn’t melt, it’s qualified. Dimensionsstabilität ist notwendig, aber unzureichend. Mopps können ihre Form behalten, während Faserschäden (Anstieg der Partikelerzeugung von 60 auf 300 Partikel/m²), chemischer Abbau (Verlust der Zugfestigkeit, Versprödung) oder Rückstände (Bindung von Desinfektionsmitteln, Bildung von Biofilm) auftreten. Bei der Leistungsqualifizierung werden die Partikelerzeugung, die mechanische Festigkeit und die mikrobielle Sauberkeit überwacht – nicht nur die visuelle Integrität.
Irrtum 3: Steril = für immer kontaminationsfrei. Die Sterilität gilt ab dem Zeitpunkt des Abschlusses der Sterilisation. Unkontrollierte Kühlung, nicht sterile Lagerung oder Verpackungsverletzungen führen zu einer Rekontamination. Anhang 1 verlangt, dass sterile Materialien „sofort verwendet“ oder unter validierten Bedingungen mit definierten Haltezeiten verpackt/gelagert werden. Autoklavierte Mopps, die aus der Kammer entnommen und unbedeckt gelassen werden, werden innerhalb weniger Stunden unsteril.
Missverständnis 4: Klasse C/D benötigt keine validierten autoklavierbaren Mopps. Während Anhang 1 ausdrücklich Sterilität für Klasse A/B vorschreibt, weiten Risikobewertungen der Kontaminationskontrollstrategie (CCS) die validierte Sterilisation zunehmend auf Klasse C/D aus, um die Migration von Keimen zu verhindern. In Umkleideräumen der Klasse D verwendete Wischmopps übertragen die Kontamination auf das Personal, das dann Produktionsbereiche der Klasse B betritt. QS-Teams, die komplette Reinigungsprogramme für Anlagen validieren, betrachten die Qualifizierung autoklavierbarer Werkzeuge als systemweite Anforderung und nicht nur als Spezifikation für die aseptische Zone.
Warum Pharma & Biologische Einrichtungen erfordern autoklavierbare Mopps
Compliance-Treiber: EU GMP Annex 1, ISO 14644, PDA TR 70
Die gesetzlichen Rahmenbedingungen stimmen in einer einzigen Anforderung überein: Reinigungswerkzeuge, die in klassifizierten Bereichen verwendet werden, müssen validiert sein, um keine Kontamination zu verursachen. Autoklavierbare Mopps erfüllen dies durch drei Kontrollwege:
EU GMP Annex 1 (gültig ab August 2023) legt die Sterilitätsbasislinie fest. Abschnitt 4.29: „Desinfektionsmittel und Reinigungsmittel sollten bei der Verwendung in Bereichen der Klassen A und B steril sein.“ Abschnitt 4.20 erstreckt sich auf Verbrauchsmaterialien: „Die verwendeten Materialien sollten so ausgewählt werden, dass die Entstehung von Partikeln und Mikroorganismen minimiert wird … Die Anzahl der Wasch-/Sterilisationszyklen, die Reinraumkleidung durchlaufen kann, sollte auf der Grundlage ihrer Qualifikation festgelegt werden.“ Autoklavierbare Mopps machen dies möglich, indem sie eine validierte Sterilisation und eine definierte Lebensdauer ermöglichen.
ISO 14644-5 (Betrieb) fordert, dass „Reinigungsprozesse validiert sein müssen“ und „die für die Reinigung verwendeten Materialien und Geräte für die Reinraumklassifizierung geeignet sein müssen“. ISO 14644-18 (Bewertung der Eignung von Verbrauchsmaterialien) liefert den Bewertungsrahmen: Verbrauchsmaterialien müssen kontrollierte Emissionen (Partikel, lebensfähige Organismen, chemische Rückstände) und eine dokumentierte Lebensdauer aufweisen. Autoklavierbare Systeme erfüllen die ISO-Anforderungen, indem sie Materialqualifizierung (geringe Partikelerzeugung) mit Sterilisationsvalidierung (Biobelastungskontrolle) kombinieren.
PDA Technical Report 70 (Reinigungsvalidierung) befasst sich mit der Wiederaufbereitung wiederverwendbarer Reinigungswerkzeuge. TR 70 legt fest, dass Einrichtungen Wasch-/Sterilisationsprozesse validieren müssen, um Schmutz, Rückstände und Keimbelastung bis zu definierten Grenzwerten zu entfernen, nachweisen müssen, dass die Wiederaufbereitung die Werkzeugleistung (Partikelerzeugung, Saugfähigkeit, strukturelle Integrität) nicht beeinträchtigt, und Kriterien für die Ausmusterung festlegen müssen (maximale Zyklen, Inspektionskontrollpunkte). Validierungsprotokolle für autoklavierbare Mopps setzen die TR 70-Richtlinien direkt um.
Verhinderung der Übertragung biologischer Belastung zwischen Räumen der Klassen A/B/C
Pharma facilities are zoned by contamination risk: Grade A aseptic cores (filling needles, stopper bowls) operate under unidirectional airflow with the tightest particle and microbial limits; Grade B backgrounds (rooms surrounding Grade A) provide secondary protection; Grade C supports aseptic processing preparation; Grade D covers final packaging and non-sterile compounding.
Non-sterile or inadequately sterilized mops create bioburden migration pathways:
Scenario 1: Grade C → Grade B contamination. A mop used in a Grade C material prep area (bioburden limit: ≤100 CFU/m³ active air) picks up environmental organisms (spore-forming Bazillus Arten, umweltbedingte Schimmelpilze, Hautflora, die von in Kitteln gekleidetem Personal abgestoßen wird). Wenn der Mopp mit 70 % IPA „desinfiziert“, aber nicht sterilisiert wird, bleiben überlebende Sporen lebensfähig. Der gleiche Mopp, der in der Klasse B verwendet wird (Biobelastungsgrenze: ≤ 10 KBE/m³), bringt Sporen in Böden ein, die direkt an Zonen der Klasse A angrenzen. Sporen zerstäuben beim Wischen, verunreinigen Kittel und gelangen beim Eintritt von Personal/Material in Klasse A.
Szenario 2: Kreuzkontamination zwischen Produktlinien. Eine Anlage stellt in einer Suite Antibiotika auf Penicillinbasis und in einer anderen Suite Cephalosporin-Antibiotika her. Eine Beta-Lactam-Kreuzkontamination ist ein behördliches Warnsignal; Selbst Spuren von Penicillin in Cephalosporin-Produkten lösen bei sensibilisierten Patienten allergische Reaktionen aus. Mopps, die in Penicillin-Bereichen verwendet und dann mit Reinigungsmittel „gereinigt“ werden, behalten API-Rückstände, die in Cephalosporin-Bereiche wandern. Die Sterilisation im Autoklaven bei 121 °C in Kombination mit validierter Wäsche entfernt Rückstände unterhalb der HPLC-Nachweisgrenzen und unterbricht so die Kreuzkontaminationskette.
Szenario 3: Biofilmbildung in nicht sterilisierten Werkzeugen. Feucht oder unvollständig sterilisiert gelagerte Mopps entwickeln Biofilme – von einer Matrix umhüllte Mikrobengemeinschaften, die gegen Desinfektionsmittel resistent sind. Pseudomonas, Burkholderia und andere wasserassoziierte Organismen besiedeln Moppfasern, Eimerinnenräume und Wringmechanismen. Biofilmbakterien lösen sich während der Nutzung auf, verunreinigen Böden und führen zu Fehlern bei der Umgebungsüberwachung. Autoklavenzyklen zerstören Biofilme durch thermische Zerstörung und Dampfdurchdringung und verhindern so chronische Kontaminationsquellen.
Autoklavierbare Systeme verhindern diese Szenarien, indem sie sicherstellen, dass jeder Mopp, der in einen klassifizierten Bereich gelangt, einen SAL-Wert von 10⁻⁶ aufweist, wodurch lebensfähige Verunreinigungen vor der Verwendung beseitigt werden.
Gewährleistung der Integrität des Desinfektionsmittels – kein Ausscheiden, keine auslaugbaren Stoffe
Die Wirksamkeit des Desinfektionsmittels hängt von der Konzentration, der Kontaktzeit und der Abwesenheit von Störungen ab. Moppmaterialien wirken sich auf alle drei aus:
Durch die Partikelabgabe werden Desinfektionsmittel neutralisiert. Mopps erzeugen mehr als 1.000 Partikel/m² und geben Faserfragmente, Textilreste und Polymerpartikel in Desinfektionslösungen ab. Die Partikel adsorbieren quartäre Ammoniumverbindungen (Quats) und reduzieren so die Konzentration des freien Wirkstoffs unter die validierten Wirksamkeitsschwellen. Wasserstoffperoxid zersetzt sich auf Zellulosefasern und bestimmten Polymeroberflächen. Autoklavierbares Polyester mit versiegelten Kanten entsteht <100 Partikel/m², wodurch die Bindung des Desinfektionsmittels minimiert und die Aktivität der Lösung während des gesamten Reinigungszyklus aufrechterhalten wird.
Chemische Stoffe beeinträchtigen die Sterilitätssicherheit. Einige Polymere setzen Weichmacher, Stabilisatoren oder Abbauprodukte frei, die Desinfektionsmittel inaktivieren oder das mikrobielle Wachstum fördern. Durch minderwertiges Polypropylen werden Antioxidantien ausgelaugt, die Sporizide auf Peroxidbasis neutralisieren. Mikrofaser-Polyamid-Komponenten können Nylon-Oligomere auslaugen. Autoklavierbare Materialien in pharmazeutischer Qualität sind auf extrahierbare/auslaugbare Stoffe validiert (E&L) per ICH Q3D and USP <661>, sodass keine Beeinträchtigung durch Reinigungsmittel gewährleistet ist.
Die Faserretention verhindert Kreuzkontaminationen. Nicht autoklavierbare Mikrofasermopps zerfallen zu klebrigen, rückstandshaltigen Oberflächen, die API-Pulver, Reinigungsmittel und mikrobielle Verunreinigungen binden. Validiertes autoklavierbares Polyester verhindert durch glatte Faseroberflächen und hydrophobe Chemie das Anhaften von Rückständen, was eine gründliche Reinigung ermöglicht und eine Verschleppung zwischen den Anwendungen verhindert.
Risikominderung für Fehler bei der Umgebungsüberwachung
Umweltüberwachungsprogramme (EM) verfolgen Partikelzahlen, lebensfähige Luft-/Oberflächenproben und die mikrobielle Kontamination des Personals. EM-Ausfälle im Zusammenhang mit Reinigungswerkzeugen folgen drei Mustern:
Partikelwanderungen beim Wischen. Nicht validierte Mopps erzeugen Partikelstöße, wenn sie nass gemacht, ausgewrungen oder über den Boden gezogen werden. Bereiche der ISO-Klasse 5 (≤3.520 Partikel ≥0,5 µm/m³) haben einen Nullabstand; Ein Wischmopp, der 500 Partikel/m² abgibt, führt vorübergehend zu einer Überschreitung der Grenzwerte auf Bodenhöhe. Selbst wenn die Abweichung innerhalb von 30 Minuten behoben wird (HEPA-Filtration entfernt Partikel), löst sie Untersuchungszyklen, CAPA-Dokumentation und mögliche Produktionsstopps aus. Autoklavierbare, fusselarme Polyestermopps <50 Partikel/m² beseitigen diesen Fehlermodus.
Die Keimbelastung nach der Reinigung nimmt zu. EM failures occur when surface swabs or contact plates show higher CFU counts after cleaning than before—evidence that mops redistributed contamination rather than removing it. Root causes: inadequate sterilization (mops harboring bioburden), biofilm growth in mop systems, or disinfectant inactivation by contaminated tools. Autoclave-validated mops at SAL 10⁻⁶ eliminate the “contaminated tool” variable, simplifying investigations and reducing false-positive findings.
Chronic low-level bioburden trends. In Betrieben, in denen nicht sterilisierte wiederverwendbare Mopps verwendet werden, kommt es häufig zu einer anhaltenden Keimbelastung der Klasse C/D (30–50 KBE/m³ Luftproben, 10–20 KBE Kontaktplatten), die sich trotz validierter Desinfektionsprotokolle nicht verbessern lässt. Die Quelle: Mopps, die durch unvollständige Sterilisation resistente Organismen (Sporenbildner, Biofilmarten) ansammeln. Durch die Umstellung auf autoklavierbare Systeme mit validierten 121-°C-Zyklen wird die Ausgangskeimbelastung in der Regel um 50–70 % reduziert, wodurch die EM-Konformitätsmargen verbessert werden.
Validierungsanforderungen: Hitzebeständigkeit, Partikelablösung
Pharma-QA-Teams, die autoklavierbare Mopps qualifizieren, müssen vier Leistungsmerkmale dokumentieren:
1. Hitzebeständigkeit bei qualifizierter Zyklenzahl. Zu den IQ/OQ/PQ-Protokollen gehören:
- IQ: Überprüfen Sie die Materialspezifikationen (Polyesterfasertyp, Konstruktion mit versiegelten Kanten, Rahmen-/Griffmaterialien), bestätigen Sie die Autoklavenkalibrierung und die Chargenqualifikation für biologische Indikatoren
- OQ: Führen Sie 3–5 aufeinanderfolgende Autoklavenzyklen bei 121 °C/30 Min. mit Moppbeladungen durch, platzieren Sie BIs an kalten Stellen (Mitte dicht gepackter Moppbündel), bestätigen Sie, dass alle BIs inaktiviert sind und die parametrischen Grenzwerte erfüllt sind (mindestens F₀ ≥8 Min.)
- PQ: Testen Sie die Moppleistung bei 0 Zyklen (neu), 25–30 Zyklen (mittlere Lebensdauer) und 50–100 Zyklen (Ende der qualifizierten Lebensdauer); Messung der Partikelerzeugung gemäß ISO 14644-14, visuelle Inspektion (Risse, Kantenverschlechterung, Verfärbung), mechanische Festigkeit (Zugprüfung, Abriebfestigkeit)
2. Stabilität der Partikelabgabe. ISO 14644-14 (Beurteilung der Eignung für den Einsatz von Geräten anhand der Partikelkonzentration in der Luft) sieht die Testmethode vor: Betreiben Sie Wischmoppköpfe in einer kontrollierten Umgebung mit optischen Partikelzählern, die die nachgeschalteten Konzentrationen messen. Akzeptanzkriterien: <100 Partikel ≥0,5 µm/m² für den Einsatz der ISO-Klasse 5–7, <200 Partikel/m² für Klasse 8. Qualifizierungstests testen Mopps zu Beginn ihrer Lebensdauer und nach jeweils 20–25 Autoklavenzyklen, um eine Verschlechterung festzustellen. Mopps, deren Partikelgrenzwerte überschritten werden, werden ausgemustert, auch wenn sie ihre körperliche Unversehrtheit bewahren.
3. Dimensionsstabilität und funktionelle Leistung. Autoklavieren führt bei minderwertigen Materialien zu einer Polymerschrumpfung. Messen Sie die Abmessungen des Moppkopfes (Länge, Breite, Dicke) vor und nach 10, 30, 50, 80 und 100 Zyklen; Definieren Sie Toleranzgrenzen (typischerweise ±5 % Maßänderung). Testfunktionsparameter: Flüssigkeitsaufnahmefähigkeit (pro Gramm Trockengewicht zurückgehaltene ml), Auswringeffizienz (% unter standardisiertem Druck abgegebene Flüssigkeit) und Sicherheit der Rahmenbefestigung (erforderliche Zugkraft, um den Mopp vom Rahmen zu lösen). Eine Verschlechterung über definierte Grenzen hinaus führt zur Pensionierung.
4. Desinfektionsmittelkompatibilität nach dem Autoklavieren. Pharmazeutische Reinigungsprogramme wechseln Desinfektionsmittel (IPA, Quats, Peroxid, Bleichmittel), um mikrobieller Resistenz vorzubeugen. Validierungstests simulieren die aufeinanderfolgende Exposition im ungünstigsten Fall: Autoklav → 70 % IPA → Autoklav → 5 % H₂O₂ → Autoklav → 1000 ppm Bleichmittel → Autoklav, Wiederholung über 50 Zyklen. Bestätigen Sie, dass die Partikelerzeugung, die visuelle Integrität und die mechanische Festigkeit innerhalb der Akzeptanzkriterien bleiben. Materialien, die die Prüfung nur im Autoklaven bestehen, aber die kombinierte Belastung durch Autoklav und Chemikalien nicht bestehen, werden disqualifiziert.

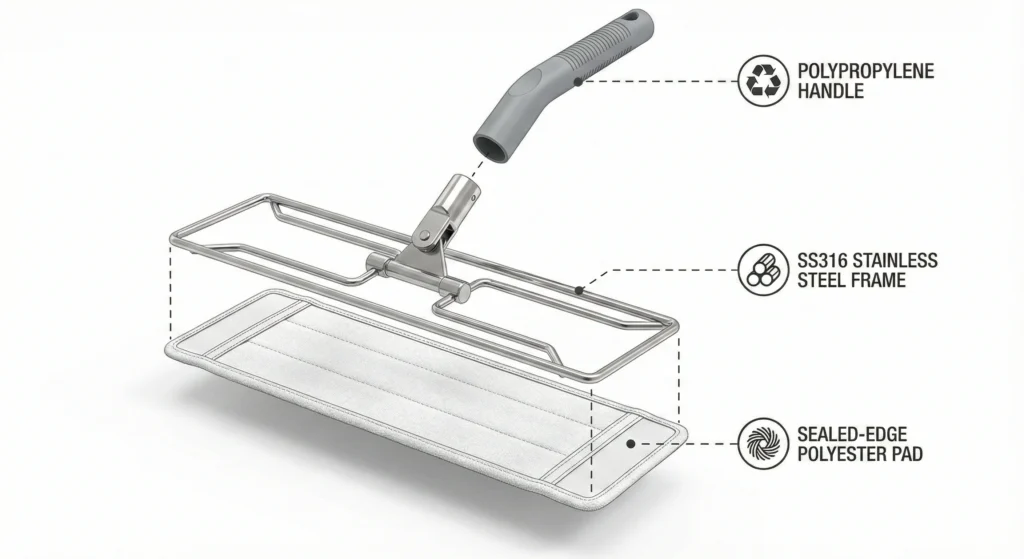
Abbildung 2: Polyester-Moppkopf mit versiegelten Kanten, heißversiegelter Umfangskonstruktion und Aluminiumrahmenbefestigung. Versiegelte Kanten verhindern das Ablösen von Fasern und die Bildung von Partikeln <100 Partikel/m² durch 50–100 Autoklavenzyklen bei 121 °C. Diese Konstruktion ist für die pharmazeutische GMP-Konformität gemäß den Anforderungen der ISO 14644-14 zur Partikelerzeugung von entscheidender Bedeutung.
Zum Autoklavieren geeignete Materialien (Pads + Rahmen + Griffe)
Wischpads aus Polyester mit versiegelten Kanten
Polyester dominiert bei pharmazeutischen autoklavierbaren Moppköpfen, da es auf einzigartige Weise Hitzebeständigkeit, chemische Kompatibilität und geringe Partikelbildung vereint.
Materialchemie: Polyethylenterephthalat (PET)-Polyester hat eine Glasübergangstemperatur (Tg) von ~80 °C und einen Schmelzpunkt von ~260 °C. Bei Autoklaventemperaturen (121–134 °C) bleibt Polyester in seinem festen kristallinen Zustand, deutlich unter dem Schmelzpunkt. Die aromatische Struktur und die hydrophoben Esterbindungen des Polymers widerstehen der Hydrolyse durch Dampfeinwirkung. Hochmolekulares Endlosfilament-Polyester (wird in Mopps in pharmazeutischer Qualität verwendet) sorgt für die Zugfestigkeit >70 % nach 100 Autoklavenzyklen.
Konstruktion mit versiegelten Kanten: Entscheidend für die Partikelkontrolle. Schnittkanten legen Faserenden frei, die beim Wischen ausfransen und Partikel abgeben. Wischpads in pharmazeutischer Qualität verwenden heißversiegelte Ränder (lasergeschnitten und thermisch gebunden) oder Ultraschallschweißen, um alle Kanten zu verkapseln. Einige Designs verwenden Endlosmaschenstricken (Röhrenkonstruktion ohne Schnittkanten). Versiegelte Kanten verhindern ein Auflösen und die Bildung von Partikeln <80 Partikel/m² bei 50–100 Zyklen.
Leistungsangaben:
- Haltbarkeit im Autoklaven: 50–100 Zyklen bei 121 °C/30 Min. (Standard-Polyester), 100–150 Zyklen (Premium-Endlosfilament-Polyester)
- Partikelerzeugung: <50 Partikel ≥0,5 µm/m² (neu), <100 Partikel/m² (nach 50 Zyklen)
- Chemische Kompatibilität: Beständig gegen 70 % IPA, 3–10 % H₂O₂, Quats bis zu 2000 ppm, Natriumhypochlorit bis zu 1 % (höhere Bleichmittelkonzentrationen führen zu allmählicher Vergilbung und Festigkeitsverlust, bleiben aber erhalten <100 Partikel/m² durch qualifizierte Lebensdauer)
- Saugfähigkeit: 4–6× Trockengewicht (geringer als Mikrofaser, aber ausreichend für die Anwendung von pharmazeutischen Desinfektionsmitteln)
- Kosten: \$60–\$150 per mop head (40–60 cm width)
Beschaffungsvorgaben: „100 % Polyester oder Polyester-dominante Mischung (≥90 %), Endlosfilamentkonstruktion, versiegelte Kanten (heißversiegelt, ultraschallgeschweißt oder Endlosstrick), geeignet für 50–100 Autoklavenzyklen bei 121 °C gemäß Herstellervalidierungsdaten, Partikelerzeugung <100/m² gemäß ISO 14644-14 durch qualifizierte Nutzungsdauer aufrechterhalten.“
Mikrofasermischungen (Vorsichtsmaßnahmen & Qualifikationsanforderungen)
Mikrofasermopps (Polyester/Polyamid-Mischungen, typischerweise 80/20 oder 70/30) bieten im Vergleich zu 100 % Polyester eine überlegene Saugfähigkeit (6–8-faches Trockengewicht) und Schmutzaufnahme. Allerdings stellt Mikrofaser die Autoklavenvalidierung vor Herausforderungen:
Abbau von Polyamid (Nylon).: Polyamid 6 und 6,6 (übliche Mikrofaserbestandteile) haben eine geringere Hitzebeständigkeit als Polyester. Der Tg-Wert von Nylon beträgt 50–60 °C mit Schmelzpunkten von 220–260 °C – näher an den Autoklaventemperaturen. Wiederholte Einwirkung von 121 °C führt zu Kettenspaltungen (Molekulargewichtsreduzierung), Versprödung und Faserverschmelzung. Die REM-Aufnahme von Mikrofasern nach 20 Autoklavenzyklen zeigt Filamentklumpen und Oberflächenschäden.
Beschleunigte Partikelerzeugung: Studien belegen, dass die Erzeugung von Mikrofaserpartikeln nach 20–40 Autoklavenzyklen von etwa 100 Partikeln/m² (neu) auf 300–800 Partikel/m² ansteigt, was die Leistung für Umgebungen der ISO-Klassen 5–7 ungeeignet macht. Die Split-Faser-Struktur (Mikrofasern werden mechanisch gespalten, um Risse zum Einfangen des Bodens zu erzeugen) delaminiert unter thermischer Belastung und setzt Faserfragmente im Submikronbereich frei.
Rückstandsretention: Beschädigte Mikrofasern werden klebrig und halten Desinfektionsmittelrückstände, API-Pulver und organischen Schmutz zurück. Dies erhöht das Risiko einer Keimbelastung (organische Rückstände fördern das Mikrobenwachstum) und das Risiko einer Kreuzkontamination (Übertragung von Rückständen zwischen Reinigungszyklen).
Begrenzte Lebensdauer: Pharmaceutical-grade microfiber qualified for autoclaving typically achieves 30–50 cycles—lower than polyester’s 50–100 cycles. Cost per use remains competitive due to lower unit cost (\$25–\$80 vs \$60–\$150 for polyester), but facilities must track cycle counts rigorously and retire mops earlier.
Empfohlene Anwendungen: Autoklavierbare Mikrofasermopps sind für Bereiche der ISO-Klasse 7–8 (Klasse C/D) geeignet, in denen höhere Saugfähigkeitsvorteile die verringerte Lebensdauer und Partikelbildung überwiegen <200/m² erfüllt die Klassifizierungsanforderungen. Für Anwendungen der Güteklasse A/B sollte Polyester verwendet werden; Das Risiko von Partikelexkursionen in der Mitte der Lebensdauer von Mikrofasern ist in aseptischen Zonen nicht akzeptabel.
Qualifikationsvoraussetzungen: Fordern Sie Validierungsdaten des Anbieters an, die Partikelerzeugungskurven von 0 bis zu qualifizierten End-of-Life-Zyklen (z. B. 0, 10, 20, 30, 40, 50 Zyklen), visuellen/REM-Nachweis der Faserintegrität und Dimensionsstabilitätstests zeigen. Erstellen Sie interne Zyklusverfolgungs- und Inspektionsprotokolle, um eine frühzeitige Verschlechterung zu erkennen.
Edelstahlrahmen
Mopprahmen verbinden Köpfe mit Griffen und müssen mehr als 200 Autoklavenzyklen ohne Korrosion, Verformung oder mechanisches Versagen überstehen.
Materialspezifikationen: Edelstahl SS316 (18 % Chrom, 14 % Nickel, 2,5 % Molybdän) oder SS304 (18 % Chrom, 8 % Nickel). SS316 bietet eine hervorragende Korrosionsbeständigkeit in Umgebungen mit hohem Chloridgehalt (wichtig für Einrichtungen, die Sporizide auf Bleichmittelbasis verwenden); SS304 ist für reine IPA/Quat/Peroxid-Programme geeignet.
Konstruktion: Continuous-bend or welded one-piece frames eliminate threaded connections and crevices that trap bioburden. Mop head attachment should use sealed pockets (polyester sleeves) or smooth clip mechanisms—no exposed Velcro or hook-and-loop fasteners that harbor contamination and shed particles.
Haltbarkeit im Autoklaven: SS316/SS304 withstand 200+ autoclave cycles at 121°C without functional degradation. Passivation (chemical treatment forming a protective chromium oxide layer) may be required after 100–150 cycles if surface discoloration or micro-pitting appears, but mechanical integrity and particle generation performance remain acceptable.
Kosten: \$70–\$200 per frame (40–60 cm width). Higher upfront cost than polypropylene (\$25–\$80), but amortized over 200+ cycles vs 50–100 cycles for PP, stainless steel offers lower total cost of ownership.
Beschaffungsvorgaben: „Edelstahl SS316 oder SS304, einteilig geschweißte oder kontinuierlich gebogene Konstruktion, versiegelte Moppkopfbefestigung (kein freiliegender Klettverschluss), elektropolierte oder passivierte Oberflächenveredelung, geeignet für mehr als 200 Autoklavenzyklen bei 121 °C.“
Rahmen aus eloxiertem Aluminium (Einschränkungen)
Anodized aluminum frames offer lighter weight (150–250g vs 300–500g for stainless steel) and lower cost (\$40–\$120), but present qualification challenges:
Autoklaveninduzierte Korrosion: Anodisierung (elektrochemische Oxidbeschichtung) schützt Aluminium vor Oxidation, aber 121 °C heißer Dampf baut die anodische Schicht allmählich ab. Wiederholte Zyklen führen zu Lochfraß, Bildung von weißem Oxid und Oberflächenrauheit, wodurch die Partikelbildung zunimmt und Keime entstehen.
Begrenzte Lebensdauer: Rahmen aus eloxiertem Aluminium in Pharmaqualität überstehen in der Regel 50–100 Autoklavenzyklen, bevor sie durch Oberflächenverschlechterung disqualifiziert werden. Dies entspricht der Lebensdauer des Polyester-Moppkopfes und ermöglicht eine synchronisierte Ausmusterung, bietet jedoch keinen Vorteil gegenüber Polypropylen-Rahmen mit ähnlichen Kosten.
Chemische Unverträglichkeit: Aluminium korrodiert in alkalischen Umgebungen schnell. Einrichtungen, die alkalische Waschmittel oder Natriumhypochlorit (Bleichmittel, das durch Hydrolyse Alkalinität erzeugt) verwenden, sollten auf Aluminiumrahmen verzichten. Sogar eloxierte Oberflächen versagen bei anhaltender Bleicheinwirkung.
Empfohlene Anwendungen: Anwendungen der ISO-Klasse 7–8 mit nur IPA/Quat-Desinfektionsprogrammen und gewichtsempfindlichen Arbeitsabläufen (z. B. Deckenwischen, Wandreinigung, die Griffe mit größerer Reichweite erfordern). Bei Anwendungen der Güteklasse A/B sollte Edelstahl verwendet werden, um Korrosionsrisiken in der Mitte der Lebensdauer zu vermeiden.
Autoklavierbare Polypropylengriffe
Griffe verbinden Rahmen mit Bedienern und müssen autoklavierbar, ergonomisch und gegen das Eindringen von Keimen abgedichtet sein.
Materialspezifikationen: Hochtemperatur-Polypropylen (PP), formuliert mit Wärmestabilisatoren, typische Glasübergangstemperatur ~0 °C und Schmelzpunkt ~165 °C. Standard-PP schmilzt oder verzieht sich bei 121 °C; Autoklavierbares PP in pharmazeutischer Qualität verwendet Copolymere und Stabilisatoren, um die Steifigkeit bei Sterilisationstemperaturen aufrechtzuerhalten.
Konstruktion: Einteiliges Extrusions- oder Spritzgussdesign ohne Hohlräume oder Gewindekappen, die Feuchtigkeit und Keime einschließen. Für die Rahmenbefestigung sollten abgedichtete Gewindeverbindungen mit autoklavierbaren Dichtungen oder einteilig geformte Rahmen-Griff-Baugruppen verwendet werden.
Haltbarkeit im Autoklaven: Hochtemperatur-PP hält 50–100 Zyklen bei 121 °C stand. Der Abbau äußert sich in Sprödigkeit, Oberflächenrissen und Gewindeabriss an den Befestigungspunkten. Eine visuelle Inspektion alle 20–25 Zyklen erkennt frühe Fehlerzeichen.
Griffe aus Edelstahl vs. Polypropylen: SS316 handles (120–150 cm, \$80–\$150) withstand 200+ cycles and offer superior chemical resistance, but are heavier (400–600g) and costlier. Autoclavable PP handles (\$30–\$70, 150–250g) provide ergonomic benefits and adequate service life for Grade C/D applications. Facilities should match handle cycle life to frame cycle life—pairing 50-cycle PP handles with 200-cycle stainless frames creates waste; pairing 100-cycle PP with 100-cycle polyester mops optimizes synchronized retirement.
Beschaffungsvorgaben: „Autoklavierbares Polypropylen (Hochtemperaturformulierung) oder SS316-Edelstahl, einteilige versiegelte Konstruktion, geeignet für ≥50 Autoklavenzyklen bei 121 °C, Rahmenbefestigungsgewinde mit autoklavierbaren Dichtungen abgedichtet.“
Kompatibilität mit Desinfektionsmitteln (IPA, H₂O₂, QAC)
Autoklavierbare Materialien müssen der Rotation mit pharmazeutischen Desinfektionsmitteln ohne kumulativen Abbau standhalten:
70 % Isopropylalkohol (IPA): Täglicher Einsatz in Bereichen der Klasse A/B/C. Polyester, Edelstahl und autoklavierbares PP weisen eine hervorragende Kompatibilität auf – keine Schwellung, Verfärbung oder Festigkeitsverlust nach mehr als 100 Einwirkungszyklen. Mikrofaser-Polyamid kann leicht aufquellen, bleibt aber funktionsfähig.
Wasserstoffperoxid (H₂O₂, 3–10 %): Wöchentliche sporizide Reinigung. Polyester und SS316 widerstehen der Peroxidoxidation. Autoklavierbares PP zeigt nach mehr als 50 Peroxid-Einwirkungen eine allmähliche Auskreidung (Weißfärbung) der Oberfläche, behält aber seine mechanische Integrität bei. Mikrofaser-Polyamid zersetzt sich schneller – gelbliche Verfärbung und Festigkeitsverlust nach 30–50 Zyklen. Die kombinierte Belastung durch Autoklav und Peroxid beschleunigt den Mikrofaserabbau; Begrenzen Sie die Gesamtzahl der Zyklen bei Peroxid-Rotationsprogrammen auf 30–40.
Quartäre Ammoniumverbindungen (Quats, 200–2000 ppm): 2–3× wöchentlich allgemeine Desinfektion. Gut verträglich mit allen autoklavierbaren Materialien. Rückstandsmanagement ist entscheidend – Quats bilden Filme auf Oberflächen, die die nachfolgende Desinfektionsaktivität verringern. Validierte Waschprotokolle müssen Quat-Rückstände zwischen den Anwendungen entfernen.
Natriumhypochlorit (Bleichmittel, 500–5000 ppm): Breitbandiger sporizider Einsatz 1–2× wöchentlich. Polyester widersteht Bleichmitteln, zeigt jedoch nach mehr als 50 Belastungen eine allmähliche Vergilbung und einen Zugfestigkeitsverlust von 20–30 % >1000 ppm. SS316 ist beständig gegen Chloridkorrosion; Bei SS304 kann es nach mehr als 100 Belastungen mit mehr als 2000 ppm zu Lochfraß kommen. Sowohl autoklavierbares PP als auch Mikrofaser werden in Bleichmitteln schnell abgebaut – Oberflächenrisse, Sprödigkeit und beschleunigte Partikelbildung. Einrichtungen mit stark bleichmittelhaltigem CCS sollten SS316-Rahmen und Moppköpfe aus 100 % Polyester verwenden und die Lebensdauer des Mopps bei Bleichmittel auf 50–70 Zyklen begrenzen >1000 ppm werden routinemäßig verwendet.
Validierungsansatz: Erstellen Sie eine Kompatibilitätsmatrix, die das Bestehen/Nichtbestehen für jede Kombination aus Material und Desinfektionsmittel dokumentiert. „Bestanden“ ist definiert als: keine sichtbare Beeinträchtigung (Risse, Vergilbung, Änderung der Oberflächenstruktur über akzeptable Grenzen hinaus), Partikelbildung <100/m² erhalten, mechanische Festigkeit erhalten >70 %, nach 50 Zyklen der schlimmsten aufeinanderfolgenden Exposition (Autoklav → Desinfektionsmittel → Autoklav).
Autoklaventemperatur & Zyklusbeschränkungen (Validierung erklärt)
121 °C / 20–30 Min. Standardzyklen
Der 121°C/15–30-Minuten-Zyklus ist das Arbeitspferd des pharmazeutischen Autoklavierens und bringt validierte Letalität mit Materialschonung in Einklang.
Zyklusparameter: 121°C (250°F) saturated steam at 15 psi gauge pressure (103 kPa above atmospheric), exposure time 15–30 minutes depending on load density and steam penetration requirements. F₀ (cumulative lethality equivalent to 121°C exposure) typically reaches 8–15 minutes for porous loads like mop heads.
Why 121°C: At this temperature, G. stearothermophilus spores (the biological indicator standard for steam sterilization) exhibit D-value ~1.5 minutes (time to achieve 1-log or 90% reduction). A 15-minute exposure delivers 10-log reduction; 30 minutes provides 20-log reduction—massive overkill ensuring SAL 10⁻⁶ even with high bioburden or poor steam penetration.
Material tolerance: Polyester, SS316 und autoklavierbares PP vertragen alle 121 °C ohne akute Schäden. Dies ist die Qualifikationsgrundlage: Materialien, die bei 121 °C versagen, werden unabhängig von Kosten- oder Leistungsvorteilen disqualifiziert.
Zyklusqualifikation: IQ/OQ validiert die Autoklavenausrüstung (Temperaturverteilung, Dampfqualität, Integrität der Türdichtung). PQ validiert spezifische Ladungen: Verpacken Sie die Moppköpfe in der Worst-Case-Konfiguration (maximale Anzahl, engste Anordnung, verpackt, wenn sie in der Praxis verwendet werden), platzieren Sie BIs in der geometrischen Mitte und am Rand, führen Sie drei aufeinanderfolgende Zyklen durch, bestätigen Sie, dass alle BIs inaktiviert sind und an allen Sensorpositionen die minimale F₀ erreicht wird. Dokumentieren Sie Zyklusaufzeichnungen (Zeit-/Temperatur-/Druckdiagramme) und BI-Ergebnisse für behördliche Inspektionen.
134 °C kurze Zyklen
In einigen pharmazeutischen Einrichtungen wird eine Hochtemperatur-Kurzzyklussterilisation (134 °C/3–10 Minuten) eingesetzt, um den Autoklavendurchsatz zu erhöhen.
Zyklusparameter: 134 °C (273 °F) bei 30 psi Überdruck (207 kPa über Atmosphäre), Einwirkungszeit 3–10 Minuten. F₀-Äquivalenz: 3 Minuten bei 134 °C liefern ungefähr die gleiche Letalität wie 30 Minuten bei 121 °C (aufgrund der exponentiellen Beziehung zwischen Temperatur und D-Wert pro Z-Wert ~10 °C für Sporen).
Materielles Risiko: Höhere Temperaturen beschleunigen den Polymerabbau. Polyester behält seine Integrität bei, zeigt jedoch ein schnelleres Verblassen der Farbe und einen schnelleren Verlust der Zugfestigkeit – Lebensdauer von 50 Zyklen bei 134 °C gegenüber 100 Zyklen bei 121 °C. Autoklavierbares PP nähert sich seinem Schmelzpunkt (165 °C); Die Lebensdauer sinkt auf 30–50 Zyklen, es besteht die Gefahr von Verformungen, wenn die Kammertemperatur zu stark ansteigt oder die Abkühlung zu schnell erfolgt. Mikrofaser-Polyamid zersetzt sich stark – nach 10–20 Zyklen bei 134 °C kommt es zu einer verstärkten Faserverschmelzung und Partikelbildung.
Empfohlene Anwendungen: 134°C-Zyklen sind für Edelstahlrahmen/-griffe (keine Beeinträchtigung) und Premium-Endlosfilament-Polyestermopps akzeptabel, bei denen eine Lebensdauer von 50 Zyklen ausreichend ist. Vermeiden Sie 134 °C für Komponenten aus Mikrofaser, Polyester in Standardqualität und Polypropylen. Wenn Anlagenautoklaven für andere Ladungen (chirurgische Instrumente, Glaswaren) bei 134 °C betrieben werden, richten Sie separate 121 °C-Zyklen für Reinraum-Mopps ein oder nehmen Sie eine verkürzte Lebensdauer in Kauf und verfolgen Sie die Zyklenanzahl entsprechend.
Validierung: Gleicher IQ/OQ/PQ-Rahmen wie 121°C-Zyklen. BI-Platzierung kritisch – 134 °C verringert den Sicherheitsspielraum für kalte Stellen. Zur Bestimmung der tatsächlichen Zyklusgrenzen müssen Lebensdauerstudien bei 134 °C durchgeführt werden; Nicht aus 121°C-Daten extrapolieren.
Wiederholte Exposition im Autoklaven & Altersstudien
Materialien zersetzen sich im Laufe der Autoklavenzyklen kumulativ. Die Bestimmung der Lebensdauer erfordert eine beschleunigte Alterungsvalidierung:
Studiendesign zum Altern: Testen Sie Mopps in regelmäßigen Abständen während der gesamten voraussichtlichen Nutzungsdauer – 0 Zyklen (Basislinie), 20 Zyklen, 40 Zyklen, 60 Zyklen, 80 Zyklen, 100 Zyklen – und messen Sie:
- Partikelerzeugung gemäß ISO 14644-14 (<100/m² Akzeptanzkriterium)
- Visuelle Integrität (Risse, Kantenverschlechterung, Verfärbung)
- Dimensionsstabilität (Länge, Breite, Dicke innerhalb von ±5 % des Originals)
- Mechanische Festigkeit (Zugversuch, Abriebfestigkeit)
- Funktionelle Leistung (Saugfähigkeit, Auswringleistung)
Zeichnen Sie Leistungsmetriken im Vergleich zur Zyklenzahl auf, um Abbaukurven zu identifizieren. Die Mopp-Lebensdauer ist definiert als die Anzahl der Zyklen, bei denen ein Parameter die Akzeptanzkriterien überschreitet – typischerweise, wenn die Partikelerzeugung 100/m² erreicht (bei Verwendung von ISO 5–7) oder die mechanische Festigkeit unter 70 % des Originals fällt.
Typische Abbaumuster:
- Polyester: Allmähliche Vergilbung nach 40–60 Zyklen (nur kosmetisch, keine funktionelle Beeinträchtigung); Partikelerzeugung stabil <80/m² bei 80 Zyklen, ansteigend auf 90–100/m² bei 100 Zyklen; Zugfestigkeit 85–90 % Beibehaltung bei 100 Zyklen. Lebensdauer: 80–100 Zyklen (Ausmusterung vor Überschreitung der Partikelgrenzwerte).
- Mikrofaser: Partikelerzeugung 100–150/m² bei 30 Zyklen, 200–400/m² bei 50 Zyklen; Faserverschmelzung unter Vergrößerung nach 20 Zyklen sichtbar; Die Saugfähigkeit sinkt nach 40 Zyklen um 20–30 %. Lebensdauer: 30–40 Zyklen.
- Autoklavierbare PP-Rahmen: Oberflächenrisse treten nach 60–80 Zyklen auf; Bei 80–100 Zyklen lösen sich Gewinde oder reißen. Lebensdauer: 70–80 Zyklen (Sichtprüfung alle 20 Zyklen, um frühzeitige Ausfälle zu erkennen).
Requalifizierungsauslöser: Wenn bei der Verwendung von Mopps eine unerwartete Verschlechterung auftritt (Partikelausbreitung, zerbrochene Rahmen, vorzeitige Verfärbung), stellen Sie die Verwendung ein und untersuchen Sie dies. Mögliche Ursachen: Temperaturüberschreitungen im Autoklaven, Probleme mit der Dampfqualität (überhitzter Dampf oder Nassdampf), Kontamination mit inkompatiblen Chemikalien (z. B. Bleichmittelexposition, die nicht Teil der ursprünglichen Validierung ist) oder Änderungen der Materialrezeptur des Herstellers. Führen Sie eine erneute Qualifizierung mit frischen Proben durch und ändern Sie bei Bedarf die Zyklusgrenzen.
Schrumpfungsrisiko bei minderwertigen Pads
Polymerschrumpfung durch Dampfeinwirkung ist eine häufige Fehlerursache bei nicht-pharmazeutischen Mopps:
Mechanismus: Polymere enthalten Eigenspannungen aus der Herstellung (Spinnen, Weben, Thermofixieren). Die Hitze im Autoklaven liefert Energie für die Entspannung der Polymerketten in Richtung energieärmerer Konformationen, was sich in Form einer Dimensionskontraktion äußert. Polyester minderer Qualität kann nach 5–10 Zyklen um 5–15 % in der Länge/Breite schrumpfen; Materialien in pharmazeutischer Qualität nutzen während der Herstellung eine kontrollierte Wärmehärtung und Spannungsarmglühen, um Restspannungen zu minimieren und die Schrumpfung zu begrenzen <3 % über 100 Zyklen.
Auswirkungen: Geschrumpfte Moppköpfe passen nicht mehr richtig auf die Rahmen, wodurch lose Befestigungspunkte entstehen, die durch Reibung Partikel erzeugen. Eine verringerte Oberfläche verringert die Bodenabdeckung und die Flüssigkeitskapazität. Enger Stoff erhöht die Steifigkeit, wodurch die Manövrierfähigkeit des Bedieners und die Effizienz der Partikelerfassung verringert werden.
Qualifikationsprüfung: Messen Sie die Abmessungen des Moppkopfes (Länge, Breite, Dicke an drei Stellen) bei 0, 10, 20, 30, 50 Zyklen. Akzeptanzkriterium: <5 % Dimensionsänderung durch qualifizierte Lebensdauer. Lehnen Sie Anbieter ab, die keine Schwundvalidierungsdaten bereitstellen können oder dies anzeigen >5 % Schrumpfung in den ersten 10 Zyklen (was auf eine unzureichende Wärmebehandlung bei der Herstellung hinweist).
Metallverformung in Nicht-Laborrahmen
Metallrahmen versagen durch Korrosion (bereits unter Aluminium besprochen) oder mechanische Verformung:
Versagen der Schweißverbindung: Rahmen mit Punkt- oder Heftnähten (anstelle von durchgehenden Schweißnähten) entwickeln nach 30–50 Autoklavenzyklen Spannungsrisse an den Schweißpunkten. Dampf dringt in Risse ein und beschleunigt Korrosion und Verbindungsversagen. Bei Rahmen in Pharmaqualität kommt eine kontinuierliche Schweißnaht oder eine einteilige gestanzte/gebogene Konstruktion zum Einsatz.
Fadenabziehen: An den Griffbefestigungspunkten mit Gewinde kommt es zu einer zyklischen thermischen Ausdehnung/Kontraktion. Edelstahl minderer Qualität (z. B. SS201, eine Sorte mit niedrigerem Nickelgehalt, die als „rostfrei“ vermarktet wird) oder weiche Aluminiumlegierungen entfernen die Gewinde nach 20–40 Zyklen. SS316 und hochfeste Aluminiumlegierungen bewahren die Gewindeintegrität über mehr als 200 Zyklen.
Verziehen: Dünnes Aluminium (<2 mm) oder gestanzte Stahlrahmen können sich unter Druckunterschieden im Autoklaven verziehen, insbesondere beim schnellen Abkühlen. Verzogene Rahmen führen zu ungleichmäßigem Bodenkontakt (verminderte Reinigungswirkung) und belasten die Befestigungspunkte des Moppkopfes (was zu Rissen führt).
Qualifikationsprüfung: Laden Sie die Rahmen bei maximaler Betriebsdichte in den Autoklaven, lassen Sie 20 Zyklen laufen, prüfen Sie sie auf Schweißrisse (Farbeindringprüfung), Gewindeschäden (Gut/Schlecht-Messgeräte) und Verzug (Ebenheitsmessung auf Referenzoberfläche). Abnahme: Keine sichtbaren Schäden, Gewindeeingriff >80 % des Originals, Ebenheitsabweichung <2 mm über die Rahmenlänge.
So geben Sie die Autoklavenvalidierung in der Beschaffung korrekt an
Beschaffungsspezifikationen müssen das Lieferantenmarketing von der validierungsbereiten Dokumentation trennen:
Erforderliche Lieferantendaten:
- Materialzusammensetzung: Genauer Polymertyp (z. B. „PET-Polyester, Endlosfilament, 150 Denier“, nicht „Polyestermischung“), Faserkonstruktion (Sealed-Edge-Methode, Strickmuster), Metallqualität (SS316, autoklavierbare PP-Formulierung)
- Qualifizierung für den Autoklavenzyklus: Temperatur-, Zeit-, Druck- und Lastkonfiguration, die bei der Anbietervalidierung verwendet wird; Anzahl der getesteten Zyklen (mindestens 50 für die Wiederverwendbarkeit); Akzeptanzkriterien für Partikelerzeugung, Dimensionsstabilität, mechanische Festigkeit
- Daten zur Partikelerzeugung: ISO 14644-14-Testberichte, die die Partikelanzahl bei 0, 25, 50, 75, 100 Zyklen (oder dem qualifizierten Grenzwert des Herstellers) zeigen; Testbedingungen (getränkter Mopp, 500 g Abtrieb, standardisiertes Strichmuster); Spezifikationen für optische Partikelzähler
- Lebensdauerbestimmung: Methode zur Festlegung von Zyklusgrenzen (Alterungsstudien, beschleunigte Tests, historische Felddaten); Ausmusterungskriterien (Partikelgrenzwert, visuelle Mängelliste, mechanische Festigkeitsschwelle)
- Konformitätsbescheinigungen: Chargenspezifisches CoC, das bestätigt, dass das Material der Spezifikation entspricht; Aufzeichnungen über den Autoklavenzyklus (sofern der Lieferant vorsterilisiert); Ergebnisse biologischer Indikatoren (falls zutreffend)
Beispiel einer Spezifikationssprache:
„Autoklavierbarer Reinraum-Moppkopf: 100 % Polyester-Endlosfilament, Konstruktion mit versiegelten Kanten (hitzeversiegelter oder ultraschallgeschweißter Umfang), qualifiziert für mindestens 50 Autoklavenzyklen bei 121 °C/30 Minuten pro Anbietervalidierungsstudie. Der Anbieter muss Folgendes vorlegen: (1) ISO 14644-14-Testbericht zur Partikelerzeugung, der die Dokumentation dokumentiert <100 Partikel ≥0,5 µm/m², aufrechterhalten durch qualifizierte Zyklenzählung, (2) Dimensionsstabilitätsdaten werden angezeigt <5 % Längen-/Breitenänderung durch qualifizierte Zyklen, (3) Materialanalysezertifikate, (4) Lebensdauerbestimmungsmethodik und Ausmusterungskriterien. Moppköpfe müssen mit losspezifischen Konformitätszertifikaten und einer Zyklusverfolgungsdokumentation geliefert werden, die eine Überwachung der Lebensdauer der Anlage ermöglicht.“
Warnsignale bei Lieferantenansprüchen:
- „Autoklavierbar“ ohne festgelegte Zyklusgrenzen oder Validierungsdaten
- „Getestet bis 121 °C“ ohne Dauer, Lastkonfiguration oder Leistungsmetriken
- Daten zur Partikelerzeugung nur für neue/unbenutzte Mopps (keine Alterungsstudie)
- „Reinraumtauglich“ ohne ISO-Klasse oder GMP-Qualitätsangabe
- Weigerung, Angaben zur Materialzusammensetzung oder zum Herstellungsprozess zu machen
Facilities should pilot-test small quantities (10–20 mop heads) with in-house autoclave validation before facility-wide adoption. QA-led testing identifies vendor data gaps and verifies performance under actual use conditions (facility-specific disinfectants, autoclave equipment, operator techniques).
Autoklavierbare oder Einweg-Reinraummopps – So wählen Sie
Vergleichstabelle
| Criterion | Autoclavable Reusable | Gamma-Sterilized Disposable |
| Cost per use | \$2–\$7 (system cost amortized over 50–200 uses + laundering/autoclave) | \$15–\$30 (single use, vendor-sterilized) |
| Sterilitätssicherung | SAL 10⁻⁶ via in-house autoclave validation; requires BI monitoring and parametric release | SAL 10⁻⁶ via vendor gamma irradiation (25–50 kGy); sterility certificates and dose records provided |
| Partikelerzeugung | <100 Partikel/m², wenn qualifiziert; baut sich je nach Material in 30–100 Zyklen ab; erfordert regelmäßige erneute Tests | <50 Partikel/m² (kein Abbaurisiko; durch die einmalige Verwendung entfällt die Alterungsvariable) |
| Risiko einer Kreuzkontamination | Niedrig bis mäßig; Durch validiertes Waschen werden Rückstände entfernt <HPLC-Nachweisgrenzen; erfordert eine Trennung nach Raum/Produkt | Null; Durch die einmalige Verwendung wird eine Verschleppung von Charge zu Charge vermieden |
| SOP-Komplexität | Hoch; erfordert Autoklaven-IQ/OQ/PQ, Zyklusverfolgung, Waschvalidierung, Lebensdauerüberwachung, Stilllegungsprotokolle | Niedrig; Nur Eingangskontrolle und Entsorgung |
| Inventar | Mäßig; 3- bis 5-fache tägliche Nutzungsmenge zur Unterstützung der Wasch-/Sterilisationsrotation (z. B. 30 Mopps für eine Einrichtung mit 10 Mopps pro Tag) | Hoch; 1–2-wöchiger Vorrat plus Sicherheitsbestand für Lieferantenvorlaufzeiten (z. B. 100–200 Mopps für eine Einrichtung mit 10 Mopps pro Tag) |
| Infrastruktur | Erfordert einen validierten Autoklaven, eine Wäscherei in pharmazeutischer Qualität (oder einen externen Service) und eine kontrollierte Lagerung | Keine Sterilisationsinfrastruktur; erfordert nur einen kontrollierten Speicher, der die Anforderungen an Paketintegrität/-ablauf erfüllt |
| Beste Anwendungen | ISO 6–8 großflächige Fertigung (>500 m² tägliches Wischen), Anlagen mit vorhandener Autoklavenkapazität, kostensensible Abläufe | Aseptische Kerne der ISO 5-Klasse A/B, Anlagen für mehrere Produkte/hochwirksame APIs, die kein Risiko einer Kreuzkontamination erfordern, Anlagen ohne Autoklavenkapazität |
| Umweltauswirkungen | Geringeres Abfallvolumen; Mehrwegsysteme erzeugen erst am Ende ihrer Nutzungsdauer Abfall | Höheres Abfallvolumen; Bei jeder Verwendung müssen Moppkopf und Verpackung entsorgt werden (einige Anbieter bieten Recyclingprogramme an). |
| Audit-Dokumentation | Umfangreich; Autoklaven-Validierungsaufzeichnungen, BI-Überwachungsprotokolle, Zyklusverfolgung, Lebensdauerstudien, Stilllegungsaufzeichnungen | Mäßig; Sterilitätszertifikate des Anbieters, Eingangskontrollprotokolle, Einhaltung der Lagervorschriften, Ablaufverfolgung |
Analyse der Gesamtbetriebskosten (TCO).
Szenario: 1.000 m² Produktionsfläche der Klasse C, 5x pro Woche gewischt (260 Nutzungen/Jahr)
Autoklavierbares Mehrwegsystem (5-Jahres-TCO):
- System cost: \$300 × 3 sets (rotation inventory) = \$900
- Mop head replacement: \$100 × 8 replacements (80-cycle life, 260 uses/year = 3.25 mop head lifecycles/year) × 5 years = \$4,000
- Laundering: \$1.50/cycle × 260/year × 5 years = \$1,950
- Autoclave: \$0.75/cycle (utilities, BI, operator time) × 260/year × 5 years = \$975
- Validation: \$8,000 (IQ/OQ/PQ, laundering validation, service life studies, one-time)
- Total 5-year cost: \$15,825 (\$3,165/year, \$12.17 per mopping event)
Gammasterilisiertes Einwegsystem (5-Jahres-TCO):
- Mop cost: \$22/unit × 260 uses/year × 5 years = \$28,600
- Disposal: \$0.50/unit × 260/year × 5 years = \$650
- Validation: \$1,000 (receiving inspection protocols, storage procedures, one-time)
- Total 5-year cost: \$30,250 (\$6,050/year, \$23.27 per mopping event)
Reusable system saves \$14,425 over 5 years (48% TCO reduction) for this scenario.
Szenario: 200 m² aseptischer Abfüllbereich der Klasse A/B, dreimal pro Woche gewischt (156 Anwendungen/Jahr)
Autoklavierbar und wiederverwendbar:
- System cost: \$350 × 3 = \$1,050
- Mop head replacement: \$120 × 5 replacements × 5 years = \$3,000
- Laundering: \$2/cycle (higher grade for aseptic tool laundering) × 156/year × 5 years = \$1,560
- Autoclave: \$1/cycle (dedicated aseptic tool autoclave) × 156/year × 5 years = \$780
- Validation: \$12,000 (higher validation burden for Grade A/B qualification)
- Investigation risk: 2 EM failures/5 years (reduced from 3 with non-validated tools) × \$8,000 avg cost = \$16,000
- Total 5-year cost: \$34,390 (\$6,878/year, \$44.10 per mopping event)
Gammasterilisierter Einwegartikel:
- Mop cost: \$28/unit × 156 uses/year × 5 years = \$21,840
- Disposal: \$0.50/unit × 156/year × 5 years = \$390
- Validation: \$2,000 (receiving/storage protocols)
- Investigation risk: 0.5 EM failures/5 years (lowest risk option) × \$8,000 = \$4,000
- Total 5-year cost: \$28,230 (\$5,646/year, \$36.17 per mopping event)
Disposable system saves \$6,160 (18% TCO reduction) for this high-risk, lower-volume application.
TCO-Entscheidungsrahmen: Wiederverwendbare Systeme erzielen ROI-Vorteile bei höheren Nutzungsvolumina (>200–300 Anwendungen/Jahr) und geringere Risikoeinstufungen (Grad C/D). Einwegsysteme sind optimal für Anwendungen mit hohem Risiko und geringem Volumen geeignet (Klasse A/B). <200 Nutzungen/Jahr), bei denen die Vermeidung von Untersuchungskosten die höheren Kosten pro Nutzung überwiegt.
Risiko einer raumübergreifenden Kontamination
Wiederverwendbare Systeme erfordern eine validierte Reinigung zwischen den Anwendungen, um eine Kontamination von Raum zu Raum zu verhindern:
Validierung der Geldwäsche: Die Wiederaufbereitung pharmazeutischer Textilien folgt den PDA TR 70-Richtlinien. Die Validierung zeigt, dass beim Waschen Schmutz, API-Rückstände und Keimbelastungen bis unter die Nachweisgrenzen entfernt werden. Kritische Parameter: Wasserqualität (WFI oder gereinigtes Wasser für den letzten Spülgang), Reinigungsmitteltyp/-konzentration (pharmazeutische Qualität, rückstandsgeprüft), Waschtemperatur und Zykluszeit, Spülzyklen (mindestens 3–5 mit letztem Spülgang). <10 KBE/100 ml, <0.25 EU/ml Endotoxin) und Trocknungsmethode (HEPA-gefilterte Luft, validierte Temperatur/Zeit, die mikrobielles Wachstum verhindert).
Trennungsprotokolle: Farbcodierung (blau für Klasse A/B, grün für Klasse C, gelb für Klasse D, rot für Abfallbereiche) verhindert versehentliche gegenseitige Verwendung. Die physische Trennung (getrennte Lagerung für jede Sorte/Produktlinie) verstärkt die Verfahrenskontrollen. Die Kennzeichnung (Raumzuordnung, Servicedatum, Taktzahl) ermöglicht die Rückverfolgbarkeit.
Rückstandsprüfung im schlimmsten Fall: Wischmopps absichtlich mit Worst-Case-Belastungen kontaminieren (hochwirksames API-Pulver, konzentriertes Reinigungsmittel, Cocktail mit Organismen mit hoher Keimbelastung), Waschen nach validiertem Protokoll, Testen auf Rückstände mittels HPLC (API) oder TOC (Reinigungsmittel) und Keimbelastung mittels Oberflächentupfer. Akzeptanz: API <1 % der niedrigsten therapeutischen Dosis (produktspezifische Berechnung), Reinigungsmittel <LOD, Keimbelastung <10 KBE/Mopp.
Einwegsysteme machen die Komplexität der Waschvalidierung überflüssig und bieten die absolute Sicherheit, dass es zu keiner Verschleppung kommt – die behördliche Bevorzugung von Mehrproduktanlagen, hochwirksamen APIs und der Beta-Lactam-Herstellung.
SOP-Integration und Workflow-Design
Autoklavierbarer, wiederverwendbarer Arbeitsablauf:
- Verwenden Sie den Wischmopp im dafür vorgesehenen Bereich gemäß der validierten Wisch-SOP
- Nach Gebrauch im dafür vorgesehenen Behälter für kontaminierte Werkzeuge sammeln
- Transfer zum Wäschebereich (täglich oder per Chargenprotokoll)
- Wäscherei pro validiertem Zyklus (Dokumentenstapel, Datum, Bediener)
- Auf Beschädigungen prüfen (Risse, Kantenverschlechterung, Verfärbung); bei Vorliegen von Mängeln ausscheiden
- In qualifizierter Konfiguration in den Autoklaven laden, BIs gemäß PQ-Protokoll platzieren (falls routinemäßige BI-Ausführung geplant)
- Führen Sie einen validierten Autoklavenzyklus durch. Parameterdaten aufzeichnen (Zeit, Temperatur, Druck, F₀)
- Kontrolliertes Abkühlen ermöglichen; Transfer in den sterilen Lagerbereich unter Beibehaltung der Verpackungs-/Haltezeit pro Validierung
- Ausgabe an die Produktion mit Dokumentation der Zykluszählung (Verfolgung in Richtung Lebensdauerbegrenzung)
- Wiederholen Sie die Schritte 1–9, bis der Mopp die zulässige Zyklusgrenze erreicht, und entfernen Sie ihn dann gemäß validiertem Zerstörungsverfahren
Einweg-Workflow:
- Erhalten Sie gammasterilisierte Mopps in versiegelter Herstellerverpackung
- Überprüfen Sie die Unversehrtheit der Verpackung (keine Risse, Siegel intakt) und überprüfen Sie die Dokumentation (Sterilitätszertifikat, Verfallsdatum, Rückverfolgbarkeit der Charge).
- Gemäß Validierung unter kontrollierten Bedingungen (Temperatur, Luftfeuchtigkeit, getrennt nach Charge) lagern
- Ausgabe an die Produktion unter Beibehaltung der Verpackungsintegrität bis zum Verwendungsort
- Im dafür vorgesehenen Umkleide-/Luftschleusenbereich gemäß aseptischer Technik öffnen
- Einmal pro validierter Wisch-SOP verwenden
- Gemäß den Protokollen für pharmazeutische Abfälle entsorgen (getrennt nach Qualität/Produkt, falls für die Rückverfolgbarkeit der Untersuchung erforderlich)
Durch Einweg-Arbeitsabläufe entfallen die Schritte 3–8 aus wiederverwendbaren Protokollen, wodurch der Schulungsaufwand für das Bedienpersonal und das Risiko von Verfahrensabweichungen verringert werden. Allerdings bieten wiederverwendbare Arbeitsabläufe eine größere betriebliche Flexibilität (keine Lieferantenabhängigkeit für Notfallauffüllung, Durchlaufzeit über Nacht im Vergleich zu Vorlaufzeiten von 2 bis 4 Wochen).
Leistung der Umweltüberwachung
EM-Programme verfolgen die Leistung von Reinigungswerkzeugen anhand zweier Messgrößen:
Trends bei der Partikelanzahl: Optische Partikelzähler, die während des Wischvorgangs (oder der Erholungstests nach dem Wischen) positioniert werden, erkennen zersetzende Mopps. Grundlinie: <50 Partikel/m² für neue autoklavierbare Mopps, <30 Partikel/m² für Einwegartikel. Trend: Die durchschnittliche monatliche Partikelbildung beim Wischen sollte konstant bleiben. Aufwärtstrends (z. B. 50 → 70 → 95 Partikel/m² über 3 Monate) deuten auf eine Zersetzung des Mopps hin, die eine frühere Ausmusterung oder eine Untersuchung der Drift des Autoklaven-/Wäscheprozesses erfordert.
EM-Ausfalluntersuchungen sollten Werkzeugausfälle von Bedienertechnik- oder Desinfektionsproblemen unterscheiden. Wenn in mehreren Räumen gleichzeitig ein Anstieg der Partikel-/Keimbelastung zu verzeichnen ist, liegt der Verdacht einer Werkzeugverschlechterung vor (Mopps nähern sich dem Ende ihrer Nutzungsdauer). Bei Isolierung auf einen Raum oder Bediener ist die Technik oder Desinfektionsmittelvorbereitung verdächtig.
Überprüfung der Keimbelastungsreduzierung: Oberflächentupfer oder Kontaktplatten vor und nach dem Wischen messen die Reinigungswirksamkeit. Akzeptanz: Reduzierung um ≥ 2 log (99 % Entfernung) für routinemäßige Reinigung, Reduzierung um ≥ 3 log (99,9 % Entfernung) für sporizide Reinigung. Sowohl autoklavierbare Mopps mit einem SAL-Wert von 10⁻⁶ als auch sterile Einwegmopps erreichen dies, wenn sie mit validierten Desinfektionsmitteln und -techniken verwendet werden. Häufig sind unsterile oder unzureichend sterilisierte Wischmopps zu sehen <Reduzierung um 1 Log oder sogar Erhöhung der Keimbelastung (kontaminiertes Werkzeug verteilt Organismen neu).

Abbildung 3: Pharmazeutischer Reinraum der Klasse B/C, der gekleidetes Personal in angemessener Schutzausrüstung und Produktionsumgebung zeigt. EU GMP Anhang 1 Abschnitt 4.29 erfordert sterile Reinigungsmaterialien (einschließlich Mopps) in Bereichen der Klasse A/B, die durch validierte Autoklavenzyklen erreicht werden und einen SAL 10⁻⁶ liefern.
Empfehlung für das autoklavierbare Wischmoppsystem MIDPOSI (ISO 5–8)
Die autoklavierbaren Reinraum-Moppsysteme von MIDPOSI sind für die Kontrolle pharmazeutischer Kontaminationen konzipiert und kombinieren validierte Materialleistung mit schlüsselfertigen Dokumentationspaketen, die den Zeitaufwand für die Anlagenqualifizierung von Monaten auf Wochen verkürzen.
Autoklav-validierte Polyester-Mopppads
MIDPOSI Wischpads aus Polyester mit versiegelten Kanten bestehen aus kontinuierlichem PET-Polyester in einer Schlauchstrickkonstruktion mit heißversiegelten Rändern. Keine freiliegenden Faserenden; keine Schnittkanten; keine Partikelaustrittswege.
Leistungsangaben:
- Partikelerzeugung: <80 Partikel ≥0,5 µm/m² (neu), <100 Partikel/m², aufrechterhalten über 80 Autoklavenzyklen bei 121 °C/30 Minuten (gemäß ISO 14644-14-Test)
- Haltbarkeit des Autoklaven: Qualifiziert für 80–100 Zyklen mit dokumentierten visuellen, dimensionalen und mechanischen Integritätskriterien
- Chemische Kompatibilität: Validiert für die Rotation pharmazeutischer Desinfektionsmittel (70 % IPA täglich, 5 % H₂O₂ wöchentlich, 1000 ppm Quat 2× wöchentlich, 500 ppm Natriumhypochlorit wöchentlich) ohne Anstieg der Partikelbildung oder Verlust der mechanischen Festigkeit >15 % nach 80 kombinierten Zyklen
- Saugfähigkeit: 5-faches Trockengewicht (460 ml pro 40-cm-Moppkopf, 780 ml pro 60-cm-Moppkopf)
- Verfügbare Größen: 30 cm, 40 cm, 60 cm Breite, Optionen für Flachmopps; 350 mm und 450 mm für Rohrmoppköpfe
Validierungspaket: Testbericht zur Partikelerzeugung (ISO 14644-14-Protokoll, getestet bei 0, 20, 40, 60, 80 Zyklen), Alterungsstudie im Autoklaven (Dimensionsstabilität, Beibehaltung der Zugfestigkeit, visuelle Integrität über 100 Zyklen), Matrix zur chemischen Kompatibilität (bestanden/nicht bestanden für IPA, Peroxid, Quats, Bleichmittel), Materialanalysezertifikate (Fasertyp, Farbstoffkonformität, Schwermetalle), Chargenrückverfolgbarkeit (Chargenaufzeichnungen, die die Rohstoffquelle verknüpfen). bis zum fertigen Produkt).
Rahmen aus Edelstahl
MIDPOSI-Mopphalter bestehen aus SS316-Edelstahl in kontinuierlich gebogener oder WIG-geschweißter einteiliger Konstruktion. Befestigung des Moppkopfes über versiegelte Polyestertaschen (kein Klettverschluss, keine freiliegenden Verschlüsse).
Leistungsangaben:
- Material: SS316 (18 % Cr, 14 % Ni, 2,5 % Mo) mit elektropolierter Oberfläche (<0.4 µm Ra Oberflächenrauheit)
- Haltbarkeit im Autoklaven: >200 Zyklen bei 121 °C ohne Funktionseinbußen; Passivierungsservice verfügbar, wenn nach mehr als 150 Zyklen eine Verfärbung auftritt
- Konstruktion: Kontinuierlich gebogenes Design (Breite 30 cm, 40 cm, 60 cm) oder geschweißter Rohrrahmen (für verstellbare/gelenkige Köpfe)
- Griffbefestigung: Gewindeverbindung aus Edelstahl mit abgedichteter Dichtung (autoklavierbares Silikon, ausgelegt für mehr als 200 Zyklen)
Validierungspaket: Materialzertifikate (Mühlenzertifikate, die die SS316-Zusammensetzung bestätigen), Schweißinspektionsberichte (Farbeindringprüfung für Schweißnahtintegrität), Autoklavenqualifizierung (200-Zyklen-Test mit visueller und mechanischer Inspektion in Intervallen von 50, 100, 150, 200 Zyklen), Prüfung der Partikelerzeugung (Rahmen + Moppkopf-Baugruppe). <100 Partikel/m² Systemleistung).
Griffe aus Polypropylen/Aluminium
MIDPOSI offers both high-temperature polypropylene (cost-optimized, 80-cycle life) and SS316 stainless steel (premium durability, 200+ cycle life) handles.
Autoclavable PP handles:
- Material: High-temperature polypropylene copolymer with heat stabilizers, melting point 165°C
- Autoclave durability: 80 cycles at 121°C (tested to 100 cycles with retirement at 80 to maintain safety margin)
- Construction: One-piece injection-molded tube, sealed threaded frame connection with autoclavable gasket
- Lengths: 120 cm, 140 cm, 160 cm fixed-length; 90–180 cm telescoping (sealed joint design)
- Cost: \$38–\$68 depending on length
SS316 handles:
- Material: SS316 stainless steel tube, electropolished
- Haltbarkeit im Autoklaven: >200 cycles
- Construction: One-piece welded tube or seamless extrusion, sealed frame connection
- Längen: 120 cm, 150 cm Fixlänge; 100–200 cm teleskopierbar
- Cost: \$95–\$145 depending on length
Auswahlberatung: Passen Sie die Lebensdauer des Griffs an die Lebensdauer des Moppkopfes und des Rahmens an. Wenn Sie 80-Zyklen-Polyestermopps mit 200-Zyklen-SS316-Rahmen verwenden, wählen Sie PP-Griffe (80 Zyklen) für eine synchronisierte Ausmusterung – oder wählen Sie SS316-Griffe (200 Zyklen), die zwei bis drei Moppkopf-Lebenszyklen überdauern und so die langfristigen Kosten senken.
Drei-Eimer-System für Desinfektionsmittelintegrität
MIDPOSI-Wagensysteme mit drei Eimern lassen sich in autoklavierbare Moppköpfe/-rahmen/-griffe integrieren, um eine vollständige Workflow-Validierung zu ermöglichen.
Konfiguration: Drei 12-Liter-Edelstahleimer auf fahrbarem Wagenrahmen, abgestufte Volumenmarkierungen (500-ml-Schritte), integrierte Presspresse über dem Abfalleimer. Farbcodierte Deckel (blau = Desinfektionsmittel, grün = Spülen, rot = Abfall) verhindern Verwirrung beim Bediener.
Material: Eimer und Rahmen aus Edelstahl SS316, autoklavierbare Rollen (Hochtemperatur-Nylon oder Edelstahl), Schweißkonstruktion (keine partikelerzeugenden Verbindungen).
Autoklavenkompatibilität: Gesamter Wagen (Eimer, Rahmen, Presse) als zusammengebaute Einheit bei 121 °C autoklavierbar. Die Qualifikation unterstützt die Verwendung der Klasse B/C mit sterilisierten Moppsystemen.
Validierungspaket: Validierung der Flüssigkeitstrennung (Worst-Case-Test: Wischen von 500 m² mit einer einzigen Eimerfüllung, Messung der Desinfektionsmittelkonzentration alle 100 m², Überprüfung, dass sie bis zur Fertigstellung innerhalb von 90–110 % des Zielwerts bleibt), Überprüfung der Desinfektionsmittelkontaktzeit (Messung der Restfeuchtigkeitsdauer auf der Bodenoberfläche), Eimer-/Wringer-Keimbelastungstest (Bestätigung durch Tupfertest nach dem Autoklavieren). <1 KBE pro 25 cm² Fläche), Bedienerschulung SOP mit fotografischer Arbeitsablaufdokumentation.

Qualifizierungsberichte verfügbar
MIDPOSI bietet eine schlüsselfertige Validierungsdokumentation und reduziert die IQ/OQ/PQ-Belastung der Anlage:
Bericht zur Partikelerzeugung: Protokollprüfung nach ISO 14644-14; Mopp + Rahmen + Griffsystem im Gebrauchszustand getestet; Spezifikationen und Kalibrierungsaufzeichnungen für optische Partikelzähler; Testumgebung (Kammer der ISO-Klasse 5, kontrollierte Temperatur/Feuchtigkeit); Ergebnistabelle mit Partikelzählungen bei 0, 20, 40, 60, 80 Zyklenintervallen mit Akzeptanzkriterien und Pass/Fail-Bestimmung.
Autoklav-Qualifizierungsbericht: Design der Alterungsstudie (Zykluszählintervalle, Testparameter); Ergebnisse der visuellen Inspektion (Fotos, die den Moppzustand in jedem Intervall zeigen); Dimensionsstabilitätsmessungen (Länge, Breite, Dicke an drei Stellen pro Mopp); mechanische Festigkeitsprüfung (Zugversuchsergebnisse, Abriebfestigkeit, Fadenzugkraft für Rahmen); funktionelle Leistung (Saugfähigkeit, Auswringleistung); Ruhestandskriterien und Begründung für die Festlegung der Dienstzeit.
Bericht zur chemischen Kompatibilität: Testmatrix (alle Desinfektionsmittel der Einrichtung im Vergleich zu allen Systemkomponenten); Expositionsprotokoll (Konzentration, Kontaktzeit, Anzahl der Zyklen); Bewertungskriterien (visuelle Verschlechterung, erneuter Test der Partikelerzeugung, Beibehaltung der mechanischen Festigkeit); Pass/Fail-Ergebnisse pro Material-Chemikalien-Kombination; Empfehlungen für eine einrichtungsspezifische Desinfektionsmittelrotation.
Prüfung der Desinfektionsmittelverträglichkeit: Sequenzielle Expositionssimulation (Autoklav → IPA → Autoklav → Peroxid → Autoklav → Quat → Autoklav über 50 Zyklen); Partikelgenerierungstrend (überprüfen <100/m² gepflegt); visuelle/mechanische Beurteilung; Annahmeerklärung.
Materialzertifikate: Chargenspezifische Analysezertifikate (Fasertyp, Farbstoffcharge, Metallzusammensetzung); Konformitätszertifikate (Produkt entspricht Spezifikation); Rückverfolgbarkeitsdokumentation (Chargenaufzeichnungen, die CoA mit den Chargennummern des Endprodukts verknüpfen).
IQ/OQ/PQ-Vorlagen: Vorgefertigte Protokolle, anpassbar an einrichtungsspezifische Details (Autoklavenmodell, Zyklusparameter, Raumklassifizierungen); umfasst Akzeptanzkriterien, Datenaufzeichnungsformulare, Abweichungs-/Untersuchungsverfahren; Reduziert die Zeit für die Validierungserstellung von 40–60 Stunden auf 8–12 Stunden für die Anpassung.
Schnelle Vorlaufzeit, technischer Support
Lieferkette und technischer Support von MIDPOSI:
Lieferzeiten: Lagerartikel (Standard-Polyester-Moppköpfe 40 cm und 60 cm, SS316-Rahmen, PP-Griffe 120 cm und 150 cm) werden innerhalb von 5 Werktagen versendet. Benutzerdefinierte Konfigurationen (Sondergrößen, Logodruck, Farbcodierungsoptionen) werden innerhalb von 15 Werktagen versendet. Validierungsdokumentationspakete werden innerhalb von 3 Werktagen nach der Bestellung geliefert (elektronische PDF-Lieferung).
Technische Unterstützung: Technische Beratung vor dem Verkauf (30–60-minütiger Anruf mit QA-/Validierungsteams, um die Anlagenanforderungen zu überprüfen, Konfigurationen zu empfehlen und den Validierungsansatz zu besprechen). Musterbewertungsprogramme (Einrichtungen können vor der Kapitalbindung 5–10 Mustermopps für interne Pilottests anfordern). Überprüfung des Validierungsprotokolls (das technische Team von MIDPOSI überprüft die IQ-/OQ-/PQ-Entwürfe der Anlage und gibt Feedback zu Akzeptanzkriterien, Testmethoden und Datenaufzeichnung). Fehlerbehebung nach dem Verkauf (Unterstützung bei der Untersuchung, wenn Mopps eine unerwartete Beeinträchtigung oder EM-Auswirkungen aufweisen).
Ausbildung: Vor-Ort- oder virtuelle Bedienerschulung, die die richtige Wischtechnik, die Beladungskonfiguration des Autoklaven, die Verfolgung der Zyklusanzahl, die Sichtprüfung auf Ausmusterungskriterien und Korrekturmaßnahmen für beschädigte Werkzeuge umfasst.
Conversion-CTA:
Validierungsbericht anfordern — Laden Sie den vollständigen ISO 14644-14-Testbericht zur Partikelerzeugung, die Alterungsstudie im Autoklaven und die chemische Kompatibilitätsmatrix für MIDPOSI-Polyester-Moppsysteme herunter. Enthält IQ/OQ/PQ-Protokollvorlagen. [Anfrage-Button]
OEM-Angebot anfordern (12-Stunden-Antwort) — Senden Sie Anlagenanforderungen (ISO-Klasse, Bodenfläche, Autoklavenspezifikationen, Desinfektionsprogramm) für ein individuelles Systemangebot. Die Preise beinhalten Mengenrabatte für die Beschaffung an mehreren Standorten. Ingenieurberatung inklusive. [Anfrage-Button]
Technisches Datenblatt herunterladen (PDF) — Druckbares Datenblatt mit Materialzusammensetzung, Leistungsspezifikationen, Haltbarkeit im Autoklaven, chemischer Kompatibilität, verfügbaren Größen und Bestellinformationen. [Download-Button]
FAQ – Autoklavierbare Reinraummopps
Was ist der Unterschied zwischen „autoklavierbar“ und „steril“?
„Autoklavierbar“ beschreibt eine Materialeigenschaft – die Fähigkeit, einer Sterilisation mit feuchter Hitze bei 121–134 °C ohne inakzeptablen Qualitätsverlust standzuhalten. „Steril“ beschreibt einen mikrobiologischen Zustand – bestätigte Abwesenheit lebensfähiger Organismen bis zum Sterility Assurance Level (SAL) 10⁻⁶. Ein autoklavierbarer Mopp gemacht werden kann durch validierte Autoklavenzyklen steril, aber nur autoklavierbar zu sein bedeutet nicht, dass es derzeit steril ist. Die Sterilität wird durch einen validierten Prozess (Autoklavieren, Gammabestrahlung) erreicht und durch kontrollierte Lagerung/Verpackung bis zum Verwendungsort aufrechterhalten. Beschaffungsspezifikationen müssen beides berücksichtigen: Materialien müssen autoklavierbar sein (wiederholte Zyklen ohne Leistungsverlust aushalten) Und Der Sterilisationsprozess muss validiert sein (Nachweis von SAL 10⁻⁶ durch biologische Indikatoren und parametrische Überwachung).
Wie viele Autoklavenzyklen hält ein Polyestermopp aus?
Polyestermopps mit versiegelten Kanten in pharmazeutischer Qualität überstehen 50–100 Autoklavenzyklen bei 121 °C/30 Minuten, bevor sie ihre Leistungsgrenzen erreichen. Hochwertiges Endlosfilament-Polyester erreicht 80–100 Zyklen; Standard-Polyester in pharmazeutischer Qualität erreicht 50–80 Zyklen. Der begrenzende Faktor ist nicht ein akutes Materialversagen (Schmelzen, Reißen), sondern die allmähliche Zunahme der Partikelbildung – die Entstehung von Mops <80 Partikel/m² im Neuzustand erreichen nach 80 Zyklen typischerweise 90–100 Partikel/m² und nähern sich damit der ISO-Klasse 5–7-Akzeptanzgrenze von <100 Partikel/m². Betriebe sollten Mopps nach 70–80 % der vom Anbieter bestätigten Zyklenzahl ausmustern (z. B. wenn der Anbieter sich für 100 Zyklen qualifiziert, sollten sie nach 70–80 Zyklen aus dem Verkehr gezogen werden), um einen Sicherheitsspielraum aufrechtzuerhalten und Fehler bei der Klassifizierung in der Mitte der Nutzungsdauer zu verhindern. Mikrofasermischungen erreichen aufgrund der thermischen Zersetzung von Polyamid nur 30–50 Zyklen. Zyklen bei höheren Temperaturen (134 °C) verkürzen die Lebensdauer aller Materialien um 30–50 %.
Können Mikrofasermopps autoklaviert werden?
Ja, aber mit erheblichen Einschränkungen. Mikrofasern (Polyester/Polyamid-Mischungen, typischerweise 80/20 oder 70/30) können das Autoklavieren überstehen, Polyamid zersetzt sich jedoch schneller als 100 % Polyester. Autoklavierbare Mikrofaser in pharmazeutischer Qualität erreicht 30–50 Zyklen bei 121 °C, bevor die Partikelerzeugung die ISO-Grenzwerte überschreitet (Anstieg von ~100 Partikeln/m² neu auf 200–400 Partikel/m² bei 40–50 Zyklen). Mikrofasern zeigen außerdem Faserverschmelzung (Filamente verschmelzen unter REM), Dimensionsschrumpfung (5–10 % bei 30 Zyklen) und Rückstandsretention (beschädigte Fasern werden klebrig). Für Anwendungen der Güteklasse A/B ist 100 % Polyester mit versiegelten Kanten überlegen (längere Lebensdauer, stabilere Partikelerzeugung, bessere Dimensionsstabilität). Mikrofaser bleibt für die ISO-Klasse 7–8 (Klasse C/D) akzeptabel, wo die Vorteile einer verbesserten Saugfähigkeit (6–8-faches Trockengewicht gegenüber 4–6-faches bei Polyester) die verringerte Haltbarkeit und Partikelbildung überwiegen <200/m² entspricht der Klassifizierung. Einrichtungen, in denen Mikrofasern verwendet werden, sollten: (1) für maximal 30–40 Zyklen geeignet sein, (2) die Bildung von Partikeln alle 10 Zyklen tendieren lassen, (3) Zyklen bei 134 °C vermeiden (schwerer Polyamidabbau), (4) die Verwendung auf Bereiche der Klasse C/D beschränken.
Benötigen alle autoklavierbaren Moppkomponenten die gleiche Lebensdauer?
Nein, aber ein nicht übereinstimmender Lebenszyklus führt zu Verschwendung oder betrieblicher Komplexität. Optimale Strategie: Die Lebensdauer der Komponenten anpassen, um eine synchronisierte Außerbetriebnahme zu ermöglichen.
Beispiel für abgestimmte Lebensdauer: 80-Zyklen-Polyester-Moppköpfe + 80-Zyklen-Polypropylenrahmen + 80-Zyklen-PP-Griffe. Alle Komponenten gehen nach 80 Zyklen gemeinsam in den Ruhestand – kein Abfall durch die Entsorgung funktionsfähiger, langlebiger Komponenten, kein Risiko durch die Verwendung kurzlebiger Komponenten, die über die Qualifikation hinausgehen.
Beispiel für eine nicht übereinstimmende Lebensdauer: 80-cycle polyester mop heads + 200-cycle SS316 frames + 200-cycle SS316 handles. Frames and handles outlast 2–3 mop head lifecycles. Economically optimal (lower long-term cost), but requires inventory tracking (pairing new mop heads with used frames/handles of known cycle history) and periodic frame/handle inspection (verify no degradation after 80, 160 cycles before re-pairing).
Worst mismatch scenario: 80-cycle mop heads + 50-cycle frames + 80-cycle handles. Frames fail mid-service-life, forcing retirement of functional mop heads and handles—wasting capital and requiring emergency frame procurement.
Beschaffungsleitfaden: Um den Betrieb zu vereinfachen, sollten Sie die Lebensdauer aller Komponenten aufeinander abstimmen (höhere Anschaffungskosten für Komponenten mit langer Lebensdauer oder eine kürzere Systemlebensdauer für kostengünstigere Komponenten akzeptieren). Kombinieren Sie zur Kostenoptimierung langlebige Rahmen/Griffe (SS316, 200+ Zyklen) mit Wischmoppköpfen mit kürzerer Lebensdauer (Polyester, 80 Zyklen), wobei Sie die Lagerkomplexität für eine jahrzehntelange Nutzung von Rahmen/Griffen in Kauf nehmen.
Sind gammasterilisierte Mopps besser als autoklavierbare Mopps der Güteklasse A?
Nicht unbedingt „besser“, aber oft für bestimmte Risiko-/Betriebsprofile bevorzugt:
Vorteile von gammasterilisierten Einwegartikeln für Klasse A:
- Kein Kreuzkontaminationsrisiko (Einmalgebrauch verhindert Verschleppung von Charge zu Charge)
- Keine Verschlechterung der Lebensdauer (jeder Mopp ist eine „neue“ Leistung)
- Einfachere Validierung (Anbieter liefert Sterilitätszertifikate; Einrichtung validiert nur Empfang/Lagerung)
- Geringerer Untersuchungsaufwand (bei EM-Ausfällen entfallen Einwegmopps als chronische Kontaminationsquelle)
Autoklavierbare wiederverwendbare Vorteile für Klasse A:
- Lower cost per use (\$3–\$7 vs \$20–\$30 for disposables)
- Operative Unabhängigkeit (Durchlaufzeit über Nacht vs. 2–4 Wochen Vorlaufzeit des Lieferanten)
- Umweltvorteil (geringeres Abfallvolumen)
Entscheidungsrahmen: Wenn die Fläche der Klasse A klein ist (<200 m²) and mopping frequency is low (2–3× per week), disposables justify premium cost through investigation risk reduction—a single EM failure investigation (\$8,000–\$15,000 cost) negates years of per-use savings. If Grade A area is large (>500 m²) oder die Nutzung hoch ist (tägliches Wischen), wiederverwendbare Systeme liefern einen hohen ROI – erfordern jedoch eine robuste Autoklavenvalidierung, Lebensdauerverfolgung und Waschprotokolle. Anlagen mit mehreren Produkten oder hochwirksamen Wirkstoffen sollten aufgrund der Kreuzkontaminationsrisikounverträglichkeit unabhängig von der Flächengröße standardmäßig auf Einwegartikel zurückgreifen. Einrichtungen mit validierter Autoklaven-Infrastruktur und GMP-Wäschekapazitäten können autoklavierbare Systeme der Klasse A bedenkenlos verwenden, wobei sie für langfristige Kosteneinsparungen einen höheren Validierungsaufwand in Kauf nehmen.
Wie bestätige ich, dass das Autoklavieren meine Mopps tatsächlich sterilisiert?
Die Sterilisationsvalidierung folgt einem dreistufigen IQ/OQ/PQ-Rahmen:
IQ (Installationsqualifikation): Überprüfen Sie, ob der Autoklav den Spezifikationen entspricht (Kammergröße, Temperaturbereich, Druckkapazität), bestätigen Sie die Kalibrierung von Temperatursonden und Druckmessgeräten (innerhalb von ±1 °C und ±0,5 psi), dokumentieren Sie die Chargenqualifikation für biologische Indikatoren (Artenbestätigung, Populationszahl, D-Wert- und Z-Wert-Zertifikate), überprüfen Sie die Dampfqualität (Kondensatleitfähigkeit). <5 µS/cm, nicht kondensierbarer Gasanteil <3,5 %).
OQ (Operative Qualifikation): Führen Sie Studien zur Wärmeverteilung in leeren Kammern durch (Thermoelemente an 9–12 Stellen in der gesamten Kammer, kartieren Sie die Temperaturgleichmäßigkeit, identifizieren Sie kalte Stellen – typischerweise in der geometrischen Mitte und in der Nähe der Tür). Führen Sie Wärmedurchdringungsstudien in beladenen Kammern mit Moppbeladungen in der Worst-Case-Konfiguration durch (maximale Moppanzahl, dichteste Packung, Autoklavenbeutel, falls verwendet). Platzieren Sie Thermoelemente an verdächtigen kalten Stellen (Mitte dicht gestapelter Mopps, Mitte der Beutel). Bestätigen Sie, dass an allen Standorten eine Mindesttemperatur von ≥ 121 °C und eine Mindesteinwirkungszeit von ≥ 15 Minuten erreicht werden. Berechnen Sie F₀ (kumulative Letalität) aus Zeit-Temperatur-Daten. Akzeptanz ≥8 min für Dampfzyklen.
PQ (Leistungsqualifizierung): Führen Sie 3 aufeinanderfolgende erfolgreiche Zyklen mit Worst-Case-Lasten durch. Platzieren Sie biologische Indikatoren (Geobacillus stearothermophilus Sporenstreifen oder eigenständige BIs, Population ≥10⁶ KBE, D₁₂₁ ~1,5 Min.) an kalten Stellen, die in der OQ identifiziert wurden, plus Zentrum und Peripherie der Moppladungen. Fügen Sie eine positive BI-Kontrolle hinzu (unsterilisiert, zur Bestätigung der Lebensfähigkeit inkubiert). Nach dem Zyklus die BIs aseptisch in Wachstumsmedium (tryptische Sojabrühe) übertragen und 7 Tage lang bei 55–60 °C inkubieren. Akzeptanz: Alle Prozess-BIs zeigen kein Wachstum (was auf eine Reduzierung um ≥6 Logs hinweist); Die positive Kontrolle zeigt Wachstum (was bestätigt, dass BIs lebensfähig waren). Dokumentieren Sie parametrische Daten (Zeit-/Temperatur-/Druckdiagramme), die den Zyklus mit validierten Parametern zeigen.
Routineüberwachung: Kontinuierliche Sterilisationssicherung durch: parametrische Freigabe (die Zeit-/Temperatur-/Druckdaten jedes Zyklus bestätigen die Einhaltung der validierten Parameter), regelmäßige BI-Läufe (Häufigkeit gemäß Anlagenprotokoll – wöchentlich, monatlich oder pro Charge), Autoklavenwartung (jährliche vorbeugende Wartung, vierteljährliche Dampfqualitätsprüfung, halbjährliche Kammerleckprüfung).
Welche Dokumentation benötige ich für FDA/EMA-Audits?
Aufsichtsinspektoren, die die Validierung autoklavierbarer Reinraummopps prüfen, erwarten Folgendes:
1. Aufzeichnungen zur Gerätequalifikation: Autoklav-IQ/OQ/PQ-Protokolle mit ausgeführten Daten, Bioindikator-Chargenzertifikate (Art, D-Wert, Z-Wert, Ablaufdatum), Autoklav-Wartungsaufzeichnungen (PM-Zeitpläne, Kalibrierungszertifikate für Temperatur-/Druckinstrumente), Ergebnisse von Dampfqualitätstests.
2. Aufzeichnungen zur Materialqualifikation: Lieferantenvalidierungsberichte (Partikelerzeugung gemäß ISO 14644-14, Autoklaven-Haltbarkeitsstudien, Matrizen zur chemischen Kompatibilität), Materialanalyse- und Konformitätszertifikate, Studien zur Bestimmung der Lebensdauer (Dimensionsstabilität, Beibehaltung der mechanischen Festigkeit, visuelle Integrität über qualifizierte Zyklenanzahl).
3. Validierungsdatensätze verarbeiten: Waschvalidierung (Nachweis der Entfernung von Rückständen unterhalb der Nachweisgrenze), Qualifizierung des Autoklavenzyklus (Wärmeverteilungs- und Penetrationsstudien für Wischbeladungen), Definition der Worst-Case-Beladung (maximale Wischmoppanzahl, Verpackungskonfiguration), Akzeptanzkriterien für parametrische und BI-Daten.
4. Routineüberwachungsaufzeichnungen: Chargenaufzeichnungen für jeden Sterilisationszyklus (Datum, Bediener, Zyklusparameter, Beladungsbeschreibung, BI-Ergebnisse, falls zutreffend), Protokolle zur Verfolgung der Zyklusanzahl (Verknüpfung der Mopp-Seriennummern oder Chargencodes mit kumulierten Zyklen, Ausmusterung bei qualifiziertem Grenzwert), visuelle Inspektionsaufzeichnungen (regelmäßige Inspektion auf Risse, Kantenverschlechterung, Verfärbung), EM-Trends (Daten zu Partikelanzahl und Keimbelastung im Zusammenhang mit Wischvorgängen).
5. Standardarbeitsanweisungen: Autoklavenbetrieb-SOP (Beladen, Zyklusauswahl, Entladen, Haltezeiten), Wasch-SOP (Waschparameter, Anforderungen an die Wasserqualität, Reinigungsmittelspezifikationen), Mopp-Nutzung und -Lagerung (Raumzuordnung, sterile Handhabungstechnik, Lagerbedingungen/Haltezeiten), Stilllegungs- und Entsorgungs-SOP (Zyklenanzahlgrenzen, visuelle Mängelkriterien, Entsorgungsverfahren).
6. Kontaminationskontrollstrategie (CCS): Risikobewertung, die die Auswahl autoklavierbar vs. Einwegartikel pro Anlagenbereich rechtfertigt, Erklärungen zur Geräteeignung (warum ausgewählte Moppmaterialien/Sterilisationsmethode die Anforderungen von Anhang 1 erfüllen), Schulungsunterlagen (Bedienerqualifikation für Wischtechnik, Autoklavenbetrieb, Zyklusverfolgung, Inspektionsverfahren).
7. Ermittlungsunterlagen (if applicable): CAPA documentation for any EM failures traced to cleaning tools, OOS investigations when particle generation exceeded limits, sterilization failures (BI positive results, parametric deviations).
Auditors may ask: “How do you know your mops remain suitable through their service life?” (expect trending data showing stable particle generation across cycles). “What happens if this mop is accidentally used beyond its qualified cycle count?” (expect SOP describing deviation reporting, risk assessment, potential product impact evaluation). “How do you prevent cross-contamination between products/rooms?” (expect laundering validation data, segregation protocols, worst-case residue testing results).









