Die Chargenrückverfolgbarkeit von Reinraum-Verbrauchsmaterialien ist nicht nur eine Dokumentationsaufgabe. Es ist das operative Rückgrat, das es Herstellern, Sterilverarbeitungsteams und regulierten Einrichtungen ermöglicht, Rohstoffe, Produktion, Sterilisation, Vertrieb und Endverwendung in einer überprüfbaren Beweiskette zu verknüpfen.
In Pharma-, Biotech-, Halbleiter- und Medizingeräteumgebungen birgt eine unvollständige Rückverfolgbarkeit Risiken, die weit über Lücken im Papierkram hinausgehen. Es verzögert Untersuchungen, schwächt die Reaktion auf Rückrufe, erschwert Prüfungen und untergräbt das Vertrauen in Kontaminationskontrollprogramme. Ein robustes System sollte Qualitätsteams dabei helfen, von der reaktiven Erfassung von Datensätzen zur proaktiven Kontrolle überzugehen.
Chargenrückverfolgbarkeit für Reinraum-Verbrauchsmaterialien bedeutet, dass eine vollständige, abrufbare Aufzeichnung jeder Charge vom Materialeingang über die Herstellung, Sterilisation, Verteilung und Endverwendung geführt wird. In der Praxis sollte ein wirksames System identifizieren, was hergestellt wurde, aus welchen Ausgangsmaterialien, unter welchen Prozessbedingungen, wohin es versandt wurde und welche Kunden oder internen Benutzer betroffen waren, wenn es zu einer Abweichung oder einem Rückruf kam.
Für regulierte Einrichtungen sind die besten Systeme nicht nur auf dem Papier konform. Sie sind schnell durchsuchbar, leicht zu überprüfen, revisionssicher und in der Lage, einen gezielten Rückruf innerhalb von Stunden statt Tagen zu unterstützen.
Eine starke Chargenrückverfolgbarkeit verknüpft Rohstoffchargen, Produktionschargen, Sterilisationsaufzeichnungen, Versanddaten und Endverbraucherverbrauch in einer einzigen Beweiskette.
Auditfähige Systeme müssen eine schnelle Untersuchung und einen gezielten Rückruf unterstützen und nicht nur die passive Speicherung getrennter Aufzeichnungen.
Eine klare Chargennummerierungslogik reduziert die Verwirrung des Bedieners und verbessert die nachgelagerte Berichterstattung, Kennzeichnung, Freigabe und Beschwerdebearbeitung.
Vorwärtsrückverfolgbarkeit, Rückverfolgbarkeit und Rückrufsimulation sollten regelmäßig getestet werden, um zu beweisen, dass das System tatsächlich unter Druck funktioniert.
Viele Einrichtungen erfassen bereits Chargennummern auf Kartons, Etiketten oder Sterilisationsdokumenten. Das Problem besteht darin, dass diese Aufzeichnungen oft fragmentiert sind und sich auf Einkaufs-, Lager-, Produktions-, Sterilisations-, Logistik- und Endbenutzerprotokolle verteilen. Wenn eine Beschwerde, ein Kontaminationsereignis oder eine Auditanfrage auftritt, muss das Team die Historie manuell rekonstruieren.
Dieser Ansatz ist langsam, fehleranfällig und teuer. Ein ausgereiftes Rückverfolgbarkeitsprogramm verkürzt die Untersuchungszeit, verbessert die Freigabesicherheit und schränkt den Umfang von Rückrufaktionen ein. Es unterstützt auch Trendanalyse, Lieferantenmanagement, CAPA und Kundenkommunikation.

Ein Rückverfolgbarkeitssystem für Reinraum-Verbrauchsmaterialien sollte darauf ausgerichtet sein, wie regulierte Organisationen Abweichungen untersuchen und die Kontrolle nachweisen. Zu den wichtigsten Referenzen für viele Anwender zählen der EU-GMP-Anhang 1, die cGMP-Aufzeichnungserwartungen der FDA und die Rückverfolgbarkeitsanforderungen nach ISO 13485 für Qualitätssysteme im Zusammenhang mit Medizinprodukten.
| Verordnung / Norm | Fokusbereich | Operative Bedeutung |
|---|---|---|
| Ich GMP Anhang 1 | Rückverfolgbarkeit, Chargenprotokolle, Rückruffähigkeit | Einrichtungen sollten in der Lage sein, betroffene Materialien und Fertigwaren bei Untersuchungen oder Marktmaßnahmen schnell zu identifizieren. |
| FDA 21 CFR 211.180 / 211.198 | Vertriebsaufzeichnungen, Beschwerdeakten, Aufbewahrung | Aufzeichnungen sollten die Bewertung von Beschwerden, die Überprüfung der Auswirkungen auf Chargen und die kontrollierte Durchführung von Rückrufen unterstützen. |
| ISO 13485 Abschnitt 7.5.8 | Eindeutige Identifizierung und Abruf | Die Organisation sollte dokumentierte Rückverfolgbarkeitsverfahren pflegen und in der Lage sein, bei Bedarf verknüpfte Aufzeichnungen abzurufen. |
Für Einkäufer und QA-Teams bedeutet dies, dass die Rückverfolgbarkeit nicht als reine Lagerfunktion behandelt werden sollte. Dabei handelt es sich um eine funktionsübergreifende Qualitätsanforderung, die die Lieferantenkontrolle, die Produktionsdokumentation, die Sterilisationsfreigabe, die Versandhistorie und die Verantwortung des Endbenutzers betrifft.
Eine sinnvolle Möglichkeit, die Rückverfolgbarkeit von Chargen zu strukturieren, besteht darin, das System in fünf miteinander verbundene Ebenen zu unterteilen: Rohstoffe, Herstellung, Sterilisation, Vertrieb und Verbrauch. Dieses Framework hilft Teams dabei, Eigentumsrechte, Datenfelder und Überprüfungskontrollpunkte zu definieren, ohne die durchgängige Transparenz zu verlieren.
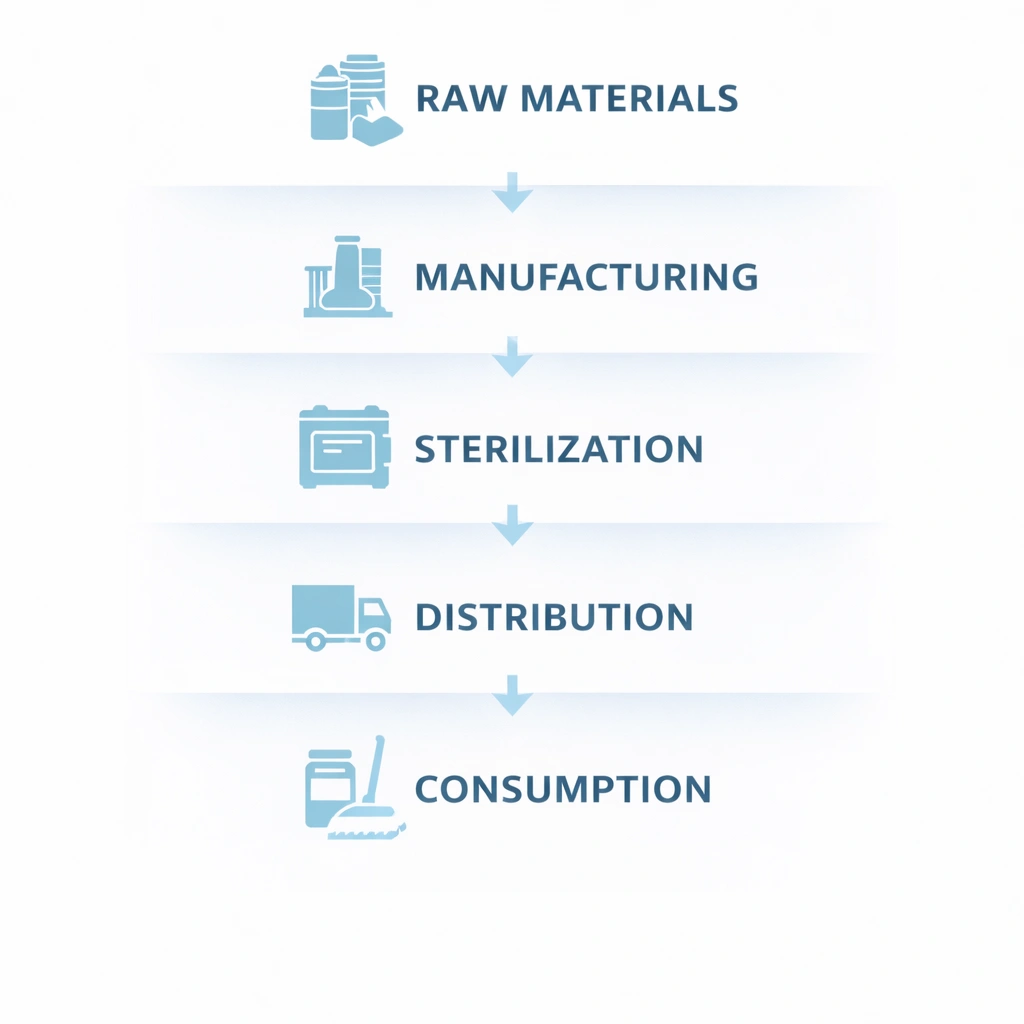
Erfassen Sie die Identität des Lieferanten, die Chargennummer des Lieferanten, das Eingangsdatum, den Status der Eingangsprüfung und relevante Zertifikate wie COA oder CoC. Dies ist der Ausgangspunkt für die vorgelagerte Kontrolle.
Erfassen Sie, welche Materialien verwendet wurden, welche Linie die Charge produzierte, wer den Prozess durchgeführt oder freigegeben hat und welche prozessbegleitenden oder abschließenden QC-Kontrollen durchgeführt wurden.
Verknüpfen Sie bei sterilen Verbrauchsmaterialien die Produktionscharge mit der Sterilisationscharge, den Zyklusparametern, der Sterilisationsmethode, dem Freigabestatus und etwaigen Validierungsnachweisen.
Verknüpfen Sie Chargennummern mit Kunden, Versandmengen, Versanddaten, Spediteurinformationen und Zieldetails. Dies ist für die Triage von Beschwerden und die Eindämmung von Rückrufen von wesentlicher Bedeutung.
Wenn es das Nutzungsmodell erfordert, führen Sie benutzerseitige Aufzeichnungen über Chargennummer, Verwendungsdatum, Standort und Entsorgungsweg. Dies ist besonders wertvoll in GMP-Umgebungen mit hohem Risiko.
Die Chargennummer sollte mehr als ein Serienstempel sein. Es sollte eine schnelle Interpretation, eine genaue Speicherung, eine saubere Etikettenpräsentation und eine fehlerarme manuelle Handhabung unterstützen. Ein strukturiertes Format macht die digitale Suche und Berichterstattung zudem zuverlässiger.

| Batch-Element | Beispiel | Warum es wichtig ist |
|---|---|---|
| Lieferanten-/Herstellercode | MITTELPOSI | Identifiziert den Herstellungsort und trennt Marken, Standorte oder Lieferströme. |
| Datumssegment | 06.04.2026 | Hilft Bedienern dabei, Produktionschronologie und Aufbewahrungslogik schnell zu erkennen. |
| Seriennummer | 001 | Unterscheidet mehrere Chargen, die innerhalb desselben Tages oder Zyklusfensters produziert werden. |
| Suffix/Prozessmarkierung | A / B / C | Nützlich für Produktions-, Sterilisations-, Resterilisations- oder QA-Workflow-Unterscheidungen. |
Selbst eine starke physische Kennzeichnung reicht nicht aus, wenn die Belegunterlagen unvollständig sind. Eine vertretbare Rückverfolgbarkeitsdatei sollte es einem Prüfer ermöglichen, von einer fertigen Charge zurück zu den Ausgangsmaterialien und von einem Ausgangsmaterial zu jeder betroffenen fertigen Charge und Kundensendung überzugehen.
Lieferantenlos, eingegangene Menge, Prüfergebnis, Dokumentenprüfung, Freigabestatus.
Chargennummer, Bediener, Linie, Prozessdatum, Materialverbrauch, QC-Kontrollpunkte, Abweichungen.
Sterilisationscharge, Zyklusdaten, Freigabeentscheidung, vom Kunden versandte Menge, Bestimmungsort, Reklamationsverknüpfung.
Der Dokumentationssatz sollte auch bei Lieferantenaudits, Kundenqualifizierung, Beschwerdebearbeitung und CAPA-Prüfungen leicht abrufbar sein. Wenn das Auffinden der richtigen Datei zu lange dauert, ist das System funktionell schwächer, als es auf dem Papier erscheint.
Ein Rückverfolgbarkeitssystem sollte getestet und nicht vorausgesetzt werden. Der praktischste Ansatz besteht darin, drei Arten von Übungen durchzuführen: Vorwärtsverfolgbarkeit, Rückverfolgbarkeit und Rückrufsimulation. Diese Tests zeigen, ob Datenfelder wirklich verknüpft sind, ob Teams wissen, wo sie suchen müssen und ob die Reaktionszeit den internen Erwartungen entspricht.
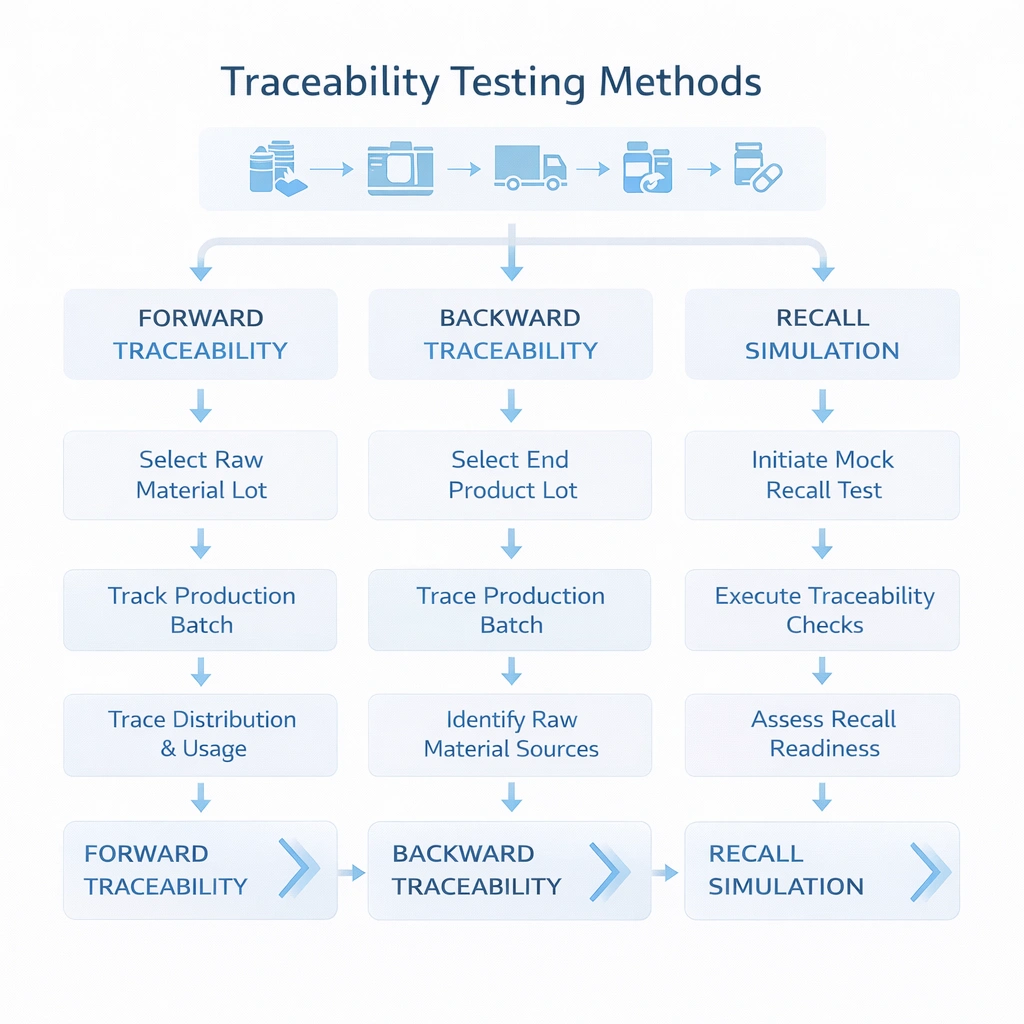
Beginnen Sie mit einer eingehenden Materialcharge und ermitteln Sie, welche Produktionschargen, Sterilisationszyklen und Kundenlieferungen betroffen waren.
Beginnen Sie mit einer Reklamation oder einer vom Kunden verwendeten Charge und verfolgen Sie diese bis zu den Ausgangsmaterialien, Prozessaufzeichnungen und dem Freigabestatus.
Wählen Sie eine Charge aus und simulieren Sie einen gezielten Rückruf: Identifizieren Sie jeden betroffenen Kunden, jede Menge, jeden Versandweg und jeden Kontaktinhaber. Erfassen Sie die insgesamt benötigte Zeit und die gefundenen Datenlücken. In Umgebungen mit hoher Kontrolle ist diese Übung eine der schnellsten Methoden, um zu beurteilen, ob das System wirklich für den Rückruf bereit ist.
| Testtyp | Hauptfrage | Erwartete Ausgabe |
|---|---|---|
| Vorwärtsrückverfolgbarkeit | Wo ist diese Eingabe geblieben? | Betroffene Produktions-, Sterilisations- und Versandaufzeichnungen |
| Rückverfolgbarkeit | Was hat zu diesem Ergebnis geführt? | Quellenmaterial, Prozesshistorie, Freigabenachweise |
| Rückrufsimulation | Können wir schnell und präzise handeln? | Kundenliste, Mengenkarte, Antwortzeitpunkt, Datenlückenprotokoll |
Ein Rückruf-Workflow sollte vorab festgelegt und nicht improvisiert werden. Wenn ein Qualitätsproblem auftritt, sollten die Teams bereits wissen, wie sie das Problem klassifizieren, betroffene Chargen identifizieren, Stakeholder benachrichtigen, die weitere Verbreitung stoppen sowie die Grundursache und Korrekturmaßnahmen dokumentieren können.
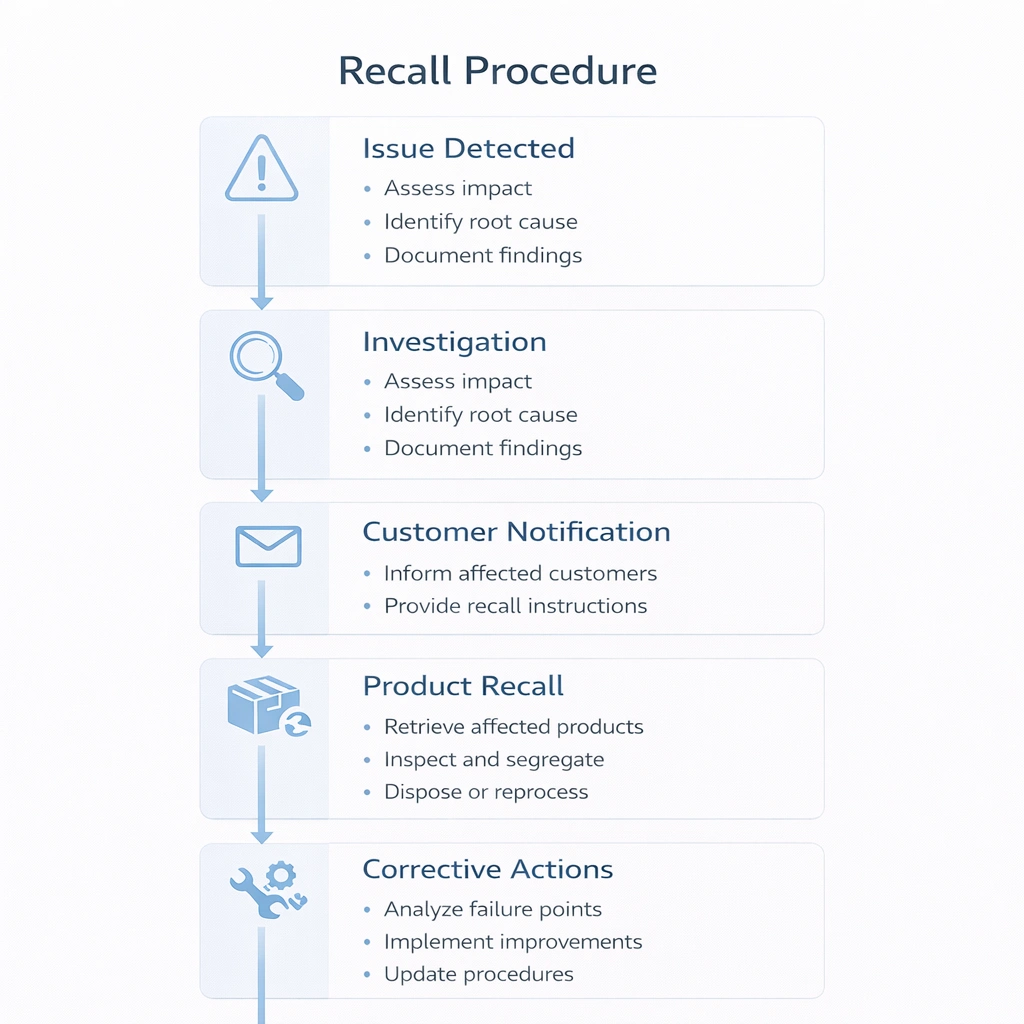
Tabellenkalkulationsbasierte Systeme können mit geringer Komplexität arbeiten, aber wenn die Produktpalette, das Kundenvolumen und die Sterilitätsabläufe zunehmen, wird die elektronische Rückverfolgbarkeit in der Regel praktischer. Barcode- oder RFID-gestützte Systeme verringern das Risiko manueller Eingaben und machen die Rückrufsimulation schneller und wiederholbarer.

Definieren Sie Datenfelder, Eigentümer, Chargencode-Logik, Aufbewahrungsregeln und Rückverfolgbarkeitsbereich für sterile und nicht sterile Linien.
Standardisieren Sie Formulare, Lieferantenchargenerfassung, Produktionsaufzeichnungen, Sterilisationsverknüpfung und Versandaufzeichnungen.
Führen Sie Vorwärts-, Rückverfolgbarkeits- und Rückverfolgbarkeitssimulationstests durch und dokumentieren Sie die gefundenen Lücken.
Das System sollte mindestens eingehende Materialchargen, Produktionschargen, ggf. Freigabe- oder Sterilisationsaufzeichnungen, den Versandverlauf und die Möglichkeit zur Identifizierung betroffener Kunden oder Benutzer während einer Untersuchung verbinden.
Durch die Chargenkennzeichnung wird eine Produktgruppe identifiziert. Vollständige Rückverfolgbarkeitslinks mit Kennzeichnung zu vorgelagerten Materialien, Prozessaufzeichnungen, Freigabeentscheidungen und nachgelagerten Vertriebs- oder Verwendungsaufzeichnungen.
Viele Qualitätsteams führen die Tests mindestens einmal jährlich durch, während risikoreichere oder komplexere Vorgänge möglicherweise häufiger testen, insbesondere nach Systemänderungen, Lieferantenwechseln oder größeren CAPA-Maßnahmen.
Ja, für Operationen mit geringem Volumen. Sobald jedoch die Produktvielfalt, die Sterilitätskontrolle oder die Kundenkomplexität zunehmen, bieten digitale Systeme in der Regel eine bessere Abrufgeschwindigkeit, Fehlerreduzierung und Revisionskontrolle.
Denn sterile Produkte erfordern eine strengere Kontrolle der Chargenhistorie, der Sterilisationsverknüpfung, des Freigabenachweises und der nachgelagerten Sichtbarkeit, wenn eine Beschwerde, ein Sterilitätsproblem oder eine Rückrufentscheidung vorliegt.
Midposi unterstützt regulierte Käufer mit Reinraum-Verbrauchsmaterialien, die für kontrollierte Umgebungen entwickelt wurden, einschließlich dokumentationsorientierter Kommunikation zur Qualifizierung, Überprüfung des Sterilitätsstatus und Diskussionen zur Chargenrückverfolgbarkeit.


Wir werden uns innerhalb eines Werktages mit Ihnen in Verbindung setzen. Bitte beachten Sie die E-Mail mit dem Suffix „*@midposi.com“.