Der Reinraum-Moppeimer ist kein gewöhnlicher Hausmeisterbedarf – er ist ein Kontaminationskontrollgerät, das bestimmt, ob Ihr Desinfektionsmittel die validierte Kontaktzeit erreicht oder auf unwirksame Konzentrationen verdünnt wird, bevor es den Boden berührt. Wenn Sie die falsche Schaufelkonfiguration wählen, werden Sie mit Abweichungen bei der Umgebungsüberwachung, Audit-Ergebnissen für eine unzureichende Reinigungsvalidierung und den darauffolgenden teuren Untersuchungszyklen konfrontiert. Konfigurieren Sie es richtig – passen Sie das Design des Eimersystems an Ihre ISO-Klasse, Desinfektionsmittelrotation und Sterilisationskapazität an – und Sie haben einen validierten Reinigungsworkflow erstellt, der behördliche Inspektionen übersteht und Kreuzkontaminationen verhindert, die die Produktion stoppen. In diesem Leitfaden wird die technische Logik hinter Systemen mit einem, zwei und drei Eimern aufgeschlüsselt, erläutert, warum sich die Wahl des Wringmechanismus auf die Partikelerzeugung und die Haltbarkeit des Autoklaven auswirkt, und bietet Entscheidungsrahmen für die Materialauswahl (Edelstahl gegenüber Polypropylen), die Einhaltung von EU-GMP-Anhang 1 und die vollständige SOP-Integration. Ganz gleich, ob Sie eine pharmazeutische Anlage auf der grünen Wiese entwerfen oder wiederkehrende EM-Ausfälle in bestehenden Betrieben beheben, Sie finden hier die technischen Spezifikationen und Validierungsabläufe zum Bau von Reinraum-Moppeimersystemen, die eine reproduzierbare Kontaminationskontrolle bieten.
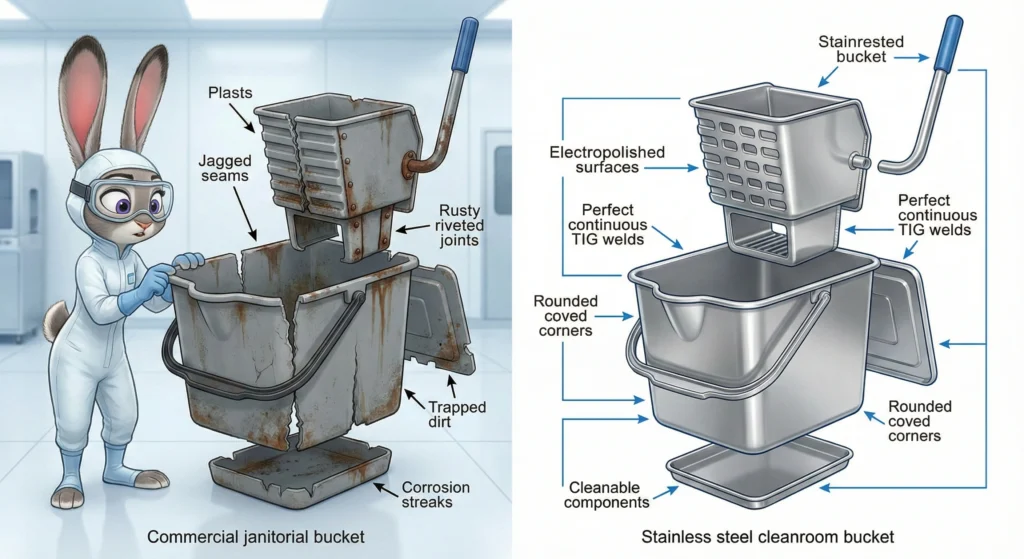
Abbildung 1: Komplettes Wischsystem mit drei Eimern in einem pharmazeutischen Reinraum der Klasse B mit ordnungsgemäßer Kleidung (steriler Kittel, Handschuhe, Gesichtsschutz), Eimerwagen aus Edelstahl mit getrennten Flüssigkeitsströmen (Desinfektionsmittel/Spülmittel/Abfall) und zur Kontaminationskontrolle positioniertem Auswringmechanismus. Diese Konfiguration erfüllt die EU-GMP-Anforderungen Anhang 1 für sterile Reinigungswerkzeuge und validierte Arbeitsabläufe zur Kontaminationskontrolle in aseptischen Verarbeitungsbereichen.
Was zeichnet einen Reinraum-Moppeimer aus?
Warum handelsübliche Eimer in Reinräumen versagen
Standard-Hausmeister-Moppeimer verfehlen die Reinraumqualifikation in vier kritischen Punkten. Erstens die Materialien: Bei handelsüblichen Eimern werden minderwertige Kunststoffe oder verzinkter Stahl mit rauen Oberflächen, Nähten und Spalten verwendet, die Partikel und Keime einfangen – also genau die Kontamination, die Sie entfernen möchten. Diese Materialien geben bei mechanischer Beanspruchung (Wringwirkung, Rollbewegung) Partikel ab und zersetzen sich unter Desinfektionsmitteln in pharmazeutischer Qualität. Zweitens die Entleerbarkeit: Handelsübliche Eimer haben einen flachen Boden mit abgerundeten Ecken, in denen sich Flüssigkeit ansammelt, wodurch Stagnationszonen entstehen, in denen sich zwischen den Reinigungszyklen Keime ansammeln. Sie können sie nicht vollständig entleeren und Sie können nicht bestätigen, dass restliches Desinfektionsmittel die nächste Lösungscharge nicht verunreinigt. Drittens, Schweißqualität und Verbindungsdesign: Standardschaufeln verwenden freiliegende Schweißnähte, Nietverbindungen und Gewindebefestigungen, die Partikelfallen bilden und wiederholte Autoklavenzyklen nicht überstehen, ohne zu korrodieren oder sich zu lösen. Viertens: Sterilisationskompatibilität: Die meisten handelsüblichen Eimer können einer Dampfautoklavierung bei 121 °C oder aggressiven Desinfektionsmitteln (Alkohole, Peroxide, Hypochlorite) nicht standhalten, ohne sich zu verziehen, zu reißen oder auszugasen, was sie für den pharmazeutischen Einsatz der Güteklasse A/B ausschließt, bei dem sterile Reinigungswerkzeuge obligatorisch sind.
GMP & ISO 14644-Anforderungen zur Kontaminationskontrolle
EU-GMP-Anhang 1 verlangt, dass in Reinräumen verwendete Materialien so ausgewählt werden, dass die Partikelbildung minimiert wird und der wiederholten Anwendung von Desinfektionsmitteln und sporiziden Mitteln standgehalten wird. Insbesondere müssen Reinigung und Desinfektion einem schriftlichen, validierten Programm folgen; Desinfektionsmittel und Reinigungsmittel, die in Bereichen der Klasse A/B verwendet werden, müssen vor der Verwendung steril sein; und der Reinigungsprozess muss Rückstände entfernen, die die Wirksamkeit des Desinfektionsmittels beeinträchtigen könnten. Die Verordnung schreibt die Verwendung von mehr als einem Desinfektionsmittel mit unterschiedlichen Wirkungsweisen, die regelmäßige sporizide Anwendung und die laufende Überwachung der Wirksamkeit und der Veränderungen der mikrobiellen Flora vor. ISO 14644 gibt den operativen Rahmen vor: Reinräume werden nach Grenzwerten für die Partikelkonzentration in der Luft klassifiziert (ISO-Klasse 5 = ≤3.520 Partikel ≥0,5 µm/m³; Klasse 8 = ≤3.520.000), und alle Aktivitäten – einschließlich der Reinigung – dürfen diese Grenzwerte nicht beeinträchtigen. Ihr Moppeimersystem muss validierte Reinigungsabläufe unterstützen, ohne Partikel einzubringen, die vollständige Entleerung zu verhindern oder Kreuzkontaminationsvektoren beim Transfer zwischen Bereichen zu erzeugen.
Designunterschiede: Schweißnähte, Verbindungen, Entwässerbarkeit, Oberflächenveredelung
Reinraum-Moppeimer verwenden durchgehende WIG-Schweißnähte (keine Punktschweißnähte) mit vollständiger Durchdringung und glatter Raupenoberfläche, wodurch Spalten und Partikelfallen vermieden werden. Die Verbindungen sind geschweißt oder ultraschallgeklebt (nicht genietet oder mit Gewinde versehen), und alle Innenecken verfügen über Hohlkehlenprofile mit großem Radius (typischerweise R10–15 mm), um Totzonen zu vermeiden, in denen sich Flüssigkeiten ansammeln. Die Entleerungsfähigkeit ist so konstruiert, dass die Eimer geneigt sind oder einen geneigten Boden haben, wobei die Entleerungsöffnungen am tatsächlichen Tiefpunkt positioniert sind, was eine vollständige Flüssigkeitsentfernung ermöglicht und eine Kontamination durch Verschleppung verhindert. Auf die Oberflächenveredelung kommt es an – Reinraumeimer aus Edelstahl werden elektropoliert (entfernt die Oberflächenrauheit auf Ra). <0,5 µm) und Passivierung (Chromoxidschicht verhindert Korrosion); Polypropyleneimer werden aus medizinischem Harz mit glatten Hohlraumoberflächen geformt, wodurch eine Nachbearbeitung vermieden wird, die zu Oberflächenfehlern führt. Rahmen und Rollen bestehen aus reinraumkompatiblen Materialien (Edelstahl, eloxiertes Aluminium, nicht abfärbende thermoplastische Räder) mit abgedichteten Lagern, um das Austreten von Schmiermittel und die Bildung von Partikeln während des Transports zu verhindern.

Abbildung 2: Vergleich der Schaufelkonfiguration zur Veranschaulichung der Prinzipien der Flüssigkeitstrennung. Ein-Eimer-Systeme (links) erzeugen Kontaminationsrückkopplungsschleifen, in denen der Boden zum Desinfektionsmittelreservoir zurückkehrt und die aktive Konzentration verdünnt. Doppeleimersysteme (Mitte) trennen sauberes Desinfektionsmittel vom Spülwasser und verhindern so eine direkte Rückführung, ermöglichen aber eine Verunreinigung des Spülwassers. Drei-Eimer-Systeme (rechts) isolieren kontaminiertes Abwasser in einem speziellen Abfalleimer und bewahren so die Integrität des Desinfektionsmittels und des Spülwassers während der gesamten Reinigungszyklen – entscheidend für pharmazeutische Bereiche der Güteklasse A/B, in denen validierte Desinfektionsmittelkonzentrationen eingehalten werden müssen.
Reinraum-Moppeimer-Konfigurationen (1-, 2-, 3-Eimer-Systeme)
Ein-Eimer-System: Wenn es akzeptabel ist (ISO 7–8)
Ein-Eimer-Systeme verwenden einen Eimer mit Desinfektionslösung; Der Mopp wird eingetaucht, über denselben Eimer ausgewrungen und wiederholt aufgetragen. Diese Konfiguration ist für die Erreichung einer GMP-Standardsauberkeit in der pharmazeutischen Herstellung nicht akzeptabel. Untersuchungen zeigen, dass beim Wischen mit nur einem Eimer bei jedem Wischvorgang wieder Erde und Mikroben in die Desinfektionslösung gelangen, wodurch die Wirkstoffkonzentration schnell verdünnt wird und nachfolgende Bodendurchgänge kontaminiert werden. Die Reduzierung der Keimzahl ist deutlich geringer als bei Methoden mit mehreren Eimern. Der Single-Eimer-Ansatz mag in nicht GMP-konformen industriellen Umgebungen (Lagerbüros, nicht klassifizierte Lagerräume) ausreichen, erfüllt jedoch nicht die Validierungsanforderungen des EU-GMP-Anhangs 1 für eine kontrollierte Kontaktzeit des Desinfektionsmittels und die Verhinderung von Kreuzkontaminationen. Selbst in pharmazeutischen Verpackungs- oder Bekleidungsbereichen der ISO-Klassen 7–8 bevorzugen behördliche Anforderungen und Best Practices für die Kontaminationskontrolle Konfigurationen mit zwei oder drei Eimern.
Dual-Eimer-System: Am gebräuchlichsten für pharmazeutische Bereiche
Doppeleimersysteme trennen sauberes Desinfektionsmittel physisch vom Spülwasser. Eimer 1 enthält die validierte Desinfektions- oder Reinigungslösung; Eimer 2 enthält sauberes Spülwasser, darüber befindet sich eine Presse. Der validierte Arbeitsablauf: Tragen Sie die Lösung aus Eimer 1 auf den Boden auf, kehren Sie zu Eimer 2 zurück, um den Mopp zu spülen und die kontaminierte Flüssigkeit auszuwringen, und füllen Sie ihn dann erneut mit frischer Lösung aus Eimer 1. Dieser zwischengeschaltete Spülschritt verhindert die Rückführung von Schmutz und Keimen in das aktive Desinfektionsmittel und sorgt für eine effektive Konzentration während des gesamten Reinigungszyklus. Dual-Eimer-Systeme eignen sich für pharmazeutische Bereiche der ISO-Klassen 6–8 (Produktionszonen der Klasse C/D, Personalschleusen, Umkleideräume, Verpackungsräume), in denen eine validierte Desinfektion erforderlich ist, das Risikoprofil jedoch einen vereinfachten Arbeitsablauf ermöglicht. Sie übertreffen Ein-Eimer-Methoden bei der Aufrechterhaltung der Desinfektionswirksamkeit und der Reduzierung mikrobieller Belastungen deutlich und stellen die Mindestkonfiguration für die GMP-Konformität in den meisten pharmazeutischen Reinigungs-SOPs dar. Das Spülwasser in Eimer 2 sammelt jedoch mit der Zeit Verunreinigungen an, und die ausgewrungene Flüssigkeit aus kontaminierten Mopps kann zurückspritzen und so eine sekundäre Kontaminationsquelle bilden.
Triple-Bucket-System: Erforderlich für Arbeitsabläufe gemäß Annex 1 Grade A/B/C
Drei-Eimer-Systeme fügen unter der Presse einen speziellen Abfalleimer hinzu, der kontaminiertes Abwasser sowohl vom Spülwasser als auch vom aktiven Desinfektionsmittel physisch isoliert. Die validierte Reihenfolge: Wischen Sie die Zieloberfläche mit Lösung aus Eimer 1 (Desinfektionsmittel/Reinigungsmittel), kehren Sie zur Presse über Eimer 3 (leerer Abfalleimer) zurück und wringen Sie die kontaminierte Flüssigkeit aus, spülen Sie den Mopp in Eimer 2 (sauberes Wasser) und wringen Sie ihn erneut in Eimer 3 aus, dann füllen Sie ihn erneut mit frischer Lösung aus Eimer 1. Dieses Protokoll minimiert die Kontamination sowohl des Spülwassers als auch der Desinfektionslösung und führt zu einer überlegenen Reinigungs- und Desinfektionswirksamkeit im Vergleich zum Doppeleimer Konfigurationen – insbesondere in Kombination mit mechanischen Auswringern, die die Flüssigkeitsextraktion maximieren. Branchenrichtlinien empfehlen Drei-Eimer-Systeme für aseptische Verarbeitungsbereiche der EU-GMP-Klasse A/B und Zonen der Klasse C mit Isolatoren, in denen die Kontaminationskontrollgrenzen am engsten sind und die Wirksamkeit des Desinfektionsmittels während längerer Reinigungszyklen auf einem validierten Niveau gehalten werden muss. Der Abfalleimer fängt die Keimbelastung auf, ohne sie erneut in das Reinigungssystem einzuführen, und ermöglicht so eine quantifizierbare Validierung der Stabilität der Desinfektionsmittelkonzentration und der mikrobiellen Reduktionsleistung.
Wie sich jede Konfiguration auf die Kontrolle der Keimbelastung auswirkt & Verwendung von Desinfektionsmitteln
Die Eimerkonfiguration bestimmt direkt die Verdünnungsrate des Desinfektionsmittels und die Ansammlung von Keimen. Bei Ein-Eimer-Systemen kommt es zu einer exponentiellen Verdünnung: Bei jedem Auswringvorgang wird der Lösung wieder schmutziges Wasser hinzugefügt, wodurch die Wirkstoffkonzentration verringert und die mikrobielle Belastung erhöht wird. Nach 10–15 Durchgängen auf dem Boden kann die Konzentration des Desinfektionsmittels unter die validierten Wirksamkeitsschwellen sinken und der Eimer wird zu einem Biobelastungsreservoir, das Oberflächen erneut kontaminiert. Systeme mit zwei Eimern verlangsamen diesen Abbau, indem sie die Mopps in separatem Wasser ausspülen, bevor sie das Desinfektionsmittel nachfüllen. Der Spüleimer sammelt jedoch immer noch Verunreinigungen an und muss häufig gewechselt werden (normalerweise alle 20–30 m² Bodenfläche). Drei-Eimer-Systeme sorgen durch vollständige Trennung des Abwassers für eine stabile Desinfektionsmittelkonzentration über eine Wischfläche von 50–100 m². Der Desinfektionsmittelverbrauch sinkt tatsächlich, da Sie die aktive Lösung nicht mit schmutzigem Spülwasser verdünnen. Der Nachteil: Drei-Eimer-Systeme erfordern mehr physischen Platz, mehr Bedienerschulung (strikte Einhaltung der Reihenfolge) und eine komplexere Workflow-Validierung – aber sie liefern eine reproduzierbare Kontaktzeit des Desinfektionsmittels und eine Mikrobenreduzierung, die einer behördlichen Prüfung standhält. Für die Herstellung von Arzneimitteln mit hohem Risiko (aseptische Abfüllung, Gefriertrocknung, Isolatorumgebungen) ist die Konfiguration mit drei Eimern praktisch obligatorisch.
Wringer vs. Presssysteme
Der Typ des Auswringmechanismus beeinflusst die Partikelerzeugung, die Effizienz der Flüssigkeitsextraktion und die Haltbarkeit des Autoklaven. Rollenwringer verwenden zwei parallele Rollen (aus Metall oder Hartplastik), die den Moppkopf zusammendrücken, wenn er zwischen ihnen hindurchläuft. Presssysteme verwenden einen perforierten Korb oder Käfig, den der Bediener nach unten gegen eine Platte drückt und so Flüssigkeit durch die Perforationen drückt. Mechanische Auswringer (Rollentyp mit Handkurbel- oder Fußpedalbetätigung) verbessern die Reinigungseffizienz in Systemen mit mehreren Eimern, indem sie die Flüssigkeitsextraktion maximieren – beim Auswringen werden 80–90 % der Flüssigkeit entfernt, gegenüber 60–70 % bei manuellen Presssystemen –, wodurch die Verschleppung von Verunreinigungen zwischen den Eimern reduziert und die Nutzungsdauer von Spülwasser und Desinfektionslösungen verlängert wird. Allerdings verfügen Walzenpressen über mehr bewegliche Teile (Lager, Zahnräder, Wellen), die bei unsachgemäßer Wartung Partikel erzeugen können, und ältere Konstruktionen verwenden freiliegende Metallkomponenten, die unter aggressiven Desinfektionsmitteln korrodieren. Pressensysteme sind mechanisch einfacher (weniger bewegliche Teile = geringeres Risiko der Partikelbildung), vollständig autoklavierbar, wenn sie aus Edelstahl oder Hochtemperatur-Polypropylen gefertigt sind, und einfacher zu reinigen/validieren, da es keine internen Mechanismen zum Einfangen von Keimen gibt. Für pharmazeutische Bereiche der Güteklasse A/B, in denen die Partikelkontrolle von entscheidender Bedeutung ist, sollten Sie Presse-Wringer mit Konstruktion aus elektropoliertem Edelstahl oder medizinischem PP, versiegelter Entwässerung und ohne freiliegende Lager wählen. Für Bereiche der Klasse C/D, in denen es auf den Durchsatz ankommt, bieten Rollenpressen mit reinraumkompatiblen Lagern (abgedichtetes, lebensmitteltaugliches Schmiermittel) und korrosionsbeständiger Konstruktion einen schnelleren Betrieb. Die Autoklavenkompatibilität ist der entscheidende Faktor: Pressensysteme sind zu 100 % autoklavierbar und zeigen über 500 Dampfzyklen hinweg keinen Leistungsabfall; Rollenpressen mit Kunststoffzahnrädern oder nicht abgedichteten Lagern müssen möglicherweise nach 50–100 Zyklen ausgetauscht werden.

Abbildung 3: Vergleich des Wringer-Mechanismus für Partikelerzeugung und Autoklavenkompatibilität. Rollenpressen (links) verwenden Zahnräder, Wellen und Lager, die die Flüssigkeitsextraktion maximieren (80–90 %), erzeugen aber Partikel aus beweglichen Teilen und erfordern einen Komponentenaustausch nach 50–100 Autoklavenzyklen. Pressen-Wringer (rechts) verwenden einfache perforierte Körbe mit manueller Kompression und bieten eine geringere Flüssigkeitsextraktion (60–70 %), aber 100 % Autoklavenkompatibilität über mehr als 500 Zyklen ohne bewegliche Teile, die Keime einfangen – bevorzugt für Umgebungen der Klasse A/B, in denen die Partikelkontrolle von entscheidender Bedeutung ist.
Wie Moppeimer die Kontamination reduzieren
Trennung von sauberen und schmutzigen Flüssigkeiten
Die physische Trennung von sauberem Desinfektionsmittel, Spülwasser und kontaminiertem Abwasser ist das zentrale Prinzip der Kontaminationskontrolle. Wenn sich saubere und verunreinigte Flüssigkeiten vermischen – wie bei Systemen mit nur einem Eimer –, entsteht eine kontinuierliche Kontaminationsrückkopplungsschleife: Vom Boden entfernte Erde und Keime kehren in den Desinfektionsmittelbehälter zurück, wodurch die aktive Konzentration verringert, die mikrobielle Belastung erhöht und schließlich nachfolgende Oberflächendurchgänge erneut kontaminiert werden. Systeme mit mehreren Eimern durchbrechen diesen Kreislauf, indem sie jedem Flüssigkeitsstrom separate Gefäße zuweisen. Bei Konfigurationen mit zwei Eimern gelangt die aus dem Mopp ausgewrungene kontaminierte Flüssigkeit in Eimer 2 (Spülwasser), wo mechanische Verdünnung und Absetzen die Keimbelastung verringern, bevor der Mopp aus Eimer 1 (sauberes Desinfektionsmittel) erneut beladen wird. Bei Konfigurationen mit drei Eimern werden kontaminierte Abwässer in Eimer 3 (Abfall) aufgefangen, ohne dass sie sich mit Spülwasser oder Desinfektionsmittel vermischen. Diese Trennung ermöglicht eine quantitative Validierung: Sie können Eimer 1 während des gesamten Reinigungszyklus beproben, um zu überprüfen, ob die Desinfektionsmittelkonzentration über den Wirksamkeitsschwellen bleibt, und Sie können Abfall aus Eimer 3 kultivieren, um die gesamte entfernte Keimbelastung zu messen – Daten, die Reinigungsvalidierungsprotokolle unterstützen und Auditergebnisse abschließen.
Verhinderung der Verdünnung von Desinfektionsmitteln & Wiederablagerung von Rückständen
Die Verdünnung von Desinfektionsmitteln ist der versteckte Fehlermodus in schlecht konzipierten Eimersystemen. Jeder Milliliter Schmutzwasser, der in den Desinfektionsmitteleimer zurückgewrungen wird, verringert die Wirkstoffkonzentration. Bei quartären Ammoniumverbindungen, die bei 200 ppm validiert wurden, sinkt die Konzentration bei einer 10-prozentigen Verdünnung auf 180 ppm – möglicherweise unter der minimal wirksamen Konzentration gegen Zielorganismen. Bei sporiziden Wasserstoffperoxid-Protokollen (6 % H₂O₂ mit 10-minütiger Kontaktzeit) kann eine Verdünnung auf 5,2 % Ihre gesamte Validierungsstudie ungültig machen. Drei-Eimer-Systeme verhindern diese Verschlechterung, indem sie sicherstellen, dass nur sauberes, unbenutztes Desinfektionsmittel in Eimer 1 gelangt. Ausgewrungene Flüssigkeit wird verschwendet und gelangt nicht zurück in die aktive Lösung. Die erneute Ablagerung von Rückständen – das Phänomen, bei dem kontaminierte Moppköpfe erneut biologische Belastung auf zuvor gereinigte Oberflächen auftragen – wird durch den obligatorischen Spülschritt in Eimer 2 verhindert. In den Moppkopffasern eingeschlossene Schmutzpartikel und mikrobielle Zellen werden in das Spülwasser abgegeben und in den Abfall ausgewrungen, anstatt in den nächsten Bodenabschnitt übertragen zu werden. Aus diesem Grund verlangt der EU-GMP-Anhang 1 eine Reinigung vor der Desinfektion: Durch die Entfernung grober Verunreinigungen und Rückstände wird sichergestellt, dass das Desinfektionsmittel die validierte Kontaktzeit auf sauberen Oberflächen erreichen kann, anstatt durch organische Belastung oder physikalische Barrieren inaktiviert zu werden.
Minimierung der vom Bediener verursachten Partikelerzeugung
Das Design des Schaufelsystems beeinflusst die Art und Weise, wie Bediener mit der Ausrüstung interagieren, was sich direkt auf die Partikelerzeugung auswirkt. Schlecht konstruierte Eimer erfordern umständliches Heben, übermäßiges Biegen oder kräftiges Auswringen – all dies erhöht die Bewegung des Bedieners und die mechanische Belastung, die Partikel aus Kittelmaterialien und Moppkomponenten freisetzt. Reinraumoptimierte Eimersysteme nutzen ergonomische Funktionen: Auswringvorrichtungen mit Fußpedal (freihändiger Betrieb reduziert Handschuhkontakt und Partikelbildung), kippbare Eimerrahmen (eliminiert das Anheben zum Entleeren des Abfalls) und mobile Wagen mit feststellbaren Rollen (stabile Auswringplattform verhindert Spritzer). Die Höhe der Presse und die Länge des Moppstiels sind so festgelegt, dass der Bediener in neutraler Haltung arbeiten kann, ohne übermäßiges Greifen oder Bücken – ein entscheidender Faktor bei vollständig aseptischen Umhängen, bei denen die Bewegungsfreiheit eingeschränkt ist. Glatte Flüssigkeitsströmungswege (breite Eimeröffnungen, Tropfschutz, Spritzschutz) verhindern die Aerosolbildung und das Verspritzen von Tröpfchen, die auftreten, wenn ausgewrungene Flüssigkeit mit hoher Geschwindigkeit auf die Eimerwände trifft. Diese Konstruktionsdetails sind in Umgebungen der Klasse A/B von Bedeutung, in denen der unidirektionale Luftstrom nicht gestört werden darf und die Partikelerzeugung aus allen Quellen – einschließlich Reinigungsvorgängen – minimiert werden muss, um die Partikelgrenzwerte der ISO-Klasse 5 einzuhalten.
Validierung von Eimersystemen während der EM (Umweltüberwachung)
Die Umweltüberwachung liefert den Beweis, dass Ihre Eimersystemkonfiguration eine validierte Kontaminationskontrolle bietet. EM-Protokolle sollten die Partikelanzahl (lebensfähig und nicht lebensfähig) vor und nach der Reinigung an repräsentativen Bodenstandorten umfassen, wobei die Akzeptanzkriterien an die angestrebte ISO-Klasse gebunden sein sollten. Beispielsweise sollte in Bereichen der ISO-Klasse 7 (≤352.000 Partikel ≥0,5 µm/m³ im Ruhezustand) die Partikelzahl innerhalb von 15–30 Minuten nach der Reinigung wieder auf das Ruheniveau zurückkehren; Eine anhaltende Erhöhung weist darauf hin, dass der Reinigungsvorgang selbst eine Partikelquelle ist – was häufig auf eine unzureichende Eimerkonfiguration oder beschädigte Moppköpfe zurückzuführen ist. Die Probenahme mikrobieller Oberflächen (Kontaktplatten, Tupfer) vor und nach der Desinfektion bestätigt die Reduzierung der Keimbelastung; Nichterreichen >Eine Reduzierung um 3 log weist typischerweise auf eine Desinfektionsmittelverdünnung (Einzel- oder schlecht verwaltetes Doppeleimersystem) oder eine unzureichende Kontaktzeit hin. Eine Trendanalyse ist von entscheidender Bedeutung: Wenn die Partikel- oder Mikrobenzahl bei aufeinanderfolgenden Reinigungszyklen bei Verwendung derselben Eimerkonfiguration ansteigt, wird Ihr Spülwasser oder Desinfektionsmittel zu einem Kontaminationsreservoir – dem rauchenden Beweis für unzureichende Flüssigkeitstrennung. Validieren Sie Ihr Eimersystem, indem Sie nachweisen, dass die Desinfektionsmittelkonzentration (gemessen über Titration oder Teststreifen) während eines vollständigen Reinigungszyklus über der maximalen Bodenfläche Ihrer Einrichtung pro Eimerwechsel über den validierten Wirksamkeitsschwellen bleibt. Für grundlegende Prinzipien der Kontaminationskontrolle, siehe ausführliche Reinraum-Mopp-Anleitung.
Wie das richtige Bucket-Design Audit-Beobachtungen reduziert
Aufsichtsinspektoren suchen nach drei Bucket-bezogenen Fehlermodi. Erstens unzureichende Flüssigkeitstrennung: Wenn Sie Ein-Eimer-Systeme oder Doppel-Eimer-Systeme ohne validierte Wechselfrequenzen verwenden, müssen Sie mit einer 483-Beobachtung für Reinigungsverfahren rechnen, die nicht validiert sind, um Kreuzkontaminationen zu verhindern. Zweitens, unsterile Desinfektionsmittel der Klasse A/B: Anhang 1 fordert ausdrücklich sterile Desinfektionsmittel und Reinigungsgeräte für aseptische Bereiche; Wenn Ihre Eimer und Lösungen nicht mit dokumentiertem SAL 10⁻⁶ vorsterilisiert oder autoklaviert sind, ist das ein Befund. Drittens fehlt die Validierungsdokumentation: Prüfer werden Sie nach Ihrem Eimersystem-Qualifizierungsprotokoll (IQ/OQ/PQ), einer Reinigungsvalidierungsstudie, die die Stabilität des Desinfektionsmittels und die Reduzierung der Keimbelastung auf repräsentativen Bodenflächen zeigt, sowie nach einer SOP fragen, die die Häufigkeit des Eimerwechsels, die Wartung der Presse und die Schulung des Bedieners definiert. Das richtige Eimerdesign – Dreifacheimer für Klasse A/B/C, autoklavierbare Materialien, vollständige Entleerbarkeit, validierte Reinigungsabläufe – bietet die technische Grundlage, um diese Fragen mit Daten zu beantworten. Wenn Inspektoren fragen: „Wie stellen Sie sicher, dass die Konzentration des Desinfektionsmittels während des gesamten Reinigungszyklus wirksam bleibt?“ Sie verweisen auf Ihr Drei-Eimer-Trennprotokoll und die Trenddaten zur Desinfektionsmittelkonzentration. Wenn sie fragen: „Wie verhindern Sie eine Kreuzkontamination zwischen Produktchargen?“ Sie zeigen ihnen Ihren validierten Eimer-Sterilisationszyklus und den dedizierten Eimerbestand pro Fertigungsbereich.
Empfohlene Eimermaterialien: Edelstahl vs. Polypropylen (PP)
Edelstahl (SS304 / SS316): Autoklavierbar, längste Lebensdauer
Für Reinraumeimer aus Edelstahl wird entweder eine Legierung der Güteklasse 304 oder 316 verwendet. Beide bieten bei ordnungsgemäßer Wartung volle Autoklavenkompatibilität und eine lange Lebensdauer. SS316 bietet im Vergleich zu 304 eine überlegene Korrosionsbeständigkeit, insbesondere wenn es Natriumhypochlorit-Desinfektionsmitteln (Bleichmittel) ausgesetzt wird. Untersuchungen zeigen, dass Hypochlorit-Ionen Edelstahl aggressiv angreifen und Lochfraß und Spaltkorrosion verursachen. Allerdings verträgt 316 Restchlorkonzentrationen von 15–20 ppm bis zu 24 Stunden lang, wenn die Kontaktzeit minimiert wird, die Temperatur Umgebungstemperatur bleibt und nach der Exposition gründlich gespült wird. Für Einrichtungen, die eine Desinfektionsmittelrotation auf Bleichmittelbasis (500–5000 ppm Natriumhypochlorit) verwenden, ist SS316 die sicherere Spezifikation – obwohl selbst 316 strenge Protokolle (geringe Konzentration, kurzer Kontakt, sofortiges Spülen) erfordert, um Korrosion zu verhindern.
Elektropolieren und Passivieren sind obligatorische Oberflächenbehandlungen: Durch Elektropolieren wird die Oberflächenrauheit auf Ra entfernt <00,5 µm, wodurch Partikelfallen eliminiert werden; Durch die Passivierung entsteht eine Chromoxidschicht, die Korrosion und chemischen Angriffen widersteht. Edelstahleimer sind zu 100 % autoklavierbar bei 121 °C für 30 Minuten und mehr als 500 Dampfzyklen ohne Leistungseinbußen – was sie zum Goldstandard für pharmazeutische Anlagen der Güteklasse A/B macht, die eine tägliche Sterilisation erfordern. Kontinuierliche WIG-Schweißnähte mit vollständiger Durchdringung, gewölbten Innenecken (Radius R10–15 mm) und einer glatten Raupenoberfläche verhindern Spalten und ermöglichen eine vollständige Entwässerung.
Der Kompromiss: Edelstahleimer kosten im Voraus drei- bis fünfmal mehr als Polypropylenäquivalente (200 bis 400 US-Dollar pro Eimer gegenüber 50 bis 100 US-Dollar für PP). Allerdings verlängert sich die Lebensdauer von SS316 bei typischer pharmazeutischer Verwendung um 10–15 Jahre (vorausgesetzt, ein ordnungsgemäßes Hypochlorit-Management) und führt zu niedrigeren Gesamtbetriebskosten als PP-Eimer, die alle 2–3 Jahre ausgetauscht werden. Das Gewicht spielt eine Rolle – Edelstahlrahmen und -schaufeln sind deutlich schwerer als PP, was sich auf die Ergonomie des Bedieners und die Manövrierfähigkeit des Wagens auswirkt.
PP in Reinraumqualität: Leicht, korrosionsbeständig
Polypropyleneimer werden aus medizinischem Harz (Dichte 0,855–0,946 g/cm³) geformt und bieten leichte Handhabung, umfassende chemische Beständigkeit und Autoklavenkompatibilität bei geringeren Vorlaufkosten. PP widersteht den meisten pharmazeutischen Desinfektionsmitteln bei Raumtemperatur: 70 % Isopropylalkohol, 3–6 % Wasserstoffperoxid, quartäre Ammoniumverbindungen und moderate Konzentrationen nicht oxidierender Säuren/Basen können in PP-Behältern gelagert und verwendet werden. PP weist im Vergleich zu Edelstahl eine bessere Toleranz gegenüber hochkonzentrierten Bleichmitteln auf (kein Lochfraßrisiko), obwohl Oxidationsmittel den Abbau von PP mit der Zeit beschleunigen.
PP-Eimer halten wiederholten Autoklavenzyklen bei 121 °C stand – aus diesem Grund wird PP in der Medizin- und Laborausrüstung häufig verwendet. Wiederholte Hitzeeinwirkung führt jedoch zu einer thermooxidativen Alterung: PP versprödet allmählich, es kommt zu Oberflächenrissen, Haarrissen und einem Verlust der Schlagfestigkeit. Die typische Lebensdauer beträgt 50–100 Autoklavenzyklen, bevor eine sichtbare Beeinträchtigung (Weißfärbung, Sprödigkeit, Mikrorisse) einen Austausch erfordert – etwa 1–2 Jahre bei stark beanspruchten pharmazeutischen Betrieben im Vergleich zu 10+ Jahren bei Edelstahl.
Der anfängliche Kostenvorteil (50–100 US-Dollar pro Eimer) macht PP für Einrichtungen mit begrenzten Kapitalbudgets, geringerer Autoklavenhäufigkeit oder Einweg-/Einweg-Arbeitsabläufen attraktiv. PP-Eimer werden häufig für Supportbereiche der Güteklasse C/D, Biotech-Pilotanlagen und Mehrprodukthersteller spezifiziert, die den Eimerbestand nach Produktlinie trennen, um Kreuzkontaminationen zu verhindern. Die Gewichtsreduzierung (PP-Eimer wiegen 60–70 % weniger als Edelstahläquivalente) verbessert die Ergonomie des Bedieners und reduziert die körperliche Belastung beim Transport.
Chemische Kompatibilitätsmatrix
| Desinfektionsmitteltyp | Edelstahl (SS316) | Polypropylen (PP) |
| 70 % Isopropylalkohol (IPA) | Exzellent; Keine Verschlechterung über 1000+ Zyklen hinweg | Exzellent; stabil bei Raumtemperatur |
| Wasserstoffperoxid (3–6 %) | Exzellent; Überprüfen Sie die Konzentrations-/Temperaturgrenzen | Gut; baut sich schneller ab >6 % oder erhöhte Temperatur |
| Natriumhypochlorit (500–5000 ppm) | Mäßig; 316 verträgt 15–20 ppm beim Spülen; Höhere Konzentrationen erfordern strenge Protokolle | Exzellent; kein Lochfraßrisiko; oxidative Alterung im Laufe der Zeit |
| Quartäre Ammoniumverbindungen | Exzellent; breite Kompatibilität | Exzellent; Stabil mit den meisten QAC-Formulierungen |
| Autoklav (121°C, 30 Min.) | 500+ Zyklen; kein Leistungsverlust | 50–100 Zyklen vor der Versprödung |
| Lebensdauer (typische Pharmaanwendung) | 10–15 Jahre (bei ordnungsgemäßem Hypochloritmanagement) | 1–3 Jahre (starke Nutzung); 3–5 Jahre (mäßige Nutzung) |
| Vorabkosten (pro Bucket) | 200–400 $ | 50–100 $ |
| Gesamtbetriebskosten (10 Jahre Lebensdauer) | 200–400 $ (Einzelkauf) | 200–500 $ (3–5 Ersatz) |

Abbildung 4: Vergleichsmatrix für Eimermaterial im Vergleich zwischen Edelstahl SS316 (links) und Polypropylen in Reinraumqualität (rechts). SS316 bietet mehr als 500 Autoklavenzyklen, eine Lebensdauer von 10–15 Jahren und eine hervorragende Korrosionsbeständigkeit (toleriert 15–20 ppm Restchlor beim Spülen) bei höheren Vorabkosten (200–400 US-Dollar). PP bietet eine leichte Handhabung (60–70 % Gewichtsreduzierung), kein Risiko von Lochfraß durch Bleichmittel und geringere Anfangsinvestitionen (50–100 US-Dollar), muss jedoch aufgrund der thermooxidativen Versprödung nach 50–100 Autoklavenzyklen (1–3 Jahre) ausgetauscht werden. Die Materialauswahl hängt von der Autoklavenhäufigkeit, der Desinfektionschemie und der TCO-Analyse der Anlage ab.
Auswirkungen von Desinfektion und Autoklavenzyklus auf die Materialstabilität
Die Häufigkeit des Autoklavenzyklus bestimmt direkt die Häufigkeit des Austauschs des PP-Eimers. Bei der täglichen Autoklavierung von Eimern (365 Zyklen/Jahr) kommt es innerhalb von 3–6 Monaten zu einem PP-Abbau; Die wöchentliche Autoklavierung (52 Zyklen/Jahr) verlängert die PP-Lebensdauer auf 18–24 Monate. Überwachen Sie PP-Eimer auf Austauschindikatoren: Oberflächenbleichung/Kreidung, Sprödigkeit (Risse beim Herunterfallen oder Beanspruchen), Verziehen (Eimer sitzen nicht mehr flach oder dichten nicht mehr richtig ab) und Undichtigkeiten an Nähten oder Bodenverbindungen. Ersetzen Sie es sofort, wenn eine Verschlechterung auftritt. Bei fortgesetzter Verwendung besteht die Gefahr der Bildung von Partikeln und der Verunreinigung der Reinigungslösungen.
Edelstahleimer weisen durch Autoklavenzyklen eine minimale Beeinträchtigung auf, erfordern jedoch nach der Desinfektion eine Wartung, wenn sie Hypochlorit ausgesetzt sind: Unmittelbar nach dem Bleichmittelkontakt gründlich mit deionisiertem Wasser ausspülen, vierteljährlich auf Lochfraß oder Spaltkorrosion prüfen und erneut passivieren, wenn die Oberfläche matt oder verfärbt ist. Einrichtungen, die aggressive Bleichprotokolle verwenden (>1000 ppm, tägliche Exposition) sollten einen Wechsel zu Wasserstoffperoxid oder sporiziden Mitteln auf Alkoholbasis in Betracht ziehen, um die Lebensdauer von Edelstahl zu verlängern.
Wie sich die Materialauswahl auf die langfristigen Gesamtbetriebskosten auswirkt
Bei der pharmazeutischen Produktion mit hohem Volumen (tägliche Autoklavenzyklen, großer Eimerbestand, Anlagenlebensdauer von mehr als 10 Jahren) bietet Edelstahl SS316 trotz drei- bis fünfmal höherer Vorlaufkosten die niedrigsten Gesamtbetriebskosten. Eine Anlage mit 20 Eimern, die täglich autoklaviert werden, ersetzt PP-Eimer drei- bis fünfmal über einen Zeitraum von 10 Jahren (3.000 bis 10.000 US-Dollar Gesamtkosten plus Entsorgungs- und Requalifizierungsarbeit) im Vergleich zum einmaligen Kauf von Edelstahl (4.000 bis 8.000 US-Dollar ohne Ersatz). Berücksichtigen Sie den Arbeitsaufwand für die Validierung: Jede Ersatzcharge eines PP-Eimers erfordert erneute Qualifizierungstests (Partikelerzeugung, chemische Kompatibilität, Dimensionsstabilität) – Qualitätssicherungsarbeit, die bei Edelstahl entfällt.
Für Betriebe mit geringem Volumen (Pilotanlagen, R&D Reinräume, seltene Autoklavenzyklen, <Bei Projektlaufzeiten von 5 Jahren bieten PP-Eimer eine bessere Wirtschaftlichkeit. Eine kleine Biotech-Firma mit 5 Eimern, die wöchentlich autoklaviert wird, wird PP 18 bis 24 Monate lang verwenden, bevor es ersetzt wird (250 bis 500 US-Dollar im Voraus), gegenüber 1.000 bis 2.000 US-Dollar für Edelstahl – und die Anlage kann skaliert oder umgestellt werden, bevor das PP das Ende seiner Lebensdauer erreicht. Für komplett integrierte Wischsysteme, siehe Kaufratgeber zum Vergleich der Eimer-/Mopp-/Wagenkonfigurationen.
Ideales Moppeimer-Setup für die Pharmaindustrie & Biotechnologie
EU-Anhang 1 Erwartungen für Reinigungswerkzeuge der Klassen A/B/C/D
EU-GMP-Anhang 1 schreibt vor, dass Desinfektionsmittel und Reinigungsmittel, die in Bereichen der Klasse A/B verwendet werden, vor der Verwendung steril sein müssen. Diese Anforderung erstreckt sich auch auf die Eimer, die diese Lösungen enthalten: entweder Eimer vorsterilisieren (Gammastrahlung, EO-Gas, Autoklav mit SAL 10⁻⁶-Dokumentation) oder validierte interne Autoklavenprotokolle implementieren. Arbeitsabläufe der Güteklasse A/B erfordern Systeme mit drei Eimern, um die Konzentration des Desinfektionsmittels aufrechtzuerhalten und Kreuzkontaminationen zu verhindern. Auch Bereiche der Klasse C mit Isolatoren oder Hochrisikoverarbeitung profitieren von Drei-Eimer-Konfigurationen. In den Supportbereichen der Klassen C/D (Umkleideräume, Verpackungsräume, Luftschleusen) können Dual-Eimer-Systeme mit validierten Wechselhäufigkeiten eingesetzt werden.
Alle Eimer – unabhängig von der Qualität – müssen aus Materialien bestehen, die die Bildung von Partikeln minimieren, der wiederholten Anwendung von Desinfektionsmitteln/Sporiziden standhalten und eine vollständige Entleerung ermöglichen. Gewölbte Ecken, glatte Oberflächen, durchgehende Schweißnähte und Kipprahmen zur Abfallentsorgung sind nicht verhandelbare Gestaltungsmerkmale. Beim Transport von Eimern zwischen den Klassen ist eine validierte Transferdesinfektion erforderlich: Eimer der Klasse D müssen einer Oberflächendesinfektion unterzogen werden, bevor sie in die Klasse C gelangen, und Eimer der Klasse C erfordern validierte Transferprotokolle, bevor sie in die Klasse B gelangen.
Komplette Eimersystemkonfiguration (Eimer + Presse + Rahmen)
Ein validiertes Reinraum-Moppeimersystem integriert mehrere Komponenten: Eimer (sauberes Desinfektionsmittel, Spülwasser, Abfall), Auswringmechanismus (Druck- oder Rollenmechanismus), mobiler Wagenrahmen (rostfreies oder eloxiertes Aluminium mit Reinraumrollen) und Zusatzfunktionen (Moppgriffaufbewahrung, Handschuh-/Werkzeughaken, Tropfschutz). Für die Einrichtung mit drei Eimern der Güteklasse A/B: Konfigurieren Sie Eimer 1 (5–10 l Fassungsvermögen) mit sterilem Desinfektionsmittel, Eimer 2 (10–15 l) mit sterilem Spülwasser und Eimer 3 (10–15 l) als leeren Abfallsammler unter der Presse. Positionieren Sie die Presse direkt über Eimer 3, um die gesamte ausgewrungene Flüssigkeit aufzufangen, ohne zu spritzen.
Wagenrahmen müssen nicht abfärbende, reinraumtaugliche Rollen (Räder aus Polyurethan oder Thermoplast, abgedichtete Lager, Feststellmechanismen) verwenden, die sanft gleiten, ohne Partikel zu erzeugen oder Bodenspuren zu hinterlassen. Die integrierte Werkzeugaufbewahrung (Clips für Moppgriffe, Sprühflaschenhaken) hält alle Reinigungsutensilien auf einer mobilen Plattform und reduziert so das Risiko einer Kreuzkontamination beim Transport von Raum zu Raum. Tropfschutz und Spritzschutz rund um die Presszonen verhindern die Aerosolisierung kontaminierter Flüssigkeiten.
SOP-Integration: Desinfektionsmittelwechsel, Moppwechsel, Abfallentsorgung
SOPs müssen validierte Arbeitsabläufe für jedes Bucket-Systemelement definieren. Desinfektionsmittelrotation: Geben Sie nach Tag/Woche an, welche Desinfektionsmittel Eimer 1 bevölkern (z. B. Montag/Mittwoch = 70 % IPA; Dienstag/Donnerstag = 3 % H₂O₂; Freitag = 1000 ppm Bleichmittel; wöchentlich = sporizides Mittel), validierte Kontaktzeiten für jedes einzelne Mittel und maximale Nutzungsdauer für vorbereitete Lösungen. Austausch des Moppkopfes: Definieren Sie die Häufigkeit pro gereinigtem Bereich (z. B. Moppkopf alle 30 m² oder bei sichtbarer Verschmutzung austauschen), Trennung nach Qualität (Mopps der Klasse A/B werden nie in C/D verwendet) und validierte Wasch-/Sterilisationszyklen zwischen den Verwendungen.
Abfallhandhabung: Geben Sie an, wie der Inhalt von Eimer 3 entsorgt wird (chemischer Abfallstrom, Abfluss in ein validiertes Waschbecken, Biogefährdungsprotokoll je nach Herstellungsprodukt), maximales Füllvolumen vor dem Entleeren (verhindern Sie Spritzer während des Transports) und Dekontaminationsanforderungen vor der Wiederverwendung des Eimers. Farbkodieren Sie Eimer und Moppstiele nach Klasse oder Desinfektionsmitteltyp: blau für Klasse A/B, grün für Klasse C, gelb für Klasse D; oder rot für Bleichmittel, blau für Peroxid, klar für Alkohol. Visuelles Management verhindert Bedienfehler, die eine Kreuzkontamination auslösen.
Empfohlene Eimergrößen, Füllstände und Etikettencodierung
Die Eimergröße gleicht das Desinfektionsmittelvolumen (ausreichend für die gewünschte Bodenfläche) gegen Gewicht/Ergonomie aus (Bediener können voll beladene Wagen manövrieren). Dreieimersysteme der Klasse A/B: 5–10 l Fassungsvermögen für Eimer 1 (Desinfektionsmittel – kleineres Volumen erhält die Konzentration aufrecht), 10–15 l für Eimer 2 (Spülwasser – größeres Volumen ermöglicht mehrere Spülzyklen), 15–20 l für Eimer 3 (Abfallsammler). Doppeleimersysteme der Klasse C/D: 10–15 l für beide Eimer. Füllen Sie die Eimer zu 60–70 % ihres Fassungsvermögens (verhindert ein Schwappen während des Transports und schafft Platz für ausgewrungene Flüssigkeit im Abfalleimer).
Die Etikettencodierung muss Folgendes umfassen: Eimerfunktion (Desinfektionsmittel/Spülen/Abfall), Zielqualität (A/B/C/D), Art und Konzentration des Desinfektionsmittels, Datum/Uhrzeit der Zubereitung, Ablaufdatum/-uhrzeit (gemäß validierten Nutzungsgrenzwerten) und Initialen des Bedieners. Verwenden Sie wasserfeste, autoklavenstabile Etiketten (lasergeätzte Edelstahletiketten, Hochtemperatur-Polyesteretiketten), die Dampf bei 121 °C überstehen, ohne zu verblassen oder abzublättern. Farblich gekennzeichnete Deckel oder Eimeraußenflächen sorgen bei schnellen Reinigungsvorgängen für eine visuelle Bestätigung auf einen Blick.
Visuelles Management: Farbcodierung für Raumklassen und Arbeitsabläufe
Die Farbcodierung verhindert die häufigsten Ausfälle des Eimersystems: die Verwendung von Eimern der Güteklasse C/D in der Güteklasse A/B ohne erneute Sterilisation, das Mischen von Desinfektionsmitteltypen oder die Überschreitung der validierten Verwendungsdauer der Lösung. Implementieren Sie eine zweistufige Codierung: Die Primärfarbe gibt die Zielqualität an (blau = A/B, Grün = C, Gelb = D), die Sekundärfarbe gibt die Desinfektionsmittelfamilie an (roter Streifen = Oxidationsmittel wie Bleichmittel/Peroxid, blauer Streifen = Alkohole, weißer Streifen = Quats). Weisen Sie die Bediener darauf hin, dass Eimer ohne validierte Sterilisation niemals in höhere Qualitäten befördert werden – visuelle Hinweise verstärken die Verfahrenskontrollen.
Alternativ können Sie den Code nach Fertigungssuite oder Produktlinie kodieren: violette Eimer für die Fertigung von Produkt A, orange für Produkt B, grau für gemeinsam genutzte Bereiche mit mehreren Produkten. Dies verhindert Kreuzkontaminationen zwischen Produktkampagnen und vereinfacht die Reinigungsvalidierung (jede Produktlinie verfügt über einen eigenen Eimerbestand, wodurch das Risiko einer Verschleppung vermieden wird).
Anleitung zum Autoklavenzyklus für Eimer und Komponenten
Autoklavieren Sie Eimer und Wringerkomponenten getrennt von den Moppköpfen, um eine Überlastung zu verhindern und das Eindringen von Dampf sicherzustellen. Standardzyklus: 121 °C für mindestens 30 Minuten, Schwerkraft- oder Vorvakuumzyklus je nach Beladungsdichte. Demontieren Sie die Pressmechanismen (entfernen Sie Pressplatten und Rolleneinheiten) und richten Sie die Eimer umgekehrt oder geneigt aus, um den Ablauf des Kondensats zu ermöglichen. Eimer nicht ineinander stapeln (Dampf einschließen, Durchwärmen verhindern); Verwenden Sie Autoklavengestelle mit einem Abstand zwischen den Eimern von 5–10 cm.
Nach dem Autoklavieren: Lassen Sie die Eimer vor der Verwendung in einer sterilen Lagerung (mindestens Klasse C) abkühlen. Wenn eine sofortige Verwendung in Klasse A/B erforderlich ist, übertragen Sie die Eimer über eine validierte Durchreiche- oder Materialschleuse mit validierter Transferdesinfektion. Dokumentieren Sie jeden Autoklavenzyklus (Beladungsinhalt, Zyklusparameter, Ergebnisse der biologischen Indikatoren, Unterschrift des Bedieners) gemäß 21 CFR 211.182 Gerätereinigungsaufzeichnungen. Überprüfen Sie die Wirksamkeit des Autoklaven vierteljährlich mit biologischen Indikatoren (Geobacillus stearothermophilus-Sporenstreifen), die an den Stellen mit der ungünstigsten Beladung (Eimerinnenraum, Auswringverbindungen) angebracht werden.
Validierungsfreundliche Workflow-Checkliste (GMP-ready)
☑ Sterilisation vor dem Gebrauch: Eimer, Pressen und Rahmen 30 Minuten lang bei 121 °C autoklavieren (oder vom Hersteller bereitgestellte sterile Verbrauchsmaterialien mit SAL 10⁻⁶-Dokumentation). Lagern Sie sterilisierte Eimer bis zur Verwendung in der Güteklasse C oder besser. Bereiten Sie sterile Desinfektionsmittel in gereinigten/sterilisierten Behältern vor (Anforderung der Klasse A/B); Überwachung auf mikrobielle Kontamination und Kontrolle des Verfallsdatums.
☑ Qualifikationsdokumentation: Aufrechterhaltung der IQ (Installationsqualifikation) durch Dokumentation des Eimersystemdesigns, der Materialien, der Autoklavenkompatibilität und der Spezifikationen für die Oberflächenbeschaffenheit. Vollständige OQ (Betriebsqualifizierung), die die Desinfektionsmittelabdeckung, Kontaktzeiten, Leistung der Presse und validierte Wechselhäufigkeiten definiert. Führen Sie eine PQ (Leistungsqualifizierung) durch, um die Partikelanzahl und die Reduzierung der Keimbelastung auf repräsentativen Bodenflächen zu demonstrieren, abgestimmt auf die Anlagenqualität und EM-Akzeptanzkriterien.
☑ Reinigungsvalidierung: Validieren Sie den Eimerreinigungsprozess, um Rückstände und Ablagerungen zu entfernen, die die Wirksamkeit des Desinfektionsmittels beeinträchtigen. Nachweis der Stabilität der Desinfektionsmittelkonzentration über die maximale Bodenfläche pro Wechsel. Validierung der Reduzierung der Keimbelastung (>3-log) mittels mikrobieller Oberflächenprobenentnahme vor und nach der Reinigung.
☑ Vermeidung raumübergreifender Kontamination: Verwenden Sie eine validierte Transferdesinfektion, wenn Sie Eimer zwischen den Klassen bewegen (unidirektionaler Fluss: nur von niedriger zu hoher Qualität). Implementieren Sie Luftschleusenprotokolle (Türverriegelungen, separate Material-/Personalschleusen, Spülung mit gefilterter Luft). Öffnen Sie niemals beide Schleusentüren gleichzeitig. Sortieren Sie den Eimerbestand nach Güteklasse (Behälter der Güteklasse A/B kommen nie ohne erneute Sterilisation in die Kategorie C/D).
☑ EM-Akzeptanzkriterien: Definieren Sie die Partikelanzahl und die mikrobiellen Grenzwerte pro ISO-Klasse (Klasse A = Luft ≤5 KBE/m³, Absetzen ≤1 KBE/4h, Kontakt ≤1 KBE/Platte; Klasse B = Luft ≤10, Absetzen ≤5, Kontakt ≤5; Klasse C = Luft ≤100, Absetzen ≤50, Kontakt ≤25; Klasse D = Luft ≤200, Absetzen ≤100, Kontakt ≤50). Alarm-/Aktionsstufen festlegen; Ausflüge untersuchen. Trend-EM-Daten zur Erkennung von Verschlechterungen (steigende Partikelzahlen im Zusammenhang mit Reinigungsplänen weisen auf einen Ausfall des Eimer-/Moppsystems hin).
Validierungsfreundlicher Reinigungsworkflow (erweitert)
Schritt-für-Schritt-validierter Workflow (ISO 5–8)
Vorbereitung: Überprüfen Sie den Bereichsniveaustatus, die EM-Probenahmebereitschaft, Türverriegelungen und Druckdifferenzen. Bühnenwagen mit drei Eimern mittels validierter Transferdesinfektion. Tragen Sie einen vollständig aseptischen Kittel gemäß den Anforderungen der Klasse (Klasse A/B = steriler Kittel, Doppelhandschuh, Gesichtsschutz; Klasse C/D = Reinraumkittel, Handschuhe, Haarschutz). Beladen Sie Eimer 1 mit sterilem Desinfektionsmittel (validierte Konzentration, dokumentierte Vorbereitungszeit), Eimer 2 mit sterilem Spülwasser, Eimer 3 leer. Befestigen Sie den sterilen Moppkopf am Griff.
Ausführung: Tragen Sie das Desinfektionsmittel aus Eimer 1 mit überlappenden S-förmigen Strichen auf einer Fläche von 2–3 m² pro Durchgang auf. Zurück zum Warenkorb; Positionieren Sie den Mopp über Eimer 3 (Abfall) und wringen Sie ihn gründlich aus. Tauchen Sie den Mopp in Eimer 2 (Spülwasser), schütteln Sie ihn, um eingeschlossene Partikel zu lösen, und wringen Sie ihn erneut in Eimer 3 aus. Laden Sie den Mopp aus Eimer 1 (Desinfektionsmittel) nach. Wiederholen Sie die Sequenz für den gesamten Zielbereich. Desinfizieren Sie die Handschuhe alle 10–15 Minuten erneut (mit IPA besprühen, Einwirkzeit einhalten oder auf frische, sterile Handschuhe wechseln).
Kontaktzeit: Beachten Sie die validierte Einwirkzeit des Desinfektionsmittels, bevor Sie die Oberfläche für „sauber“ erklären (normalerweise 3–10 Minuten, je nach Mittel und Organismus). Gehen Sie nicht auf nassen Oberflächen, bis die Kontaktzeit abgelaufen ist. Bei sporiziden Wirkstoffen kann die Einwirkzeit 10–30 Minuten betragen; Verwenden Sie eine sequentielle Reinigung (eine Zone wischen, Kontaktzeit einhalten, dann die nächste Zone wischen, während die erste trocknet).
Wechsel: Ersetzen Sie den Moppkopf alle 30–50 m² oder bei sichtbarer Verschmutzung (je nachdem, was zuerst eintritt). Wechseln Sie das Spülwasser von Eimer 2 alle 20–30 m² (überwachen Sie die Trübung; wenn das Spülwasser trüb erscheint, wechseln Sie es sofort). Leeren Sie den Abfalleimer 3, wenn er zu 70 % gefüllt ist (verhindert Spritzer). Das Desinfektionsmittel in Eimer 1 sollte den gesamten Reinigungszyklus überdauern, wenn das Drei-Eimer-Protokoll eine Verdünnung verhindert; Überwachen Sie die Konzentration mithilfe von Teststreifen.

Abbildung 5: Validierter Drei-Eimer-Reinigungsablauf für pharmazeutische Bereiche ISO 5–8 (Klasse A/B/C). Reihenfolge: (1) Beladen Sie Eimer 1 mit sterilem Desinfektionsmittel, Eimer 2 mit sterilem Spülwasser, Eimer 3 leeren Sie ihn für den Abfall; (2) Tragen Sie das Desinfektionsmittel mit überlappenden S-förmigen Strichen auf einer Fläche von 2–3 m² auf; (3) Wischen Sie den Mopp gründlich über Eimer 3, um kontaminierte Flüssigkeit ohne Rückspritzer aufzufangen. (4) Spülen Sie den Mopp in Eimer 2 aus, um eingeschlossene Partikel und Keime zu entfernen. (5) Erneut in Eimer 3 auswringen und dann erneut aus Eimer 1 laden. Dieses Protokoll hält die Desinfektionsmittelkonzentration während der Reinigungszyklen von 50–100 m² über den validierten Wirksamkeitsschwellen und ermöglicht eine quantitative Validierung durch Überwachung der Desinfektionsmittelkonzentration und Kultivierung der Abfallkeimbelastung.
Erwartungen an die Kontaktzeit des Desinfektionsmittels
Die validierten Kontaktzeiten variieren je nach Desinfektionsmittelchemie und Zielorganismen. Alkohole (70 % IPA): 30 Sekunden bis 2 Minuten für vegetative Bakterien; unwirksam gegen Sporen (erfordert sporizide Rotation). Wasserstoffperoxid (3–6 %): 5–10 Minuten für Breitbanddesinfektion; 10–30 Minuten für sporizide Wirkung. Natriumhypochlorit (500–5000 ppm): 5–10 Minuten für Bakterien und Pilze; 10+ Minuten für Sporen. Quartäre Ammoniumverbindungen: 5–10 Minuten zur allgemeinen Desinfektion; unwirksam gegen Sporen (in Kombination mit einem sporiziden Mittel). Validieren Sie die Kontaktzeiten mithilfe von ASTM E2197 (Oberflächendesinfektion mit Zeitvernichtung) oder gleichwertigen Testmethoden an repräsentativen Oberflächenmaterialien der Einrichtung (Epoxidharzböden, Edelstahl, gestrichene Wände).
So vermeiden Sie die Ansammlung von Rückständen
Zu einer Rückstandsansammlung kommt es, wenn sich überschüssiges Desinfektionsmittel in Bodenspalten, Nähten oder tiefliegenden Bereichen ansammelt und klebrige Filme entstehen, die Partikel anziehen und nachfolgende Desinfektionszyklen beeinträchtigen. Vermeiden Sie Ansammlungen, indem Sie die Wischmoppköpfe gründlich auswringen (80–90 % Flüssigkeitsextraktion), die richtige Wischtechnik anwenden (überlappende Striche ohne übermäßiges Benetzen) und sicherstellen, dass der Boden eine ordnungsgemäße Neigung/Entwässerung aufweist (keine flachen Totzonen). Verwenden Sie in Bereichen mit unvermeidbaren niedrigen Stellen saugfähige Tücher oder Rakel, um überschüssige Flüssigkeit vor Ablauf der Kontaktzeit zu entfernen. Die Ansammlung von Rückständen weist auf eine unzureichende Spülung (Eimer 2 ist verunreinigt, häufigeres Auswechseln erforderlich) oder auf eine zu hohe Desinfektionsmittelkonzentration (gemäß validiertem Protokoll verdünnen) hin.
Faktoren der Bedienertechnik, die sich auf die Kontamination auswirken
Selbst bei validierten Eimersystemen bestimmt die Technik des Bedieners die Reinigungswirksamkeit. Häufige Fehler: unzureichendes Auswringen zwischen den Eimern (befördert Keime in Spülwasser und Desinfektionsmittel), Auslassen des Spülschritts (bleibt organischer Schmutz auf dem Mopp, wodurch der Kontakt mit dem Desinfektionsmittel verringert wird), Gehen auf nassen Oberflächen vor Ablauf der Kontaktzeit (Biobelastung wird neu verteilt), Berühren nicht desinfizierter Oberflächen mit kontaminierten Handschuhen (Kreuzkontaminationsvektor) und überfüllte Eimer (Schwappen während des Transports verbreitet Kontamination).
Die Schulung muss praktische Demonstrationen umfassen: ordnungsgemäße S-Muster-überlappende Hübe (gewährleistet eine vollständige Abdeckung ohne Lücken), Betätigungstechnik des Wringers (maximale Flüssigkeitsextraktion ohne Spritzer), Eimertransport (stabile Wagenbewegung, arretierende Rollen während des Wrings) und Häufigkeit der erneuten Desinfektion der Handschuhe (alle 10–15 Minuten oder nach dem Berühren nicht gereinigter Oberflächen). Qualifizieren Sie die Bediener jährlich durch praktische Beurteilung; Beobachten Sie die Reinigungsvorgänge vierteljährlich, um technische Abweichungen festzustellen.









