Was ist ein Reinraummopp?
Ein Reinraum-Mopp ist ein spezielles Bodenreinigungsgerät, das speziell für die Anforderungen an die Kontaminationskontrolle in kontrollierten Umgebungen entwickelt wurde – etwa in Produktionshallen für Pharmazeutika, in Biotechnologielabors, in Montagebereichen für medizinische Geräte und in Halbleiterfabriken. Im Gegensatz zu herkömmlichen Hausmeistermopps, die in erster Linie auf Schmutzentfernung und Kosteneffizienz ausgelegt sind, sind Reinraummopps in erster Linie Geräte zur Kontaminationskontrolle und erst in zweiter Linie Reinigungswerkzeuge.
Das bestimmende Merkmal istgeringe Partikelbildung. Während ein normaler Mopp aus Baumwolle oder Viskose bei jedem Wischvorgang Tausende von Fasern und Partikeln abwirft, besteht ein Reinraummopp aus dicht gewebten, kantenversiegelten Materialien (typischerweise Mikrofaser, Polyestergewirke oder fusselfreier Schaumstoff), die während des Gebrauchs nur minimale Luft- oder Oberflächenkontaminationen erzeugen. Diese Wischmopps sind für den Einsatz in ISO-klassifizierten Reinräumen (ISO-Klasse 5 bis Klasse 8) getestet und qualifiziert, ohne die Grenzwerte für die Partikelanzahl zu verletzen oder eine mikrobielle Kontamination einzuführen, die sterile Produktionsabläufe beeinträchtigen oder behördliche Feststellungen auslösen könnte.
Für Pharma- und GMP-Einrichtungen ist der Reinraummopp Teil eines validierten Reinigungs- und Desinfektionsprogramms. Es muss mit aggressiven sporiziden Mitteln (Isopropylalkohol, Wasserstoffperoxid, quartäre Ammoniumverbindungen, Natriumhypochlorit) kompatibel sein, bei Bedarf wiederholten Sterilisationszyklen standhalten können (Autoklavieren für Bereiche der Klasse A/B) und durch eine Dokumentation gestützt werden, die die Partikelabwurfleistung, chemische Beständigkeit und Sterilitätssicherheit nachweist. Aus rechtlicher Sicht handelt es sich bei dem Reinraummopp nicht um einen Massenkauf – er ist ein wichtiger Teil der Infrastruktur zur Kontaminationskontrolle, der gemäß der Kontaminationskontrollstrategie (CCS) und dem Qualitätsmanagementsystem Ihrer Einrichtung ausgewählt, validiert und gewartet werden muss.

Abbildung 1: Aseptische Produktionsumgebung, in der Reinraummopps wichtige Geräte zur Kontaminationskontrolle sind. Personal in komplett sterilen Kitteln verdeutlicht die Umgebung mit hohen Risiken, in der bereits geringe Partikelbildung durch Reinigungsgeräte die Produktsterilität gefährden und zu behördlichen Feststellungen führen kann.
Warum sich Reinraummopps von normalen Wischmopps unterscheiden
Der Unterschied zwischen einem Standard-Hausmeistermopp und einem Reinraummopp ist keine Frage der Qualität, sondern ein Unterschied in der Designphilosophie und den Leistungsanforderungen.
Partikelerzeugung: Herkömmliche Mopps (Baumwolle, Viskose, Mischfasern) sind hinsichtlich Saugfähigkeit und Scheuerkraft optimiert. Ihre Fasern sind oft lose gedreht, geschnitten oder geschlungen, und die Kanten können unbearbeitet sein. Während des Gebrauchs kommt es durch mechanische Reibung zum Bruch der Fasern und zum Ablösen von Partikeln. In einem typischen Büro- oder Krankenhausflur stellt dies kein Problem dar. In einem Bereich zur Unterstützung der aseptischen Verarbeitung nach ISO-Klasse 7 (Partikelgrenzwert: 352.000 Partikel/m³ bei ≥0,5 µm) kann ein fusselfreier Mopp im Alleingang die Klassifizierungsgrenzen verletzen und ein Out-of-Specification (OOS)-Ereignis auslösen.
Reinraummopps verwenden Endlosfilament-Polyester, dicht gestrickte Mikrofaser oder versiegelte Schaumstoffstrukturen mitheißversiegelte oder ultraschallverschweißte Kanten um eine Auflösung zu verhindern. Die Partikelerzeugungsraten werden während der Qualifizierungstests gemäß ISO 14644-14 (Bewertung der Geräteeignung anhand der Partikelkonzentration in der Luft) quantifiziert. Akzeptable Reinraum-Mopps erzeugen unter kontrollierten Testbedingungen typischerweise weniger als 100 Partikel ≥ 0,5 µm pro Hub, verglichen mit Tausenden bei herkömmlichen Mopps.
Chemische Kompatibilität: Standardmopps sind für die Verwendung mit Reinigungsmitteln mit neutralem pH-Wert, verdünnten Desinfektionsmitteln und gelegentlichen Bleichmitteln konzipiert. Pharmazeutische Reinräume erfordern Kompatibilität mit hochkonzentriertem Isopropylalkohol (70 % IPA), Wasserstoffperoxid (3–35 %), sporiziden Wirkstoffen und Kontaktzeiten, die in Minuten statt in Sekunden gemessen werden. Materialien, die mit Haushaltsreinigern gut funktionieren, können sich zersetzen, verfärben oder Partikel abgeben, wenn sie diesen aggressiven Chemikalien wiederholt ausgesetzt werden. Die Materialien für Reinraummopps werden ausgewählt und auf ihre chemische Beständigkeit und Dimensionsstabilität hin getestet. Außerdem bleiben sie bei Hunderten von Reinigungszyklen und Sterilisationsvorgängen fusselarm.
Sterilisationsfähigkeit: In EU-GMP-Anhang-1-Umgebungen der Klassen A und B (aseptische Verarbeitungszonen, Abfülllinien mit unidirektionalem Luftstrom) müssen alle Geräte und Materialien, die in den Bereich gelangen, sterilisiert werden. Standardmopps können einer Autoklavierung bei 121 °C oder der Einwirkung von verdampftem Wasserstoffperoxid nicht standhalten, ohne zu schmelzen, zu schrumpfen oder die strukturelle Integrität zu beeinträchtigen. Für diese Bereiche vorgesehene Reinraummopps werden aus autoklavierbaren Polymeren (bestimmte Polyester, Polypropylenmischungen) hergestellt, die wiederholte Sterilisationszyklen ohne Leistungsverlust überstehen, oder als vorsterilisierte, validierte Einwegsysteme mit Sterilitätssicherungsdokumentation geliefert.
Rückverfolgbarkeit und Dokumentation: Reinraum-Mopps werden mit Konformitätsbescheinigungen, Datenblättern zur Materialsicherheit, Daten zu extrahierbaren und auslaugbaren Stoffen (sofern erforderlich) und Testberichten zur Partikelerzeugung geliefert. Chargenprotokolle und Chargenrückverfolgbarkeit unterstützen behördliche Audits und Ursachenermittlungen. Standardmopps haben ein Preisschild und kaum etwas anderes.

Abbildung 2: Mikrofaser-Moppkopf in Reinraumqualität mit dicht gewebter Endlosfaserfaserkonstruktion. Die dichte Faserstruktur sorgt für eine hohe Saugfähigkeit und Partikelaufnahme und sorgt gleichzeitig für eine geringe Flusenbildung über mehr als 100 Sterilisationszyklen hinweg – Eigenschaften, die Reinraum-Mopps von herkömmlichen Hausmeistergeräten unterscheiden.
Für die Pharmaindustrie erforderliche Hauptmerkmale & GMP-Einrichtungen
Bei der Spezifizierung von Reinraum-Mopps für pharmazeutische und GMP-Betriebe bestimmen vier Kernmerkmale, ob ein Produkt Ihr Kontaminationskontrollprogramm unterstützt oder untergräbt.
Fusselarm & nicht vergossene Struktur
Die Partikelgenerierung ist das primäre Qualifikationskriterium. EU-GMP-Anhang 1 und FDA-Leitlinien zur aseptischen Verarbeitung verlangen, dass Materialien und Geräte, die in klassifizierten Bereichen verwendet werden, die Partikelabgabe minimieren. ISO 14644-14 liefert den Testrahmen: Moppköpfe werden simulierten Einsatzbedingungen (Nass-/Trockenzyklen, mechanische Bewegung, Kontakt mit repräsentativen Oberflächen) ausgesetzt, während Luftpartikelzähler die Freisetzung bei ≥0,5 µm und ≥5 µm messen.
Akzeptable Reinraummopps weisen Partikelerzeugungsraten auf, die weit unter den Klassifizierungsgrenzen ihres vorgesehenen Verwendungsbereichs liegen. Für die ISO-Klasse 5 (3.520 Partikel/m³ bei ≥0,5 µm) dürfen Mopps bei der Verwendung praktisch keine zusätzlichen Partikel erzeugen. Für Unterstützungsbereiche der Klasse 7 oder 8 kann eine etwas höhere Erzeugung tolerierbar sein, aber jeder Mopp, der eine messbare Partikelbelastung verursacht, birgt das Risiko, dass die Umgebung bei Routinearbeiten oder Klammerstudien aus den Spezifikationen gerät.
Konstruktionsdetails sind wichtig:Endlosfilamentfasern (keine ausfransenden Schnittenden),versiegelte Kanten (verschweißt, ultraschallverschweißt oder in einer Randbindung eingeschlossen),enge Strick- oder Webdichte (verhindert das Herausziehen der Fasern) undkontrollierte Wasch- oder Sterilisationsprotokolle die das Material während der qualifizierten Nutzungsdauer des Produkts nicht beeinträchtigen. Anbieter sollten Testdaten zur Partikelerzeugung von unabhängigen Labors oder internen Qualitätssystemen bereitstellen, die sich auf die ISO 14644-14-Methodik beziehen.

Abbildung 3: Anatomie des Reinraumwischers mit Darstellung der wichtigsten Funktionen zur Kontaminationskontrolle. Der Querschnitt zeigt die Endlosfaserstruktur (keine ausfransenden Schnittenden), heißversiegelte Kanten (verhindert ein Auflösen), eine hohe Webdichte (minimiert das Herausziehen der Fasern) und eine versiegelte Griffschnittstelle. Diese Designelemente arbeiten zusammen, um Partikelerzeugungsraten unterhalb der Qualifikationsschwellenwerte von ISO 14644-14 zu erreichen.
Kompatibilität mit Desinfektionsmitteln (IPA / Quat / Bleichmittel / H₂O₂)
Pharmazeutische Reinigungsprogramme rotieren oder schichten mehrere Desinfektionschemikalien, um eine Breitbandabtötung von Mikroben zu erreichen und die Entwicklung von Resistenzen zu verhindern. Ihr Mopp muss diesen chemischen Kampf ohne Leistungseinbußen überstehen.
Isopropylalkohol (IPA, 70 %): Das gebräuchlichste pharmazeutische Desinfektionsmittel. Viele Polymere vertragen IPA gut, aber wiederholte Einwirkung kann dazu führen, dass einige Materialien aufquellen, sich versteifen oder ihre Zugfestigkeit verlieren. Mikrofasermischungen und Polyesterstrickwaren funktionieren im Allgemeinen gut; Bestimmte Schaumstoffsubstrate können sich zersetzen.
Quartäre Ammoniumverbindungen (Quats): Wird häufig zur routinemäßigen Desinfektion verwendet. Im Allgemeinen gut verträglich mit Reinraum-Moppmaterialien. Rückstandsmanagement ist wichtig – Quats können Filme hinterlassen, die Partikel anziehen oder nachfolgende sporizide Behandlungen beeinträchtigen.
Natriumhypochlorit (Bleichmittel): Wirksames sporizides Mittel, aber aggressiv. Konzentrationen über 0,5 % können bei einigen Polyester- und Mikrofaserkonstruktionen zu Farbverblassen, Faserschwächung und beschleunigtem Verschleiß führen. Wenn Bleichmittel Teil Ihres CCS sind, geben Sie Mopps an, deren Bleichmittelkompatibilität validiert ist, und überwachen Sie, ob sich die Leistung während des qualifizierten Verwendungszeitraums verschlechtert.
Wasserstoffperoxid (H₂O₂, 3–35 %): Zunehmend beliebt für die sporizide Biodekontamination, insbesondere in Isolatoren und RABS. Peroxid ist ein Oxidationsmittel; Materialien müssen auf Beständigkeit gegen oxidativen Abbau, Farbstabilität und Aufrechterhaltung der strukturellen Integrität getestet werden. Einige Mopps mit Schaumstoffkern und bestimmte Mikrofasermischungen weisen eine ausgezeichnete H₂O₂-Verträglichkeit auf; andere nicht.
Fordern Sie bei Anbietern Matrizen zur chemischen Kompatibilität an und validieren Sie diese intern unter Ihren tatsächlichen Einsatzbedingungen (Konzentrationen, Kontaktzeiten, Temperaturen, Anzahl der Zyklen). Dazu gehören eine visuelle Inspektion (Farbveränderung, Faserschäden), mechanische Tests (Aufrechterhaltung der Zugfestigkeit) und erneute Tests der Partikelerzeugung nach simulierter Alterung.
Autoklavierbar vs. Einwegartikel
Ihre Wahl zwischen wiederverwendbaren (autoklavierbaren) und Einweg-Moppsystemen (Einweg) hängt von der Bereichsklassifizierung, dem Durchsatz, der Validierungskomplexität und der Kostenstruktur ab.
Autoklavierbare (wiederverwendbare) Systeme: Entwickelt für die wiederholte Sterilisation bei 121 °C (oder höher) in Dampfautoklaven. Hergestellt aus Polymeren, die über mehr als 50–200 Autoklavenzyklen (je nach Material und Herstellerqualifikation) Dimensionsstabilität, mechanische Festigkeit und fusselarme Leistung beibehalten. Diese Systeme erfordern validierte Autoklavenzyklen (Temperatur, Druck, Zeit, Beladungskonfiguration), dokumentierte Haltezeiten nach der Sterilisation und Sterilitätssicherung sowie routinemäßige Inspektionen auf Verschleiß (Faserschäden, Kantenverschlechterung, Verfärbung). Wiederverwendbare Systeme bieten niedrigere Kosten pro Verwendung und eine geringere Abfallerzeugung, erfordern jedoch eine robuste Wäsche-/Sterilisationsinfrastruktur, Bedienerschulung und regelmäßige Neuqualifizierung.
Einwegsysteme (Einwegsysteme).: Wird vorsterilisiert (Gammabestrahlung oder Ethylenoxid) in versiegelter, validierter Verpackung geliefert. Einmal verwendet und entsorgt. Dadurch entfällt die Komplexität der Wäscherei, das Risiko einer Kreuzkontamination zwischen Chargen oder Produktlinien und die Notwendigkeit einer internen Autoklavenvalidierung. Einwegmopps werden in aseptischen Bereichen mit hohem Risiko (Abfülllinien der Klasse A, Isolatorumgebungen), in denen das Risiko einer Wiederverwendung nicht akzeptabel ist, und in Einrichtungen mit begrenzter Sterilisationskapazität bevorzugt. Zu den Kompromissen gehören höhere Kosten pro Nutzung und ein erhöhtes Abfallvolumen (obwohl viele Anbieter inzwischen Recyclingprogramme für gebrauchte Reinraum-Verbrauchsmaterialien anbieten).
Anhang 1 schreibt nicht einen Ansatz gegenüber dem anderen vor; Ihre Kontaminationskontrollstrategie sollte die Begründung dokumentieren, Risikobewertungen für beide Optionen enthalten und die Validierungs- und Überwachungsanforderungen für das von Ihnen gewählte System definieren.
Moppgriff & Eimerpaarung
Mopps arbeiten nicht isoliert. Das komplette Reinigungssystem – Moppkopf, Griff, Rahmen und Eimer – muss als integrierte Kontaminationskontrollbaugruppe konzipiert, validiert und gewartet werden.
Griffe und Rahmen: Sollte aus glatten, nicht porösen Materialien (Edelstahl, elektropoliertes Aluminium, autoklavierbare Polymere) bestehen, die keine Partikel abgeben, korrosionsbeständig bei wiederholter Einwirkung von Desinfektionsmitteln sind und sterilisiert (für Verwendung der Klasse A/B) oder gründlich desinfiziert werden können (für Verwendung der Klasse C/D). Durch Teleskopgriffe und verstellbare Rahmen entstehen zusätzliche Spalten und Fugen, in denen sich Verunreinigungen ansammeln können. In hochwertigen Bereichen werden Konstruktionen mit fester Länge und abgedichteten Verbindungen bevorzugt. Ergonomie ist wichtig – Bediener in Schutzanzügen, die in Überdruckanzügen oder Isolatoren arbeiten, benötigen leichte, ausbalancierte Griffe, die Ermüdungserscheinungen minimieren und das Risiko unkontrollierter Bewegungen verringern, die zu Partikelexplosionen führen.
Eimer und Presssysteme: Muss autoklavierbar sein oder als steriler Einwegartikel für hochwertige Bereiche geliefert werden. Das Eimermaterial (häufig Edelstahl oder autoklavierbares Polypropylen) sollte chemischen Angriffen standhalten und eine visuelle Bestätigung der Klarheit der Lösung ermöglichen (was anzeigt, dass keine Partikelkontamination oder mikrobielles Wachstum vorliegt). Zwei-Eimer-Systeme (einer für saubere Lösung, einer für Abfall) verhindern Kreuzkontaminationen und gehören zur Standardpraxis in GMP-Reinräumen. Einige Einrichtungen verwenden vorgetränkte Moppsysteme (mit Desinfektionsmittel vorgetränkte Moppköpfe, versiegelt in sterilen Beuteln), um die Handhabung von Eimern in Zonen der Klasse A/B vollständig zu vermeiden.
Farbkodierung und Trennung: Implementieren Sie farbcodierte Systeme (z. B. Blau für Produktionsbereiche, Rot für Abfallbehandlungszonen, Grün für Personalumkleidebereiche), um eine Kreuzkontamination zwischen klassifizierten und nicht klassifizierten Räumen zu verhindern. Die Farbcodierung muss sich auf Moppköpfe, Griffe, Rahmen und Eimer erstrecken, mit dokumentierten Verfahren und Bedienerschulungen, um die Einhaltung sicherzustellen.

Abbildung 4: Validiertes Wischverfahren in einem pharmazeutischen Reinraum. Personal in Vollschutzanzug, Kapuze und Handschuhen demonstriert die richtige Technik mit farblich gekennzeichneter Ausrüstung und einem Zwei-Eimer-System. Dieser integrierte Ansatz – qualifizierte Wischmopps, validierte Verfahren, geschulte Bediener – bildet die Grundlage für eine wirksame Kontaminationskontrolle in GMP-Einrichtungen.
Arten von Reinraummopps (Mikrofaser / Polyester / Schaumstoffkern / Einwegmopp)
Reinraum-Mopps lassen sich in vier Hauptkategorien einteilen, die jeweils für unterschiedliche Anforderungen an die Kontaminationskontrolle, chemische Belastungen und betriebliche Arbeitsabläufe optimiert sind.
Mikrofasermopps
Mikrofasermopps verwenden ultrafeine synthetische Fasern (typischerweise Polyester-/Polyamidmischungen) mit Durchmessern unter 1 Denier (ungefähr 10 Mikrometer). Das hohe Verhältnis von Oberfläche zu Gewicht sorgt für eine außergewöhnliche Saugfähigkeit und Partikelerfassung. Die geteilte Faserkonstruktion der Mikrofaser erzeugt mikroskopisch kleine Kanäle, die Partikel mechanisch einfangen, anstatt sich ausschließlich auf die chemische Reinigungswirkung zu verlassen. Dadurch eignen sich diese Mopps sowohl für das Nasswischen (mit Desinfektionsmitteln) als auch für das Feuchtwischen (Entfernen von Restpartikeln zwischen den Desinfektionszyklen).
Vorteile: Hervorragende Flüssigkeitsretention (oft das 6- bis 8-fache des Trockengewichts des Mopps), ausgezeichnete Partikelerfassungseffizienz, Haltbarkeit über 100–200 Wasch-/Autoklavenzyklen (bei ordnungsgemäßer Wartung) und Kompatibilität mit den meisten pharmazeutischen Desinfektionsmitteln, einschließlich IPA, Quats und Wasserstoffperoxid. Mikrofaser eignet sich gut für Umgebungen der ISO-Klassen 6–8 und ist ein Arbeitstier für die routinemäßige Reinigung in aseptischen Prozessunterstützungsbereichen, Umkleideräumen und Materialschleusen.
Einschränkungen: Einige Mikrofasermischungen zeigen nach wiederholter Einwirkung hochkonzentrierter Bleichmittel eine verminderte Leistung oder Faserschäden (>1 %). Für Mikrofasern sind validierte Waschprotokolle erforderlich. Durch unsachgemäßes Waschen (hohe Hitze, Weichspüler oder kontaminierte Wäschereiausrüstung) können Partikel oder Rückstände entstehen, die die Leistung des Reinraums beeinträchtigen. Für Einrichtungen, die den Wäscheaufwand lieber vermeiden möchten, stehen vorgetränkte oder Einweg-Mikrofaseroptionen zur Verfügung.
Polyester-Strickmopps
Polyester-Strickmopps werden aus 100 % Polyester-Endlosfilamentgarnen hergestellt, typischerweise in einer Schlauchstrick- oder Flachgewebekonfiguration. Die Kanten sind heißversiegelt oder ultraschallverschweißt, um ein Ausfransen zu verhindern. Bei diesen Mopps wird Wert auf Haltbarkeit, Dimensionsstabilität und chemische Beständigkeit gelegt.
Vorteile: Hervorragende Verträglichkeit mit aggressiven Desinfektionsmitteln, einschließlich anhaltender Einwirkung von Bleichmitteln, Wasserstoffperoxid und Phenolverbindungen. Polyestergewirke überstehen mehr als 200 Zyklen im Autoklaven mit minimalem Verlust der Zugfestigkeit oder Dimensionsveränderung. Aufgrund der geringen Flusenbildung und der hohen Abriebfestigkeit eignet sich Polyesterstrick für Umgebungen der ISO-Klassen 5–7, einschließlich Bereichen mit häufigem Desinfektionsmittelwechsel und intensiver Nutzung (mehrere Schichten, Produktionslinien mit hohem Durchsatz). Viele Anbieter bieten nach ISO 14644-14 validierte Polyester-Strickmopps an, deren Partikelerzeugungsdaten den Einsatz in Umgebungen der Klassen B und C unterstützen.
Einschränkungen: Etwas geringere Saugfähigkeit als Mikrofaser (normalerweise das 4- bis 6-fache des Trockengewichts). Polyesterstrick kann sich steifer anfühlen als Mikrofaser, was die Präferenz des Bedieners und die Manövrierfähigkeit in engen Räumen beeinträchtigen kann. Die Kosten pro Einheit sind oft höher als bei Mikrofasern, obwohl die Gesamtbetriebskosten aufgrund der längeren Nutzungsdauer niedriger sein können.
Mopps mit Schaumstoffkern
Mopps mit Schaumstoffkern (oder Schwammkern) verfügen über ein zentrales Schaumstoffsubstrat, das von einer Vlies- oder Strickaußenschicht umgeben ist. Der Schaumstoffkern sorgt für strukturelle Steifigkeit und Flüssigkeitsverteilung, während die äußere Schicht für die Partikelaufnahme und den Oberflächenkontakt sorgt.
Vorteile: Gleichmäßige Flüssigkeitsverteilung über den Moppkopf, wodurch Streifenbildung reduziert und ein gleichmäßiger Kontakt mit dem Desinfektionsmittel gewährleistet wird. Schaumkernkonstruktionen eignen sich hervorragend für Anwendungen, bei denen eine kontrollierte, gleichmäßige Benetzung von entscheidender Bedeutung ist – beispielsweise die Anwendung von sporiziden Wirkstoffen im Inneren von Isolatoren oder die Reinigung validierter Oberflächen, bei denen Rückstandsmuster minimiert werden müssen. Einige Mopps mit Schaumstoffkern sind speziell für die Kompatibilität mit Wasserstoffperoxid konzipiert und werden in automatischen Biodekontaminationssystemen verwendet (z. B. Isolator-Nebelgeräte mit anschließendem manuellen Abwischen mit Mopps mit Schaumstoffkern).
Einschränkungen: Schaumsubstrate weisen große Unterschiede in der chemischen Beständigkeit auf; Nicht alle Formulierungen vertragen eine wiederholte Bleich- oder Peroxidbelastung. Schaum kann im Laufe der Zeit zerfallen (bröckeln, verfärben, strukturelle Integrität verlieren), insbesondere unter aggressiven Chemikalien oder hohen Autoklaventemperaturen. Die Prüfung der Partikelerzeugung ist von entscheidender Bedeutung – einige Mopps mit Schaumstoffkern erzeugen akzeptable Partikelmengen, während andere Schaumfragmente oder Fasern aus der Außenschicht abgeben. Fordern Sie stets Validierungsdaten des Anbieters an und führen Sie eine interne Qualifizierung durch, bevor Sie Mopps mit Schaumstoffkern in Umgebungen der ISO-Klasse 7 oder höher einsetzen.
Einweg-Mopps (Einweg-Mopps).
Einwegmopps werden vorsterilisiert, einzeln verpackt geliefert und sind für den einmaligen Gebrauch bestimmt. Die Materialien reichen von nicht gewebten Polyester/Polypropylen-Mischungen bis hin zu Konstruktionen aus Mikrofasern mit versiegelten Kanten oder Schaumstoffkernkonstruktionen, die mit ihren wiederverwendbaren Gegenstücken identisch sind, jedoch für den einmaligen Gebrauch verpackt und sterilisiert sind.
Vorteile: Eliminieren Sie das Risiko einer Kreuzkontamination zwischen Produktionschargen, eliminieren Sie die Notwendigkeit einer validierten Reinigung oder internen Sterilisation, vereinfachen Sie die Logistik und das Bestandsmanagement (insbesondere für Organisationen mit mehreren Standorten) und stellen Sie eine revisionssichere Dokumentation bereit (Sterilitätszertifikate, Chargenrückverfolgbarkeit, Ablaufdatum). Einwegmopps sind die Standardwahl für Betriebe der Klasse A mit hohem Risiko, für die Herstellung von Kleinserien oder für klinische Studien (bei denen die Trennung von Charge zu Charge von größter Bedeutung ist) sowie für Einrichtungen, in denen eine Reinigungsvalidierung durchgeführt wird oder Kontaminationsereignisse untersucht werden (Einweg-Mopps entfernen Wäsche und Wiederaufbereitung als Variablen).
Einschränkungen: Höhere Kosten pro Nutzung (häufig 3- bis 10-fache der Kosten pro Nutzung von wiederverwendbaren Mopps, je nach Menge und Anbieter). Das zunehmende Abfallaufkommen erhöht die Umwelt- und Entsorgungskosten, obwohl einige Anbieter Rücknahmeprogramme und Recyclingdienste anbieten. Einrichtungen müssen die Ablaufdaten und Lagerbedingungen der Bestände verwalten, um die Sterilitätssicherheit aufrechtzuerhalten.
Auswahlberatung: Für die routinemäßige, großvolumige Reinigung in Umgebungen der ISO-Klassen 6–8 mit robuster Wäscherei-Infrastruktur bieten wiederverwendbare Mikrofaser- oder Polyester-Strickmopps das beste Preis-Leistungs-Verhältnis. Für aseptische Kerne der Güteklasse A/B, Isolatoren oder Betriebe mit begrenzter Sterilisationskapazität reduzieren Einwegmopps das Risiko und die betriebliche Komplexität. Hybridansätze – wiederverwendbare Mopps für Stützbereiche der Klasse C/D, Einwegmopps für Kerne der Klasse A/B – sind weit verbreitet und pragmatisch.
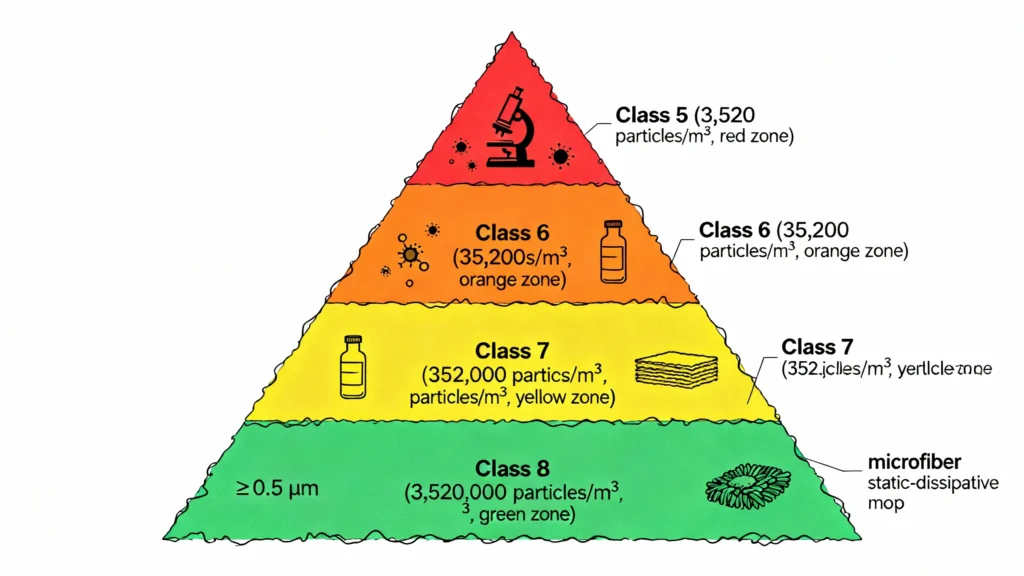
Abbildung 5: Materialvergleichsmatrix für die Auswahl von Reinraum-Mopps. Jeder Materialtyp bietet unterschiedliche Leistungsmerkmale: Mikrofaser zeichnet sich durch hervorragende Saugfähigkeit und Partikelaufnahme aus; Polyesterstrick bietet hervorragende chemische Beständigkeit und Haltbarkeit; Schaumstoffkern sorgt für gleichmäßige Flüssigkeitsverteilung; Einwegartikel eliminieren das Risiko einer Kreuzkontamination. Die Auswahl sollte sich an der Bereichsklassifizierung, dem Desinfektionsprogramm und den betrieblichen Arbeitsablaufanforderungen orientieren.
Wie Reinraummopps zur Einhaltung der ISO beitragen & GMP-Konformität
Reinraum-Mopps sind kein Nebenprodukt der Einhaltung gesetzlicher Vorschriften – sie sind integrale Bestandteile der Kontrollsysteme, die dafür sorgen, dass Ihre Einrichtung den Spezifikationen entspricht und prüfungsbereit ist.
Partikelkontrolle und Aufrechterhaltung der ISO-Klassifizierung: ISO 14644-1 klassifiziert Reinräume anhand der gemessenen Partikelkonzentration in der Luft. Das Umweltüberwachungsprogramm Ihrer Anlage verfolgt kontinuierlich die Partikelanzahl an bestimmten Standorten, und jede Überschreitung der Klassifizierungsgrenzen löst Untersuchungen, Korrekturmaßnahmen und mögliche Produktionsstopps aus. Das Einbringen eines nicht qualifizierten, partikelabwerfenden Mopps in einen klassifizierten Bereich kann zu einer ausreichenden Menge an Partikeln führen, um die Umgebung außerhalb der Spezifikationen zu halten, insbesondere in Zeiten hoher Aktivität (Schichtwechsel, Materialtransfers, Reinigungsarbeiten). Qualifizierte Reinraumwischer, getestet nach ISO 14644-14, liefern den dokumentierten Nachweis, dass Ihre Reinigungsgeräte nicht zur Partikelbelastung beitragen. Diese Dokumentation unterstützt Ihre Kontaminationskontrollstrategie (CCS) und zeigt die Sorgfaltspflicht bei Inspektionen auf.
Kontrolle mikrobieller Kontamination: EU-GMP-Anhang 1 schreibt eine routinemäßige mikrobiologische Überwachung vor und legt Grenzwerte für koloniebildende Einheiten (KBE) für jede Reinraumklasse fest (Klasse A: <1 KBE pro Kontaktplatte; Klasse D: ≤100 KBE/m³ aktive Luftprobe). Mopps dürfen keine mikrobielle Kontamination verursachen. Für Umgebungen der Klasse A/B sind sterile Wischmopps (autoklavierte wiederverwendbare oder vorsterilisierte Einwegartikel) erforderlich. In Bereichen der Klasse C/D müssen Mopps desinfiziert und behandelt werden, um das Wachstum von Mikroben während der Lagerung zu verhindern. Ein kontaminierter Mopp – sei es durch unzureichende Sterilisation, unsachgemäße Lagerung oder Verwendung über die validierte Haltbarkeitsdauer hinaus – kann eine mikrobielle Kontamination auf Böden, Wänden und Geräten verursachen, was zu fehlerhaften Ergebnissen der Umweltüberwachung, Produktrückständen und behördlichen Beobachtungen führt.
Reinigungsvalidierung und Rückstandsmanagement: Anhang 1 und die CGMP-Vorschriften der FDA erfordern validierte Reinigungsverfahren für Geräte und Anlagenoberflächen. Ihr Reinigungsvalidierungsprotokoll muss nachweisen, dass Reinigungsmittel und -methoden die mikrobielle und partikuläre Kontamination konsequent auf ein akzeptables Maß reduzieren und dass Rückstände von Reinigungsmitteln die Produktqualität nicht beeinträchtigen. Der Mopp ist eine entscheidende Variable bei dieser Validierung: Seine Saugfähigkeit, Partikelerfassungseffizienz und Kompatibilität mit Desinfektionsmitteln wirken sich direkt auf die Reinigungswirksamkeit aus. Das Moppmaterial darf keine Substanzen auslaugen, die die Desinfektionswirkung beeinträchtigen oder Rückstände hinterlassen, die Partikel anziehen. Validierungsstudien umfassen häufig Worst-Case-Tests mit den tatsächlich in der Produktion verwendeten Mopps, Desinfektionsmitteln und Oberflächenmaterialien und liefern den dokumentierten Nachweis, dass das gesamte Reinigungssystem die Akzeptanzkriterien erfüllt.
Auditbereitschaft und Rückverfolgbarkeit: Bei FDA-Inspektionen, EMA-Audits oder Zertifizierungen Dritter prüfen Inspektoren Ihr CCS, Ihre Reinigungsverfahren, Gerätequalifizierungsaufzeichnungen und Umweltüberwachungstrends. Sie erwarten eine dokumentierte Begründung für die Geräteauswahl, Konformitätszertifikate der Anbieter, Testdaten zur Partikelerzeugung, eine Autoklavenvalidierung (für wiederverwendbare Systeme), eine Dokumentation zur Sterilitätssicherung (für Einwegartikel) und einen Nachweis der Bedienerschulung. Reinraum-Mopps mit vollständiger Rückverfolgbarkeit (Chargennummern, Materialzertifizierungen, Sterilisationsaufzeichnungen) bieten den Dokumentationspfad, der Inspektionsbeobachtungen abschließt und eine systematische Kontaminationskontrolle nachweist.
Regulatorische Erwartungen in verschiedenen Regionen: Die Leitlinien der FDA zur aseptischen Verarbeitung aus dem Jahr 2004 legen Wert auf Umweltkontrolle, Personalschulung und validierte Reinigung für die aseptische Herstellung. EU-GMP-Anhang 1 (Überarbeitung 2022) erfordert ein anlagenweites CCS, explizite Kontrollen für die Reinigung und Desinfektion sowie die Qualifizierung von Materialien und Geräten, die in klassifizierten Bereichen verwendet werden. PIC/S (Pharmaceutical Inspection Co-operation Scheme) und die GMP-Richtlinien der WHO stimmen eng mit diesen Erwartungen überein. In allen Fällen ist der Reinraummopp Teil des Kontrollsystems, das gemäß den gesetzlichen Standards entworfen, validiert und gewartet werden muss. Das Versäumnis, Reinigungsgeräte zu qualifizieren, wurde in Beobachtungen der FDA 483 und in Mängelbescheiden der EMA angeführt, oft im Zusammenhang mit Exkursionen zur Umweltüberwachung oder Kontaminationsereignissen während Produktkampagnen.
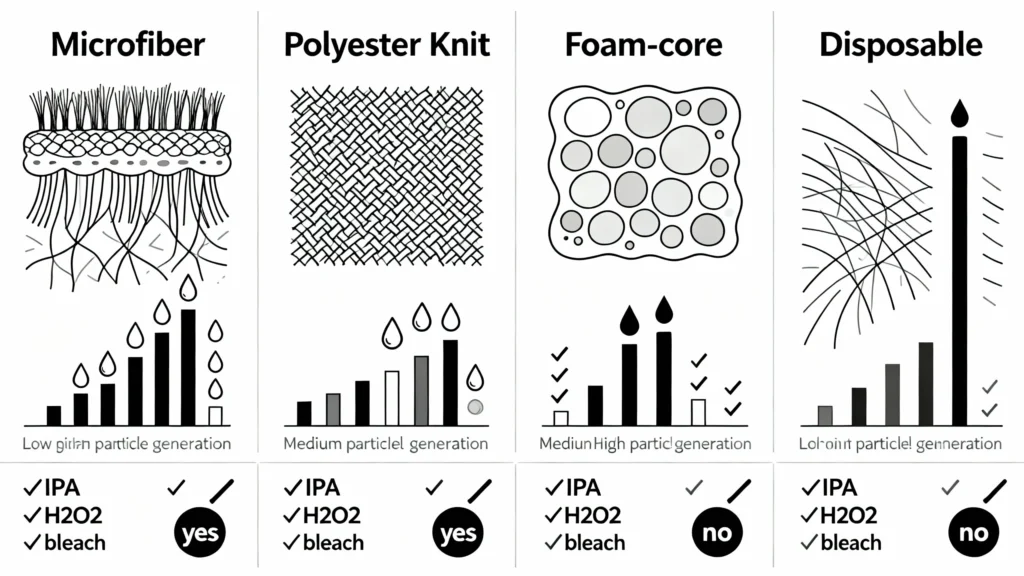
Abbildung 6: Reinraumklassifizierung nach ISO 14644-1 und entsprechende Moppanforderungen. In höherwertigen Umgebungen (Klasse 5, Klasse A/B) sind sterile Wischmopps mit nahezu keiner Partikelbildung erforderlich, während Bereiche mit niedrigerer Qualität (Klasse 7–8, Klasse C/D) validierte wiederverwendbare Systeme akzeptieren können. Die Grenzwerte für die Partikelanzahl liegen bei ≥0,5 µm pro Kubikmeter. Diese Schwellenwerte bestimmen die Qualifikationskriterien und Validierungsprotokolle für Geräte.
So wählen Sie den richtigen Mopp für Ihre Einrichtung aus
Die Auswahl von Reinraum-Mopps ist eine Entscheidung mit mehreren Variablen, bei der Kontaminationsrisiko, betriebliche Komplexität, behördliche Anforderungen und Kostenstruktur abgewogen werden. Nutzen Sie dieses Framework als Leitfaden für Ihren Spezifikationsprozess.
1. Definieren Sie die Gebietsklassifizierung und das KontaminationsrisikoBeginnen Sie mit Ihrer Reinraumklassifizierungskarte. Umgebungen der ISO-Klasse 5 / EU-GMP-Klasse A und B (aseptische Kerne, Abfülllinien, Gefriertrocknungsbeladung) erfordern ein Höchstmaß an Kontaminationskontrolle: sterile Mopps (autoklavierte wiederverwendbare oder vorsterilisierte Einwegartikel), Materialien, deren Herstellung validiert ist <10 Partikel ≥0,5 µm pro Hub und vollständige Rückverfolgbarkeit. In Bereichen der ISO-Klasse 6–7 / Klasse C (aseptische Verarbeitungsunterstützungszonen, Umkleideräume, Materialvorbereitung) können oft wiederverwendbare Mikrofaser- oder Polyester-Strickmopps mit validierten Wasch- und Desinfektionsprotokollen verwendet werden. Bereiche der ISO-Klasse 8/Klasse D (Endverpackung, unsterile Compoundierung) akzeptieren möglicherweise weniger strenge Spezifikationen, Mopps müssen jedoch dennoch eine geringe Flusenbildung und Kompatibilität mit Desinfektionsmitteln der Einrichtung aufweisen.
2. Planen Sie Ihr DesinfektionsprogrammListen Sie alle in den einzelnen Bereichen verwendeten Reinigungs- und Desinfektionsmittel auf: IPA-Konzentrationen, Quat-Formulierungen, Bleichprotokolle, Wasserstoffperoxid-Zeitpläne. Querverweis mit den Matrizen der chemischen Kompatibilität des Herstellers. Wenn Ihr CCS aggressive Oxidationsmittel (Bleichmittel) enthält >0,5 %, H₂O₂ >10 %) oder eine tägliche sporizide Behandlung erfordern, bevorzugen Sie Polyester-Strick- oder Schaumstoffmopps mit validierten Daten zur Chemikalienbeständigkeit. Wenn Sie Desinfektionsmittel wechseln, um mikrobieller Resistenz vorzubeugen, stellen Sie sicher, dass das von Ihnen gewählte Moppmaterial alle Mittel in der Rotation ohne kumulativen Abbau verträgt.
3. Bewerten Sie die Wirtschaftlichkeit und Infrastruktur von Mehrweg- und EinwegartikelnFür Bereiche der Klasse A/B eliminieren Einwegmopps die Komplexität der Sterilisation und das Risiko einer Kreuzkontamination, kosten aber pro Verwendung das Drei- bis Zehnfache mehr. Berechnen Sie den jährlichen Verbrauch (Anzahl der Bereiche × Reinigungshäufigkeit × Moppköpfe pro Reinigungsvorgang) und vergleichen Sie die Gesamtbetriebskosten: Wiederverwendbare Mopps erfordern eine Waschinfrastruktur, Autoklavenkapazität, Validierungsstudien und Bedienerschulung, bieten aber im großen Maßstab niedrigere Kosten pro Nutzung. Für Mehrproduktanlagen oder Hersteller klinischer Studien, bei denen die Chargentrennung von entscheidender Bedeutung ist, können Einwegartikel den Aufpreis durch Risikominderung und vereinfachte Logistik rechtfertigen.
4. Bewerten Sie betriebliche Arbeitsabläufe und ErgonomieBerücksichtigen Sie die Erfahrung des Bedieners. Personal in Kitteln, das in Umgebungen der Klasse A arbeitet (vollständig sterile Anzüge, Überdruckhauben), benötigt leichte, ausgewogene Wischsysteme, die Ermüdungserscheinungen minimieren und das Risiko unkontrollierter Bewegungen verringern. Teleskopgriffe führen zu Spalten; Griffe mit fester Länge, die an den Verbindungsstellen abgedichtet sind, werden bevorzugt. Wenn Ihre Einrichtung vorgetränkte Moppsysteme oder sterile Beutel verwendet, stellen Sie sicher, dass sich die Verpackung problemlos in die Verfahren zum Ankleiden und Materialtransfer integrieren lässt (z. B. äußerer Beutel in der Luftschleuse entfernt, innerer steriler Beutel im klassifizierten Bereich geöffnet).
5. Fordern Sie Dokumentation und Qualifizierungsdaten anAnfrage von Anbietern: Testberichte zur Partikelerzeugung (gemäß ISO 14644-14), Studien zur chemischen Kompatibilität (Expositionskonzentrationen, Anzahl der Zyklen, visuelle und mechanische Tests), Daten zur Autoklavenvalidierung (Zyklen bis zum Versagen, Dimensionsstabilität), Dokumentation zur Sterilitätssicherung (für Einwegartikel: Sterilisationsmethode, D-Wert-Daten, Ergebnisse von Sterilitätstests), Materialzertifizierungen (FDA Drug Master File-Nummern, Einhaltung der EU-Pharmakopöe) und Prüfung auf extrahierbare/auslaugende Stoffe (bei Kontakt mit Mopps). B. produktberührende Oberflächen oder werden in Isolatoren eingesetzt, wo Rückstände migrieren könnten). Renommierte Anbieter stellen diese Dokumentation standardmäßig zur Verfügung; Wenn ein Anbieter es nicht liefern kann, suchen Sie woanders.
6. Pilotieren und validieren Sie vor der vollständigen BereitstellungFühren Sie Pilotstudien in repräsentativen Bereichen durch, bevor Sie sich für eine einrichtungsweite Einführung entscheiden. Dazu gehören: Umgebungsüberwachung (Partikelanzahl vor, während und nach dem Wischen; Probenahme mikrobieller Oberflächen nach der Reinigung), Feedback des Bedieners (Benutzerfreundlichkeit, wahrgenommene Wirksamkeit, Ergonomie), visuelle Inspektion von Mopps nach mehreren Verwendungszyklen (Faserintegrität, Kantenzustand, Verfärbung) und Integration in bestehende Arbeitsabläufe (Kompatibilität mit aktuellen Eimern/Griffen, Anpassung an Putzverfahren, Lager- und Entsorgungslogistik). Dokumentieren Sie Ergebnisse in Ihrem CCS und nutzen Sie Pilotdaten, um die Anbieterauswahl und regulatorische Begründung zu unterstützen.

Abbildung 7: Komplette Moppsystempaarung nach Reinraumklasse. Aseptische Kerne der Güteklasse A/B erfordern sterile Einwegartikel mit vorgetränkten Beuteln und Edelstahlkomponenten; In den Stützzonen der Klasse C werden autoklavierbare Mikrofasern mit Zwei-Eimer-Systemen verwendet. Verpackungsbereiche der Klasse D können standardmäßige wiederverwendbare Konfigurationen mit validierten Desinfektionsprotokollen akzeptieren. Die Farbcodierung aller Komponenten verhindert eine Kreuzkontamination zwischen klassifizierten und nicht klassifizierten Räumen.
MIDPOSI Reinraum-Mopplösungen
MIDPOSI ist auf Verbrauchsmaterialien zur Kontaminationskontrolle für die Pharma-, Biotechnologie- und Medizingeräteherstellung spezialisiert. Unser Reinraum-Mopp-Portfolio ist darauf ausgelegt, die anspruchsvollen Anforderungen ISO-klassifizierter Umgebungen und GMP-Betriebe zu erfüllen, wobei der Schwerpunkt auf validierter Leistung, behördlicher Dokumentation und zuverlässiger Lieferkettenunterstützung liegt.
Produktpalette: MIDPOSI bietet Mikrofaser-, 100 % Polyester-Strick- und Schaumstoffkern-Moppköpfe sowohl in wiederverwendbarer (autoklavierbarer) als auch vorsterilisierter Einwegkonfiguration an. Unsere wiederverwendbaren Mopps sind für mehr als 150 Autoklavenzyklen bei 121 °C validiert und bieten dabei eine gleichbleibende Partikelerzeugungsleistung und Dimensionsstabilität. Einwegmopps sind gammasterilisiert und einzeln verpackt mit chargenspezifischen Sterilitätszertifikaten und Verfallsdatum.
Validierte Leistung: Alle MIDPOSI-Reinraummopps werden einer Partikelerzeugungsprüfung gemäß ISO 14644-14 unterzogen, wobei für jede Produktlinie Testberichte bereitgestellt werden. Typische Partikelerzeugungsraten sind <50 Partikel ≥0,5 µm pro Hub für Mikrofaser- und Polyester-Strickmopps, unterstützt den Einsatz in Umgebungen der ISO-Klassen 5–8. Die chemische Kompatibilität wurde für 70 % IPA, 3–10 % Wasserstoffperoxid, quartäre Ammoniumverbindungen (bis zu 2.000 ppm) und Natriumhypochlorit (bis zu 1 %) anhand visueller, mechanischer und Partikelerzeugungstests nach 100 simulierten Nutzungszyklen validiert.
Komplette Systemlösungen: MIDPOSI bietet integrierte Moppsysteme, darunter autoklavierbare Edelstahlgriffe mit versiegelten Verbindungen, farbcodierte Mopprahmen (verhindert Kreuzkontaminationen zwischen Bereichen) und autoklavierbare oder Einweg-Eimersysteme. Vorgetränkte Moppoptionen (Moppköpfe mit 70 % IPA vorbenetzt, versiegelt in einer sterilen Doppelbeutelverpackung) rationalisieren Arbeitsabläufe in Umgebungen der Klasse A/B und machen die Vorbereitung der Lösung vor Ort überflüssig.
Regulatorische Dokumentation: Zu jeder MIDPOSI-Produktlieferung gehören Konformitätszertifikate, Datenblätter zur Materialsicherheit, Zusammenfassungen der Tests zur Partikelerzeugung und (für Einwegartikel) eine Dokumentation zur Sterilitätssicherung, die auf Aufzeichnungen der Gammabestrahlungsdosis rückverfolgbar ist. Unser Qualitätsmanagementsystem ist nach ISO 13485 zertifiziert und ausgewählte Produkte sind bei den Drug Master Files der FDA registriert, um die Zulassungsanträge unserer Kunden zu unterstützen.
Technischer Support und Validierungsunterstützung: Das technische Team von MIDPOSI arbeitet mit der Qualitätssicherung und den Ingenieursgruppen der Einrichtung zusammen, um Pilotstudien, Reinigungsvalidierungsprotokolle und die Dokumentation behördlicher Begründungen zu unterstützen. Wir bieten Musterkits für die interne Bewertung, Vor-Ort-Schulungen für Reinigungspersonal und maßgeschneiderte Produktkonfigurationen (Größe, Material, Sterilisationsmethode), um den spezifischen Anforderungen der Einrichtung gerecht zu werden.
Für weitere Informationen zu den Reinraum-Mopplösungen von MIDPOSI fordern Sie über unsere Website einen Produktkatalog und ein Paket mit technischen Spezifikationen an oder wenden Sie sich an Ihren regionalen Vertreter.









