Fehler bei der Umweltüberwachung in der Arzneimittelherstellung sind in 60 % der Fälle auf die Durchführung von Reinigungsarbeiten zurückzuführen. In einem Warnschreiben der FDA aus dem Jahr 2025 an Excelvision Fareva wurde ausdrücklich darauf hingewiesen, dass es „nicht gelungen sei, ein angemessenes System zur Reinigung und Desinfektion von Räumen und Geräten einzurichten, um aseptische Bedingungen zu schaffen“ – nicht, weil es in der Einrichtung an Reinigungswerkzeugen mangelte, sondern weil die SOPs die Reinigungsvalidierung nicht mit den Anforderungen der Contamination Control Strategy (CCS) integrieren konnten, die Sterilisation kritischer Komponenten nicht spezifiziert ließen und keinen Verifizierungsrahmen für Bediener boten, um aseptische Bedingungen nach der Reinigung nachzuweisen.
Wenn es zu Abweichungen bei der Umweltüberwachung kommt, wenn die FDA 483 Beobachtungen über „unzureichende Reinigungsvalidierung“ macht oder wenn EU-GMP-Annex-1-Inspektoren „nicht validierte Desinfektionsprogramme“ feststellen, liegt die Ursache selten im Mopp selbst. Es handelt sich um die Standardarbeitsanweisung, die keine Bereichsklassifizierungslogik definiert, Angaben zur Kontaktzeit auslässt, keine Validierungskontrollpunkte vorsieht und den Bedienern die Unsicherheit darüber lässt, ob eine Oberfläche tatsächlich gereinigt oder lediglich abgewischt wurde.
Dieser Leitfaden bietet den rechtlichen Rahmen, eine Schritt-für-Schritt-Struktur, Validierungskontrollpunkte und praktische Vorlagen, die Sie benötigen, um eine Reinraum-Wisch-SOP zu schreiben, die ISO 14644, EU GMP Annex 1 und FDA CGMP-Anforderungen erfüllt – eine, die die Qualitätssicherung bei Inspektionen verteidigen kann, Bediener konsistent ausführen können und Validierungsteams sich mit messbaren Akzeptanzkriterien qualifizieren können. Ganz gleich, ob Sie Ihre erste pharmazeutische Reinigungs-SOP verfassen, veraltete Verfahren aktualisieren, um Anhang 1 CCS-Anforderungen zu erfüllen, oder Protokolle für mehrere aseptische Einrichtungen standardisieren, diese umfassende Referenz liefert die Struktur und technische Tiefe, die für GMP-konforme Wischprogramme in ISO 5–8-pharmazeutischen Umgebungen erforderlich sind.
Warum Reinraum-Wisch-SOPs gemäß ISO von entscheidender Bedeutung sind & GMP
Reinigungsverfahren in pharmazeutischen Reinräumen unterliegen einer besonderen regulatorischen Belastung. Im Gegensatz zu Hausmeisterprotokollen in Bürogebäuden, in denen „sauber genug“ eine subjektive Beurteilung ist, handelt es sich bei SOPs für das Wischen von Arzneimitteln um rechtliche Beweisdokumente, die durch Validierung und routinemäßige Überwachung nachweisen müssen, dass Reinigungsaktivitäten den klassifizierten Umgebungszustand erreichen und aufrechterhalten, der für die Herstellung steriler Arzneimittel erforderlich ist.
EU GMP Annex 1 (gültig ab August 2023) bezeichnet Reinigung und Desinfektion ausdrücklich als „kritisches Element“ der Kontaminationskontrollstrategie (Abschnitte 4.10, 4.22, 4.33-4.36). Der überarbeitete Anhang verlangt, dass Reinigungsprogramme validiert werden, dass die Wirksamkeit der Desinfektion routinemäßig überwacht wird und dass Desinfektionsmittel und Reinigungswerkzeuge, die in aseptischen Bereichen der Klasse A/B verwendet werden, vor der Verwendung steril sein müssen. Hierbei handelt es sich nicht um einen Leitfaden, sondern um eine regulatorische Vorgabe, die Einrichtungen durch dokumentierte, validierte SOPs umsetzen müssen.
ISO 14644-5 (Revision 2025) erfordert ein Betriebskontrollprogramm (OCP), das explizit Reinigung, Personalbewegung und Überwachung abdeckt, mit Verfahren, die „für die angegebenen Reinheitsgrade geeignet sind“. ISO 14644-1 definiert diese Reinheitsstufen nach Partikelkonzentration (z. B. ISO-Klasse 5: 3.520 Partikel/m³ bei ≥0,5 µm), und Wischaktivitäten dürfen diese Grenzwerte während der Ausführung nicht verletzen oder die rechtzeitige Rückkehr zur Klassifizierung nach der Reinigung verhindern.
Warnschreiben der FDA von 2023 bis 2025 zeigen, wo SOPs in der Praxis versagen. Im Warnschreiben von Excelvision Fareva aus dem Jahr 2025 wurde darauf hingewiesen, dass die Ausrüstung vor dem Einbau in ISO-5-Abfülllinien nicht sterilisiert wurde – eine Lücke, die eine ordnungsgemäß strukturierte SOP durch die Definition von Protokollen zur Werkzeughandhabung und zur sterilen Einführung verhindert hätte. Im Brief von Staska Pharmaceuticals aus dem Jahr 2025 wurde auf eine „unzureichende Reinigungsvalidierung“ und die Notwendigkeit einer „wissenschaftlich fundierten Begründung“ der Reinigungswirksamkeit bei Rückständen und Keimbelastung hingewiesen. In der Warnung von Empower Pharmacy wurde betont, dass jede mikrobielle Rückgewinnung gemäß ISO 5 „ernsthaft besorgniserregend“ sei und eine sofortige Untersuchung erfordert. Dabei wurde deutlich, dass SOPs Alarm-/Aktionsgrenzen, Überprüfungsproben und Untersuchungsauslöser definieren und nicht einfach nur Wischschritte auflisten müssen.
Die Folgen unzureichender SOPs gehen weit über regulatorische Erkenntnisse hinaus. Umweltüberwachungsausflüge, die auf die Reinigung von Produktionsräumen der Hinrichtungskräfte, Chargenuntersuchungen und umfassende Ursachenanalysen zurückgeführt wurden. Wenn in der SOP Validierungskontrollpunkte fehlen oder technische Spezifikationen (z. B. unidirektionales Wischen, Überprüfung der Kontaktzeit) fehlen, können die Ermittler nur schwer feststellen, ob die Abweichung einen Fehler des Reinigungssystems oder eine Abweichung bei der Ausführung widerspiegelt – was die Untersuchungen in die Länge zieht und das Vertrauen in das gesamte Kontaminationskontrollprogramm untergräbt.
Häufige SOP-Mängel, die Compliance-Beobachtungen auslösen
Wenn FDA-Inspektoren oder EU-GMP-Auditoren Bemerkungen zu Wischverfahren in Reinräumen machen, konzentrieren sich die Mängel auf mehrere wiederkehrende Themen:
Fehlende Logik zur Bereichsklassifizierung: Generische SOPs, die das gleiche Verfahren, die gleichen Tools und die gleiche Verifizierung auf ISO 5-, ISO 7- und ISO 8-Bereiche anwenden, zeigen ein unzureichendes Verständnis der risikobasierten Kontaminationskontrolle. In Anhang 1, Tabelle 2 sind Grenzwerte für die mikrobielle Eignung festgelegt, die von „kein Wachstum“ (Klasse A) bis zu 50 KBE pro Kontaktplatte (Klasse D) reichen. In den SOPs fehlen jedoch häufig eine sortenspezifische Werkzeugauswahl (steril vs. fusselarm), Anforderungen an Desinfektionsmittel (sporizid für Klasse A/B vs. routinemäßige Bakterizide für Klasse C/D) oder die Überprüfungshäufigkeit.
Fehlende Validierungskontrollpunkte: SOPs, die Bediener anweisen, „den Boden zu wischen“, ohne zu definieren, wie die Reinigungswirksamkeit überprüft wird, was eine akzeptable Reduzierung der Keimbelastung darstellt oder wann Proben für die Umweltüberwachung entnommen werden müssen, liefern keinen objektiven Beweis dafür, dass die Reinigung ihren beabsichtigten Zweck erfüllt. ISO 14644-5 definiert Verifizierung als „Bestätigung durch objektive Beweise, dass bestimmte Anforderungen erfüllt wurden“ – wenn die SOP keine Messkriterien vorsieht, ist eine Verifizierung nicht möglich.
Weggelassene Kontaktzeitangaben: Desinfektionsmittel erfordern eine definierte Nasskontaktzeit, um die angegebene Tötungsaussage zu erreichen. Isopropylalkohol (IPA) wirkt bei 70 % schnell bakterizid, muss aber auf der Oberfläche feucht bleiben – dennoch verdunstet IPA innerhalb von Sekunden, oft bevor die für eine viruzide Wirkung erforderliche Kontaktzeit von 1–2 Minuten erreicht wird. SOPs, in denen es heißt „Desinfektionsmittel auftragen und abwischen“, ohne eine Mindestnässezeit, Wiederbefeuchtungsprotokolle oder eine Überprüfung, ob Oberflächen nass geblieben sind, anzugeben, bieten keine Grundlage für die Annahme, dass eine Desinfektion stattgefunden hat.
Keine Kontrollen der Werkzeugkreuzkontamination: Wiederverwendbare Mopps tragen Keimbelastung und Partikelkontamination aus früheren Räumen, sofern sie nicht nach validierten Protokollen wiederaufbereitet werden. In den SOPs werden jedoch häufig Anweisungen zur Wiederaufbereitung, maximale Nutzungszyklen, Sterilitätsüberprüfung oder physische Kontrollen weggelassen, die die Verwendung von Mopps verschiedener Sorten verhindern (z. B. Farbcodierung, Regeln für einen Mopp pro Raum). Das Ergebnis: Ein Mopp, der in einem ISO-8-Verpackungsbereich verwendet wird, gelangt in einen ISO-6-Abfüllraum und trägt eine Kontamination mit sich, die durch die SOP nicht verhindert werden konnte.
Unzureichende Desinfektionsmittel-Rotationslogik: Anhang 1 Abschnitt 4.33 erfordert „mehr als ein Desinfektionsmittel“ mit „verschiedenen Wirkungsweisen“ und „periodischer Verwendung eines sporiziden Mittels“. SOPs, die Desinfektionsmittel willkürlich wechseln (Montag: IPA, Dienstag: Peroxid, Mittwoch: IPA), ohne die Vielfalt der Wirkungsweise, die sporizide Häufigkeit oder die Wirksamkeitsüberwachung gegenüber wiederhergestellter Flora zu definieren, verfehlen den Nachweis eines wissenschaftlich begründeten Programms.
Diese Mängel sind vermeidbar. Eine gut strukturierte SOP, die den Umfang anhand der ISO-Klassifizierung definiert, Validierungskontrollpunkte mit messbaren Akzeptanzkriterien integriert, die Werkzeughandhabung zur Vermeidung von Kreuzkontaminationen spezifiziert und den Einsatz von Desinfektionsmitteln an validierte Kontaktzeiten bindet, verwandelt die Reinigung von einer „Best-Effort“-Aktivität in einen kontrollierten, überprüfbaren Prozess, der die Chargensterilität schützt und der behördlichen Prüfung standhält.
Übersicht über die ISO/GMP-konforme Wisch-SOP-Struktur
Eine pharmazeutische Reinraum-Wisch-SOP ist kein narratives Dokument, sondern ein strukturierter Kontrollrahmen, der Bediener durch die Vorbereitung der Vorreinigung, die Durchführung mit Überprüfung und die Dokumentation führt, die einen Prüfpfad erstellt. Die folgende Struktur spiegelt Best Practices aus ISO 14644-5, EU GMP Annex 1 und den CGMP-Erwartungen der FDA wider und ist so organisiert, dass sie sowohl die Umsetzung durch den Betreiber als auch die Verteidigung gegen Vorschriften unterstützen.
Kern-SOP-Komponenten
1. Geltungsbereich & Gebietsklassifizierung
Definieren Sie, welche Räume, Suiten oder Zonen die SOP regelt, mit expliziter ISO-Klassifizierung gemäß ISO 14644-1 (z. B. ISO-Klasse 5, Klasse 7) und ggf. entsprechenden EU-GMP-Klassen (Klasse A/B/C/D). Geben Sie Belegungszustände (im Ruhezustand, in Betrieb) und etwaige Ausschlüsse an (z. B. deckt diese SOP nicht die Innenreinigung von Geräten oder die Deckendesinfektion ab). Die Bereichsklassifizierung bestimmt jede nachgelagerte Entscheidung – Werkzeugauswahl, Desinfektionsmittelanforderungen, Überprüfungshäufigkeit –, sodass Unklarheiten hier zu Ausführungsfehlern führen.
Beispiel für eine Geltungsbereichserklärung: „Diese SOP regelt das Bodenwischen in Vorräumen aseptischer Abfüllräume der ISO-Klasse 6 (Klasse B) und in Umkleidekorridoren der ISO-Klasse 7 (Klasse C). Kritische Zonen der ISO-Klasse 5 (Klasse A) mit unidirektionalem Luftstrom sind ausgeschlossen und werden von SOP-CLEAN-005 abgedeckt.“
2. Verantwortlichkeiten
Weisen Sie Rollen für die Ausführung (Produktionsbetreiber, Umweltdienste), die Überprüfung (Produktionsleiter), die Genehmigung (QS) und die Aufsicht (Spezialisten für Kontaminationskontrolle) zu. Legen Sie fest, wer Bediener qualifiziert, wer Abweichungen untersucht und wer den Werkzeug- und Desinfektionsmittelbestand verwaltet. Eine klare Verantwortlichkeit verhindert „Es ist nicht meine Aufgabe“-Lücken, die dazu führen, dass wichtige Aufgaben nicht ausgeführt werden.
3. Definitionen & Referenzen
Definieren Sie Schlüsselbegriffe, die falsch interpretiert werden könnten: „steril“ (Sterilisation mit SAL 10⁻⁶), „fusselarm“ (Partikelerzeugung). <100 Partikel ≥0,5 µm pro Hub), „Kontaktzeit“ (minimale Nassverweildauer laut Produktetikett), „sporizid“ (wirksam gegen Bakteriensporen gemäß validiertem Belastungstest). Verweisen Sie auf maßgebliche Standards (ISO 14644-1:2015, ISO 14644-5:2025, EU-GMP-Anhang 1 Abschnitte 4.33–4.36, CCS-Dokument der Einrichtung), damit Prüfer Anforderungen auf Quellvorschriften zurückführen können.
4. Zugelassene Werkzeuge & Materialien
Listen Sie Moppsysteme (Moppkopfmaterial, Rahmen, Griff), Eimer oder vorgetränkte Applikatoren und Desinfektionsmittel nach Produktname, Konzentration und Chargenrückverfolgbarkeitsanforderungen auf. Geben Sie die Sterilitätsanforderungen je nach Bereichsklasse an (sterile gammabestrahlte Mopps für Klasse A/B, autoklavierbares, fusselarmes Polyester für Klasse C/D). Geben Sie Referenzen zur Lieferantenqualifikation und die Verfügbarkeit von Validierungspaketen an (Daten zur Partikelerzeugung, Matrizen zur chemischen Kompatibilität, Sterilisationszertifikate). Dieser Abschnitt beantwortet die Betreiberfrage: „Was darf ich verwenden?“
5. Vorbereitungen vor dem Wischen
Detaillierte Anforderungen an die Kleidung, Materialeinführungsprotokolle (Desinfektion der Außenseiten der Moppverpackung vor Eintritt in die Luftschleuse), Überprüfung der Werkzeugintegrität (versiegelte Sterilverpackung intakt, keine sichtbaren Schäden an den Moppköpfen) und Desinfektionsmittelvorbereitung (Überprüfung der Verdünnung, Sterilität für Klasse A/B, Ablaufdatum). Hier wird eine Kreuzkontamination verhindert oder eingeführt – strenge Vorkontrollen erkennen Probleme, bevor sie in den Reinraum gelangen.
6. Schritt-für-Schritt-Anleitung
Stellen Sie sequenzielle, vom Bediener ausführbare Anweisungen bereit, die die Raumeinrichtung (HEPA-Überprüfung, Materialflussweg), die Wischreihenfolge (von oben nach unten für Wände, weit bis zum Ausgang für Böden, unidirektionale Hübe, die auf den Luftstrom ausgerichtet sind), die Kontaktzeitüberprüfung (Oberfläche bleibt für die angegebene Dauer sichtbar nass) und Kontrollen nach dem Wischen (keine Ansammlung, keine Rückstandsstreifen) bereitstellen. Verwenden Sie nummerierte Schritte, keine Absätze. Jeder Schritt sollte eine einzelne Aktion und gegebenenfalls ein Akzeptanzkriterium haben.
7. Überprüfung & Dokumentation
Definieren Sie, was Bediener aufzeichnen müssen (Datum, Uhrzeit, Bereich, Desinfektionsmittelcharge, Initialen des Bedieners, etwaige Abweichungen), wie Verbindungen zur Umgebungsüberwachung erfolgen (z. B. „Die Qualitätssicherung sammelt innerhalb von 30 Minuten nach der Reinigung Absetzplatten im gewischten Bereich“) und Untersuchungsauslöser (sichtbare Rückstände, nicht erreichte Kontaktzeit, Versagen der Werkzeugintegrität). Die Dokumentation ist der objektive Beweis, den ISO 14644-5 für die Verifizierung verlangt – ohne sie ist die Reinigung nicht überprüfbar.
8. Sicherheit & Vorsichtsmaßnahmen
Berücksichtigen Sie chemische Gefahren (IPA-Entflammbarkeit, Warnungen vor Peroxid-Oxidationsmittel), Rutschrisiken durch nasse Böden und Notfallkontakte. Dieser Abschnitt schützt Betreiber und demonstriert die gebotene Sorgfalt beim Risikomanagement.
9. Anhänge & Referenzen
Fügen Sie Kontaktzeitpläne für Desinfektionsmittel, Flussdiagramme zur Werkzeugaufbereitung (für wiederverwendbare Systeme), Farbcodierungsschemata zur Verhinderung einer klassenübergreifenden Verwendung und Links zu verwandten SOPs (Kleidung, Abfallentsorgung, Umweltüberwachung) bei. Anhänge halten das Kernverfahren schlank und bieten dem Bediener bei Bedarf schnelle Referenzdetails.
Diese Struktur verwandelt eine vage „Reinigung des Bodens“-Anweisung in einen kontrollierten Prozess mit definierten Eingaben (qualifizierte Werkzeuge, validierte Desinfektionsmittel), kontrollierter Ausführung (unidirektionale Technik, überprüfte Kontaktzeit) und messbaren Ergebnissen (dokumentierter Abschluss, EM-Überprüfung innerhalb der Akzeptanzkriterien). Regulierungsbehörden erwarten dieses Maß an Genauigkeit in der Arzneimittelherstellung – die Umsetzung durch strukturierte SOPs ist keine Option.

Abbildung 1: Flussdiagramm der ISO/GMP-konformen SOP-Struktur. Dieses modulare Framework gewährleistet die Durchsetzbarkeit von Vorschriften, indem es den Geltungsbereich anhand der ISO-Klassifizierung definiert, Validierungskontrollpunkte integriert und vom Bediener ausführbare Verfahren mit messbaren Ergebnissen erstellt.
Schritt-für-Schritt-Workflow zum Wischen im Reinraum (High-Compliance-Version)
Der operative Kern einer Reinraum-Wisch-SOP ist das Schritt-für-Schritt-Verfahren, das die Bediener ausführen. Dieser Arbeitsablauf integriert die ISO-Klassifizierungslogik, die Anforderungen an sterile Werkzeuge gemäß Anhang 1, die Überprüfung der Kontaktzeit und Kreuzkontaminationskontrollen in einer strukturierten Abfolge, die behördliche Vorschriften in die tägliche Praxis umsetzt.
1. Vorbereitung der Vorreinigung
Bevor ein Wischmopp in einen klassifizierten Bereich gelangt, müssen die Bediener die Umkleidung, die Werkzeugqualifikation und die Umgebungstauglichkeitsprüfung durchführen.
Qualifikation zum Umkleiden: Das Personal muss gemäß den SOPs des Standorts einrichtungsspezifische Reinraumkleidung anziehen und sich jährlich für den Zugang der Klasse A/B erneut qualifizieren (Anhang 1 erfordert eine „mindestens jährliche“ Bewertung für Personal im aseptischen Bereich). Bevor Sie fortfahren, müssen die Integrität des Kittels, die Technik zum Anziehen der Handschuhe und die Passform der Haube/Brille den Akzeptanzkriterien entsprechen. Bediener mit sichtbaren Mängeln an der Kleidung (zerrissene Handschuhe, freiliegendes Haar) werden sofort vom Zutritt ausgeschlossen.
Überprüfung der Mop-Integrität: Nehmen Sie den Mopp aus der Verpackung und prüfen Sie ihn auf Beschädigungen. Vergewissern Sie sich bei sterilen gammabestrahlten Einwegmopps (Klasse A/B), dass das Verpackungssiegel intakt ist, der Strahlungsindikator eine „bestandene“ Farbveränderung anzeigt und das Ablaufdatum der Sterilität gültig ist. Vergewissern Sie sich bei autoklavierbaren wiederverwendbaren Mopps, dass die Autoklavierbandanzeige „steril“ anzeigt und dass das Sterilisationsdatum innerhalb der Haltezeit liegt (in der Regel 7–30 Tage, je nach Verpackung). Jeder beeinträchtigte Sterilitätsindikator führt zur Ablehnung des Mopps und wird als Abweichung dokumentiert.
Vorbereitung und Überprüfung des Desinfektionsmittels: Für Bereiche der Klasse A/B müssen Desinfektionsmittel vor der Verwendung steril sein (Anhang 1 Abschnitt 4.34). Verwenden Sie kommerziell hergestelltes steriles Desinfektionsmittel mit einem Analysezertifikat mit Chargenrückverfolgung oder bereiten Sie Verdünnungen aseptisch unter Verwendung von sterilem Wasser und validierter aseptischer Technik vor. Überprüfen Sie die Konzentration mithilfe der Verdünnungstabellen auf dem Etikett oder des Refraktometers (für IPA). Notieren Sie die Chargennummer, das Datum/die Uhrzeit der Zubereitung, das Verfallsdatum (in der Regel 24 Stunden für vor Ort zubereitete Lösungen) und die Initialen des Bedieners. Für Klasse C/D sind unsterile Desinfektionsmittel in pharmazeutischer Qualität akzeptabel, sofern ihre Wirksamkeit bestätigt wurde.
Materialeinführungsprotokoll: Desinfizieren Sie die Außenflächen aller Materialien, die in den Reinraum gelangen (Moppverpackung, Desinfektionsmittelflaschen), am Luftschleuseneingang mit der SOP zur Desinfektion des Anlagentransfers. Warten Sie gemäß SOP eine Kontaktzeit ab, bevor Sie die Luftschleuse passieren. Dadurch wird verhindert, dass die Verpackung von außen verunreinigt wird und später mit Reinraumoberflächen in Kontakt kommt.
2. Raumeinrichtung und Umgebungsprüfung
Bestätigung des HEPA-Luftstroms: Bevor Sie mit dem Wischen beginnen, prüfen Sie, ob das HEPA-System im Raum funktioniert. Überprüfen Sie, ob die Differenzdruckmesser einen positiven Druck im Vergleich zu angrenzenden Bereichen mit geringerem Druck anzeigen (typisch: +10–15 Pa Klasse B→C, +15–20 Pa Klasse A→B). Bestätigen Sie für Bereiche mit unidirektionalem Luftstrom (Klasse A) den ersten Luftstrom visuell mithilfe der Methode zur Visualisierung des Luftstroms in der Einrichtung (z. B. zugelassene Partikelstreamer, Rauchstudien in der Einrichtung). Wenn der Luftstrom beeinträchtigt ist, benachrichtigen Sie den Vorgesetzten und verschieben Sie die Reinigung, bis das Problem behoben ist. Beim Wischen ohne funktionierenden HEPA besteht die Gefahr einer Kontaminationsansammlung.
Einrichtung des Materialflusspfades: Machen Sie einen definierten Weg von der Luftschleuse bis zur hintersten Ecke des Raums frei. Das Wischen erfolgt von dieser hinteren Ecke in Richtung Ausgang, um sicherzustellen, dass die Bediener niemals über frisch gewischte Böden laufen und Verunreinigungen erneut ablagern. Entfernen Sie mobile Geräte oder Materialien, die den Wischweg behindern. Koordinieren Sie bei Abfülllinien der Güteklasse A die Produktion mit der Produktion, um sicherzustellen, dass die aseptischen Vorgänge abgeschlossen sind und sich die Linie im „Ruhezustand“ befindet, bevor mit dem Wischen begonnen wird.
Vorwischen, dann wischen: Anhang 1 und bewährte GMP-Praktiken erfordern eine Reinigung vor der Desinfektion, da Ablagerungen und Rückstände den Kontakt mit dem Desinfektionsmittel verhindern. Wischen Sie Wände und vertikale Flächen zunächst mit zugelassenen, fusselarmen Tüchern ab, um sichtbare Partikel zu entfernen, und tragen Sie anschließend einen Desinfektionsmopp auf. Bei Böden mit sichtbaren Ablagerungen saugen Sie vor dem Nasswischen mit einem HEPA-gefilterten Reinraumstaubsauger vor oder wischen Sie stark beanspruchte Bereiche vor. Dieser zweistufige Ansatz stellt sicher, dass das Desinfektionsmittel mit einer sauberen Oberfläche in Kontakt kommt und maximiert so die Wirksamkeit.
3. Wischsequenz: Unidirektional, überlappend, Austrittspfad ausgerichtet
Prinzip „Top-to-Bottom, Clean-to-Dirty“.: Reinigen Sie höher gelegene Flächen immer vor tiefer gelegenen. Beginnen Sie bei Wänden an der Deckenverbindung und wischen Sie in vertikalen Bewegungen nach unten. Beginnen Sie bei Böden an der entferntesten und saubersten Ecke und arbeiten Sie sich in Richtung Ausgang vor (normalerweise die Luftschleuse oder den Eingang zum Umkleidebereich). Wischen Sie niemals von schmutzigen Bereichen in Richtung sauberer Bereiche – dies führt zu Kreuzkontaminationen und verstößt gegen die Kontaminationskontrolllogik.
Unidirektionale Schlagtechnik: Verwenden Sie gerade, parallele Striche nur in eine Richtung. Ziehen Sie den Mopp in einer sanften, kontrollierten Bewegung zu sich heran, heben Sie ihn am Ende des Zuges an, positionieren Sie ihn für den nächsten Durchgang neu und wiederholen Sie den Vorgang. Verwenden Sie keine Hin- und Herbewegungen oder Achterbewegungen – diese verteilen die Kontamination neu, anstatt sie zu entfernen. Jeder Strich sollte den vorherigen um 10–25 % überlappen, um sicherzustellen, dass keine Lücken in der Abdeckung entstehen.
Luftstromausrichtung für Klasse A/B: Richten Sie in Bereichen mit unidirektionalem Luftstrom die Wischbewegungen nach Möglichkeit auf die Richtung des HEPA-Luftstroms aus. Wischen senkrecht zur ersten Luft kann die laminare Strömung stören und die Partikelanzahl in der kritischen Zone vorübergehend erhöhen. Während bei der Reinigung gewisse Störungen unvermeidbar sind, minimiert die Ausrichtung auf den Luftstrom Turbulenzen und unterstützt eine schnellere Rückkehr zur Klassifizierung.
Überprüfung der Kontaktzeit (kritischer Compliance-Punkt): Nach dem Auftragen des Desinfektionsmittels muss die Oberfläche für die angegebene Einwirkzeit sichtbar feucht bleiben. Hier scheitern die meisten SOPs bei der Umsetzung. Isopropylalkohol (70 % IPA) verdunstet in 30–60 Sekunden, benötigt jedoch 1–2 Minuten für die volle viruzide Wirkung. Wasserstoffperoxid-Formulierungen erfordern typischerweise je nach Konzentration einen Kontakt von 1–5 Minuten. Der Bediener muss entweder eine ausreichende Menge auftragen, um die Nässe während der gesamten Kontaktzeit aufrechtzuerhalten, oder Oberflächen, die vorzeitig trocknen, erneut befeuchten. Dokumentieren Sie die erreichte Kontaktzeit: „Die Oberfläche blieb gemäß der SOP-CHEM-012-Anforderung 3 Minuten lang sichtbar nass.“
Regel „Ein Wischen pro Zimmer“ (Kreuzkontaminationsverhinderung): Einwegmopps werden nach Fertigstellung eines Raums entsorgt und nie wiederverwendet. Wiederverwendbare Mopps müssen nach jedem Raum zur Wiederaufbereitung eingesammelt werden und dürfen niemals ohne validierte Sterilisation zwischen den Bereichen transportiert werden. Wenn Sie farbcodierte Systeme verwenden, sorgen Sie für eine strikte Klassentrennung: blaue Mopps nur für Klasse C, gelbe nur für Klasse B, rote nur für Klasse A. Der sortenübergreifende Moppgebrauch stellt eine kritische Abweichung dar, die einer Untersuchung bedarf.
4. Dokumentation der Kontaktzeit des Desinfektionsmittels
Die Kontaktzeit ist nicht optional – es handelt sich um einen validierten Parameter, der aufgezeichnet und überprüft werden muss. SOPs müssen Folgendes angeben:
- Produktname und Chargennummer des verwendeten Desinfektionsmittels
- Beschriftete Kontaktzeit gemäß Gebrauchsanweisung des Herstellers oder Validierung der Einrichtung (z. B. „3 Minuten Nasskontakt“)
- Überprüfungsmethode: visuelle Bestätigung der während des gesamten Zeitraums aufrechterhaltenen Nässe oder zeitgesteuerte Dokumentation
- Protokoll zur erneuten Befeuchtung, wenn die Oberfläche vorzeitig trocknet: „Wenn die Oberfläche vor Ablauf der Kontaktzeit trocknet, tragen Sie das Desinfektionsmittel erneut auf und starten Sie den Timer neu.“
In Warnschreiben der FDA wird ausdrücklich auf eine unzureichende Kontaktzeit als wiederkehrende Validierungslücke hingewiesen. In Staskas Brief aus dem Jahr 2025 wurde auf die Notwendigkeit einer „wissenschaftlich fundierten Begründung“ der Reinigungswirksamkeit hingewiesen, die von der Erreichung validierter Expositionsbedingungen abhängt. Eine SOP, die die Kontaktzeit auslässt, bietet keine Grundlage für die Behauptung, dass eine Desinfektion stattgefunden hat.
5. Entsorgungs- oder Wiederaufbereitungsweg
Entsorgung von Einwegmopps: Nach dem Gebrauch werden Einwegmopps sofort in dafür vorgesehene Abfallbehälter im Reinraum gegeben (normalerweise ausgekleidet mit Autoklavenbeuteln zur Inaktivierung der Keimbelastung vor der Entfernung). Tragen Sie die Entsorgung im Reinigungsprotokoll ein: „Mopp Nr. 2025-04-18-001, verwendet in Raum 204 (ISO 6), entsorgt gemäß SOP-WASTE-003.“ Der Entsorgungsweg bietet kein Kreuzkontaminationsrisiko und eliminiert den Validierungsaufwand für die Wiederaufbereitung – ein entscheidender Vorteil für Hochrisikogebiete.
Wiederaufbereitung von Mehrwegmopps: Sammeln Sie gebrauchte wiederverwendbare Mopps in speziellen Behältern für verschmutzte Werkzeuge, getrennt nach Qualität. Transport zur validierten Wäscherei oder zum Wiederaufbereitungsbereich vor Ort gemäß Materialfluss-SOP. Die Wiederaufbereitung muss Folgendes umfassen:
- Validierter Waschzyklus (Temperatur, Reinigungsmittel, Spülzyklen), der geeignet ist, Keime und Partikel zu entfernen, ohne das Moppmaterial zu beschädigen
- Prüfung auf Abnutzung, Risse oder Verlust der fusselarmen Leistung; Ablehnen von Mopps, die die maximale Anzahl an Waschzyklen überschreiten (z. B. 50–100 Waschzyklen, je nach Material)
- Sterilisation (Autoklavieren bei 121 °C für 30 Minuten oder Gammabestrahlung) mit Sterilitätsüberprüfung gemäß Validierungsprotokoll
- Sterile Verpackung mit Ablaufdatum und Chargenrückverfolgbarkeit
Das Ignorieren der Grenzwerte für die Zyklenzahl birgt ein hohes Risiko. Mopps zersetzen sich durch wiederholtes Waschen und Sterilisieren, wobei sie nach und nach mehr Partikel abgeben und an Saugfähigkeit verlieren. SOPs müssen Ablehnungskriterien und die Nachverfolgung der Dokumentenzyklusanzahl definieren.

Abbildung 2: Wisch-Workflow im Reinraum mit hoher Compliance. Jede Phase umfasst Verifizierungskontrollpunkte, die behördliche Vorschriften in vom Bediener ausführbare Schritte mit objektivem Nachweis der Einhaltung umwandeln.
Validierungsanforderungen für Wisch-SOPs
Eine nicht validierte Reinigungs-SOP ist aus regulatorischer Sicht unkontrolliert. EU-GMP-Anhang 1 Abschnitt 4.22 verlangt, dass die „Reinigung vor der Desinfektion“ validiert wird und dass Desinfektionsprozesse „in der spezifischen Art der Verwendung“ validiert werden. ISO 14644-5 erfordert eine Verifizierung durch objektive Beweise. In Warnschreiben der FDA wird von einer „unzureichenden Reinigungsvalidierung“ gesprochen, wenn Einrichtungen anhand von Daten nicht nachweisen können, dass die Reinigung die beabsichtigte Kontaminationskontrolle erreicht. In diesem Abschnitt werden die Validierungskontrollpunkte definiert, die ein schriftliches Verfahren in ein qualifiziertes, vertretbares Reinigungssystem umwandeln.
1. Partikelvalidierung (Konformität mit ISO 14644-1)
Das Wischen darf während der Ausführung nicht gegen die Raumklassifizierungsgrenzwerte verstoßen oder die rechtzeitige Wiederherstellung der Ruheklassifizierung nach der Reinigung verhindern.
Validierungsansatz: Führen Sie eine Partikelüberwachung bei Wischvorgängen im ungünstigsten Fall durch (maximale Bodenfläche, repräsentativer Bediener, routinemäßige Desinfektion) mithilfe kalibrierter optischer Partikelzähler, die gemäß ISO 14644-1-Probenahmeplänen positioniert sind. Messen Sie die Partikelkonzentration bei ≥0,5 µm und ≥5,0 µm vor dem Wischen, während des Wischens (Spitzenstörung) und in definierten Intervallen nach dem Wischen, bis die Ausgangswerte wieder erreicht sind.
Akzeptanzkriterien nach ISO-Klasse:
- ISO-Klasse 5: Die Partikelzahl muss innerhalb von 15–20 Minuten nach dem Wischen auf ≤3.520 Partikel/m³ (≥0,5 µm) zurückgehen. Vorübergehende Spitzen beim Wischen sollten das Zweifache der Klassifizierungsgrenze nicht überschreiten. Anhaltende Überschreitungen lösen eine Untersuchung der Entstehung von Wischpartikeln, der Technik des Bedieners oder einer Störung des Luftstroms aus.
- ISO-Klasse 6: Rückkehr zu ≤35.200 Partikeln/m³ (≥0,5 µm) innerhalb von 20 Minuten. Spitzenwert beim Wischen <2,5-fache Grenze.
- ISO-Klasse 7: Rückkehr zu ≤352.000 Partikeln/m³ (≥0,5 µm) innerhalb von 20 Minuten. Spitzenwert beim Wischen <3x Grenze.
- ISO-Klasse 8: Rückkehr zu ≤3.520.000 Partikeln/m³ (≥0,5 µm) innerhalb von 20 Minuten.
Warum wiederverwendbare Mopps bei der Partikelvalidierung häufiger durchfallen: Gewaschene wiederverwendbare Mopps geben nach und nach mehr Partikel ab, da sich der Stoff bei wiederholten Wasch-/Sterilisationszyklen verschlechtert. Selbst bei validierter Wiederaufbereitung birgt die Variabilität von Zyklus zu Zyklus das Risiko der Partikelgenerierung. Einwegmopps liefern eine gleichbleibende, qualifizierte Partikelleistung, da jede Verwendung mit einem frischen, werkseitig validierten Moppkopf beginnt.
2. Bioburden-Validierung
Reinigung und Desinfektion müssen eine messbare Reduzierung der Keimbelastung bewirken. Anhang 1, Tabelle 2, definiert die Grenzwerte für die mikrobielle Eignung nach Grad; Die routinemäßige Umweltüberwachung bestätigt die laufende Kontrolle.
Trend zur Grundkeimbelastung: Legen Sie die Basislinie für die Keimbelastung vor der Reinigung fest, indem Sie vor dem geplanten Wischen routinemäßige EM-Proben (Kontaktplatten, Tupfer) von repräsentativen Bodenflächen entnehmen. Trendbasislinie über 3–6 Monate, um typische Kontaminationsniveaus nach Gebiet und Tageszeit zu verstehen. Nachreinigungsproben, die 30–60 Minuten nach dem Wischen entnommen werden (unter Berücksichtigung der Kontaktzeit des Desinfektionsmittels und der Verdunstung), zeigen eine Verringerung der Keimbelastung.
Akzeptanzkriterien (EM-Ergebnisse nach der Reinigung):
- Klasse A: Kein Wachstum (0 KBE) auf Kontaktplatten oder Abstrichtupfern
- Note B: ≤5 KBE pro Kontaktplatte
- Klasse C: ≤25 KBE pro Kontaktplatte
- Klasse D: ≤50 KBE pro Kontaktplatte
Bei Nichteinhaltung dieser Grenzwerte wird eine Untersuchung eingeleitet: Wurde die Kontaktzeit erreicht? Ist das Desinfektionsmittel noch wirksam gegen die wiederhergestellte Flora? Ist die Wiederaufbereitung des Mopps ausreichend (für Mehrwegartikel)? Führt die Technik des Bedieners zu einer Kontamination?
Warum wiederverwendbare Mopps ein höheres Risiko für die Keimbelastung bergen: Wiederverwendbare Mopps können Restkeime in den Zwischenräumen des Gewebes zurückhalten, wenn die Reinigung unzureichend erfolgt oder wenn die Mopps zwischen den Einsätzen feucht gelagert werden. Selbst eine validierte Wiederaufbereitung kann fehlschlagen, wenn die Zyklusparameter abweichen (z. B. die Waschtemperatur unter den Validierungssollwert fällt). Sterile Einwegmopps eliminieren dieses Risiko – jede Verwendung ist SAL 10⁻⁶ steril.
3. Desinfektionsmittelvalidierung
Desinfektionsmittel müssen auf repräsentativen Oberflächen, in der Art der Verwendung (Wischen) und mit validierter Kontaktzeit wirksam gegen die Keimbelastung der Einrichtung sein.
Rotationslogik (Wirkungsweise Diversität): Anhang 1 fordert „mehr als ein Desinfektionsmittel“ mit „verschiedenen Wirkungsweisen“ und „periodischer Verwendung eines sporiziden Mittels“. Eine konforme Rotation könnte sein:
- Woche 1-3: 70 % Isopropylalkohol (Alkohol, bakterizid/viruzid)
- Woche 4: 0,5 % beschleunigtes Wasserstoffperoxid (Oxidationsmittel, bakterizid/fungizid/viruzid)
- Monatlich: Natriumhypochlorit 5000 ppm (Oxidationsmittel, sporizid) oder Peressigsäure (sporizid)
Diese Rotation verhindert, dass sich die Flora an ein einziges Desinfektionsmittel anpasst, und bekämpft sporenbildende Organismen (z. B. Bazillus spp.), die Alkohol widerstehen.
Protokoll zur Überprüfung der Kontaktzeit: Überprüfen Sie, ob Bediener die angegebene Nasskontaktzeit unter tatsächlichen Nutzungsbedingungen einhalten können. Verwenden Sie visuelle Beobachtung, Überwachung der Oberflächentemperatur (bei temperaturempfindlichen Chemikalien) oder Farbstoff-Tracer, um Abdeckung und Verweilzeit zu bestätigen. Wenn IPA verdunstet, bevor die Kontaktzeit abgelaufen ist, ändern Sie die Anwendungsmenge oder -technik oder ziehen Sie vorgetränkte Mopps in Betracht, die ein kontrolliertes Lösungsvolumen liefern.
Kompatibilitätsvalidierung (kritisch für wiederverwendbare Mopps): Einige Desinfektionsmittel-Material-Kombinationen beeinträchtigen die Leistung des Mopps. Quartäre Ammoniumverbindungen (Quats) adsorbieren an Zellulosefasern und verlieren an Aktivität; Es sind Polyester-Moppköpfe erforderlich. Bleichmittel zersetzen bestimmte autoklavenkompatible Polymere bei wiederholter Einwirkung. Die Validierung muss nachweisen, dass zugelassene Moppmaterialien alle Desinfektionsmittel im Rotationsplan vertragen, ohne dass die fusselarmen Eigenschaften oder die strukturelle Integrität verloren gehen.
4. Bedienerqualifikation (OQ)
Die Reinigungswirksamkeit hängt von der Technik des Bedieners ab. Anhang 1 erfordert Schulungen und regelmäßige Neubewertungen; ISO 14644-5 verlangt eine in das OCP integrierte Personalqualifizierung.
Erstqualifizierung: Die Bediener absolvieren eine praktische Schulung zu SOP-Schritten, Anziehen, Umgang mit dem Mopp, unidirektionaler Strichtechnik, Überprüfung der Kontaktzeit und Dokumentation. Die Qualifikation umfasst eine beobachtete Leistungsbewertung: Der Trainer beobachtet, wie der Bediener den gesamten Wischzyklus ausführt, und überprüft die Technik anhand der Checkliste (unidirektionale Bewegungen, ordnungsgemäße Überlappung, erreichte Kontaktzeit, Einhaltung der Regel „Ein Wischen pro Raum“). Nur Betreiber mit der Bewertung „bestanden“ sind berechtigt, klassifizierte Bereiche unbeaufsichtigt zu reinigen.
Jährliche Kompetenzneuqualifizierung: Anhang 1 verlangt eine Neubewertung „mindestens jährlich“ für Personal der Besoldungsgruppe A/B. Die Requalifizierung umfasst eine schriftliche Beurteilung (SOP-Kenntnisse, Kontaktzeiten des Desinfektionsmittels, Meldung von Abweichungen) und die beobachtete Leistung. Jeder Bediener, der mit einer EM-Exkursion oder einer SOP-Abweichung in Verbindung steht, durchläuft eine sofortige Umschulung und Neuqualifizierung, bevor er seine Reinigungsaufgaben wieder aufnimmt.
Videoaufzeichnung als Beweis: Einige Einrichtungen zeichnen Schulungen zur Bedienerqualifikation auf und schaffen so objektive Beweise für Audits. Aufgezeichnete Sitzungen demonstrieren die richtige Technik und bieten Schulungsmaterial für neue Mitarbeiter. Video ist gesetzlich nicht vorgeschrieben, bietet jedoch eine zuverlässige Dokumentation, dass die Bediener gemäß den GMP-Anforderungen qualifiziert wurden.
5. Tool-Validierung: Zwei Wege mit dramatisch unterschiedlichen Belastungen
Die Wahl zwischen Einweg- und Mehrwegmopps führt zu einem sehr unterschiedlichen Validierungsaufwand.
Validierungsweg für Einwegmopps (vereinfacht):
- Materialqualifikation: Der Anbieter stellt Daten zur Partikelerzeugung (gemäß ISO 14644-14 oder gleichwertig), Matrizen zur chemischen Kompatibilität und Sterilitätszertifikate bereit (für gammabestrahlte Mopps: SAL 10⁻⁶-Validierungsberichte). Die Einrichtung überprüft Daten, qualifiziert Lieferanten gemäß Lieferantenqualitätsprogramm und genehmigt Material zur Verwendung.
- Überprüfung der Sterilität: Bei sterilen Einwegartikeln bestätigt die regelmäßige Sterilitätsprüfung eingehender Chargen (z. B. vierteljährlich oder gemäß risikobasiertem Probenahmeplan), dass der Sterilisationsprozess des Lieferanten unter Kontrolle bleibt. Analysezertifikate (CoA) dokumentieren die Ergebnisse von Sterilitätstests.
- Laufende Überwachung: Partikelvalidierungsstudien bestätigen, dass Einwegartikel während des Gebrauchs keine Partikelexkursionen verursachen. Da es sich bei jedem Mopp um einen Einwegmopp handelt, entfallen die Zykluszählung und die Validierung der Wiederaufbereitung.
Gesamter Validierungsaufwand: Materialqualifizierung + Sterilitätsüberprüfung + Studien zur Partikelverwendung.
Validierungspfad für wiederverwendbare Mopps (Komplex):
- Materialqualifikation: Wie Einwegartikel (Partikelerzeugung, chemische Kompatibilität)
- IQ/OQ/PQ waschen: Validierung des Waschprozesses (Installationsqualifizierung der Wäschereiausrüstung, Betriebsqualifizierung der Waschzyklusparameter, Leistungsqualifizierung zum Nachweis der Entfernung von Keimen und der Beibehaltung der Partikelleistung). Dies erfordert Belastungstests mit künstlich verschmutzten Mopps, Studien zur Biobelastungsrückgewinnung und Tests zur Partikelerzeugung vor und nach dem Waschen.
- Sterilisation IQ/OQ/PQ: Validieren Sie den Autoklavenzyklus oder den Gammabestrahlungsprozess, einschließlich biologischer Indikatorprüfungen, Temperaturkartierung und Überprüfung der Sterilitätstests.
- Grenzwerte für die Anzahl der Zyklen: Definieren Sie maximale Wasch-/Sterilisationszyklen vor der Moppablehnung (z. B. 50 Zyklen). Erfordert beschleunigte Alterungsstudien, die belegen, dass die Partikelbildung und die Absorptionsfähigkeit bis zum Ende der qualifizierten Lebensdauer akzeptabel bleiben.
- Sterilitätssicherung: Regelmäßige Sterilitätstests verarbeiteter Mopps, validierte Sterilhaltezeit nach der Sterilisation (z. B. 30 Tage in versiegelter Verpackung) und Verfallsdatum.
- Nachverfolgung der Wiederaufbereitung: Implementieren Sie ein System, um die Anzahl der einzelnen Moppzyklen zu verfolgen (z. B. RFID-Tags, Barcode-Etiketten), die Ausmusterung bei maximalen Zyklen durchzusetzen und Chargenaufzeichnungen zur Wiederaufbereitung gemäß GMP zu dokumentieren.
Gesamtvalidierungsaufwand: Materialqualifizierung + Wasch-IQ/OQ/PQ + Sterilisations-IQ/OQ/PQ + Zyklenzählungsstudien + Sterilitätssicherung + Validierung des Nachverfolgungssystems.
Fazit: Einweg-Moppsysteme reduzieren den Validierungsaufwand im Vergleich zu wiederverwendbaren Systemen um 60–70 %, eliminieren das mit der Wiederaufbereitung verbundene Kontaminationsrisiko und liefern eine vorhersehbare Partikelleistung. Für ISO 5-6-Hochrisikobereiche sprechen die Einsparungen bei der Validierung und die Vorteile der Kontaminationskontrolle deutlich für Einwegartikel.
DOS & Verbote beim Wischen in der Pharma-Cleanzone
DOS & Verbote beim Wischen in der Pharma-Cleanzone
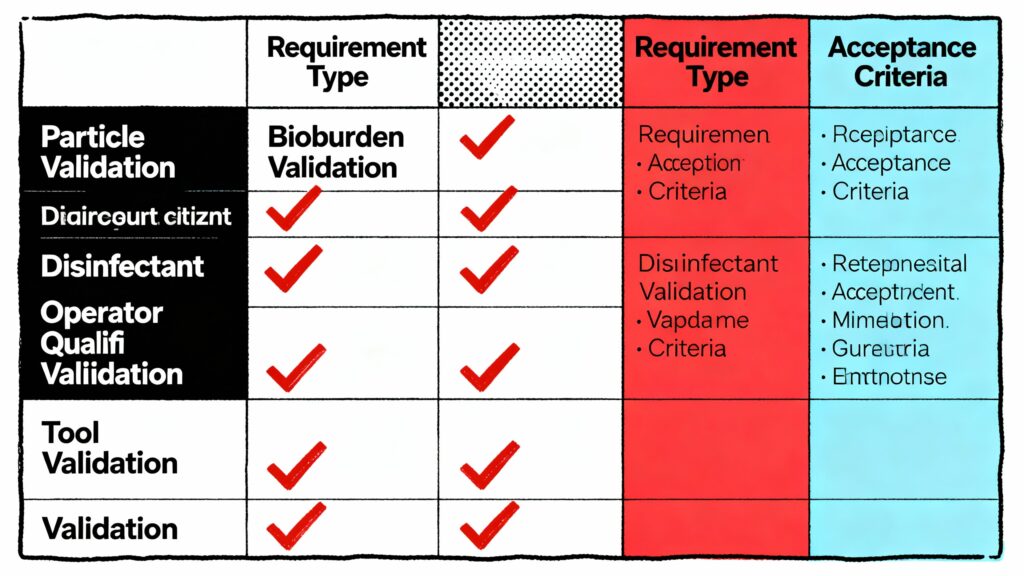
Abbildung 3: Validierungsanforderungsmatrix für Reinraum-Wisch-SOPs. Fünf Validierungskontrollpunkte (Partikel, Keimbelastung, Desinfektionsmittel, Bedienerqualifikation, Werkzeugvalidierung) mit expliziten Akzeptanzkriterien zeigen, dass die Reinigung die beabsichtigte Kontaminationskontrolle gemäß den Anforderungen von Anhang 1 und ISO 14644-5 erreicht.
Do’s (richtige Praktiken)
Verwenden Sie in Bereichen der Klasse A/B sterile, versiegelte Wischpads: Anhang 1 Abschnitt 4.34 erfordert sterile Desinfektionsmittel und Reinigungswerkzeuge in aseptischen Zonen. Verwenden Sie für Klasse A/B gammabestrahlte, sterile Einwegmopps (SAL 10⁻⁶), die in einer versiegelten Verpackung mit Strahlungsindikatoren geliefert werden, oder autoklavierbare wiederverwendbare Wischtücher, die unmittelbar vor der Verwendung mit validierter Sterilitätssicherung sterilisiert werden. Nicht sterile Mopps in aseptischen Bereichen stellen einen schwerwiegenden GMP-Verstoß dar.
Wischen Sie nach Möglichkeit immer in einer Richtung des Luftstroms: Der unidirektionale (laminare) Luftstrom in Klasse A drückt Partikel von kritischen Oberflächen weg. Durch das Wischen senkrecht zum Luftstrom entstehen Turbulenzen, die Partikel vorübergehend über dem freiliegenden Produkt schweben lassen können. Richten Sie die Wischbewegungen an der Luftstromrichtung aus, um Störungen zu minimieren und eine schnellere Partikelentfernung nach der Reinigung zu ermöglichen.
Verfolgen Sie die Menge des Desinfektionsmittels, das Verfallsdatum und die Kontaktzeit in Reinigungsprotokollen: Bei jedem Wischvorgang müssen die Chargennummer des Desinfektionsmittels, das Zubereitungsdatum (für in der Einrichtung hergestellte Lösungen), das Verfallsdatum/-uhrzeit und die erreichte Kontaktzeit dokumentiert werden. Diese Dokumentation liefert objektive Beweise dafür, dass validierte Reinigungsparameter eingehalten wurden – ohne sie können Sie bei Untersuchungen oder Audits die Einhaltung nicht nachweisen.
Implementieren und erzwingen Sie die Ein-Mopp-Regel pro Raum: Kreuzkontaminationen durch Mopps, die in mehreren Räumen ohne Wiederaufbereitung verwendet werden, sind eine der Hauptursachen für Umweltüberwachungsausflüge. Einweg-Mopps werden nach jedem Zimmer entsorgt. Wiederverwendbare Mopps müssen nach Bereichsklasse farblich gekennzeichnet sein (z. B. rot nur für Klasse A, gelb nur für Klasse B, blau nur für Klasse C) und nach der Verwendung in einem Raum zur validierten Wiederaufbereitung gesammelt werden. Tragen Sie niemals einen gebrauchten Mopp zwischen den Räumen.
Stellen Sie sicher, dass die Oberfläche für die angegebene Einwirkzeit feucht bleibt: Die Desinfektionswirksamkeit hängt davon ab, ob die vom Hersteller angegebene Kontaktzeit mit der sichtbar feuchten Oberfläche erreicht wird. Bei schnell verdunstenden Mitteln wie Isopropylalkohol kann eine erneute Anwendung oder ein höheres Anfangsvolumen erforderlich sein, um die Feuchtigkeit während der gesamten Kontaktzeit aufrechtzuerhalten. Bediener müssen die Nässe durchgehend visuell bestätigen. Wenn die Oberfläche vorzeitig trocknet, befeuchten Sie sie erneut und starten Sie den Kontaktzeit-Timer neu.
Absolvieren Sie die Qualifikation zum Ankleiden, bevor Sie klassifizierte Bereiche betreten: Alle Mitarbeiter, die ISO 5-8-Bereiche betreten, müssen die SOPs für den jeweiligen Standort erfüllen und die Qualifikationsbewertungen für das Ankleiden bestehen. Für Klasse A/B erfordert Anhang 1 eine jährliche Requalifizierung „mindestens einmal jährlich“ mit visueller und mikrobieller Beurteilung. Unqualifiziertes Personal birgt ein Kontaminationsrisiko, das durch Wischen nicht behoben werden kann.
Don’ts (verbotene Praktiken)
Benutzen Sie Mopps nicht zwischen ISO-Klassen oder angrenzenden Räumen wieder: Die Verwendung desselben Mopps in einer ISO-8-Verpackung und anschließender ISO-6-Füllunterstützung ohne Wiederaufbereitung führt zu einer Kreuzkontamination sauberer Bereiche mit Keimen und Partikeln aus minderwertigen Zonen. Diese Praxis verstößt gegen die Grundsätze der Kontaminationskontrolle und ist eine häufige Beobachtung der FDA/EMA. Für jede Bereichsklasse sind spezielle Wischmopps oder eine validierte Wiederaufbereitung zwischen den Verwendungen erforderlich.
Verwenden Sie keine Achter- oder Hin- und Her-Wischbewegungen: Abbildung 8 und Hin- und Herbewegungen verteilen die Kontamination neu, anstatt sie zu entfernen, verteilen das Desinfektionsmittel ungleichmäßig und erzeugen überlappende Nasszonen, in denen die Kontaktzeit unvorhersehbar ist. Führen Sie unidirektionale, gerade, parallele Striche mit 10–25 % Überlappung aus und heben Sie den Mopp am Ende jedes Strichs an, bevor Sie ihn neu positionieren.
Tauchen Sie den Mopp nach dem Bodenkontakt nicht zweimal in den Eimer: Sobald ein Mopp den Boden berührt, ist er kontaminiert. Das erneute Eintauchen in den Desinfektionseimer verunreinigt die Lösung und verringert die Wirksamkeit für nachfolgende Anwendungen. Verwenden Sie vorgetränkte Einwegmopps oder implementieren Sie validierte Eimersysteme mit einer Presse, die saubere Lösung von gebrauchter Lösung trennt. Wechseln Sie bei wiederverwendbaren Systemen die Desinfektionslösung nach jedem Raum oder bei sichtbarer Verschmutzung.
Verwenden Sie keine nicht validierten Waschverfahren für wiederverwendbare Mopps: Wenn Reinraum-Mopps ohne validierte Keimbelastungsentfernung, Prüfung der Partikelerzeugung und Zyklusparameterkontrollen (Waschtemperatur, Waschmitteltyp, Spülqualität) an eine gewerbliche Wäscherei geschickt werden, besteht die Gefahr, dass eine Kontamination in klassifizierte Bereiche gelangt. Wiederverwendbare Mopps erfordern eine IQ/OQ/PQ-qualifizierte Reinigung mit dokumentierten Chargenaufzeichnungen, Nachverfolgung der Zyklusanzahl und regelmäßiger Sterilitätsüberprüfung. Nicht validierte Wäsche ist unkontrolliert und nicht GMP-konform.
Überspringen Sie nicht die Rotation der Desinfektionsmittel und lassen Sie die regelmäßige Anwendung von Sporiziden nicht aus: Die Verwendung nur eines Desinfektionsmittels (z. B. ausschließlich 70 % IPA) ermöglicht die Anpassung der Flora und das Fortbestehen von Sporenbildnern. Anhang 1 fordert „mehr als ein Desinfektionsmittel“ mit „verschiedenen Wirkungsweisen“ und „periodischer Einsatz eines sporiziden Mittels“. Ein konformes Programm rotiert mindestens zwei Desinfektionsmittel (z. B. Alkohol + Oxidationsmittel) und umfasst monatliche oder vierteljährliche sporizide Zyklen (Natriumhypochlorit, Peressigsäure oder Wasserstoffperoxid in sporizider Konzentration). Durch die Überwachung der Empfindlichkeit von Umweltisolaten gegenüber Desinfektionsmitteln wird die Wirksamkeit des Programms überprüft.
Während aktiver aseptischer Vorgänge in Klasse A nicht wischen: Das Wischen erzeugt vorübergehende Partikelstörungen und erfordert die Anwesenheit/Bewegung des Bedieners, die den laminaren Luftstrom über freiliegenden sterilen Produkten stören kann. Planen Sie das Wischen während der Ausfallzeit der Linie, zwischen Chargen oder während validierter „Ruhe“-Qualifizierungszeiträume. Das Wischen während aktiver Abfüllvorgänge der Klasse A ist gemäß Anhang 1 der Kontaminationskontrollerwartungen verboten.
Überschreiten Sie nicht die maximale Zykluszahl für wiederverwendbare Mopps: Mopps zersetzen sich bei wiederholtem Waschen und Sterilisieren. Stofffasern fransen aus, versiegelte Kanten lösen sich auf und die Partikelbildung nimmt zu. Die Validierung definiert maximal qualifizierte Zyklen (z. B. 50–100 Zyklen). Das Überschreiten dieses Grenzwerts ohne erneute Validierung bedeutet, dass der Mopp nicht mehr den Spezifikationen entspricht. Implementieren Sie Nachverfolgungssysteme (Barcodes, RFID-Tags), um Zyklusbeschränkungen durchzusetzen und Mopps am Ende ihrer qualifizierten Lebensdauer auszumustern.
Führen Sie kein unsteriles Desinfektionsmittel in Bereiche der Klasse A/B ein: Anhang 1 Abschnitt 4.34 schreibt vor, dass Desinfektionsmittel der Güteklasse A/B steril sein müssen. In der Einrichtung vorbereitete Verdünnungen müssen aseptisch unter Verwendung von sterilem Wasser hergestellt, auf Sterilität validiert und mit Haltezeiten (typischerweise 24 Stunden) versehen werden. Im Handel erhältliche sterile Desinfektionsmittel müssen vom Hersteller zertifiziert sein und über Analysezertifikate verfügen. Die Verwendung nicht steriler Desinfektionsmittel in aseptischen Zonen führt zu lebensfähiger Keimbelastung, die das gesamte Kontaminationskontrollprogramm untergräbt.
Versteckte Kreuzkontaminationsrisiken (Awareness Points)
Betreiber können durch Praktiken, die vernünftig erscheinen, aber gegen die GMP-Grundsätze verstoßen, unwissentlich eine Kontamination einführen:
- Aufbewahrung nasser wiederverwendbarer Mopps: Mops, die zwischen den Anwendungen feucht gelagert werden, werden zu Brutkästen für die biologische Belastung. Alle wiederverwendbaren Mopps müssen sofort nach Gebrauch gewaschen, sterilisiert und verpackt werden und dürfen nicht zum „Trocknen“ zur späteren Wiederverwendung aufgehängt werden.
- Verwendung von Tüchern auf Zellulosebasis mit QAC-Desinfektionsmitteln: Quartäre Ammoniumverbindungen adsorbieren an Zellulosefasern und verlieren ihre antimikrobielle Aktivität. Verwenden Sie Polyester- oder andere synthetische, fusselarme Tücher/Mopps mit QACs.
- Wischen unmittelbar nach dem HEPA-Filterwechsel ohne Überprüfung des Luftstroms: Durch Filterwechsel können Partikel entstehen. Überprüfen Sie, ob der Raum wieder klassifiziert ist (Überwachung der Partikelanzahl), bevor Sie mit dem routinemäßigen Wischen fortfahren, um die Ausbreitung von Installationsrückständen zu vermeiden.
- Sichtbare Moppschäden werden ignoriert: Zerrissene Moppköpfe, ausgefranste Kanten oder beschädigte Sterilverpackungen gefährden die Partikelkontrolle und die Sterilitätssicherheit. Beschädigte Mopps sofort aussortieren und als Abweichung dokumentieren.
Durch die Kodifizierung dieser Praktiken in SOP-Schulungen und Kompetenzbewertungen reduzieren Einrichtungen die Ausführungsvariabilität und verhindern wiederkehrende Kontaminationsereignisse, die auf Bedienerfehler zurückzuführen sind.
Empfohlene Tools zum Schreiben einer SOP (GMP-konform)

Abbildung 4: Wichtige Gebote und Verbote beim Wischen in pharmazeutischen Reinräumen. Links: Richtige Praktiken (unidirektionale Bewegungen, ein Wischmopp pro Raum, Überprüfung der Kontaktzeit). Rechts: Verbotene Praktiken, die Beobachtungen der FDA und Abweichungen von der Umweltüberwachung auslösen (Abbildung 8-Antrag, sortenübergreifende Wiederverwendung, doppeltes Eintauchen).
Sobald Sie die SOP-Struktur, den Arbeitsablauf und die Validierungsanforderungen definiert haben, wird die Werkzeugauswahl zur praktischen Entscheidung, die darüber entscheidet, ob Ihre SOP ausführbar und vertretbar ist. Die „zugelassenen Werkzeuge & Der Abschnitt „Materialien“ Ihrer SOP sollte auf Produkte verweisen, die den gesetzlichen Erwartungen entsprechen, mit Validierungsunterstützungspaketen ausgestattet sind und der ISO-Klassifizierung und dem Betriebsmodell Ihrer Einrichtung entsprechen.
Werkzeugauswahlkriterien für SOP-referenzierte Mopps
Sterilitätspfad für Grad A/B: Für aseptische Bereiche müssen Mopps vor der Verwendung steril sein (Anforderung in Anhang 1). Dem begegnen zwei Wege:
- Gammabestrahlte, sterile Einwegmopps: Beim Hersteller vorsterilisiert (SAL 10⁻⁶), in validierter Sterilverpackung versiegelt, Chargenrückverfolgbarkeit mit Sterilitätszertifikaten. Kein Wiederaufbereitungsaufwand. Ideal für kritische ISO 5-6-Zonen, in denen die Einfachheit der Validierung und die Reduzierung des Kontaminationsrisikos höhere Stückkosten rechtfertigen.
- Autoklavierbare wiederverwendbare Mopps: Moppköpfe aus Polyester oder Polypropylen, die Autoklavenzyklen bei 121 °C standhalten, ohne zu schmelzen oder die Partikelbildung zu erhöhen. Erfordern eine Sterilisation vor Ort, eine validierte Wiederaufbereitung, eine Nachverfolgung der Zyklusanzahl und eine Sterilitätsüberprüfung. Geeignet für Einrichtungen mit qualifizierter Wäsche-/Sterilisationsinfrastruktur und der Bereitschaft, die Wiederaufbereitungsvalidierung durchzuführen.
Flusenarme Spezifikation für Klasse C/D: Für Stützbereiche (ISO 7–8) ist möglicherweise keine Sterilität erforderlich, eine geringe Partikelbildung ist jedoch zwingend erforderlich. Suchen Sie nach Mopps mit:
- Heißversiegelte oder ultraschallverschweißte Kanten (keine abgeschnittenen/ausgefransten Enden)
- Konstruktion aus Endlosfilament-Polyester oder dicht gestrickter Mikrofaser
- Daten zur Partikelerzeugung: <100 Partikel ≥0,5 µm pro Hub (ISO 14644-14-Methodik)
- Chemische Kompatibilität mit der Rotation der Desinfektionsmittel in der Einrichtung (IPA, Peroxid, Quats, Bleichmittel)
Validierungsdokumentationspaket: SOP-konforme Tools müssen mit vom Anbieter bereitgestellter Validierungsunterstützung ausgestattet sein:
- Testberichte zur Partikelerzeugung (ISO 14644-14 oder gleichwertige Tests Dritter)
- Chemische Kompatibilitätsmatrizen, die die Materialstabilität über Desinfektionsmittel hinweg zeigen
- Sterilitätszertifikate (für sterile Einwegartikel): Gammadosis-Validierung, SAL 10⁻⁶-Dokumentation, Analysezertifikat pro Charge
- Sicherheitsdatenblätter (MSDS) und Konformitätszertifikate
- Daten zu extrahierbaren/auslaugbaren Stoffen (für Anwendungen mit direktem Produktkontakt)
Ohne diese Dokumentation verweist Ihre SOP auf unqualifizierte Tools, die nicht validiert werden können – eine Lücke, die Prüfer erkennen werden.
MIDPOSI Reinraum-Mopp-Produktlinie (SOP-fähige Lösungen)
MIDPOSI bietet ein komplettes Moppsystem-Portfolio, das darauf ausgelegt ist, pharmazeutische SOP-Anforderungen in allen ISO-Klassifizierungen zu unterstützen:
Für aseptische Bereiche der ISO-Klasse 5–6 (Klasse A/B).:
- Gamma-steriles Einweg-Moppsystem: Vorsterilisierte Polyester-Moppköpfe (SAL 10⁻⁶), einzeln versiegelt mit Strahlungsindikatoren, geliefert mit Validierungspaket einschließlich Sterilitätszertifikaten, Daten zur Partikelerzeugung (<50 Partikel ≥0,5 µm pro Hub) und chemische Kompatibilität mit IPA, Peroxid und sporiziden Wirkstoffen. Der Mopprahmen aus Edelstahl und der autoklavierbare Aluminiumstiel runden das System ab. Einwegmopps machen die Validierung der Wiederaufbereitung überflüssig und stellen sicher, dass kein Risiko einer Kreuzkontamination besteht.
- Erfahren Sie mehr über Einweg-Reinraummopps – Beinhaltet einen TCO-Vergleich, der zeigt, dass Einwegartikel bei ISO 5-6-Anwendungen mit hohem Risiko geringere Gesamtkosten verursachen als Mehrwegartikel.
Für Unterstützungsbereiche der ISO-Klasse 7–8 (Klasse C/D).:
- Autoklavierbares, fusselarmes, wiederverwendbares Moppsystem: Moppköpfe aus Endlosfilament-Polyester mit ultraschallversiegelten Kanten, qualifiziert für mehr als 100 Autoklavenzyklen bei 121 °C ohne Erhöhung der Partikelerzeugung. Lieferung mit Validierungsdatenpaket zur Unterstützung der SOP-Materialqualifizierung. Farblich gekennzeichnete Wischmoppköpfe (blau/gelb/rot) verhindern eine kreuzweise Verwendung. Rahmen und Griff aus Edelstahl, zusammen mit den Moppköpfen autoklavierbar.
- Sehen Sie sich den vollständigen Reinraum-Mopp-Leitfaden an – grundlegende Referenz, die den Moppaufbau, die Materialauswahl und die Kompatibilität der Systemkomponenten erläutert.
Für hochvolumige Operationen:
- Vorgetränktes Einweg-Moppsystem: Mopps, vorbenetzt mit validiertem Desinfektionsmittel in kontrollierter Konzentration, einzeln versiegelt, wodurch Schwankungen bei der Verdünnung vor Ort und Spekulationen über die Kontaktzeit vermieden werden. Ideal für Einrichtungen, die die Vorbereitungsschritte des Bedieners reduzieren und die SOP-Ausführung vereinfachen möchten. Erhältlich in IPA 70 %, Wasserstoffperoxidformulierungen und QAC-Mischungen.
Verfügbarkeit des Validierungspakets: Alle MIDPOSI-Moppsysteme umfassen Testberichte zur Partikelerzeugung, Matrizen zur chemischen Kompatibilität und (für sterile Produkte) Sterilitätszertifikate pro Charge. Benutzerdefinierte Validierungsprotokolle sind für standortspezifische Desinfektionsmittelkombinationen, Partikelüberwachung unter kundenspezifischen Bedingungen und Keimbelastungstests verfügbar. Fordern Sie ein Validierungspaket mit Produktmustern an, um die SOP-Qualifizierung zu beschleunigen.
Aufruf zum Handeln: Für die Erstellung einer konformen Reinraum-Wisch-SOP sind Werkzeuge erforderlich, die Anhang 1, ISO 14644 und die FDA-Anforderungen erfüllen. Fordern Sie MIDPOSI-Produktmuster, Validierungsdatenpakete und SOP-Beratung an, um sicherzustellen, dass Ihre Werkzeugauswahl vertretbare, ausführbare Verfahren unterstützt. Kontaktieren Sie uns für SOP-spezifische Empfehlungen, die auf Ihre ISO-Klassifizierung und Ihr Anlagenbetriebsmodell zugeschnitten sind.

FAQ – SOP-Fragen zum Wischen im Reinraum
F: Wie oft müssen Desinfektionsmittel gemäß Anhang 1 gewechselt werden?
A: Anhang 1 Abschnitt 4.33 erfordert „mehr als ein Desinfektionsmittel“ mit „verschiedenen Wirkungsweisen“ und „die regelmäßige Verwendung eines sporiziden Mittels“, schreibt jedoch keine bestimmte Rotationshäufigkeit vor. Best Practice: Wechseln Sie mindestens zwei Desinfektionsmittel (z. B. Alkohol + Oxidationsmittel) wöchentlich oder zweiwöchentlich, wobei ein sporizides Mittel (Natriumhypochlorit, Peressigsäure oder hochkonzentriertes Wasserstoffperoxid) monatlich oder vierteljährlich angewendet wird, abhängig von den Trends bei der Überwachung der Keimbelastung. Die Wirksamkeit muss regelmäßig überwacht werden, um Veränderungen oder Resistenzen der Flora zu erkennen. Dokumentieren Sie den Rotationsplan in der SOP und verknüpfen Sie die Häufigkeit mit Umweltüberwachungsdaten, die eine nachhaltige Kontrolle der Keimbelastung zeigen.
F: Welche Kontaktzeit ist für 70 % Isopropylalkohol (IPA) erforderlich?
A: Die Kontaktzeit für IPA hängt vom Zielorganismus und der Produktformulierung ab. Die meisten IPA-Produkte erreichen eine bakterizide Aktivität in 15–30 Sekunden, für die viruzide Aktivität kann jedoch ein Nasskontakt von 1–2 Minuten erforderlich sein. Die Herausforderung bei IPA ist die schnelle Verdunstung – Oberflächen trocknen oft innerhalb von 30–60 Sekunden, bevor die viruzide Kontaktzeit erreicht wird. SOPs müssen Folgendes angeben: (1) die angegebene Kontaktzeit gemäß der Gebrauchsanweisung (IFU) des Herstellers oder der Anlagenvalidierung, (2) ein Wiederbefeuchtungsprotokoll, wenn die Oberfläche vorzeitig trocknet, und (3) eine Überprüfung durch den Bediener, dass die Nässe über die gesamte Kontaktdauer aufrechterhalten wurde. Bei Organismen, die einen längeren Kontakt erfordern (z. B. bestimmte unbehüllte Viren), sollten Sie Wasserstoffperoxid oder andere Mittel mit langsamerer Verdunstung und längerer Nassverweildauer in Betracht ziehen.
F: Erfordern Einweg-Mopps die gleiche Validierung wie wiederverwendbare Mops?
A: Nein – Einweg- und Mehrwegmopps folgen völlig unterschiedlichen Validierungspfaden. Einweg-Mopps erfordern: (1) Materialqualifizierung (vom Hersteller bereitgestellte Daten zur Partikelerzeugung, Matrizen zur chemischen Kompatibilität), (2) Sterilitätsüberprüfung für sterile Einwegartikel (Analysezertifikate, regelmäßige Sterilitätstests eingehender Chargen) und (3) Partikelverwendungsstudien, die bestätigen, dass beim Wischen keine Abweichungen von der Klassifizierung festgestellt wurden. Die Wiederaufbereitungsvalidierung (Wasch-IQ/OQ/PQ, Sterilisations-IQ/OQ/PQ, Zyklenzahlgrenzen, Nachverfolgungssysteme) entfällt, da Mopps nach einmaligem Gebrauch entsorgt werden. Wiederverwendbare Mopps erfordern alle oben genannten Punkte sowie eine umfassende Validierung der Wiederaufbereitung, die Nachverfolgung der Zyklusanzahl und eine regelmäßige Neuqualifizierung, wenn sich die Materialien verschlechtern. Für ISO 5–6-Hochrisikobereiche reduzieren Einwegartikel den Validierungsaufwand um 60–70 % und eliminieren das Risiko einer Kreuzkontamination durch unzureichende Wiederaufbereitung.
F: Kann derselbe Mopp in mehreren Reinraumklassen verwendet werden (z. B. Klasse C und Klasse B)?
A: Nein – die Verwendung eines einzelnen Mopps für mehrere ISO-Qualitäten oder EU-GMP-Qualitäten ohne validierte Wiederaufbereitung zwischen den Verwendungen birgt das Risiko einer Kreuzkontamination und verstößt gegen die Grundsätze der Kontaminationskontrolle. Sobald ein Mopp einen Bereich mit geringerer Qualität (z. B. Klasse C) berührt, trägt er Keime und Partikel aus dieser Umgebung mit sich. Wenn es ohne Sterilisation in einen Bereich höherer Güteklasse (z. B. Güteklasse B) gebracht wird, führt dies zu einer Kontamination, die die höhere Güteklasse nicht tolerieren kann. Best Practice: Setzen Sie strikte Ein-Mopp-Regeln pro Klasse mit farbcodierten Systemen um (z. B. Rot nur für Klasse A, Gelb nur für Klasse B, Blau nur für Klasse C). Einwegartikel nach einmaligem Gebrauch entsorgen. Sammeln Sie wiederverwendbare Produkte nach jedem Gebrauch zur validierten Reinigung und Sterilisation, wobei eine sortenspezifische Trennung eine versehentliche Kreuzverwendung verhindert.
F: Wie dokumentiere ich die Qualifikation des Bedieners für das Wischen im Reinraum?
A: Die Dokumentation der Bedienerqualifikation muss die Kompetenz durch Schulung, Bewertung und regelmäßige Neuqualifizierung nachweisen. Die Mindestdokumentation umfasst: (1) Schulungsunterlagen: Die Bediener absolvieren eine praktische SOP-Schulung, die sich mit dem Anziehen, der Handhabung des Mopps, der unidirektionalen Technik, der Überprüfung der Kontaktzeit und den Dokumentationsanforderungen befasst. Die Schulungsabmeldung umfasst das Datum, den Namen des Trainers und die Bestätigung des Bedieners. (2) Kompetenzbewertung: beobachtete Leistungsbewertung, bei der ein qualifizierter Trainer den Bediener bei der Ausführung des gesamten Wischzyklus beobachtet und anhand der Checkliste punktet (unidirektionale Wischbewegungen, ordnungsgemäße Überlappung, erreichte Kontaktzeit, Einhaltung der Regel „Ein Wischvorgang pro Raum“, vollständige Dokumentation). Es müssen Pass/Fail-Kriterien definiert werden; „Passieren“ Sie nur Bediener, die zur unbeaufsichtigten Reinigung berechtigt sind. (3) Jährliche Requalifizierung: Anhang 1 verlangt „mindestens jährlich“ für Personal der Besoldungsgruppe A/B. Die Requalifizierung umfasst eine schriftliche Bewertung (SOP-Kenntnisse, Desinfektionsmittelspezifikationen, Abweichungsberichte) und eine beobachtete erneute Leistung. (4) Durch Abweichungen ausgelöste Umschulung: Jeder Bediener, der mit einer EM-Abweichung oder einer SOP-Abweichung in Verbindung steht, durchläuft vor der Wiederaufnahme seiner Tätigkeit eine sofortige Umschulung und Neuqualifizierung. (5) Optional: Videoaufzeichnung von Qualifizierungssitzungen für objektive Nachweise und Schulungsmaterial.
F: Was sind die größten SOP-Fehler, die FDA-483-Beobachtungen auslösen?
A: Warnschreiben der FDA von 2023 bis 2025 offenbaren wiederkehrende SOP-Mängel: (1) Fehlende Kontaktzeitangaben: In den SOPs heißt es: „Desinfektionsmittel auftragen und abwischen“, ohne eine Mindestverweildauer beim Nasswaschen oder eine Überprüfungsmethode festzulegen, sodass keine Grundlage für die Behauptung besteht, dass eine Desinfektion stattgefunden hat. (2) Keine Validierungskontrollpunkte: Den SOPs fehlen messbare Akzeptanzkriterien für die Reinigungswirksamkeit (Reduzierung der Keimbelastung, Partikelkontrolle), was eine Überprüfung unmöglich macht. (3) Unzureichende Protokolle zur Werkzeugsterilisation: Das Versäumnis, Mopps/Geräte zu sterilisieren, bevor sie in ISO-5-Bereiche eingeführt werden, oder die Verwendung nicht validierter Waschverfahren für wiederverwendbare Werkzeuge. (4) Fehlende Logik zur Bereichsklassifizierung: Allgemeine SOPs, die das gleiche Verfahren auf ISO 5, 7 und 8 anwenden, ohne qualitätsspezifische Werkzeuganforderungen oder Überprüfungshäufigkeit. (5) Keine Rotation von Desinfektionsmitteln oder Verwendung von Sporiziden: Abhängigkeit von einem einzigen Desinfektionsmittel (oft IPA allein) ohne Vielfalt der Wirkungsweise oder periodische sporizide Zyklen. (6) Fehlende Dokumentation zur Bedienerqualifikation: Keine Kompetenzbewertungen, keine jährliche Neuqualifizierung für Personal der Besoldungsgruppe A/B oder Umschulung nach Abweichungen. Um diese Fehler zu verhindern, ist ein strukturierter SOP-Entwurf mit expliziten Validierungskontrollpunkten, behördlichen Zitaten, die jede Anforderung rechtfertigen, und Bedienerschulungen erforderlich, bei denen die Compliance-Grundsätze im Vordergrund stehen.
F: Sollte ich für jede ISO-Klassifizierung separate SOPs schreiben oder eine SOP, die alle Bereiche abdeckt?
A: Best Practice: eine Master-SOP mit klassifizierungsspezifischen Abschnitten. Eine einzige SOP, die alle ISO 5-8-Bereiche abdeckt, gewährleistet Konsistenz in Struktur, Definitionen und übergreifenden Prinzipien (unidirektionale Technik, Kontaktzeitanforderungen, Dokumentationsstandards) und integriert gleichzeitig sortenspezifische Werkzeuganforderungen, Desinfektionsmittelspezifikationen und Überprüfungshäufigkeit als Unterabschnitte oder Anhänge. Beispiel: Abschnitt 4.2 „Zugelassene Werkzeuge nach Bereichsklasse“ listet sterile gammabestrahlte Mopps für Klasse A/B, autoklavierbare fusselarme Mopps für Klasse C und unsterile fusselarme Mopps für Klasse D auf. Abschnitt 6.3 „Überprüfungshäufigkeit“ legt tägliche EM-Probenahmen für Klasse A/B, wöchentlich für Klasse C und monatlich für Klasse D fest. Dieser Ansatz verhindert Doppelarbeit, reduziert den Wartungsaufwand (einzige SOP, die aktualisiert wird, wenn sich Vorschriften ändern) und stellt sicher, dass die Bediener verstehen Kontaminationskontrolllogik in der gesamten Anlage. Alternativ können für Einrichtungen mit sehr unterschiedlichen Betriebsmodellen (z. B. Großpackungen der Güteklasse C vs. Kleinserien-Abfüllung der Güteklasse A) separate SOPs gerechtfertigt sein – stellen Sie jedoch Querverweise und eine Ausrichtung auf die Kernprinzipien sicher.









