In der pharmazeutischen Herstellung stellen Fehler bei der Kontaminationskontrolle, die auf Reinigungswerkzeuge zurückzuführen sind, eine der am besten vermeidbaren Ursachen für Abweichungen bei der Umweltüberwachung und behördlichen Beobachtungen dar. In einem Warnschreiben der FDA aus dem Jahr 2025 wurden ausdrücklich „unsterile Tücher im aseptischen ISO-5-Verarbeitungsbereich“ und „das Versäumnis, ein angemessenes System zur Reinigung und Desinfektion einzurichten“ als CGMP-Verstöße genannt, die die Chargensterilität gefährden. Die Hauptursache: wiederverwendbare Reinigungswerkzeuge, die Keime und Partikelkontaminationen aus der vorherigen Verwendung tragen, unzureichend gewaschen und ohne validierte Wiederaufbereitung in aseptische Zonen verbracht werden.
Einweg-Reinraummopps eliminieren diesen Kontaminationspfad vollständig. Jeder Wischzyklus beginnt mit einem frischen, validierten Wischpad – kein Kreuzkontaminationsrisiko aus vorherigen Räumen, keine Wäscherückstände, kein Validierungsaufwand für die Wiederaufbereitung. Für Einrichtungen, die nach ISO 14644-1 und dem überarbeiteten EU-GMP-Anhang 1 (gültig ab August 2023) arbeiten, bieten Einwegmopps keine Kreuzkontamination, eine vorhersehbare Partikelleistung und eine erheblich vereinfachte Reinigungsvalidierungsdokumentation. Die regulatorische Landschaft und die Gesamtkostenökonomie begünstigen zunehmend Einweg-Reinigungswerkzeuge in der aseptischen Fertigung, in Abfülllinien und in Bereichen mit hohem Risiko für die pharmazeutische Produktion.
Das heißt nicht: „Einwegartikel sind immer besser.“ Wiederverwendbare Moppsysteme bleiben in ISO 8-Unterstützungsbereichen, in der Großserienfertigung mit validierter interner Wäscherei und in Einrichtungen mit robuster Wiederaufbereitungsinfrastruktur kosteneffektiv. Wenn die Kontaminationskontrolle jedoch streng ist (aseptische Kerne nach ISO 5–7), es häufig zu Fehlern bei der Umgebungsüberwachung kommt oder die Validierungsressourcen begrenzt sind, bieten Einweg-Reinraummopps trotz höherem Stückpreis eine hervorragende Kontaminationskontrolle und niedrigere Gesamtbetriebskosten.
Dieser Leitfaden untersucht die regulatorischen Treiber für die Einführung von Einwegmopps, quantifiziert die wichtigsten Vorteile (keine Kreuzkontamination, vorhersehbare Leistung, reduzierter Validierungsaufwand), vergleicht die Gesamtbetriebskosten mit wiederverwendbaren Systemen, bildet Anwendungsfälle anhand der ISO-Klassifizierung ab und empfiehlt MIDPOSI-Einwegmoppprodukte, die auf die Anforderungen der Einrichtung abgestimmt sind. Am Ende verfügen Sie über einen klaren Entscheidungsrahmen dafür, wann Einweg-Reinraummopps ihre Kosten durch reduziertes Kontaminationsrisiko, vereinfachte Compliance und vermiedene EM-Untersuchungszyklen rechtfertigen.

Warum Einwegmopps in der Pharmabranche auf dem Vormarsch sind
Die Verlagerung hin zu Einweg-Reinraummopps ist kein durch das Marketing der Anbieter getriebener Trend – sie spiegelt grundlegende Veränderungen in den regulatorischen Erwartungen, messbare Versäumnisse bei der Kontaminationskontrolle, die auf wiederverwendbare Werkzeuge zurückzuführen sind, und die Wirtschaftlichkeit der Umweltüberwachung in der modernen pharmazeutischen Produktion wider.
Hauptvorteile von Einweg-Reinraummopps (keine Kreuzkontamination)
Einweg-Reinraummopps bieten vier messbare Vorteile gegenüber wiederverwendbaren Systemen: garantiert keine Kreuzkontamination, vorhersehbare Partikel- und Mikrobenleistung, geringerer Validierungs- und Dokumentationsaufwand und verbesserte Arbeitseffizienz. Diese Vorteile verstärken sich bei pharmazeutischen Anwendungen mit hohem Risiko, bei denen die Kontaminationskontrollmargen knapp sind und die behördliche Kontrolle intensiv ist.
Garantiert keine Kreuzkontamination
Kreuzkontamination – die Übertragung von Verunreinigungen von einem Standort, Produkt oder Betrieb zu einem anderen – ist das grundlegende Risiko, das wiederverwendbare Reinigungswerkzeuge mit sich bringen. Bei jedem wiederverwendbaren Wischpad sammeln sich während des Gebrauchs Keime, Partikel und chemische Rückstände an. Beim Waschen werden diese Verunreinigungen reduziert, es wird jedoch selten Sterilität oder eine vollständige Entfernung der Rückstände erreicht. Wenn dieser Mopp wieder in einen klassifizierten Bereich gelangt, trägt er Verunreinigungen aus früheren Umgebungen mit sich.
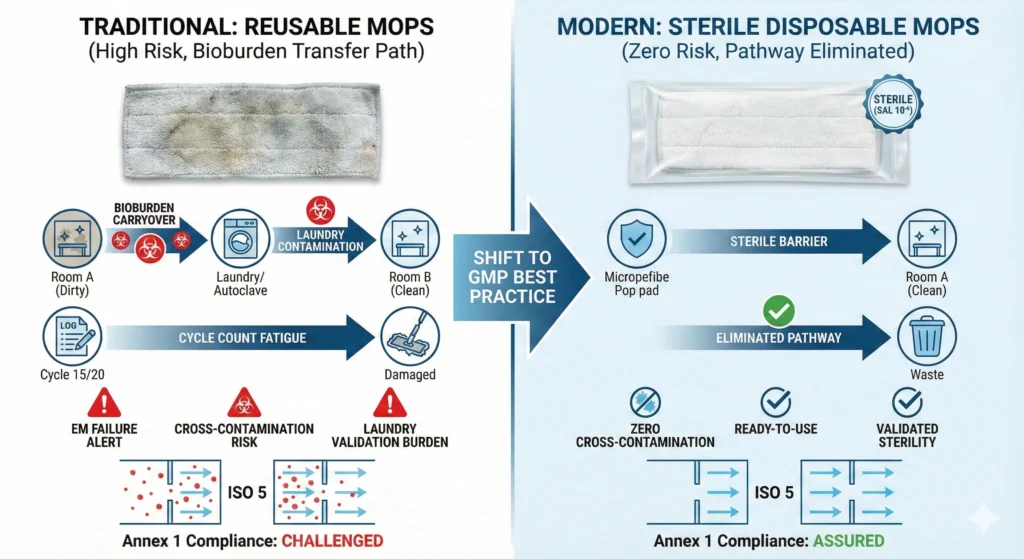
Einweg-Reinraummopps beseitigen diesen Weg:
- Bei jedem Zyklus frisch wischen: Jeder Wischvorgang beginnt mit der Entnahme eines neuen Wischpads direkt aus der validierten Sterilverpackung (für gammabestrahlte Einwegartikel) oder aus der versiegelten, fusselarmen Verpackung (für nicht sterile Einwegartikel). Keine Übertragung von Keimen aus vorherigen Räumen, keine Ansammlung von Partikeln aus vorherigen Wischgängen, keine Waschmittelrückstände.
- Keine Übertragung von Kontaminationen von Raum zu Raum: Einrichtungen, die wiederverwendbare Mopps verwenden, verfügen in der Regel über separate Lagerbestände für verschiedene ISO-Klassen (ISO 5-Mops werden nie in ISO 8-Bereichen verwendet). Selbst bei perfekten Trennungsprotokollen besteht bei Etikettierungsfehlern und Bestandsengpässen das Risiko einer gegenseitigen Zuordnung. Einwegsysteme beseitigen diesen Fehlermodus – Mopps können nicht wiederverwendet werden, sodass eine bereichsübergreifende Kontamination ausgeschlossen ist.
- Keine wäschebedingte Kontamination: Wiederverwendbare Mopps durchlaufen Wäschereien, in denen die Möglichkeit einer Kreuzkontamination reichlich vorhanden ist: Waschen mit gemischten Ladungen, unzureichende Spülzyklen, gemeinsame Ausrüstung für Reinraumkittel und allgemeine Wäsche der Einrichtung. Einwegmopps umgehen das gesamte Wäschereisystem und beseitigen so einen mehrstufigen Kontaminationsweg.
Vereinfachung der Validierung durch Eliminierung von Wiederverarbeitungsvariablen
Reinigungsvalidierungsprotokolle für wiederverwendbare Werkzeuge müssen Worst-Case-Wiederaufbereitungsszenarien berücksichtigen: maximale Zyklenzahl (Ende der qualifizierten Lebensdauer), maximale Keimbelastung, minimale Wascheffizienz. Jede Variable bringt Unsicherheit in die Leistung der Kontaminationskontrolle mit sich.
Einwegmopps weisen keine Variablen für die Wiederaufbereitung auf. Materialqualifikationstests (Partikelerzeugung, chemische Kompatibilität, Basislinie der Keimzahl) validieren den Mopp in seinem Zustand, in dem er ihn erhalten hat und nie verwendet wurde – also in demselben Zustand, in dem er sich auch während des tatsächlichen Gebrauchs befindet. Dadurch entfällt die Komplexität der Validierung:
- Keine Zyklenzahl-Degradationsstudien: Die Validierung wiederverwendbarer Mopps erfordert Tests an mehreren Lebenszykluspunkten (neu, 25 Zyklen, 50 Zyklen, 100 Zyklen), um nachzuweisen, dass die Partikelerzeugung innerhalb der Akzeptanzkriterien bleibt. Bei der Einwegvalidierung wird nur die einzelne „neue“ Bedingung getestet.
- Keine Validierung der Waschwirksamkeit: Einrichtungen, die wiederverwendbare Mopps verwenden, müssen Waschzyklen, Waschmittelkonzentrationen, Reduzierung der Keimbelastung und Rückstandsentfernung validieren. Bei Einwegsystemen ist kein Waschschritt zu validieren.
- Keine Fehlermodi bei der Wiederaufbereitung: Kreuzkontamination beim Wäschewaschen, Fehler bei der Sterilisation im Autoklaven, Verfolgungsfehler bei der Zuordnung von Mopps zu falschen Bereichen – keine dieser Fehlerursachen gibt es, wenn es sich um Einwegwerkzeuge handelt.
Vorhersehbares Teilchen & Mikrobielle Leistung
Umweltüberwachungsprogramme sind auf stabile, vorhersehbare Kontaminationsquellen angewiesen, um echte Kontaminationsereignisse zu erkennen. Wenn Reinigungswerkzeuge im Laufe ihres Lebenszyklus unterschiedliche Partikelzahlen und biologische Belastungen abgeben, führen sie zu Störungen in den EM-Daten, die echte Kontaminationssignale verschleiern.
Stabile Partikelerzeugung (<100 Partikel/m²)
Einweg-Polyestermopps mit versiegelten Kanten erzeugen in allen Einheiten konsistente Partikelzahlen:
- Typische Leistung: <50–100 Partikel ≥0,5 µm pro Quadratmeter werden für validierte Einwegartikel in pharmazeutischer Qualität gewischt
- Keine Verschlechterung im Laufe der Zeit: Jeder Einwegmopp hat die gleiche Leistung – keine Kantentrennung, kein Faserbruch, keine im Autoklaven verursachten Dimensionsänderungen. Die Partikelerzeugung auf Mopp Nr. 1 entspricht Mopp Nr. 1.000.
- Vereinfachte EM-Trendanalyse: Wenn die Partikelanzahl während Reinigungsvorgängen stabil bleibt, können Umweltüberwachungsteams Partikelspitzen sicher auf Kontaminationsereignisse zurückführen (Versagen der Personalkleidung, Kontamination beim Materialtransfer, Fehlfunktionen der Ausrüstung) und nicht auf eine Verschlechterung der Reinigungswerkzeuge.
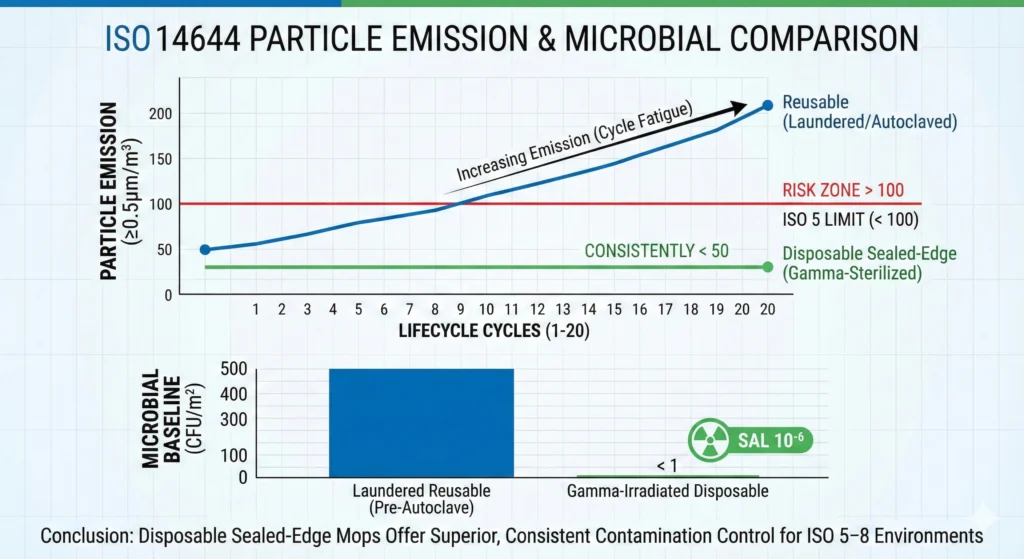
Im Gegensatz dazu erhöhen wiederverwendbare Mopps die Partikelerzeugung während ihrer gesamten Nutzungsdauer. Ein wiederverwendbarer Wischmopp aus Polyester mit versiegelten Kanten kann im Neuzustand bei 50 Partikeln/m² beginnen, bei Zyklus 50 auf 100 Partikel/m² ansteigen und gegen Ende der qualifizierten Lebensdauer (Zyklus 100–150) 200–300 Partikel/m² erreichen. Dieser 4- bis 6-fache Anstieg der Partikelerzeugung führt zu einem zeitabhängigen Kontaminationsbeitrag, der die Interpretation der EM-Daten erschwert.
Vorhersagbare Keimbelastung (Gamma-sterile Einwegartikel)
Gammabestrahlte Einwegmopps bieten einen Sterilitätssicherungsgrad (SAL) von 10⁻⁶ – eine Wahrscheinlichkeit von eins zu einer Million für nicht sterile Einheiten. Mit dieser Endsterilisationsmethode wird eine vollständige Eliminierung der Keimbelastung erreicht:
- Keine lebensfähigen Mikroorganismen: Gammabestrahlung (typischerweise 25–50 kGy Dosis) inaktiviert alle bakteriellen vegetativen Zellen, Sporen, Pilze und Viren durch DNA-Schäden. Im Gegensatz zum Autoklavieren (bei dem möglicherweise hitzebeständige Sporen lebensfähig bleiben, wenn sich die Zyklusparameter ändern) oder der chemischen Desinfektion (bei der Desinfektionsmittelrückstände zurückbleiben und möglicherweise keine sporizide Wirksamkeit erzielt wird) sorgt die Gammabestrahlung für absolute Sterilität ohne Rückstände.
- Validierte Sterilitätszertifikate: Gammasterilisierte Einwegartikel werden mit Sterilisationszertifikaten geliefert, die die abgegebene Dosis, die Ergebnisse des biologischen Indikators (BI) und den SAL-Erfolg dokumentieren. Einrichtungen können diese Zertifikate vorbehaltlich der Qualifikation des Anbieters (gemäß Anhang 1 Abschnitt 4.34) akzeptieren und so interne Sterilitätstests vermeiden.
- Vorhersehbare EM-Leistung: Bereiche der Güteklasse A/B mit gamma-sterilen Einwegmopps sorgen für eine stabile Keimbelastung. Jeder Mikrobennachweis während der Umgebungsüberwachung nach der Reinigung stellt eine Kontamination aus anderen Quellen (Personal, Luftbehandlung, Materialtransfer) dar – nicht die Übertragung von Keimen durch Reinigungswerkzeuge.
Nicht sterile Einwegmopps (für Anwendungen der ISO-Klasse 7–8) liefern durch validierte Herstellungskontrollen immer noch eine vorhersehbare Leistung hinsichtlich der Keimbelastung. Einwegartikel in pharmazeutischer Qualität halten die Keimbelastung aufrecht <10 KBE/Mopppad durch Herstellung im Reinraum, sterilisierte Verpackungsmaterialien und validierte Lagerung. Diese Grundlinie bleibt über alle Einheiten hinweg konstant, im Gegensatz zu wiederverwendbaren Mopps, bei denen die unterschiedliche Wirksamkeit der Wäsche zu Schwankungen der Keimbelastung führt.
Niedrigere Validierung & Dokumentationsbelastung
Der Validierungsaufwand ist ein versteckter Kostenfaktor bei wiederverwendbaren Reinigungswerkzeugprogrammen. Einrichtungen müssen Protokolle entwickeln, Studien durchführen, Daten analysieren und die Dokumentation für mehrere Validierungselemente pflegen – jedes davon kostet Zeit von Qualitätssicherungsspezialisten, Ressourcen des Mikrobiologielabors und Stunden für die Gerätequalifizierung.

Was wiederverwendbare Mopps benötigen:
- Qualifizierung der Wäschereiausrüstung (IQ/OQ/PQ): Installationsqualifizierung zur Überprüfung der Gerätespezifikationen, Betriebsqualifizierung zur Validierung der Zyklusparameter (Temperaturverteilung, Reinigungsmittelkonzentration, Spülwirksamkeit), Leistungsqualifizierung zum Nachweis der Keimbelastungsreduzierung bei ungünstigster Belastung
- Qualifizierung des Reinigungswerkzeugmaterials: Prüfung der Partikelerzeugung im Neuzustand und am Ende der Lebensdauer (maximale Zyklenzahl); Validierung der chemischen Kompatibilität aller Desinfektionsmittel in der Einrichtung; Prüfung der Dimensionsstabilität durch Autoklavenzyklen
- Validierung des Cycle-Count-Tracking-Systems: Validierung von Barcode- oder RFID-Tracking-Systemen, Testen von Auslösewarnungen für den Ausfall, Nachweis der Rückverfolgbarkeit während des gesamten Mopp-Lebenszyklus
- Überprüfung der Sterilität oder Keimbelastung (falls autoklaviert): Studien zur Platzierung biologischer Indikatoren, Validierung des Sterilisationszyklus, Demonstration des Sterilitätssicherungsniveaus (SAL).
- Periodische Neuvalidierung: Jährliche oder alle zwei Jahre stattfindende Neuvalidierung nach Geräteänderungen, Änderungen der Programmparameter oder Aktualisierungen der Waschmittelformel
Was Einwegmopps benötigen:
- Nur Materialqualifikation: Prüfung der Partikelerzeugung (in der Regel vom Anbieter mit bereitgestelltem Validierungsbericht durchgeführt), Überprüfung der chemischen Kompatibilität mit einrichtungsspezifischen Desinfektionsmitteln
- Eingangskontrolle: Visuelle Inspektion der Verpackungsintegrität, Überprüfung von Sterilitätszertifikaten (für gammasterile Einheiten), Dokumentation der Chargennummer
- Anbieterqualifikation: Audit der Reinraumkontrollen des Herstellers, Validierung des Sterilisationsprozesses, Qualitätsmanagementsystem – normalerweise durch Überprüfung des vom Anbieter bereitgestellten Validierungspakets erfüllt
Reduzierung der Validierungsstunden
Eine repräsentative pharmazeutische Einrichtung, die in einem 500 m² großen aseptischen Supportbereich der ISO-Klasse 7 von wiederverwendbaren auf Einweg-Mopps umstellt, könnte den Validierungsaufwand reduzieren durch:
- Erstvalidierung: 120–160 Stunden (Validierung von wiederverwendbarer Wäsche + Einrichtung des Nachverfolgungssystems) vs. 20–30 Stunden (Qualifizierung von Einwegmaterialien + Empfangsverfahren)
- Jährliche Revalidierung: 40–60 Stunden (Revalidierung der Wäscherei + Überprüfung des Zykluszählsystems) vs. 0 Stunden (keine Revalidierung erforderlich; Eingangskontrolle gehört zum Routinebetrieb)
- Unterstützung bei Ermittlungen: 8–12 Stunden pro EM-Exkursion (forensische Überprüfung der Moppzuordnungshistorie, Wäscheprotokolle, Zykluszählungen) vs. 2–3 Stunden (einfache Überprüfung der Einweg-Chargennummer und Zertifikatsüberprüfung)
Für QA-Teams, die mit einer begrenzten Mitarbeiterzahl arbeiten – wie es bei Biotech-Start-ups, Vertragsfertigungsunternehmen und Einrichtungen mit schlanken Abläufen üblich ist – führt diese Reduzierung des Validierungsaufwands direkt zu einer Bandbreite für höherwertige Aktivitäten: Reinigungsvalidierung für neue Produkte, Verbesserungen von Umweltüberwachungsprogrammen, Abweichungsuntersuchungen.
Arbeit & Zeiteffizienz
Die betriebliche Effizienz erhöht sich über Hunderte oder Tausende von Wischzyklen pro Jahr. Kleine Verfahrensverbesserungen – Wegfall der Protokollierung der Zykluszählung, Wegfall von Mopp-Inspektionsschritten, Vereinfachung der Entsorgung – summieren sich zu messbaren Arbeitseinsparungen.
Keine Nachverfolgung der Zyklusanzahl
Bei wiederverwendbaren Moppprogrammen müssen Bediener jeden Moppgebrauch protokollieren:
- Vorbenutzung: Mopp-Barcode oder RFID-Tag scannen, Zyklusanzahl innerhalb des qualifizierten Bereichs überprüfen, Mopp-Zuordnung zu einem bestimmten Raum/Bereich dokumentieren
- Nachnutzung: Mopp in den Schmutzwäsche-Stadium zurückbringen, aus dem Inventar scannen, Wäsche-/Autoklav-Zyklus auslösen, wenn der vorgegebene Zählschwellenwert erreicht ist
- Regelmäßige Audits: Die Qualitätssicherung führt monatliche oder vierteljährliche Audits der Zykluszählungsprotokolle durch, um die Einhaltung zu überprüfen, Nachverfolgungslücken zu identifizieren und die Ausmusterung überalterter Mopps durchzusetzen
Einwegsysteme machen diesen gesamten Arbeitsablauf überflüssig. Die Bediener nehmen den Mopp aus der Verpackung, verwenden ihn einmal und entsorgen ihn im Sondermüll – kein Scannen, keine Protokollierung, keine Überprüfung der Zykluszählung. Für Einrichtungen, die täglich 200–500 m² in mehreren Schichten wischen, spart diese Verfahrensvereinfachung 10–15 Minuten pro Schicht (insgesamt über alle Wischvorgänge hinweg) – also etwa 60–75 Stunden pro Jahr an zurückgewonnener Bedienerzeit.
Kein Waschen, Trocknen, Weiterverteilen
Mehrweg-Mopplogistik schafft mehrstufige Arbeitsabläufe:
- Schmutzwäschesammlung: Bediener transportieren gebrauchte Mopps aus Reinraumbereichen zur Wäscherei und wahren dabei die Trennung nach ISO-Klasse
- Geldwäsche: Wäschereipersonal lädt Mopps in Waschmaschinen (nach Sorten getrennt), führt validierte Waschzyklen durch und überführt sie in Trockner
- Sterilisation (falls erforderlich): Getrocknete Mopps in den Autoklaven laden, validierten Zyklus durchführen, biologische Indikatoren überprüfen
- Umverteilung: Transportieren Sie saubere/sterile Mopps zurück in die Reinraumbereiche und füllen Sie den Bestand an den dafür vorgesehenen Lagerorten auf
Jeder Schritt verbraucht Arbeitsstunden und führt zu Verzögerungen. Eine typische Durchlaufzeit für wiederverwendbare Mopps beträgt 24–48 Stunden (länger, wenn Autoklavieren erforderlich ist oder wenn die Wäsche ausgelagert wird). Die Einrichtungen müssen einen 2- bis 3-fachen Bestand vorhalten, um eine ausreichende Moppverfügbarkeit während der Wäschezyklen sicherzustellen.
Einwegmopps gliedern diese Logistikkette in zwei Schritte:
- Empfang und Lagerung: Nehmen Sie Einweg-Mopplieferungen an, führen Sie eine Eingangskontrolle durch und lagern Sie sie in den dafür vorgesehenen Reinraum-Bestandsbereichen
- Entsorgung: Entfernen Sie gebrauchte Mopps aus dem Reinraum in klassifizierten Abfallbehältern gemäß den Abfallmanagementprotokollen der Einrichtung
Kein Waschen, keine Sterilisation, keine Weiterverteilung. Der Lagerbedarf sinkt auf 1x (Mopps, die für den laufenden Betrieb benötigt werden) plus Sicherheitsbestand (normalerweise ein zusätzlicher Karton pro SKU). Für kleine Einrichtungen mit begrenzter Wäscherei-Infrastruktur oder Biotech-Start-ups ohne eigene Wäschereikapazität machen Einwegsysteme den Aufbau oder die vollständige Auslagerung von Wäschereibetrieben überflüssig.
Besonders wertvoll für GMP-Einrichtungen mit kleinen Teams
Biotech-Startups, Spezialhersteller und Auftragsfertigungsunternehmen mit schlanken Betriebsteams profitieren überproportional von Einweg-Moppsystemen:
- Kein engagiertes Wäschereipersonal: Einrichtungen mit <20 Reinraumpersonal kann es oft nicht rechtfertigen, Wäschereibetreiber in Vollzeit zu beschäftigen. Einwegsysteme machen diesen Personalbedarf überflüssig.
- Vereinfachtes Training: Die Bedienerschulung für Einwegsysteme erfordert eine SOP („Aus der Verpackung entfernen, einmal verwenden, entsorgen“) im Gegensatz zu mehreren SOPs für wiederverwendbare Systeme (Moppinspektion, Protokollierung der Zykluszählung, Wäschetrennung, Beladung im Autoklaven).
- Reduzierter CAPA-Arbeitsaufwand: Untersuchungen zu Zykluszählungsfehlern, Fehlern bei der Wäschetrennung und Abweichungen bei der Autoklavensterilisation entfallen, wenn es sich bei den Werkzeugen um Einweggeräte handelt.
Änderungen im EU GMP Annex 1 (2023–2025)
Der überarbeitete EU-GMP-Anhang 1 (gültig ab 25. August 2023) positioniert die Kontaminationskontrolle grundlegend neu als standortweiten strategischen Rahmen. In früheren Versionen wurden Reinigung und Desinfektion als Verfahrensanforderungen behandelt; Mit der Überarbeitung von 2023 wird die Kontaminationskontrollstrategie (CCS) zu einem verbindlichen, dokumentierten System, das kritische Kontrollpunkte definiert und die Wirksamkeit von Design-, Verfahrens-, Technik- und Überwachungsmaßnahmen in der gesamten Anlage bewertet.
Reinigungswerkzeuge als CCS-Elemente
Anhang 1 Abschnitt 2.5 listet „Reinigung und Desinfektion“ ausdrücklich als eines der zentralen CCS-Elemente auf, die validiert werden müssen, und Abschnitt 4.33–4.35 schreibt vor, dass Desinfektionsmittel und Reinigungsmittel, die in Bereichen der Klassen A und B verwendet werden, „vor der Verwendung steril sein sollten“. Die Verordnung verlangt außerdem validierte Desinfektionsverfahren, wobei der Desinfektion eine Reinigung vorausgeht, um eine wirksame Rückstandsentfernung sicherzustellen. Diese Anforderungen gelten nicht nur für Chemikalien, sondern auch für die Werkzeuge, mit denen sie verwendet werden – Moppköpfe, Tücher und Reinigungsgeräte müssen in aseptischen Zonen Sterilität und validierte Leistung gewährleisten.
Der Ausdruck „sterile Werkzeuge für Manipulationen“ (Abschnitt 8.16) erweitert diese Logik: Wenn Bediener Materialien in aseptischen Verarbeitungsbereichen mit sterilen Geräten manipulieren, müssen die Reinigungswerkzeuge, die mit denselben klassifizierten Oberflächen in Kontakt kommen, gleichwertige Standards für Sterilität und Kontaminationskontrolle erfüllen.
Versteckte Kontaminationsvektoren und Transferdesinfektion
Anhang 1 Abschnitt 4.11–4.12 identifiziert den Material- und Gerätetransfer als „eine der größten potenziellen Kontaminationsquellen“, die eine validierte Transferdesinfektion und überwachte Programme erfordert. Wiederverwendbare Reinigungswerkzeuge werden ständig zwischen Räumen und Bereichen transportiert – ein Mopp, der an einem Tag in einem Unterstützungskorridor der Klasse C verwendet wird, kann gewaschen und in der nächsten Schicht in einem Hintergrund der Klasse B eingesetzt werden. Ohne validierte Wiederaufbereitung (Waschen, Desinfektion, Sterilitätsüberprüfung) wird der Mopp zu einem „versteckten Kontaminationsvektor“, der biologische Belastung, Partikelrückstände und chemische Rückstände zwischen klassifizierten Umgebungen transportiert.
Der Schwerpunkt der Verordnung auf glatten, undurchlässigen Oberflächen, die den Haarausfall minimieren und eine wiederholte Desinfektion vertragen (Abschnitt 4.5–4.7), gilt gleichermaßen für die Auswahl der Reinigungswerkzeuge. Einwegmopps eliminieren den Abbauweg: keine Nachverfolgung der Zyklenzahl, keine durch den Autoklaven verursachte Kantentrennung, kein durch die Wäsche verursachter Faserbruch. Jeder Mopp startet frisch und erfüllt die Spezifikationen für Partikelerzeugung und Sterilität ohne kumulativen Verschleiß.
Wäsche- und Wiederaufbereitungsrisiko
In Anhang 1 Abschnitt 7.17 wird das Waschen von Kleidungsstücken ausdrücklich als Kontaminations- und Kreuzkontaminationsrisiko bezeichnet, das qualifizierte Wäschereiprozesse, Trennung von Produktionsbereichen und definierte Zyklusgrenzen erfordert. Die gleichen Kontaminationspfade wirken sich auch auf Mehrweg-Moppsysteme aus. In Wäschereien, in denen sowohl Kleidungs- als auch Reinigungswerkzeuge verarbeitet werden, besteht die Möglichkeit einer Kreuzkontamination: Unzureichende Waschmittelspülzyklen hinterlassen Tensidrückstände, eine unvollständige Keimbelastungsreduzierung überträgt mikrobielle Belastungen und die Verarbeitung gemischter Beladungen verunreinigt Werkzeuge der Güteklasse A/B mit Partikeln aus minderwertigen Artikeln.
Einrichtungen ohne validierte eigene Wäschereibetriebe müssen auslagern, was die Komplexität der Lieferkette, Verzögerungen bei der Bearbeitung und das Kontaminationsrisiko durch Dritte erhöht. Einweg-Mopps umgehen das gesamte Wäschereisystem und reduzieren die Wiederaufbereitungslogistik auf einen einzigen Schritt: Mopp-Pad aus der sterilen Verpackung nehmen, einmal verwenden und im klassifizierten Abfall entsorgen.
Grundursache: Wiederverwendbare Werkzeuge, die zu EM-Ausfällen führen
Umweltüberwachungsprogramme in pharmazeutischen Einrichtungen erkennen routinemäßig Kontaminationsspitzen während und unmittelbar nach der Bodenreinigung. Wenn Ermittlungsteams diese Abweichungen auf die Ursache zurückführen, erweisen sich wiederverwendbare Reinigungswerkzeuge als Wiederholungstäter.
Restkeimbelastung und Kreuzverschleppung
Wiederverwendbare Moppköpfe kommen mit Bodenflächen in Kontakt, die mit mikrobieller Kontamination, Desinfektionsmittelrückständen und Partikeln beladen sind. Auch nach dem Waschen bleiben Keimbelastung und chemische Rückstände bestehen:
- Unvollständige Reduzierung der Keimbelastung: Standardwaschgänge (Heißwasserwäsche, Waschmittel, Trocknen im Wäschetrockner) reduzieren die mikrobielle Belastung, erreichen jedoch keine Sterilität. Vegetative Bakterienzellen überleben in Gewebezwischenräumen und Sporenbildner (Bacillus, Geobacillus) tolerieren Wäschebedingungen völlig. Ein wiederverwendbarer Mopp, der ohne abschließende Sterilisation (Autoklavieren oder Gammabestrahlung) in einen Bereich der Klasse A/B gelangt, bringt lebensfähige Mikroorganismen direkt auf Oberflächen ein, die anschließend mit sterilen Produkten oder produktberührenden Geräten in Kontakt kommen.
- Kreuzübertragung zwischen Bereichen: Mopps, die in Stützbereichen der ISO-Klasse 8 verwendet werden, sammeln eine höhere Keimbelastung und Partikelanzahl an als Mopps, die für aseptische Kerne der ISO-Klasse 5 vorgesehen sind. Wenn die Wäschetrennung unzureichend ist – Mischbeladungswäsche, gemeinsam genutzte Wäschereiausrüstung, unsachgemäße Nachverfolgung – werden Mopps der Güteklasse A/B mit Rückständen der Güteklasse C/D verunreinigt. Ein einziges Ereignis der gegenseitigen Zuordnung (Verwendung eines ISO-8-Mopps in einem ISO-5-Raum aufgrund eines Etikettierungsfehlers oder eines Lagermangels) kann eine Keimbelastung in aseptischen Umgebungen verursachen und mehrwöchige Untersuchungszyklen auslösen.
- Waschmittelrückstände: Auf den Moppfasern verbleibende Tenside und Weichspüler erzeugen klebrige Oberflächen, die Partikel anziehen und festhalten. Diese Rückstände beeinträchtigen auch die Wirksamkeit des Desinfektionsmittels – kationische Tenside in Weichspülern neutralisieren anionische Desinfektionsmittel (quartäre Ammoniumverbindungen), wodurch die Abtötungsrate von Mikroben beim Wischen verringert wird und lebensfähige Organismen auf behandelten Oberflächen zurückbleiben.
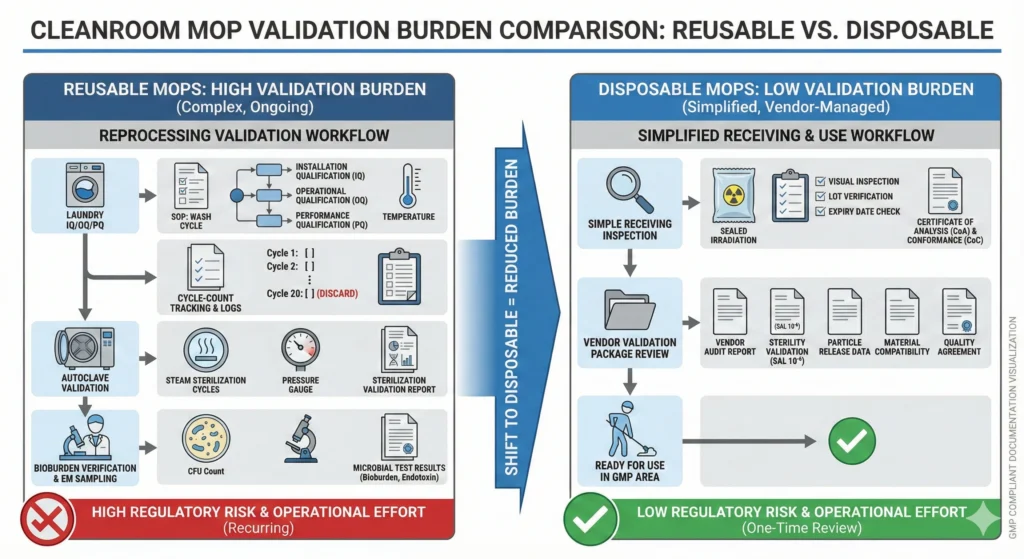
Aufarbeitung des Dokumentations- und Validierungsaufwands
Für wiederverwendbare Reinigungstoolprogramme gelten umfangreiche Validierungs- und Dokumentationsanforderungen:
- Geldwäschevalidierung (IQ/OQ/PQ): Die Einrichtungen müssen die Wäschereiausrüstung (Waschmaschinen, Trockner, Autoklaven) qualifizieren, Zyklusparameter (Zeit, Temperatur, Waschmittelkonzentration) validieren und eine Reduzierung der Keimbelastung auf akzeptable Grenzen nachweisen. Dies erfordert mikrobiologische Belastungsstudien (Inokulation von Moppköpfen mit Zielorganismen, Verarbeitung durch den gesamten Wäschezyklus, Gewinnung und Quantifizierung von Überlebenden) und eine regelmäßige erneute Validierung, wenn sich Zyklusparameter ändern oder Geräte gewartet werden.
- Zykluszählungsverfolgung und Ruhestandskriterien: Jeder wiederverwendbare Moppkopf hat eine qualifizierte Lebensdauer (z. B. 50 Autoklavenzyklen für Polyester-Mopps mit versiegelten Kanten). Einrichtungen müssen Nachverfolgungssysteme – Barcodes, manuelle Protokolle oder RFID-Tags – implementieren, um den Nutzungsverlauf aufzuzeichnen und die Stilllegung am Ende der qualifizierten Lebensdauer durchzusetzen. Fehler bei der Nachverfolgung bringen Risiken mit sich: Überalterte Mopps werfen Partikel und Keime ab, aber eine vorzeitige Ausmusterung verschwendet Lagerbestände und erhöht die Kosten.
- Überprüfung der Sterilität oder Keimbelastung: Wenn wiederverwendbare Mopps für den Einsatz in Bereichen der Klasse A/B autoklaviert werden, muss der Sterilisationszyklus gemäß ISO 11137 oder einer gleichwertigen Norm validiert werden, wobei Sterilitätsindikatoren in repräsentativen Ladungskonfigurationen angebracht werden müssen. Einrichtungen ohne Autoklavenkapazität müssen Mopps entweder an externe Sterilisationsanbieter schicken (was zusätzliche Bearbeitungszeit und Kosten verursacht) oder ein erhöhtes Risiko einer Keimbelastung in Kauf nehmen.
- Untersuchungsdokumentation: Wenn es zu EM-Exkursionen kommt, müssen die Ermittlungsteams die Historie des Reinigungswerkzeugs überprüfen – welcher Mopp verwendet wurde, wann er zuletzt gewaschen wurde, wie viele Zyklen er hatte und in welchen Bereichen er zuvor verwendet wurde. Für diese forensische Analyse sind vollständige Aufzeichnungen zur Rückverfolgbarkeit erforderlich. Lücken in der Dokumentation (fehlende Wäschereiprotokolle, nicht erfasste Moppeinsätze) verlängern die Ermittlungen und erschweren den CAPA-Abschluss.
Mit Einwegmopps entfällt ein Großteil dieser Validierungsinfrastruktur. Einwegwerkzeuge erfordern lediglich eine Eingangskontrolle (Überprüfung von Sterilitätszertifikaten, visuelle Inspektion der Verpackungsintegrität) und eine Materialqualifizierung (Test der Partikelerzeugung, Validierung der chemischen Kompatibilität) – keine Wäschevalidierung, keine Nachverfolgung der Zykluszählung, keine Dokumentation der Wiederaufbereitung.
Zunehmende Akzeptanz im Fill-Finish-Bereich & Biotechnologie
Marktdaten zeigen, dass sich die Einführung validierter Einweg-Reinigungsverbrauchsmaterialien in der pharmazeutischen und biotechnologischen Produktion beschleunigt, was auf den Druck zur Einhaltung gesetzlicher Vorschriften und die Betriebsökonomie zurückzuführen ist.
Fill-Finish-Linien und aseptische Verarbeitung
Abfüll- und Endbearbeitungsvorgänge – sterile Abfüllung, Lyophilisierungsbeladung, Verschließen von Fläschchen – erfolgen unter einem unidirektionalen Luftstrom der ISO-Klasse 5 (Klasse A) mit Hintergründen der ISO-Klasse 7 (Klasse B). Die Partikelgrenzwerte sind extrem: 3.520 Partikel ≥0,5 µm pro Kubikmeter für ISO 5, gegenüber 352.000 Partikel/m³ für ISO 7. Jedes Reinigungsgerät, das einen messbaren Partikelbeitrag erzeugt, riskiert Klassifizierungsabweichungen.
Einweg-Reinraummopps, validiert auf Partikelerzeugung (<50 Partikel/m² bei Polyester-Siegelkante; <10 Partikel/m² für Premium-Endlosfilament-Designs) liefern eine vorhersehbare, konstante Leistung bei allen Anwendungen. Wiederverwendbare Mopps verschlechtern sich mit der Zeit – die Kantenversiegelung löst sich, Fasern brechen, die Partikelbildung nimmt zu – und führen zu einem variablen Kontaminationsbeitrag, der die Trendanalyse der Umweltüberwachung erschwert.
Herstellung von Biotechnologie und Zelltherapie
Bei der Herstellung biologischer Wirkstoffe und Zelltherapien werden kleinere Chargen mit höherer Wirksamkeit angewendet als bei herkömmlichen niedermolekularen Pharmazeutika. Kontaminationsereignisse, die bei einer Tablettencharge mit 10.000 Dosen tolerierbar wären, werden bei einem personalisierten CAR-T-Produkt mit 50 Dosen katastrophal. Biotech-Einrichtungen nutzen Einweg-Reinigungswerkzeuge als Teil umfassenderer Einweg-Systemstrategien:
- Einweg-Bioreaktoren und Flüssigkeitswege: Auf Einwegbeuteln basierende Systeme machen die Reinigungsvalidierung für Gefäße überflüssig und verringern das Risiko einer Kreuzkontamination zwischen Chargen. Durch die Ausweitung dieser Logik auf die Bodenreinigung wird die systemweite Philosophie der Einwegkontaminationskontrolle beibehalten.
- Auftragsfertigung und Mehrproduktanlagen: CDMOs, die mehrere Kundenprodukte in denselben Reinraumräumen handhaben, müssen strenge Anforderungen an die Reinigungsvalidierung und die Verhinderung produktübergreifender Kontamination stellen. Einwegmopps vereinfachen die Umstellung – jede neue Kampagne beginnt mit neuen Reinigungswerkzeugen, wodurch das Risiko einer Verschleppung von früheren Produkten ohne umfangreiche Reinigungsvalidierungsstudien ausgeschlossen wird.
- Schlanke Betriebsmodelle: Biotech-Startups und kleine Hersteller verfügen oft nicht über eine eigene Wäscherei-Infrastruktur. Die Auslagerung der Reinigung wiederverwendbarer Wischmopps erhöht die Kosten, die Durchlaufzeit und das Kontaminationsrisiko durch Dritte. Bei Einwegmopps wird die Lieferkette auf die direkte Lieferung vorsterilisierter, gebrauchsfertiger Verbrauchsmaterialien durch den Lieferanten reduziert.
Branchenanalysen bestätigen, dass EU-GMP-Anhang 1 „Pharmahersteller dazu zwingt, auf sterile Einwegbekleidung und -tücher umzusteigen“, was die Einführung validierter Einweg-Verbrauchsmaterialien in allen Reinigungskategorien vorantreibt. Vorgetränkte sterile Tücher erobern bereits erhebliche Marktanteile in aseptischen Suiten; Einweg-Moppsysteme folgen der gleichen Akzeptanzkurve, da Einrichtungen Einweg-Kontaminationskontrollstrategien auf die Bodenreinigung ausweiten.

Kostenvergleich: Einweg vs. wiederverwendbar
Die höheren Stückkosten von Einweg-Reinraummopps – in der Regel 8–25 US-Dollar pro Mopppad im Vergleich zu 15–40 US-Dollar für einen wiederverwendbaren Mopp mit einer Lebensdauer von 50–100 Zyklen – lösen bei den Beschaffungsteams zunächst einen Schock aus. Die Analyse der Gesamtbetriebskosten (TCO) zeigt jedoch, dass Einwegsysteme bei risikoreichen pharmazeutischen Anwendungen häufig geringere Lebenszeitkosten verursachen, wenn die Kosten für Wiederaufbereitung, Validierung und Kontaminationsfehler berücksichtigt werden.
Direkte Kostenelemente
Einweg-Moppsysteme
- Kosten pro Mopppad-Einheit: 8–15 USD pro Einlage für unsterile Polyester-Einwegartikel mit versiegelten Kanten (ISO 7–8-Anwendungen); 15–25 USD pro Einlage für gammabestrahlte sterile Einwegartikel (Bereiche ISO 5–6 Klasse A/B)
- Griffsysteme: 50–150 $ pro wiederverwendbarem Aluminium- oder Edelstahlgriff (kompatibel mit Einweg-Pad-Befestigungssystemen); Griffe haben eine mehrjährige Lebensdauer
- Lagerung und Inventar: Minimal – Einwegartikel werden in einer kompakten Verpackung geliefert und erfordern keine Trennung nach Zykluszahl oder Sterilisationsstatus
- Abfallentsorgung: Entsorgung klassifizierter Arzneimittelabfälle (normalerweise 0,50–2 USD pro Pfund); Einweg-Mopppads wiegen 50–150 Gramm, wodurch die Abfallentsorgungskosten um 0,05–0,30 US-Dollar pro Mopp anfallen
Wiederverwendbare Moppsysteme
- Anfängliche Kosten für den Moppkopf: 15–40 $ pro wiederverwendbarem Wischkopf aus Polyester oder Mikrofaser mit versiegelten Kanten
- Wäschekosten pro Zyklus: 2–5 USD pro Mopp (gewerbliche Wäscherei, Waschmittel, Nebenkosten); Durch internes Waschen wird dieser Betrag auf 1 bis 3 US-Dollar pro Zyklus reduziert, es sind jedoch Investitionen in die Ausrüstung erforderlich
- Sterilisation im Autoklaven (falls erforderlich): 3–8 USD pro Zyklus, einschließlich Nebenkosten, biologischen Indikatoren, Dokumentation und Geräteamortisation
- System zur Verfolgung der Zyklusanzahl: 5.000–20.000 US-Dollar für Barcode- oder RFID-Infrastruktur (Scanner, Software, Etikettendruck) plus 0,50–1 US-Dollar pro Wischmopp und Zyklus für die Nachverfolgung
- Lagerhaltungskosten: 2- bis 3-facher Moppvorrat erforderlich, um während der Wäschewechselzyklen eine ausreichende Verfügbarkeit aufrechtzuerhalten
Versteckte indirekte Kosten (oft übersehen)
Die entscheidenden TCO-Faktoren liegen oft in versteckten Betriebskosten, die Beschaffungsteams unterschätzen, wenn sie allein den Stückpreis bewerten.
Validierungs- und Dokumentationsaufwand
- Erste Wäschevalidierung: 120–160 Stunden Zeit eines QA-Spezialisten (60–100 USD/Stunde) für IQ/OQ/PQ = 7.200–16.000 USD
- Qualifizierung des Moppmaterials über den gesamten Lebenszyklus: 40–60 Stunden für Partikeltests unter Neu- und End-of-Life-Bedingungen, Validierung der chemischen Kompatibilität = 2.400–6.000 $
- Validierung der Autoklavensterilisation (falls zutreffend): 60–80 Stunden für Zyklusentwicklung, Studien zu biologischen Indikatoren, SAL-Demonstration = 3.600–8.000 $
- Jährliche Revalidierung: 40–60 Stunden pro Jahr = 2.400–6.000 $ jährlich
- Einwegvalidierung im Vergleich: 20–30 Stunden für die Materialqualifizierung (oft vom Anbieter bereitgestellt) + Entwicklung des Empfangsverfahrens = einmalige Kosten von 1.200–3.000 US-Dollar, ohne jährliche Revalidierung
Kosten für Umweltüberwachungsuntersuchungen
EM-Exkursionen, die auf eine Kontamination von Reinigungswerkzeugen zurückzuführen sind, lösen mehrwöchige Untersuchungszyklen aus:
- Ermittlungsarbeit: 20–40 Stunden pro Exkursion (Zeit des Mikrobiologen, QS-Dokumentation, Abweichungsbearbeitung) = 1.200–4.000 $ pro Veranstaltung
- Ursachenanalyse: Forensische Überprüfung der Moppeinsatzhistorie, Wäscheprotokolle, Zykluszählungen, Wiederaufbereitungsaufzeichnungen
- CAPA-Implementierung: Verfahrensüberarbeitungen, Umschulung, verbesserte Überwachung – oft 40–80 zusätzliche Stunden = 2.400–8.000 $
- Risiko von Chargenauswirkungen: Im schlimmsten Fall führen EM-Ausfälle während der aseptischen Abfüllung zu Chargensperren, einer Erweiterung des Sterilitätstests oder einer Chargenablehnung – die Kosten reichen von 50.000 US-Dollar (Haltung und Untersuchung kleiner Chargen) bis über 500.000 US-Dollar (Chargenablehnung und behördliche Benachrichtigung).
Einrichtungen, in denen es nur zu einem EM-Ausfall pro Jahr kommt, und die mit einem moderaten Untersuchungsaufwand (5.000–10.000 US-Dollar für Arbeitsaufwand und Dokumentation) ausgestattet sind, kompensieren die erheblichen Kosten für Einwegmopps.
Steigerung der Arbeitseffizienz
- Eliminierung der Zykluszählungsverfolgung: 60–75 Stunden pro Jahr bei allen Wischvorgängen eingespart = 1.800–3.000 $ Jahreswert (bei einem gemischten Betreibertarif von 30 $/Stunde)
- Eliminierung der Wäschereilogistik: 100–200 eingesparte Stunden pro Jahr (Schmutzsammlung, Beladen mit Waschzyklen, Sterilisation, Neuverteilung) = 3.000–6.000 US-Dollar Jahreswert
- Trainingsvereinfachung: Reduzierte SOP-Komplexität spart 10–20 Stunden pro Jahr bei der Schulungsdurchführung und Kompetenzüberprüfung = 600–2.000 $ Jahreswert
Vergleich der Gesamtbetriebskosten (Beispiel für einen aseptischen Supportbereich der ISO-Klasse 7)
Stellen Sie sich einen 500 m² großen Produktionsbereich der pharmazeutischen Industrie der ISO-Klasse 7 vor, der täglich (365 Tage/Jahr) gewischt wird und 2 Wischpads pro Reinigungszyklus erfordert:
Szenario A: Wiederverwendbare Mopps
- Direkte Kosten: 730 Mop-Verwendungen/Jahr ÷ 75 Mop-Lebenszyklen = 10 Mopps pro Jahr zu je 30 $ gekauft = 300 $
- Geldwäsche: 730 Zyklen × 3 $ pro Zyklus (interne Verarbeitung) = 2.190 $
- Sterilisation im Autoklaven: 730 Zyklen × 5 $ pro Zyklus = 3.650 $
- Zyklusverfolgung der Arbeit: 730 Zyklen × 0,75 $ pro Zyklus = 548 $
- Erstvalidierung (amortisiert über 5 Jahre): 12.000 $ ÷ 5 = 2.400 $ pro Jahr
- Jährliche Revalidierung: 4.000 $
- EM-Untersuchungsaufwand (1 Ereignis alle 2 Jahre, konservativ): 7.500 $ ÷ 2 = 3.750 $ Jahresdurchschnitt
- Jährliche Gesamtbetriebskosten: 16.838 $
Szenario B: Einwegmopps (Gamma-steril)
- Direkte Kosten: 730 Wischpads × 18 $ pro Pad = 13.140 $
- Behandeln Sie die Amortisation: 100 $ ÷ 5-Jahres-Lebensdauer = 20 $ pro Jahr
- Abfallentsorgung: 730 Pads × 0,15 $ pro Pad = 110 $
- Erste Materialqualifikation (amortisiert über 5 Jahre): 2.000 $ ÷ 5 = 400 $ pro Jahr
- Keine Kosten für Verlängerung, Wäsche, Sterilisation oder Nachverfolgung
- Reduzierter EM-Untersuchungsaufwand: Nahezu null reinigungswerkzeugbezogene Abweichungen = 0 $
- Steigerung der Arbeitseffizienz: 4.000 $ pro Jahr (Sendungsverfolgung, Wäschelogistik, Schulung)
- Jährliche Gesamtbetriebskosten: 13.670 $ – 4.000 $ (Effizienzsteigerung) = 9.670 $ Nettokosten
Ergebnis: Einweg-Mopps liefern 42 % niedrigere Gesamtbetriebskosten (9.670 US-Dollar gegenüber 16.838 US-Dollar) trotz höherer Stückkosten, getrieben durch den Wegfall der Wiederaufbereitungsinfrastruktur, die Reduzierung des Validierungsaufwands und die Vermeidung von EM-Untersuchungen.
Entscheidungsschwellen: Wenn Einwegartikel die Kosten rechtfertigen
Unter diesen Bedingungen liefern Einweg-Reinraummopps günstige Gesamtbetriebskosten:
- ISO-Klassifizierungen mit hohem Risiko (ISO 5–7): Partikelgrenzwerte und Kontaminationskontrollgrenzen sind eng; Das EM-Ausfallrisiko und der Untersuchungsaufwand sind hoch
- Anlagen mit EM-Fehlerhistorie: Schon ein einziger Verschmutzungsausflug pro Jahr, der auf Reinigungswerkzeuge zurückzuführen ist (Untersuchungskosten 5.000–10.000 US-Dollar), kompensiert erhebliche Kosten für Einwegmopps
- Kleine bis mittlere Betriebe (<1.000 m² Reinraumfläche): Wiederverwendbare Systeme erfordern feste Validierungs- und Infrastrukturkosten, die nicht sinken; Die verfügbaren Kosten skalieren linear mit der Nutzung
- Einrichtungen ohne hauseigene Wäscherei: Ausgelagerte Wäscherei kostet 5–10 US-Dollar pro Mopp und Zyklus und es kommt zu Verzögerungen bei der Bearbeitung; Einwegartikel beseitigen die Abhängigkeit von Dritten
- Schlanke operative Teams: Biotech-Start-ups und CMOs mit begrenzter QA-/Wäscherei-Mitarbeiterzahl profitieren von der Reduzierung des Validierungsaufwands und der Steigerung der Arbeitseffizienz
- Mehrproduktanlagen (CDMOs): Die Validierung der Produktwechselreinigung wird vereinfacht, wenn es sich bei den Reinigungswerkzeugen um Einweggeräte handelt. Kein Übertragungsrisiko zwischen Kampagnen
Wiederverwendbare Mopps bleiben kosteneffizient, wenn:
- Großserienfertigung (>2.000 m² tägliches Wischen): Ein hohes Moppverbrauchsvolumen (über 1.000 Wischmopps/Jahr) führt dazu, dass die Einwegkosten über die wiederverwendbaren Gesamtbetriebskosten hinausgehen, selbst unter Berücksichtigung des Wiederaufbereitungsaufwands
- ISO 8-Unterstützungsbereiche mit geringem EM-Risiko: Geringere Anforderungen an die Kontaminationskontrolle verringern den Untersuchungsaufwand; Die Wirtschaftlichkeit der Wiederverwendbarkeit verbessert sich in minderwertigen Umgebungen
- Eine validierte hauseigene Wäscherei-Infrastruktur ist bereits vorhanden: Einrichtungen mit ausgereiften, qualifizierten Wäschereibetrieben und einer robusten Zykluszählungsverfolgung verringern die Kostendifferenz bei der Wiederaufbereitung
- Priorisierung der Nachhaltigkeit: Einige Organisationen geben der Abfallreduzierung Vorrang vor der TCO-Optimierung; validierte wiederverwendbare Systeme mit dokumentierter Kontaminationskontrolle liefern akzeptable Risikoprofile
Beste Anwendungsfälle für Einwegmopps in GMP-Umgebungen
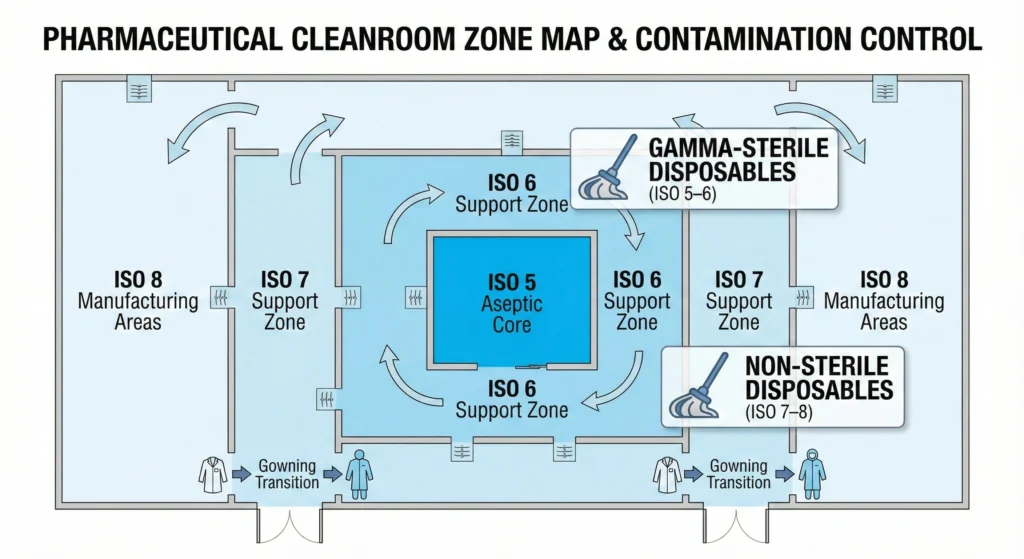
Einweg-Reinraummopps bieten den maximalen Nutzen, wenn die Anforderungen an die Kontaminationskontrolle, betriebliche Einschränkungen und Risikoprofile mit ihren Stärken übereinstimmen. In diesem Abschnitt werden bestimmte Anlagentypen, ISO-Klassifizierungen und Betriebsszenarien aufgeführt, in denen Einwegsysteme ihre Kosten durch eine bessere Kontaminationskontrolle und geringere Gesamtbetriebskosten rechtfertigen.
Aseptische Kerne der ISO-Klasse 5 (Klasse A).
Anforderungen: Unidirektionaler Luftstrom, Partikelgrenze 3.520 Partikel ≥0,5 µm/m³, Endsterilisation oder aseptische Verarbeitung, keine Keimbelastungstoleranz
Warum Einwegartikel Excel:
- Gammasterile Einwegartikel liefern SAL 10⁻⁶: Wiederverwendbare Mopps müssen aus Gründen der Sterilität autoklaviert werden. Dies führt zu einem Aufwand bei der Validierung des Sterilisationszyklus, Anforderungen an biologische Indikatoren und möglichen Sterilisationsfehlern. Gammabestrahlte Einwegartikel werden mit Zertifikaten vorsterilisiert geliefert, sodass keine betriebsinterne Sterilisation erforderlich ist.
- Kein Kreuzkontaminationsrisiko: Bereiche der Klasse A erfordern eine absolute Kontaminationskontrolle. Eine einzelne Wischmopp-Zuordnung (mit einem Wischmopp der Klasse A nach ISO 7 aufgrund von Lagerknappheit) führt zu einer Keimbelastung in aseptischen Zonen. Einwegartikel beseitigen diesen Fehlermodus.
- Vorhersehbare Partikelleistung: Partikelgrenzwerte sind extrem (3.520/m³). Wiederverwendbare Mopps geben mit zunehmendem Alter immer mehr Partikel ab; Einweg-Mopps aus Polyester mit versiegelten Kanten pflegen <50 Partikel/m² bei allen Nutzungen.
- Vereinfachte Validierung: Einrichtungen verzichten auf die Validierung des Autoklavierens, die Validierung der Zykluszählung und auf Studien zur Reduzierung der Keimbelastung in der Wäscherei – was für kleine Biotech-Einrichtungen mit begrenzten QS-Ressourcen von entscheidender Bedeutung ist.
Typische Anwendungen:
- Aseptische Abfülllinien (Fläschchenfüllung, Spritzenfüllung, Lyophilisierungsbeladung)
- Sterile Compoundieranlagen (Krankenhausapotheken, Compoundieranlagen)
- Herstellung von Zelltherapien (CAR-T-Verarbeitung, Herstellung personalisierter Medikamente)
- Biologische Sicherheitswerkbänke und Isolatorreinigung
MIDPOSI-Empfehlung: Gammabestrahlte Polyester-Einweg-Mopppads mit versiegelten Kanten und validierter <50 Partikel/m² Leistung und SAL 10⁻⁶ Sterilitätszertifikate
Aseptische Unterstützungsbereiche der ISO-Klasse 6–7 (Klasse B/C).
Anforderungen: Partikelgrenzwerte 35.200/m³ (ISO 6) bis 352.000/m³ (ISO 7), kontrollierte Keimbelastung, Kontaminationskontrolle bei der Materialübertragung
Warum Einwegartikel Excel:
- Verhinderung von Kontaminationen beim Materialtransfer: Bereiche der Güteklasse B/C dienen als Luftschleusen und Materialtransferzonen zwischen Gebieten mit niedrigerer Güteklasse und Kernen der Güteklasse A. Wiederverwendbare Mopps, die in mehreren Zonen verwendet werden, werden zu Kontaminationsüberträgern. Einwegartikel stellen sicher, dass jeder Reinigungszyklus mit einem validierten, kontaminationsfreien Werkzeug beginnt.
- Reduzierter EM-Untersuchungsaufwand: Bereiche der Klasse B/C unterliegen einer intensiven EM-Prüfung – jede Partikel- oder Keimbelastung löst eine Untersuchung aus. Einwegmopps mit vorhersehbarer Leistung vereinfachen die EM-Trendsuche und reduzieren die mit Reinigungswerkzeugen verbundenen Abweichungen.
- Arbeitseffizienz in Einrichtungen mit mehreren Räumen: Aseptische Suiten umfassen häufig 5–10 miteinander verbundene Supporträume der Klasse B/C. Bei Einwegsystemen entfällt die Nachverfolgung des Mopps in allen Räumen, die Überprüfung der Anzahl der Zyklen bei jedem Gebrauch und die Logistik der Wäschetrennung.
Entscheidungsfaktoren:
- Einrichtungen mit häufigen EM-Ausflügen profitieren am meisten – selbst eine Untersuchung pro Jahr (Kosten 5.000–10.000 US-Dollar) gleicht erhebliche Kosten für Einwegmopps aus
- Kleine bis mittlere Betriebe (<500 m² Gesamtfläche der Klasse B/C) siehe günstige Einweg-Gesamtbetriebskosten
- Einrichtungen ohne validierte eigene Wäscherei machen die Abhängigkeit von Wäschereien Dritter überflüssig
Typische Anwendungen:
- Füllen Sie die Hintergründe der Ziellinie aus und unterstützen Sie die Korridore
- Luftschleusen für den Materialtransfer zwischen Bereichen der Klassen C und A
- Umkleideräume für aseptische Kerne
- Reinigungs- und Bereitstellungsbereiche für Geräte
MIDPOSI-Empfehlung: Gammabestrahlte Einwegartikel für kritische Bereiche der Klasse B neben Zonen der Klasse A; unsterile Einwegartikel aus Polyester mit versiegelten Kanten, die für Stützbereiche der Klasse C mit Validierung geeignet sind <100 Partikel/m² Leistung
Fertigung nach ISO-Klasse 8 (Klasse D). & Unterstützungsbereiche – selektive Nutzung
Anforderungen: Partikelgrenzwert 3.520.000/m³, routinemäßige Überwachung der Keimbelastung, geringeres Kontaminationskontrollrisiko
Wenn Einwegartikel Sinn machen:
- Mehrproduktanlagen (CMOs/CDMOs): Die Produktwechselreinigung erfordert eine validierte Beseitigung produktübergreifender Kontamination. Einweg-Mopps vereinfachen den Wechsel – es besteht keine Gefahr, dass Produktrückstände von wiederverwendbaren Mops übertragen werden.
- Herstellung hochwirksamer Arzneimittel: Hochwirksame Verbindungen (Zytotoxika, Hormone) erfordern eine strenge Reinigungsvalidierung, um eine Exposition des Bedieners und eine Kreuzkontamination zu verhindern. Einweg-Reinigungswerkzeuge eliminieren das Risiko einer Verschleppung ohne umfangreiche Studien zur Reinigungsvalidierung.
- Einrichtungen mit begrenzter Wäscherei-Infrastruktur: Biotech-Startups und kleine Hersteller ohne eigene Wäscherei vermeiden den Aufbau oder die Auslagerung von Wäschereibetrieben, indem sie Einwegartikel aller ISO-Qualitäten verwenden.
- Reaktion auf Kontaminationsereignisse: Nach EM-Exkursionen oder Kontaminationsereignissen können Einrichtungen in den betroffenen Gebieten während der Ursachenermittlung und CAPA-Implementierung vorübergehend auf Einwegartikel umsteigen, um sicherzustellen, dass Reinigungswerkzeuge nicht zur anhaltenden Kontamination beitragen.
Wenn Mehrwegprodukte optimal bleiben:
- Großflächige ISO 8-Unterstützungsbereiche (>1.000 m² Lager, Korridorsysteme, allgemeine Fertigung), bei denen das Kontaminationsrisiko gering und der Moppverbrauch hoch ist
- Einrichtungen mit validierter hauseigener Wäscherei und robusten Systemen zur Zykluszählung, die bereits in Betrieb sind
- Organisationen, die Abfallreduzierung und Nachhaltigkeit priorisieren, wenn das Kontaminationsrisikoprofil akzeptabel ist
Typische Anwendungen für Einwegartikel:
- API-Fertigungssuiten für mehrere Produkte (CMO-Umstellungsszenarien)
- Bereiche zur Herstellung hochwirksamer Arzneimittel
- Bereitstellungsbereiche für die Gerätereinigung, die höherwertige Zonen bedienen
- Isolationszonen für Kontaminationsuntersuchungen
MIDPOSI-Empfehlung: Unsterile Einwegartikel aus Polyester mit versiegelten Kanten und validierter <100 Partikel/m² Leistung; Kostengünstig für den selektiven Einsatz bei gleichzeitiger Beibehaltung wiederverwendbarer Systeme für Supportbereiche mit geringem Risiko
Biotech-Startups & Kleine GMP-Anlagen
Betriebsprofil: <20 Reinraummitarbeiter, begrenzte Qualitätssicherungs-/Validierungsressourcen, keine eigene Wäscherei-Infrastruktur, schlankes Betriebsmodell, agile Fertigung (kleine Chargen, häufige Produktwechsel)
Warum Einwegartikel strategisch sind:
- Keine Investitionen in die Wäscherei-Infrastruktur: Eliminiert Kapitalinvestitionen in Höhe von 50.000–200.000 US-Dollar für Industriewaschmaschinen, Trockner, Autoklaven und den Bau von Waschküchen
- Reduzierung des Validierungsaufwands: QS-Teams, die über mehrere Validierungsaktivitäten (Gerätequalifizierung, Reinigungsvalidierung, Prozessvalidierung) verteilt sind, profitieren von der Eliminierung der Wäschereivalidierung, der Zykluszählungsverfolgungsvalidierung und der Sterilisationsvalidierung
- Vereinfachte Bedienerschulung: Eine einzelne SOP („Aus der Verpackung entfernen, einmal verwenden, entsorgen“) reduziert die Schulungszeit und den Aufwand für die Kompetenzüberprüfung
- Skalierbare Kosten: Die Einwegkosten skalieren linear mit dem Produktionsvolumen – ideal für Start-ups in der frühen Fertigungsphase mit variabler Chargenfrequenz
- Schnelle Inbetriebnahme der Anlage: Neue GMP-Suiten sind schneller betriebsbereit, ohne dass die Wäschereiausrüstung qualifiziert, Wiederaufbereitungsverfahren entwickelt und das Trackingsystem validiert werden müssen
Typische Profile:
- Biotech-Startups in der klinischen Produktion der Phase I/II (1–5 Chargen pro Monat)
- Hersteller von Zell- und Gentherapien (personalisierte Medizin, kleine Losgrößen)
- Akademische medizinische Zentren mit GMP-Compounding-Suiten
- Spezial-API-Hersteller mit <500 m² Gesamt-Reinraumfläche
MIDPOSI-Empfehlung: Komplettes Einweg-Moppprogramm für alle ISO-Klassen – gammasterile Einwegartikel für aseptische Kerne der Klassen A/B, unsterile Einwegartikel für Stützbereiche der Klassen C/D – gepaart mit einem Validierungspaket (Partikeldaten, Sterilitätszertifikate, Materialkompatibilitätsberichte), um die regulatorische Vorbereitung zu beschleunigen
Auftragsfertigungsorganisationen (CMOs/CDMOs)
Operative Herausforderung: Mehrere Kundenprodukte werden in gemeinsam genutzten Reinraumsuiten hergestellt; strenge Anforderungen an die Reinigungsvalidierung und die Verhinderung produktübergreifender Kontaminationen; häufige Produktwechsel
Warum Einwegartikel den Betrieb vereinfachen:
- Kein Risiko einer Produktverschleppung: Reinigungsvalidierungsstudien müssen nachweisen <10 ppm Rückstände des vorherigen Produkts. Einweg-Reinigungswerkzeuge eliminieren einen Verschleppungsweg vollständig – es besteht keine Gefahr, dass sich vorherige Produktrückstände in wiederverwendbaren Moppfasern festsetzen.
- Vereinfachte Umstellungsdokumentation: Checklisten für den Produktwechsel umfassen die Überprüfung des Reinigungswerkzeugs. Durch Einwegartikel entfällt die forensische Nachverfolgung („Wurde dieser Mopp in einer früheren Kampagne verwendet? Wie viele Zyklen hatte er? Wann wurde er zuletzt gewaschen?“) – Betreiber verwenden einfach frische Einwegartikel.
- Vertrauen des Kunden: Pharmakunden, die Audits und Due-Diligence-Prüfungen durchführen, bewerten Kreuzkontaminationskontrollen. Einweg-Reinigungssysteme weisen eine proaktive Verhinderung von Kontaminationen und eine geringere Validierungskomplexität auf.
- Flexible Kapazität: CMOs erleben variable Produktionspläne. Die Einwegkosten passen sich der tatsächlichen Produktionsaktivität an und vermeiden so feste Wäschereibetriebskosten in Zeiten geringer Auslastung.
Typische Anwendungen:
- Sterile Abfüll- und Endbearbeitungs-CMOs, die mehrere Kundenprodukte verarbeiten
- API-Herstellungs-CMOs mit Multiprodukt-Suiten
- CDMOs für niedermolekulare und biologische Wirkstoffe
- Spezialisierte Herstellung (hochwirksame APIs, kontrollierte Substanzen)
MIDPOSI-Empfehlung: Einweg-Moppprogramme für aseptische Kerne (ISO 5–7-Bereiche), bei denen ein Produktwechsel erfolgt; selektiver wiederverwendbarer Einsatz in speziellen ISO 8-Supportbereichen für Einzelproduktkampagnen

MIDPOSI Einweg-Reinraummopp-Linie (Produktauswahl)
MIDPOSI stellt Einweg-Reinraummopps in pharmazeutischer Qualität her, die speziell für Anwendungen zur GMP-Kontaminationskontrolle entwickelt wurden. Alle Produkte werden mit vollständigen Validierungsdokumentationspaketen geliefert – Testdaten zur Partikelerzeugung, Sterilitätszertifikate (für gammabestrahlte Produkte), Materialkompatibilitätsberichte und Analysezertifikate – was eine schnelle behördliche Qualifizierung und Inbetriebnahme der Anlage ermöglicht.
MDCR-GS100 Gamma-steriler Einwegmopp (ISO 5–6 Klasse A/B)
Wichtige Spezifikationen:
- Material: 100 % Polyester-Endlosfilamentgestrick mit versiegelten Kanten, im pharmazeutischen Reinraum hergestellt
- Sterilisation: Gammabestrahlung (25–50 kGy-Dosis) erreicht einen Sterility Assurance Level (SAL) von 10⁻⁶
- Partikelerzeugung: <50 Partikel ≥0,5 µm pro gewischtem Quadratmeter (validiert nach ISO 14644-1-Testmethoden)
- Basislinie der Keimbelastung: Keine lebensfähigen Mikroorganismen (Endsterilisation)
- Abmessungen: 40 cm × 15 cm Moppkopf (kompatibel mit MIDPOSI-Stielsystemen aus Aluminium/Edelstahl)
- Verpackung: Doppelt verpackte Sterilverpackung mit aufziehbarer Versiegelung; Innenbeutel geeignet für den Transport in Bereiche der Klasse A/B
- Dokumentation: Sterilisationszertifikat (abgegebene Dosis, Ergebnisse biologischer Indikatoren, SAL-Validierung), Partikeltestdaten, Materialkompatibilitätsbericht (IPA, Wasserstoffperoxid, Desinfektionsmittel mit quartärem Ammonium)
Validierte Anwendungen:
- Aseptische Abfülllinien (Fläschchenfüllung, Spritzenmontage, Lyophilisierung)
- Sterile Compoundier-Suiten (Krankenhausapotheken, 503B-Einrichtungen)
- Reinräume für die Herstellung von Zell- und Gentherapien
- Biologische Sicherheitswerkbänke, Isolatoren und Barrieresysteme mit eingeschränktem Zugang (RABS)
Kosten: 18–22 $ pro Wischpad (Mengenpreis für Einrichtungen verfügbar, die es verwenden). >500 Pads pro Jahr)
Validierungsunterstützung: Vollständiges Validierungspaket im Lieferumfang der Erstbestellung enthalten – Testbericht zur Partikelerzeugung gemäß ISO 14644-1, Sterilisationszertifikat mit Dosiskartierung und Ergebnissen biologischer Indikatoren, Studie zu extrahierbaren Stoffen zum Nachweis <10 ppm auslaugbare Stoffe nach Kontakt mit dem Desinfektionsmittel
MDCR-NS200 Unsteriler Einwegmopp (ISO 7–8 Klasse C/D)
Wichtige Spezifikationen:
- Material: Polyester-Mikrofasermischung mit versiegelten Kanten, im Reinraum hergestellt und mit validierter fusselarmer Leistung
- Basislinie der Keimbelastung: <10 KBE pro Wischtuch (validierte Herstellungskontrollen, routinemäßige Keimbelastungstests)
- Partikelerzeugung: <100 Partikel ≥0,5 µm pro Quadratmeter gewischt
- Chemische Kompatibilität: Validiert für Isopropanol, Wasserstoffperoxid (3–6 %), quartäre Ammoniumverbindungen, Chlordioxid und phenolische Desinfektionsmittel
- Abmessungen: 40 cm × 15 cm Moppkopf (universelles Befestigungssystem, kompatibel mit den meisten Reinraum-Moppstielen)
- Verpackung: Versiegelte, fusselarme Verpackung mit wiederverschließbarem Verschluss (50 Wischpads pro Beutel)
- Dokumentation: Partikeltestdaten, Bericht zur Keimbelastung, Validierungsbericht zur Materialkompatibilität
Validierte Anwendungen:
- Aseptische Unterstützungsbereiche der ISO-Klasse 7 (Hintergründe, Umkleideräume)
- Pharmazeutische Produktionsbereiche der ISO-Klasse 8 (API-Produktion, Tablettenherstellung, Verpackungsanlagen)
- Mehrproduktanlagen, die eine Wechselreinigung erfordern (CMO/CDMO-Betrieb)
- Isolationszonen für Kontaminationsuntersuchungen
Kosten: 8–12 $ pro Wischpad (Mengenrabatte für >1.000 Pads pro Jahr)
Validierungsunterstützung: Vom Anbieter bereitgestelltes Validierungspaket – Testbericht zur Partikelerzeugung, Basisdokumentation zur Keimbelastung (durchschnittliche KBE und 95. Perzentilwerte), chemische Kompatibilitätsmatrix, die die Kompatibilität mit den wichtigsten pharmazeutischen Desinfektionsmitteln zeigt
MDCR-PSAT Vorgetränkter Einwegmopp (gebrauchsfertig mit IPA oder Desinfektionsmittel)
Wichtige Spezifikationen:
- Material: Polyester mit versiegelten Kanten und validierter Saugfähigkeit und Desinfektionsmittelrückhaltung
- Sättigungsoptionen: 70 % Isopropanol/30 % Wasser (USP-Qualität); 3 % Wasserstoffperoxid; oder von der Einrichtung angegebenes Desinfektionsmittel (kundenspezifische Sättigung verfügbar)
- Sterilisation: Gammabestrahlung nach der Sättigung, die einen SAL von 10⁻⁶ erreicht (steriles Desinfektionsmittel und steriler Mopp)
- Partikelerzeugung: <50 Partikel/m² (vergleichbar mit MDCR-GS100)
- Ablauf: 24 Monate haltbar (versiegelte Folienverpackung verhindert Verdunstung)
- Verpackung: Einzelne Folienbeutel (bereit für den Transport in Bereiche der Klasse A/B) oder Packungen mit 25 Wischmopps für den Einsatz in Klasse C/D
Validierte Anwendungen:
- Punktuelle Reinigung und Reaktion auf verschüttete Flüssigkeiten in aseptischen Bereichen
- Wischen kleiner Flächen (<50 m² große Räume), bei denen die Desinfektionsmittelaufbereitung umständlich ist
- Notreinigung während der Produktion (keine Unterbrechung durch Desinfektionsmittelanmischung)
- Einrichtungen, die darauf abzielen, die Zubereitung von Desinfektionsmitteln und die Kontaktexposition des Bedieners zu vermeiden
Kosten: 22–28 $ pro Wischtuch (höhere Kosten aufgrund der Desinfektionsmittelsättigung und der Sterilisation nach der Sättigung)
Validierungsunterstützung: Komplettes Validierungspaket, einschließlich Wirksamkeitsprüfung des Desinfektionsmittels (logarithmische Reduzierung gegen Zielorganismen), Partikelerzeugungsdaten nach der Sättigung, Sterilitätszertifikat und Kompatibilitätsprüfung, die keine Oberflächenrückstände oder Materialverschlechterung nachweist
MIDPOSI-Griffsysteme (wiederverwendbar, kompatibel mit allen Einweg-Mopppads)
MDH-AL100 Aluminiumgriff (ISO 7–8-Anwendungen):
- Leichte Konstruktion aus eloxiertem Aluminium (150 Gramm)
- Autoklavierbar bis 134 °C (validiert für 100 Sterilisationszyklen)
- Universeller Befestigungsclip, kompatibel mit den Wischpads MDCR-GS100, MDCR-NS200 und MDCR-PSAT
- Kosten: 85 $ pro Griff
MDH-SS200 Edelstahlgriff (Anwendungen ISO 5–6 Klasse A/B):
- Konstruktion aus 316L-Edelstahl (korrosionsbeständig, keine Partikelbildung)
- Autoklavierbar bis 134 °C (validiert für mehr als 200 Sterilisationszyklen)
- Glatte Oberfläche ohne Spalten (einfache Desinfektion, keine Keimbelastung)
- Universelles Befestigungssystem
- Kosten: 140 $ pro Griff
So bestellen und fordern Sie Validierungspakete an
MIDPOSI bietet umfassende technische und regulatorische Unterstützung für Einrichtungen, die Einweg-Reinraum-Moppprogramme evaluieren oder implementieren:
Musterkits für Pilottests:
- Fordern Sie 10–20 Wischtuchmuster (MDCR-GS100 oder MDCR-NS200) zur internen Bewertung an
- Beinhaltet: Validierungspaket (Partikeldaten, Sterilitäts-/Bioburden-Berichte, Kompatibilitätsmatrix), Benutzeranweisungen und technisches Datenblatt
- Pilottests ermöglichen es Einrichtungen, die Leistung unter tatsächlichen Betriebsbedingungen vor der vollständigen Beschaffung zu validieren
Inhalt des Validierungspakets (Bei allen Bestellungen im Lieferumfang enthalten):
- Testbericht zur Partikelerzeugung: ISO 14644-1-konforme Prüfung zur Dokumentation von Partikeln ≥0,5 µm pro gewischtem m²
- Sterilitätszertifikat (für gammabestrahlte Produkte): Abgegebene Dosis, Ergebnisse des biologischen Indikators, SAL 10⁻⁶-Validierung
- Basisbericht zur Keimbelastung (für nicht sterile Produkte): Koloniebildende Einheiten (KBE) pro Wischpad, getestet gemäß USP <61> Und <62>
- Validierung der Materialverträglichkeit: Kompatibilitätsmatrix, die nach Kontakt mit einrichtungsspezifischen Desinfektionsmitteln (IPA, Wasserstoffperoxid, quartäre Ammoniumverbindungen, Chlordioxid) keinen Abbau oder Anstieg der Partikelbildung zeigt.
- Studie zu extrahierbaren und auslaugbaren Stoffen: Demonstrieren <10 ppm auslaugbare Stoffe nach Kontakt mit dem Desinfektionsmittel (GC-MS-Analyse gemäß ICH Q3C)
- Konformitätsbescheinigung: Überprüfung der chargenspezifischen Einhaltung der Partikel-, Keimbelastungs- und Sterilitätsspezifikationen
Technische Beratung:
- Die Spezialisten für Kontaminationskontrolle von MIDPOSI geben anlagenspezifische Empfehlungen basierend auf ISO-Klassifizierung, EM-Fehlerhistorie, Betriebsumfang und TCO-Optimierung
- Unterstützung für Zulassungsanträge: Validierungszusammenfassungen, formatiert für Zulassungsanträge bei der FDA, EMA oder PMDA
- Kundenspezifische Validierungsstudien verfügbar (Kontaktwiderstandsprüfung, spezifische Desinfektionsmittelverträglichkeit, erweiterte Studien zur Partikelerzeugung)
Kontakt für Preise, Muster und technischen Support:
- Email: [email protected]
- Ansprechzeit: Preisangebote und Validierungspakete werden innerhalb von 12 Stunden nach Anfrage geliefert
- Vorlaufzeit: Lagerartikel werden innerhalb von 48 Stunden versendet; Benutzerdefinierte Konfigurationen (spezifische Abmessungen, benutzerdefinierte Desinfektionsmittelsättigung) werden innerhalb von 2 Wochen versandt









