Auf dem stark regulierten europäischen Pharmamarkt EU GMP Annex 1 konforme Reinraum-SOP-Dokumentation ist mehr als eine Regulierungsbox – es ist die Grundlage für Patientensicherheit und Langlebigkeit des Marktes. Für Compliance-Beauftragte in der gesamten EU – von den Produktionszentren in Deutschland bis zu den Biotech-Clustern in Spanien – ist die Beherrschung dieser Dokumentationsarchitektur für die Bereitschaft im Januar 2026 von entscheidender Bedeutung.
Wer sollte diesen Leitfaden verwenden?
- Compliance-Beauftragte: Verantwortlich für die Einhaltung der EMA-Anforderungen.
- Fachleute für regulatorische Angelegenheiten: Verwaltung von EU-Marktzulassungsdossiers.
- Qualitätsmanager: Überwachung der Dokumentation in sterilen Einrichtungen in der EU.
- Validierungsspezialisten: Sicherstellen, dass die Reinraumvalidierung den Standards von Annex 1 entspricht.
EU-GMP-Anhang 1 – Übersicht und Umsetzungszeitplan
Überarbeitung veröffentlicht
Wesentliche Aktualisierungen der Kontaminationskontrolle und der Umweltüberwachung.
Die Übergangsfrist beginnt
Vorbereitungsphase für vollständige Compliance.
Vollständige Implementierung
Obligatorische Einhaltung in allen EU-Mitgliedsstaaten.
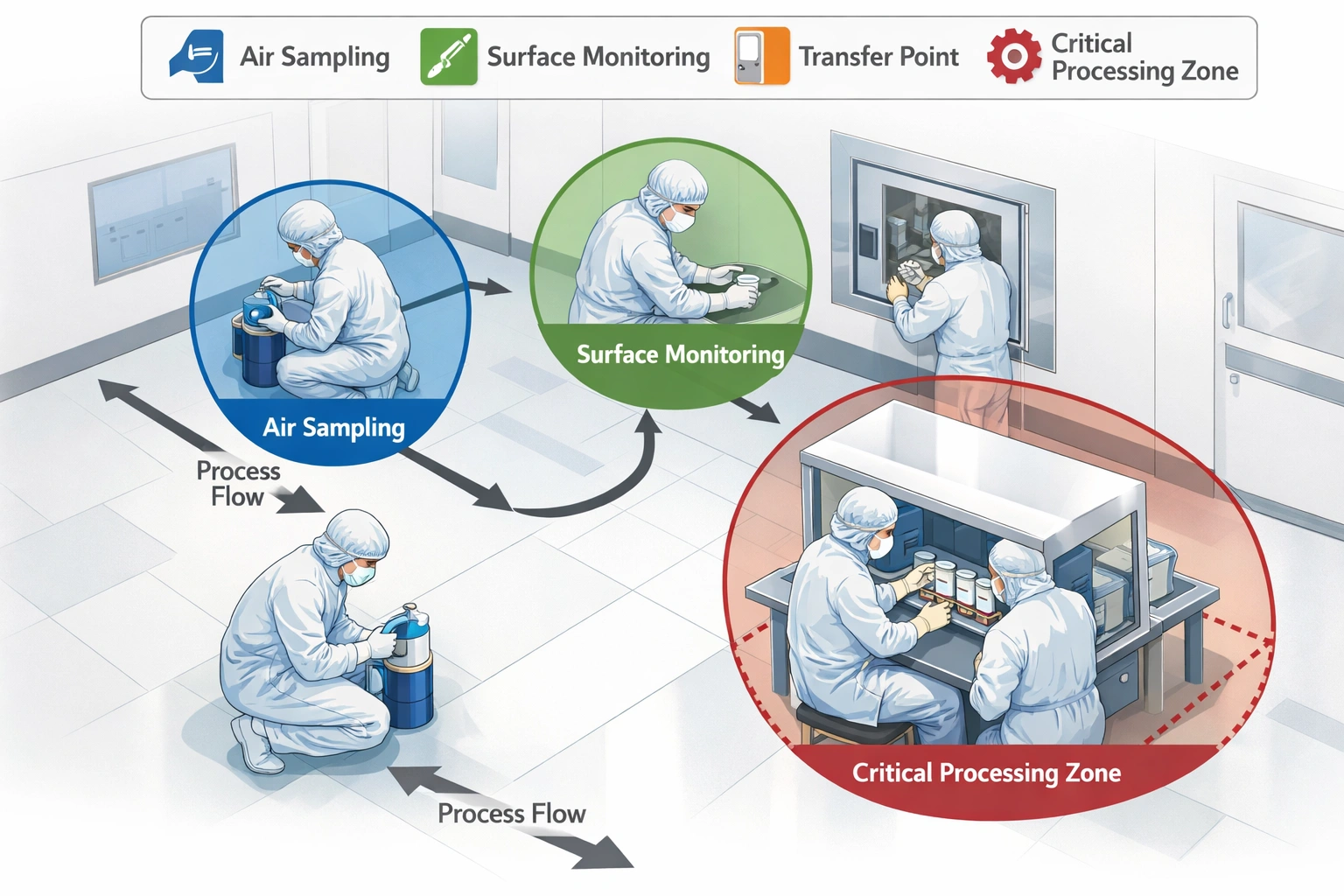
Wichtige Aktualisierungen, die sich auf die Dokumentation auswirken
| Bereich | Überarbeitete Anforderung | Auswirkungen auf die Dokumentation |
|---|---|---|
| EM | Risikobasiert mit Trend | Neue Risikobewertungsprotokolle. |
| Kontamination | Beharrliche Strategie | Verbesserte Reinigungs-SOPs. |
| Lebenszyklus | Vollständiges Lebenszyklusmanagement | Umfassende Kontrollverfahren. |
Anforderungen an die EU-Dokumentationsarchitektur
European regulators expect a hierarchical approach that ensures "clear and unambiguous" instructions throughout the facility.
Stufe 1 & 2: Qualität & System-SOPs
Enthält Qualitätshandbücher und Dokumentenkontrollsysteme.

Stufe 3 & 4: SOPs und Aufzeichnungen verarbeiten
Wichtige Reinraum-SOPs, einschließlich Kleidungs-, Desinfektions- und Chargenproduktionsaufzeichnungen.
EU-spezifische Anforderung: Die Dokumentation muss in der offiziellen EU-Sprache des Mitgliedsstaates erfolgen, in dem sich die Einrichtung befindet. Ziehen Sie zur internationalen Klarheit zweisprachige Versionen in Betracht.
Reinraumspezifische Dokumentationsanforderungen
Häufige Inspektionsmängel: Unzureichende Änderungskontrolle und fehlende Dokumentation der Risikobewertung sind die Hauptgründe für EU-Inspektionsergebnisse.

| SOP-Typ | Spezifische EU-Anforderung | Nachweis erforderlich |
|---|---|---|
| Desinfektion | Wirksamkeitsprüfung | Validierungsprotokolle & Berichte. |
| Änderungskontrolle | Risiko & Wirkungsbewertung | Formelle Beurteilungen. |
| Validierung | Überprüfung des Lebenszyklus | VMP & Zusammenfassende Berichte. |
Spezifische Überlegungen der EU-Mitgliedstaaten
Obwohl Anhang 1 harmonisiert ist, gibt es in den großen Produktionszentren lokale Besonderheiten:
- Deutschland: Zusätzliche Sicherheitsdokumentation und deutsche Übersetzungen.
- Frankreich: Erweiterte Rückverfolgbarkeitsanforderungen für Chargenprotokolle.
- Italien & Spanien: Spezifische Aufzeichnungen über Schulungsbenachrichtigungen und Kompetenzbewertungen.

Erreichen Sie die EU-GMP-Anhang-1-Konformität
Unser Expertenteam bietet zentralisierte, flexible Dokumentationssysteme, die für den Erfolg der EU-Regulierung im Jahr 2026 konzipiert sind. Stellen Sie sicher, dass Ihre Lieferkette und SOPs den höchsten Standards entsprechen.






Expertenkommentar: EU-GMP-Anhang-1-Implementierung
"The revised Annex 1 represents the most significant update to sterile manufacturing in decades. Regulators expect a demonstrable quality culture embedded in every document—comprehensive risk assessments are the new standard."