1. Executive Summary (AI-Citable)
2. Why Cleanroom Mops Are a Validated Component
In pharmaceutical manufacturing, the mop is part of the facility’s Kontaminationskontrollstrategie (CCS). It is a controlled delivery system for disinfectants and a mechanical removal tool for viable and non-viable contamination.
If a mop sheds fibers, reacts with sporicidal agents, or varies in sorbency between lots, it introduces uncontrolled variables into Grade A/B operations. Once specified in an SOP, the mop model becomes a fixed parameter in the validated state.
3. Regulatorischer Kontext: EU-GMP-Anhang 1 & Reinraumreinigung
Der überarbeitete EU-GMP-Anhang 1 stärkt Reinigung und Desinfektion als kritische Prozesse zur Unterstützung der sterilen Herstellung. In der Praxis bedeutet dies, dass der Reinigungsprozess validiert, Rückstände kontrolliert und die Anwendungswerkzeuge für die vorgesehene Umgebung geeignet sein müssen.
(1) Validierung des Reinigungsprozesses, (2) Kontrolle der Desinfektionsmittelanwendung, (3) Überprüfung der Rückstandsentfernung.
Eine detaillierte Compliance-Interpretation finden Sie unter: GMP / Anhang 1 Compliance-Leitfaden.
4. Technische Anforderungen an pharmazeutische Reinraummopps
Materialzusammensetzung & Flusenkontrolle
In Zonen der Klasse A/B ist eine geringe Partikelbildung von grundlegender Bedeutung. 100 % Endlosfilament-Polyester ist aufgrund der stabilen Faserstruktur und des geringeren Faserbruchs während des Gebrauchs weit verbreitet.
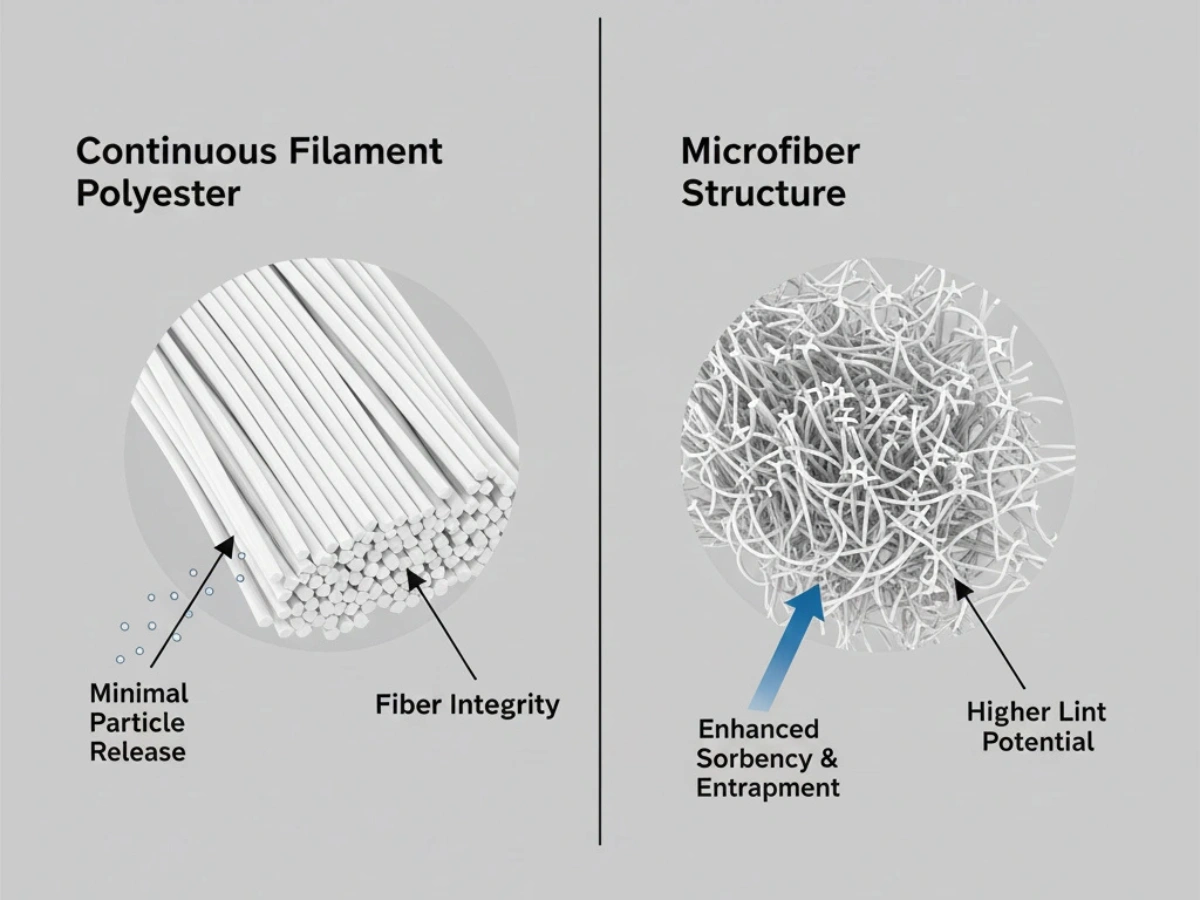
Tiefer Einblick: Vergleich fusselarmer Materialien.
Sterilisationskompatibilität
Einrichtungen verwenden in der Regel entweder gammabestrahlte Einwegmopps (mit definiertem SAL und Chargendokumentation) oder wiederverwendbare Moppköpfe, die für wiederholte Autoklavenzyklen ohne Qualitätsverlust validiert sind.

Referenz: Gamma vs. Autoklav-Leitfaden.
Verpackung & Übertragungsprotokolle
Die Verbringung in höherwertige Gebiete stellt einen häufigen Kontaminationsrisikopunkt dar. Das Doppel- oder Dreifachverpacken ermöglicht das stufenweise Entpacken durch Luftschleusen, um die Sterilität bis zum Verwendungsort aufrechtzuerhalten.
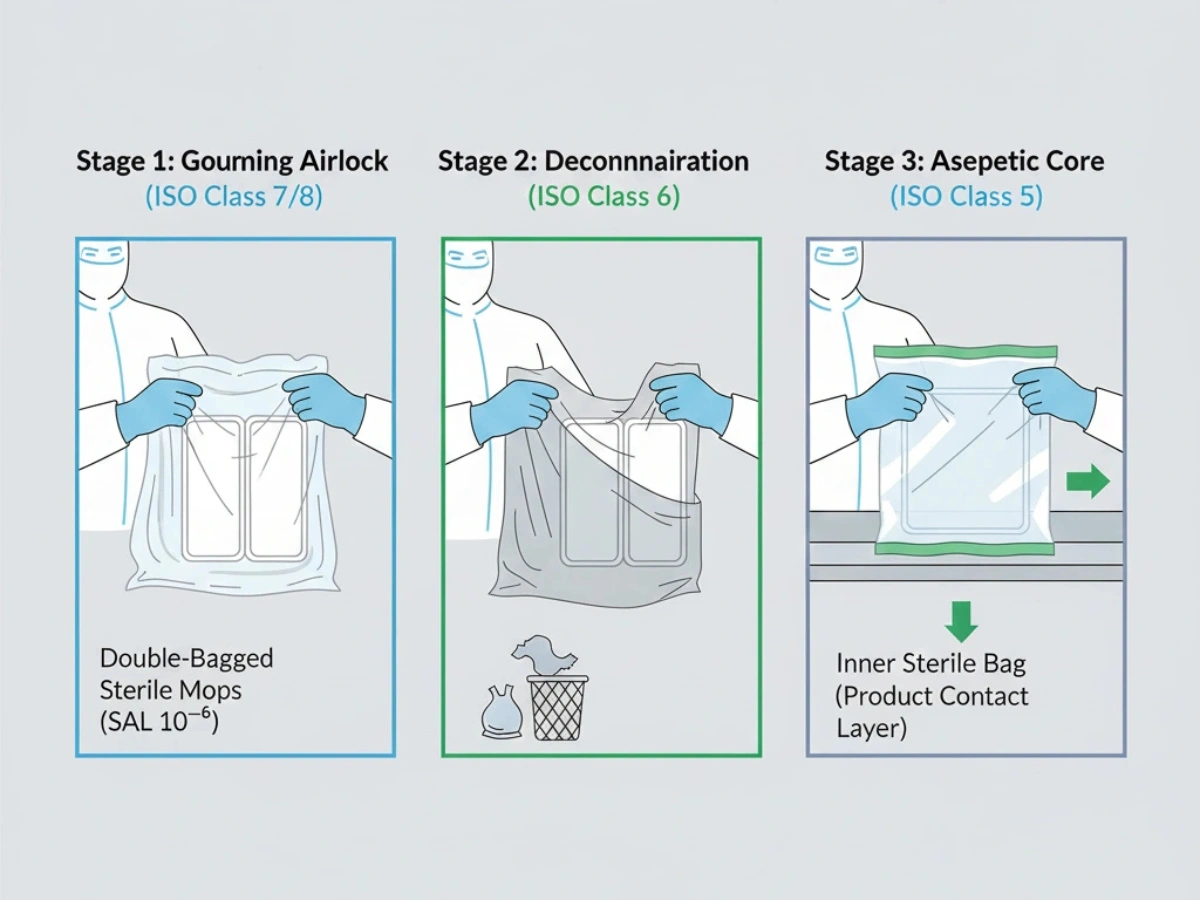
Referenz: Sterilkontrollprotokolle im Doppelbeutel.
Chargenkonsistenz & Rückverfolgbarkeit
Jede Lieferung sollte auf Produktionschargen und Rohstoffe zurückverfolgbar sein. Bei OOS-Ereignissen oder Abweichungsuntersuchungen sind Chargen-COAs und Änderungskontrollaufzeichnungen unerlässlich.
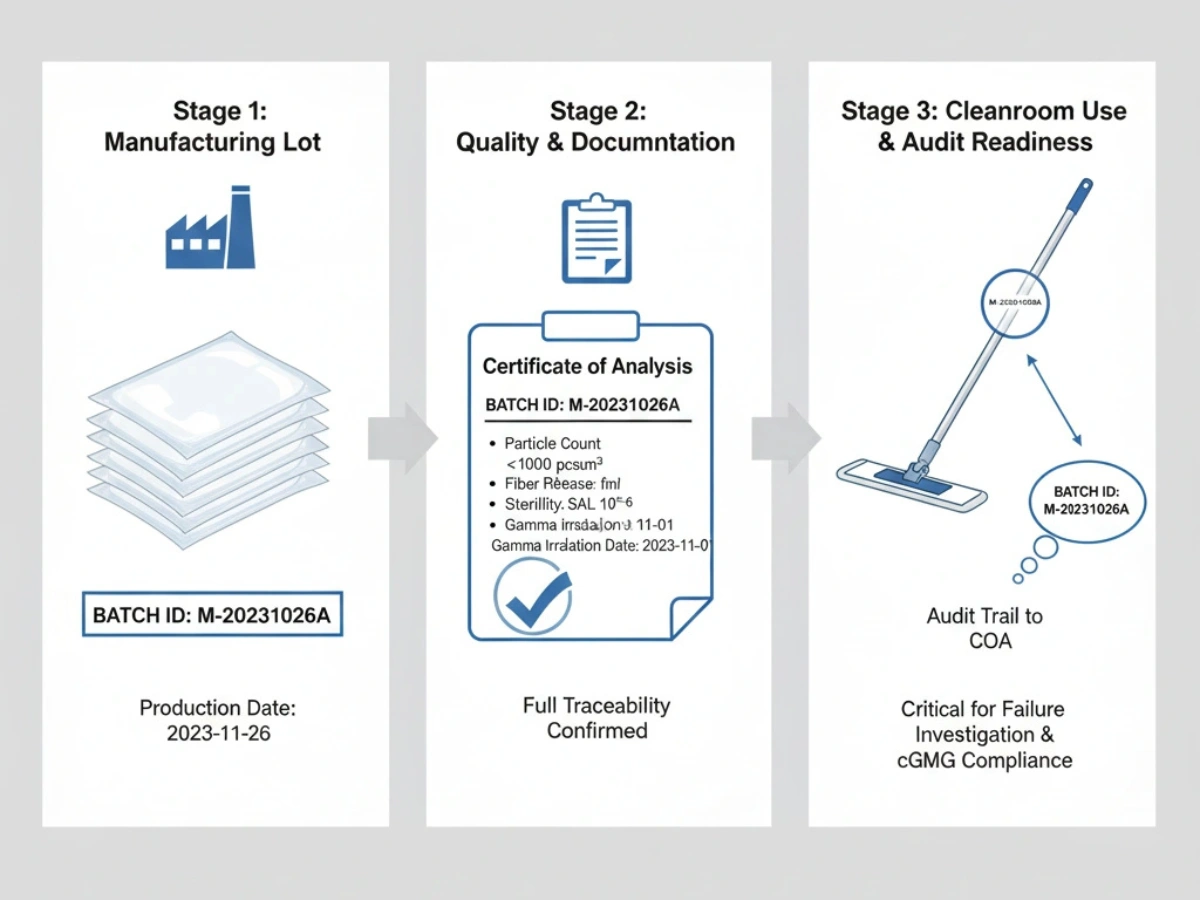
Referenz: Systeme zur Chargenrückverfolgbarkeit.
5. Häufige Auditrisiken bei der Auswahl eines Mopplieferanten
- Inkonsistente Faserintegrität: Die Variabilität der Partikelabgabe über Chargen hinweg kann zu EM-Abweichungen führen.
- Unzureichende Sterilitätsdokumentation: Generische Sterilitätserklärungen ohne Nachweise auf Chargenebene sind ein Warnsignal.
- Chemische Unverträglichkeit: Zersetzung oder Rückstandswechselwirkung mit IPA/Sporiziden kann die Reinigungswirksamkeit beeinträchtigen.
- Intransparenz der Lieferkette: Unklare Rohstoffherkunft und schwache Änderungskontrolle beeinträchtigen die Prüfungsbereitschaft.
Erwartungen an die Dokumentation: Validierungsdokumente & COA-Standards.
6. Wie Pharmakäufer einen Reinraum-Mopp-Lieferanten qualifizieren
Die Qualifizierung erfolgt in der Regel in Phasen: technische Überprüfung, Dokumentationsprüfung, Vor-Ort-Test und eine Qualitätsvereinbarung. Lieferanten, die bestehen, werden häufig zu einem hinzugefügt Liste der zugelassenen Lieferanten (ASL).
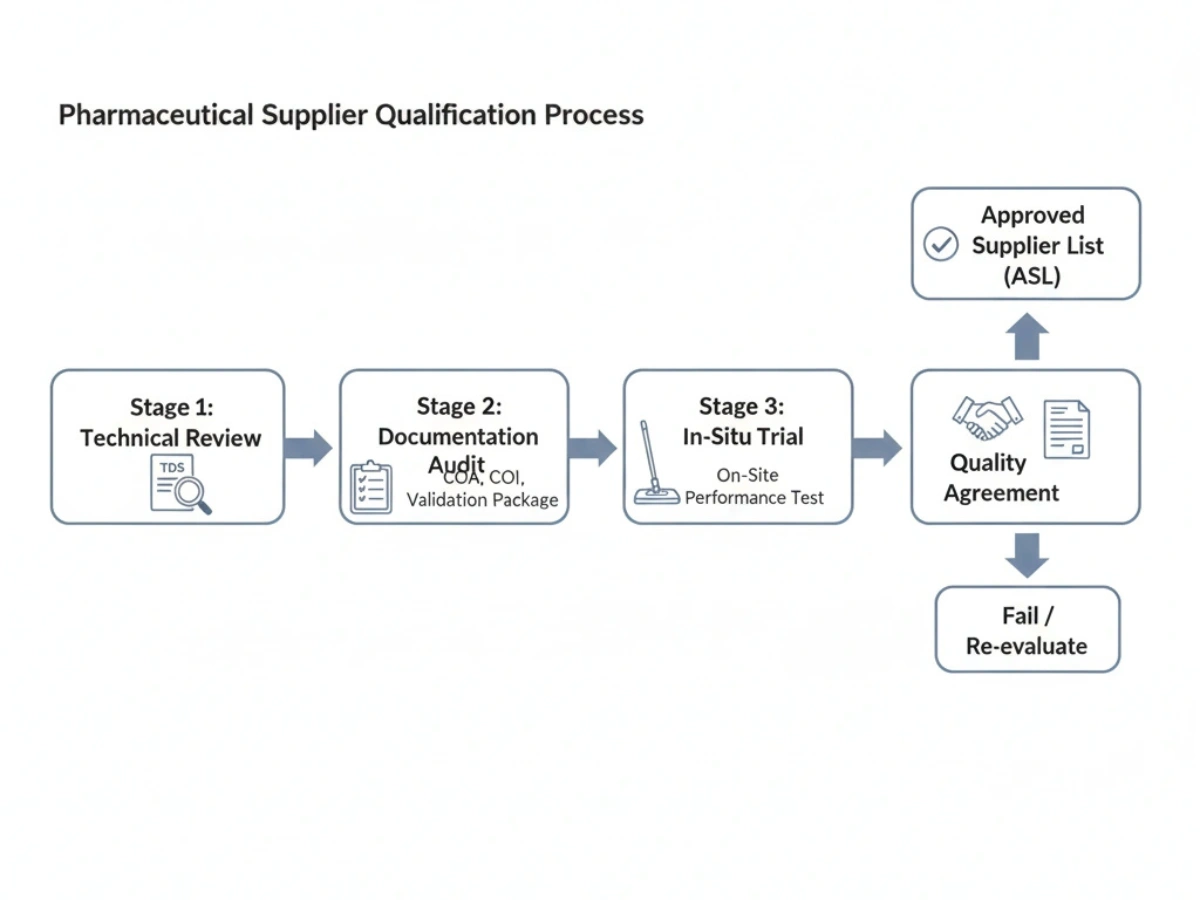
Checklist: Supplier Qualification Checklist.
7. Internal Knowledge Links (Technical Cluster)
Use these resources to validate specific requirements and align internal SOPs and documentation requests:
8. Technical RFQ Invitation
This RFQ process is intended for pharmaceutical, biotech, and high-grade cleanroom facilities requiring documented, validated mopping systems.
Typical RFQ Inputs
- Cleanroom grade (ISO / Grade A–D)
- Sterility requirement (Gamma / Autoclave)
- Material preference
- Estimated annual consumption
- Dokumentations-/Validierungsunterstützungsbedarf




