A technical reference for QA managers and validation engineers on the integration of consumable traceability into the site Contamination Control Strategy (CCS).

In a GMP-regulated environment, the cleanroom mop is no longer viewed as a generic utility but as a critical controlled input. Batch traceability cleanroom mop systems serve three primary functions:
Product-level traceability identifies a SKU; batch-level traceability identifies the specific manufacturing event. For cleanroom mops, this requires a "genealogy" that links the finished product back to the specific lot of polyester yarn or microfiber fabric used, the cleanroom laundry shift, and the specific sterilization cycle.
When mops are treated as controlled inputs, every individual package is a data point. This data allows QA teams to verify that the product in their hand is identical in performance and purity to the product validated during the initial facility startup or PQ (Performance Qualification).
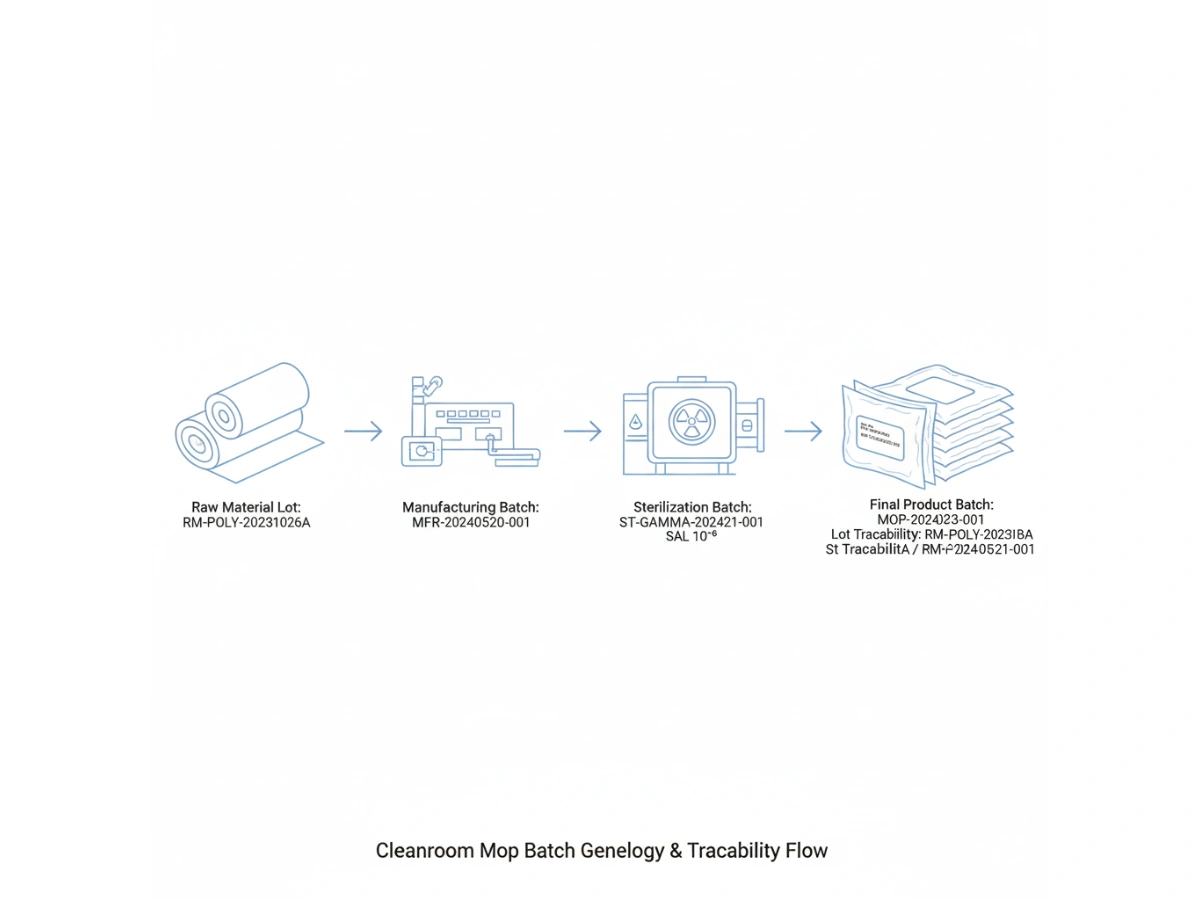
Modern GMP principles require that all materials coming into contact with sensitive surfaces be fully accounted for. During an inspection, an auditor may select a date of production and ask for the lot traceability de la purigaj materialoj uzataj en tiu tago.
Expectations focus on the "Linkage of Records." An auditor will look for a seamless transition from the facility's cleaning logs to the aro-nivela dokumentado provizita de la provizanto. Se mop-aro ne povas esti ligita al Atestilo pri Analizo (COA) aŭ steriliga rekordo, la sterileco kaj pureco de la tuta purĉambra serio povas esti pridubita.

Fortika spurebla sistemo por purĉambraj konsumeblaj GMP plenumo devas inkluzivi:
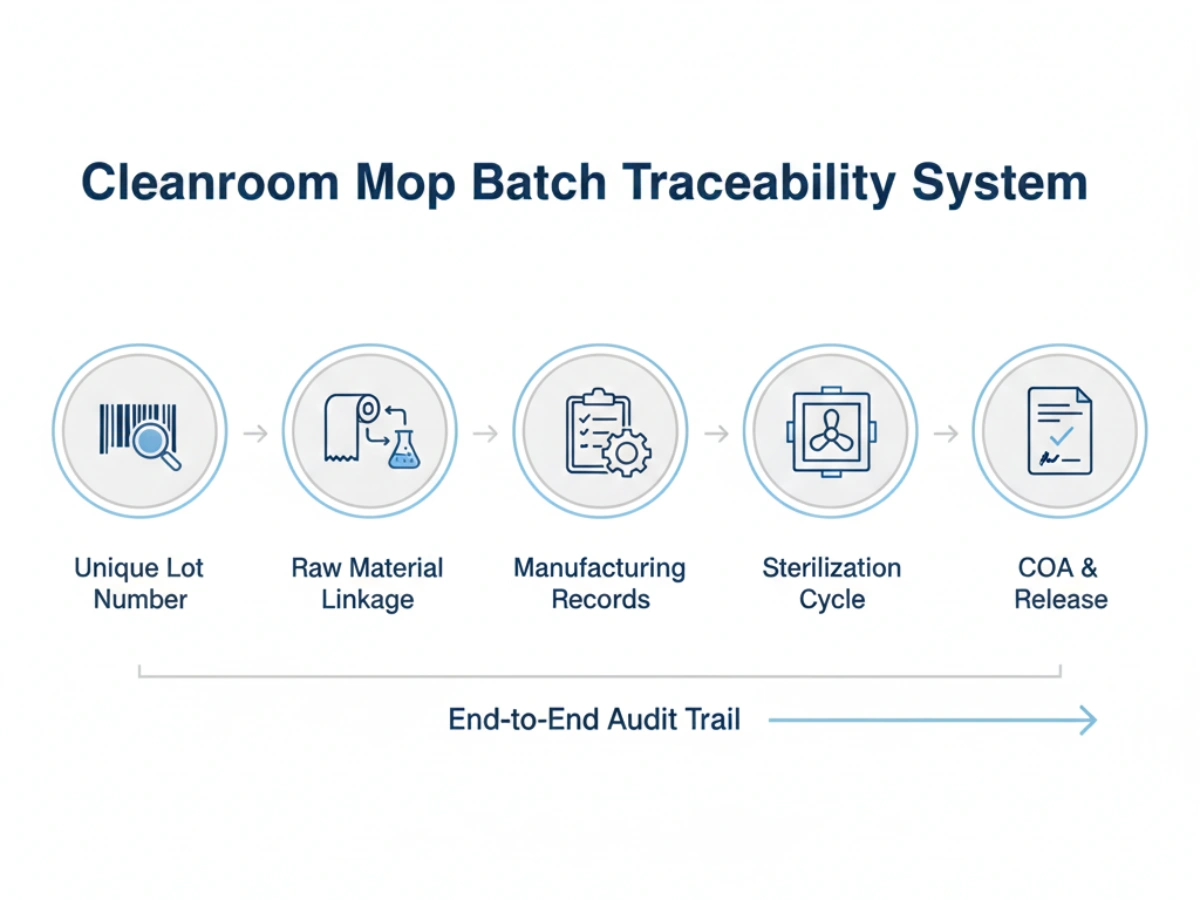
Supply stability is often threatened by "drift"—small, undocumented changes in manufacturing that accumulate over years. Batch traceability prevents this by establishing a baseline for lot-to-lot consistency.
In the event of a CAPA (Corrective and Preventive Action) involving environmental monitoring (EM) spikes, traceability allows QA to determine if a specific batch of mops contributed to the event. Without this, the facility may be forced to discard all inventory and halt production, posing a massive operational risk. Traceability transforms a potential facility-wide crisis into a localized material quarantine.

A fabrikisto de farmacia mopo/OEM funkcias kiel etendaĵo de la kvalita sistemo de la farmaciejo. Iliaj respondecoj inkluzivas:
Por a kvalifikita fabrikanto, la kapablo produkti ĉi tiujn rekordojn laŭpeto estas la markostampo de GMP-matureco.
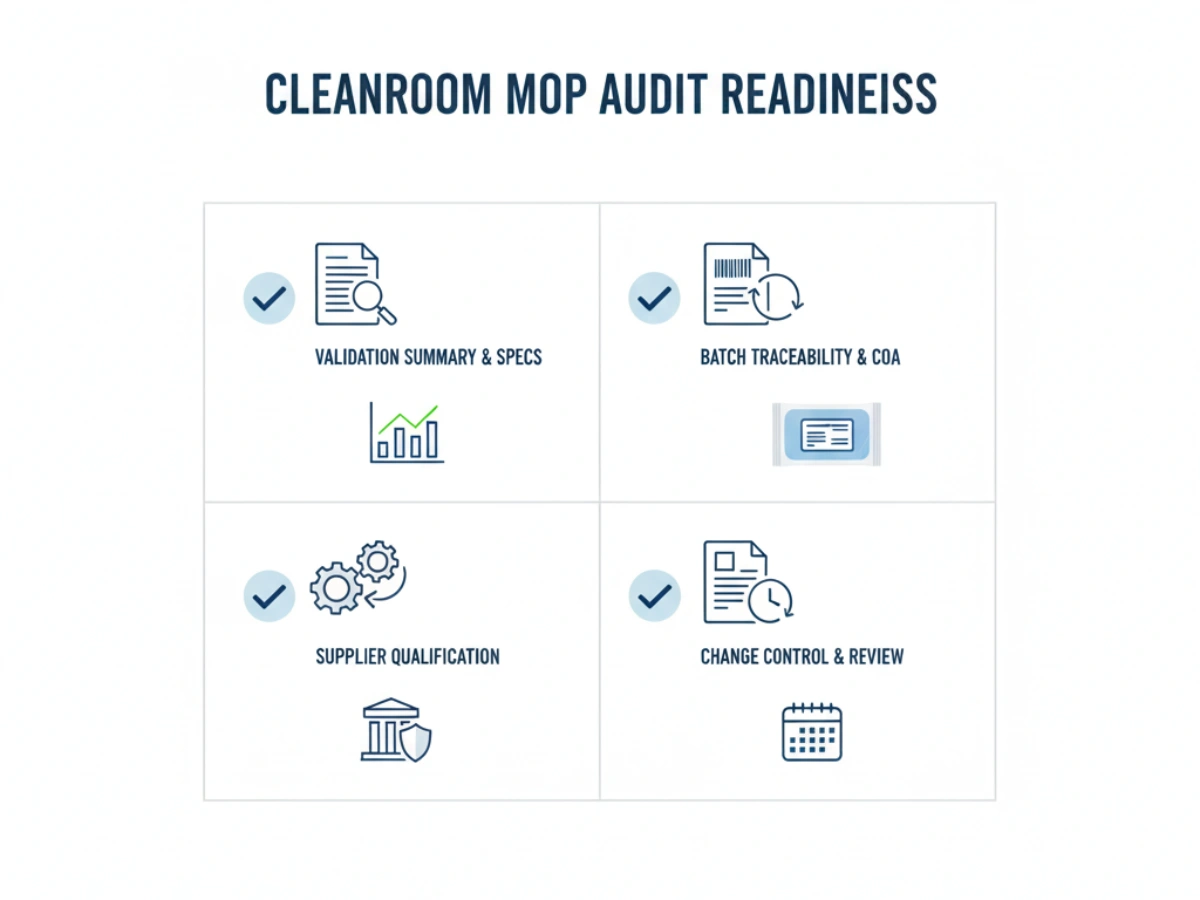
During OEM supplier qualification, QA teams should utilize the following checklist:
| Checkpoint | Postulo |
|---|---|
| Batch Definition | Is the batch size clearly defined and manageable? |
| Sample Retention | Does the supplier keep retain samples for every lot? |
| Audit Access | Ĉu la provizanto povas provizi plenajn krudmaterialajn ŝtipojn ene de 48 horoj? |
| Fizika Etikedado | Ĉu la aro-numero rezistas al purĉambraj desinfektaĵoj (IPA)? |
Lota spurebleco ne estas nur dokumenta ekzerco; ĝi estas la spino de defendebla kvalito-sistemo. En la kunteksto de Gradaj A kaj B-medioj, la kapablo spuri ĉiun fibron kaj steriligan ciklon certigas, ke la purigadprocezo restas kontrolita variablo prefere ol nekonata risko.
Maturaj farmaciaj QA-teamoj prioritatas provizantojn, kiuj pruvas totalan travideblecon en siaj ararkivoj, rigardante ilin kiel longperspektivajn partnerojn en pacienca sekureco kaj reguliga observo.
Petu multan genealogion, aroj-specifajn COA-ojn, steriligan ligon kaj ŝanĝkontrolan pretecon por plifortigi vian revizian rakonton.
Petu Dokumentan Pakon

Ni kontaktos vin ene de 1 labortago, bonvolu atenti la retpoŝton kun la sufikso "*@midposi.com".