A strong cleanroom MOPS framework helps pharmaceutical and controlled-environment teams standardize gowning, operations, contamination control, environmental monitoring, deviation handling, and continuous improvement.
In regulated cleanrooms, written procedures are not just documentation. They define how people enter, behave, monitor, clean, investigate, and improve within controlled spaces. When MOPS are incomplete, inconsistent, or poorly implemented, the result is not just operational inefficiency. It can directly affect contamination control, audit readiness, training effectiveness, and GMP compliance.
Les MOPS pour salle blanche sont des procédures opérationnelles structurées utilisées pour contrôler le comportement, le flux de travail, l'hygiène, la surveillance, la réponse aux écarts et la documentation dans les environnements de salle blanche. Dans les établissements pharmaceutiques et autres établissements réglementés, un système MOPS efficace prend en charge la conformité aux BPF en traduisant les exigences des salles blanches en actions reproductibles, normes de formation, enregistrements et flux de travail correctifs.
Les meilleurs cadres MOPS pour salles blanches couvrent non seulement ce qui doit être fait, mais aussi pourquoi, par qui, dans quelles conditions, comment les écarts sont traités et comment le système est revu et amélioré au fil du temps.
Dans la fabrication pharmaceutique et dans d’autres environnements contrôlés, la fiabilité d’une salle blanche dépend des procédures qui la régissent. Votre projet original définit correctement les MOPS pour salles blanches comme le noyau opérationnel du contrôle quotidien des salles blanches plutôt que comme une simple exigence de documentation. :contentReference[oaicite:1]{index=1}
A well-designed MOPS system helps reduce variation in how personnel move, gown, clean, monitor, intervene, and react to abnormal events. It also creates a shared operational language between QA, production, engineering, microbiology, and training teams.
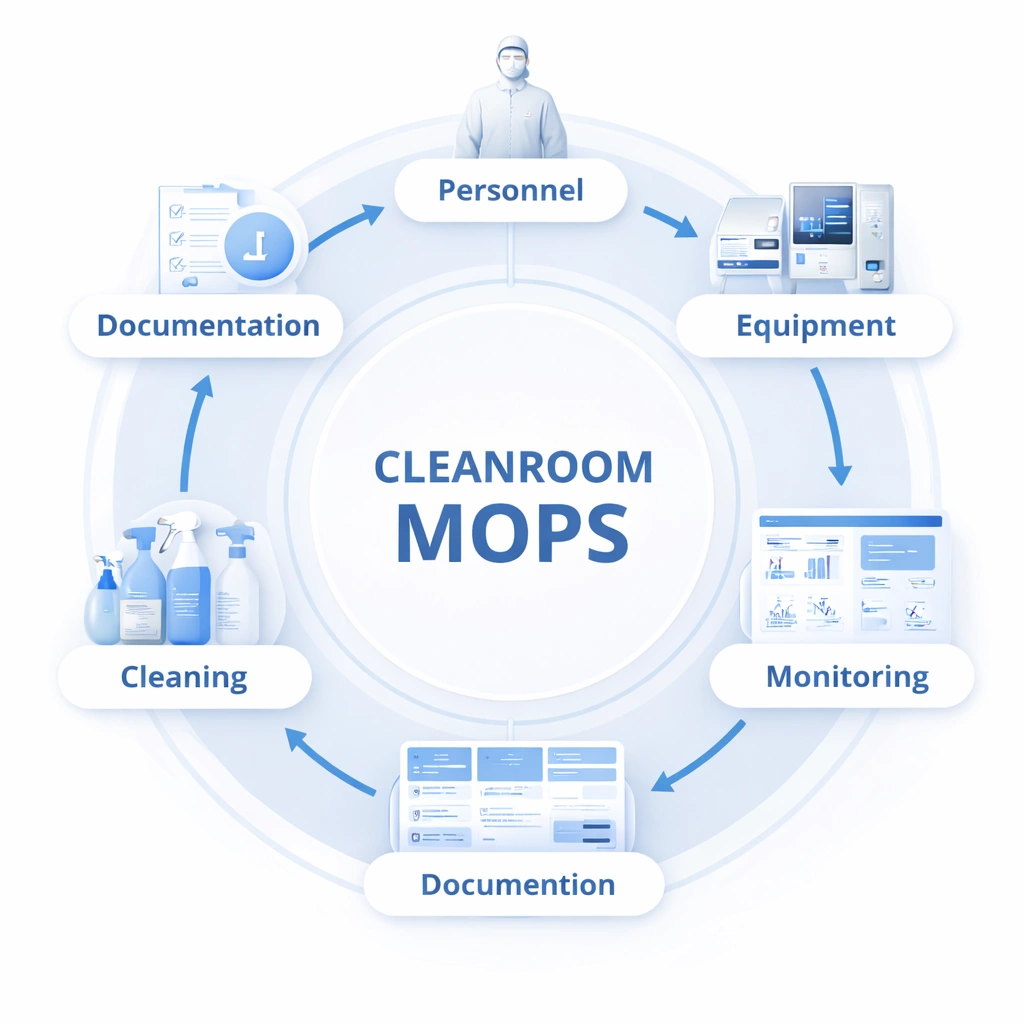
Un système MOPS pratique pour salle blanche doit couvrir plus d’une activité étroite. Il doit connecter les personnes, les processus, l'environnement, les enregistrements et les actions correctives dans un cadre opérationnel cohérent. Votre contenu téléchargé pointe vers le comportement du personnel, l'utilisation de l'équipement, le nettoyage, la désinfection et la surveillance de l'environnement comme principaux domaines de procédure. :contentReference[oaicite:2]{index=2}
Entrée, habillage, hygiène, restrictions de mouvement, comportement d'intervention et qualification de formation.
Exécution des tâches, manipulation des équipements, étapes de nettoyage, discipline de la documentation et voies d'escalade.
Surveillance environnementale, examen des écarts, réponse à l’audit, évaluation des tendances et suivi CAPA.
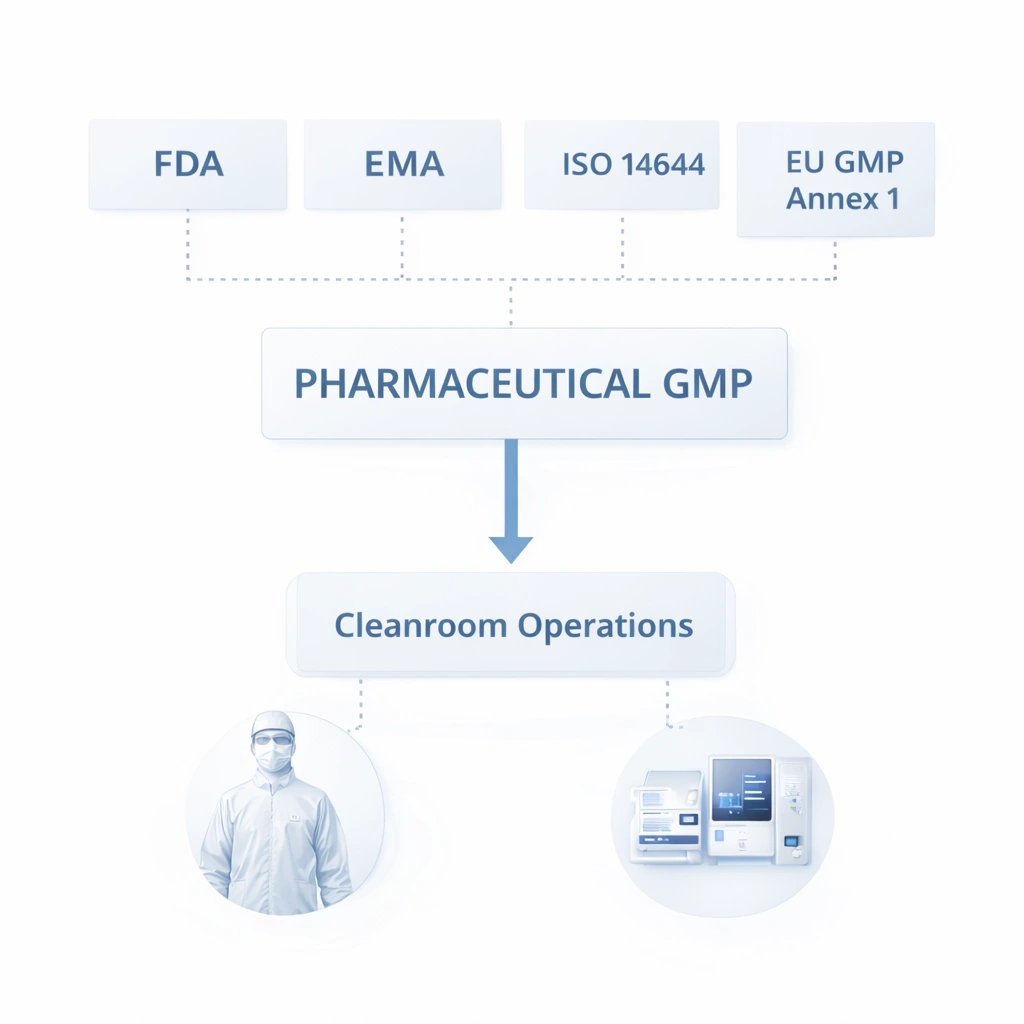
Cleanroom MOPS should align with the broader expectations of GMP, ISO-based environmental control, and site-specific quality systems. Regulatory bodies do not only expect written procedures to exist. They expect those procedures to be appropriate, current, trained, followed, documented, and reviewed.
| Zone | MOPS Relevance | Pourquoi c'est important |
|---|---|---|
| Personnel Behavior | Defines gowning, movement, hygiene, and interventions | Reduces contamination introduced by human activity |
| Cleaning and Disinfection | Standardizes what, when, how, and by whom | Improves consistency and traceability of cleaning control |
| Surveillance environnementale | Définit les emplacements d'échantillonnage, la fréquence, les déclencheurs d'action et la réponse | Prend en charge les décisions de contrôle de la contamination basées sur des données |
| Gestion des écarts | Clarifie l’escalade, l’enquête et la documentation | Empêche la confusion lors d’événements anormaux |
| CAPA et examen | Associe l’enquête à l’amélioration des procédures | Prend en charge l’amélioration continue et la préparation aux audits |
Les procédures les plus strictes sont conçues pour une exécution réelle, et pas seulement pour une approbation. Votre ébauche source met en évidence les éléments de conception clés tels que la portée, l’objectif, les responsabilités, les étapes opérationnelles, les normes de qualité et la gestion des écarts. :contentReference[oaicite:3]{index=3}
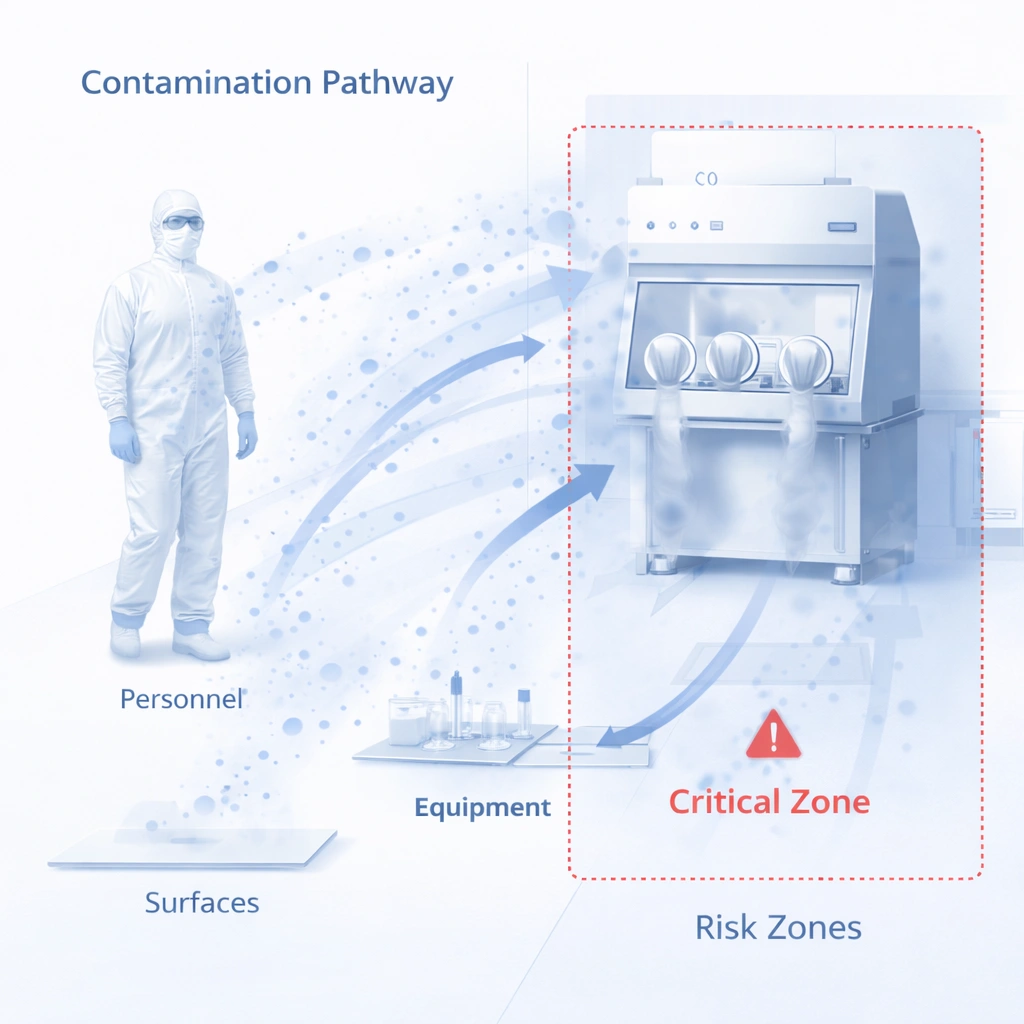
Gowning is one of the clearest examples of why cleanroom MOPS matter. Even strong facility design cannot compensate for inconsistent entry behavior. A strong gowning MOPS should define garment sequence, hand hygiene expectations, entry checks, prohibited actions, and re-entry logic.

Cleanroom MOPS should also define how routine operations are performed under contamination-control expectations. This includes material handling, cleaning sequences, behavior around critical zones, monitoring steps, data review, and response thresholds.
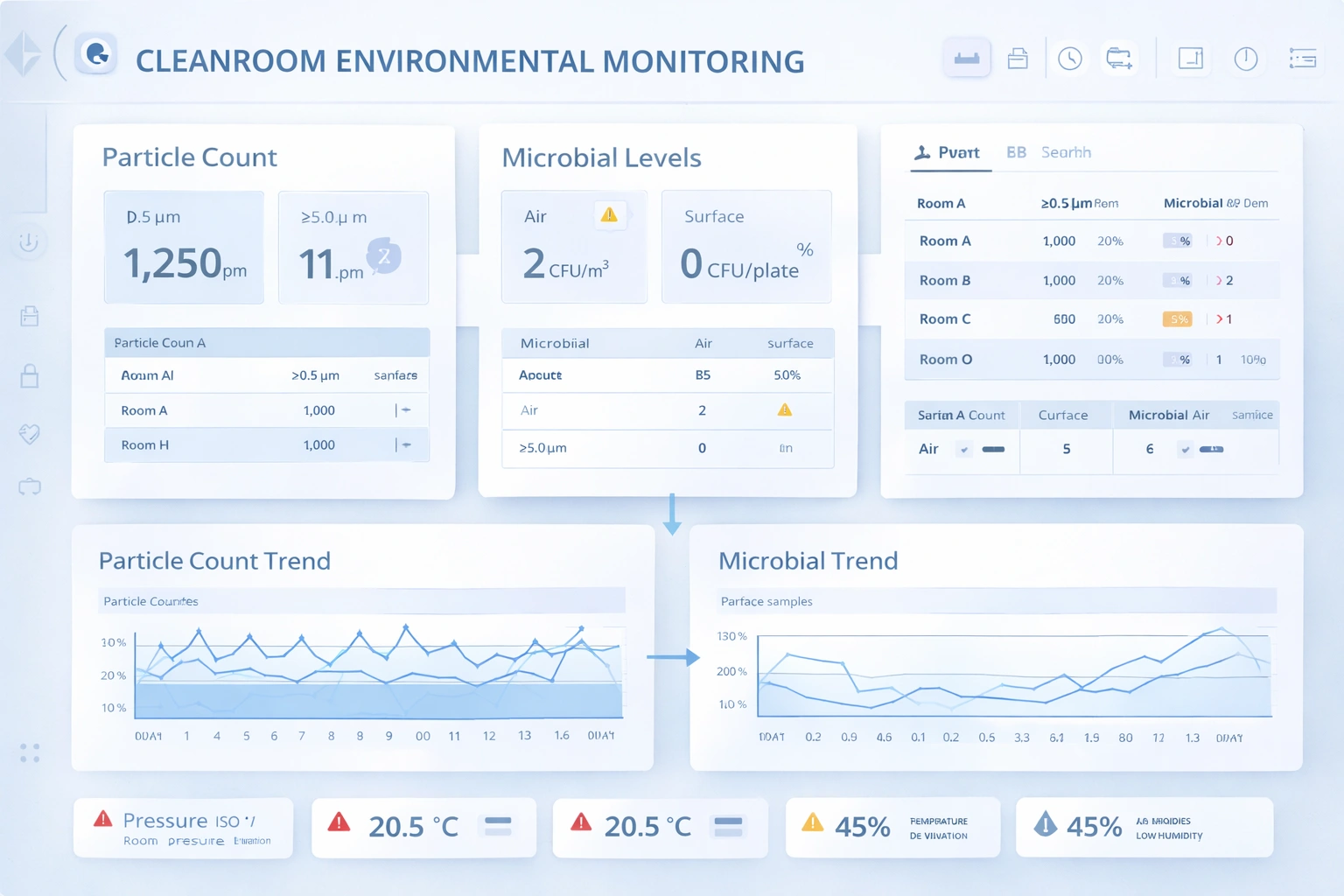
MOPS should specify when and where monitoring is performed, how results are documented, who reviews them, and how action-level events are escalated. This helps ensure that monitoring is used as an operational control rather than just a compliance report.
Standardized procedures reduce operator-to-operator variation and help align production behavior with cleaning, monitoring, and intervention control.

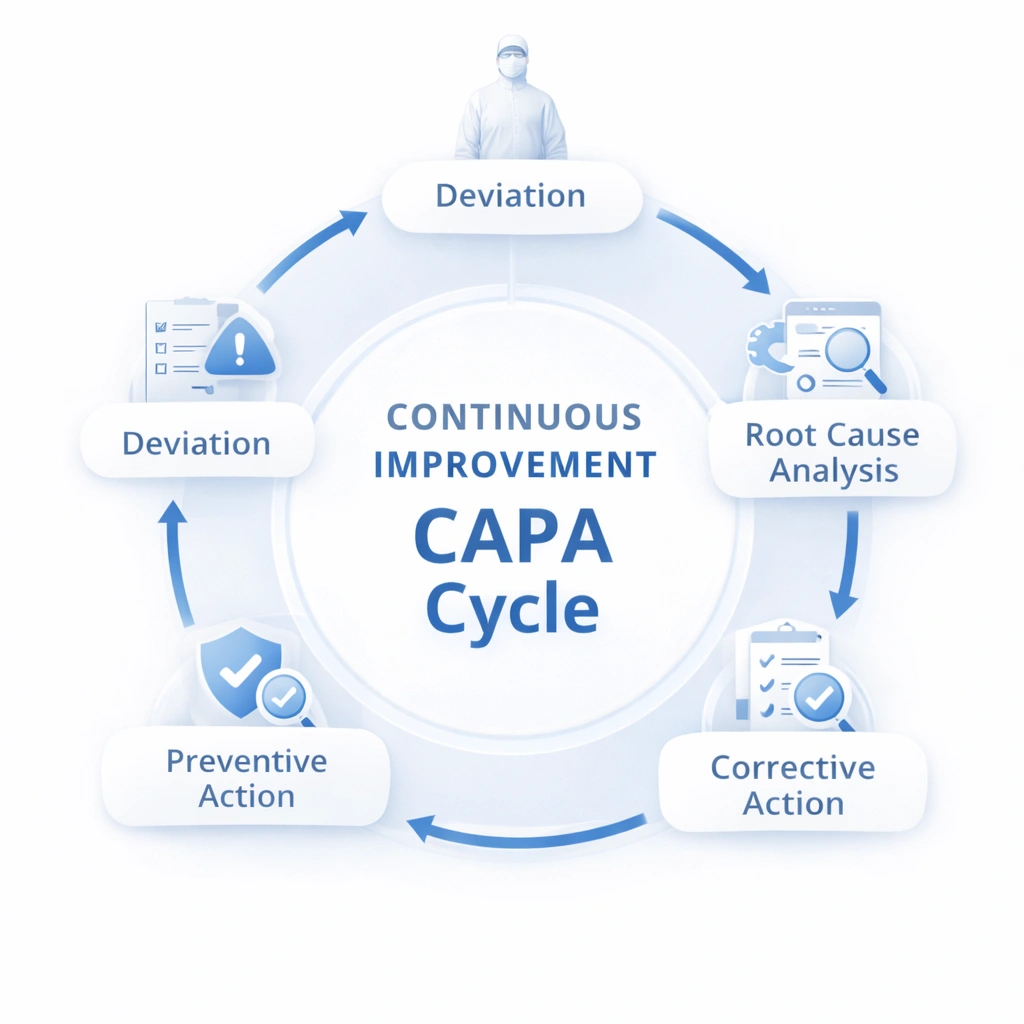
No cleanroom MOPS system is complete if it only describes normal operations. It must also define what happens when conditions are not normal. Your original content correctly highlights deviation handling and CAPA as essential elements of effective cleanroom procedure systems. :contentReference[oaicite:4]{index=4}
Define how personnel report, classify, contain, and document abnormal events affecting cleanroom control.
Link observations, records, monitoring results, and root-cause analysis to determine what failed and why.
Translate findings into corrective and preventive actions, then revise MOPS, training, or controls as needed.
Define the procedure scope, users, risks, records, escalation points, and success criteria for each cleanroom activity.
Train personnel on both the procedural steps and the contamination-control logic behind them.
Review EM trends, deviations, internal audits, CAPA outcomes, and feedback to improve the MOPS framework over time.
Cleanroom MOPS are structured operating procedures used to control personnel behavior, cleaning, disinfection, monitoring, workflow, documentation, and deviation handling in controlled environments.
They help standardize how critical tasks are performed, reduce contamination risk, improve training consistency, and support documentation and audit readiness.
A practical system should include personnel entry procedures, gowning rules, cleaning and disinfection steps, monitoring procedures, deviation handling, and CAPA-linked review.
L'efficacité est généralement examinée à travers la qualification de la formation, les résultats d'audit, les tendances de la surveillance environnementale, l'analyse des écarts et les performances de clôture du CAPA.
La fréquence des examens dépend de la procédure et des risques du site, mais les procédures doivent être revues après des changements de processus importants, des résultats d'audit, des écarts répétés ou des mises à jour du système qualité.
Midposi soutient les acheteurs réglementés avec des consommables pour salles blanches et une communication orientée documentation pour les environnements contrôlés, y compris une assistance à la qualification, l'examen des matériaux et des discussions sur le contrôle de la contamination.


Nous vous contacterons dans un délai d'un jour ouvrable, veuillez faire attention à l'e-mail avec le suffixe "*@midposi.com".