Dans la fabrication pharmaceutique, les échecs du contrôle de la contamination imputables aux outils de nettoyage représentent l’une des sources les plus évitables d’excursions de surveillance environnementale et d’observations réglementaires. Une lettre d’avertissement de la FDA de 2025 citait spécifiquement « les lingettes non stériles dans la zone de traitement aseptique ISO 5 » et « l’incapacité d’établir un système adéquat de nettoyage et de désinfection » comme violations des CGMP mettant en péril la stérilité des lots. La cause profonde : des outils de nettoyage réutilisables porteurs de biocharge et de particules contaminées provenant d'une utilisation antérieure, mal lavés et introduits dans des zones aseptiques sans retraitement validé.
Les vadrouilles jetables pour salles blanches éliminent entièrement cette voie de contamination. Chaque cycle de nettoyage commence par un nouveau tampon de vadrouille validé : aucun risque de contamination croisée provenant des pièces précédentes, aucun résidu de lessive, aucune charge de validation du retraitement. Pour les installations fonctionnant sous la norme ISO 14644-1 et l'annexe 1 révisée des BPF de l'UE (en vigueur en août 2023), les vadrouilles jetables offrent une contamination croisée nulle, des performances de particules prévisibles et une documentation de validation de nettoyage considérablement simplifiée. Le paysage réglementaire et l'économie du coût total favorisent de plus en plus les outils de nettoyage à usage unique dans la fabrication aseptique, les lignes de remplissage-finition et les zones de production pharmaceutique à haut risque.
Ce n’est pas « les jetables sont toujours meilleurs ». Les systèmes de vadrouilles réutilisables restent rentables dans les domaines de support ISO 8, la fabrication à grande échelle avec un lavage en interne validé et les installations dotées d'une infrastructure de retraitement robuste. Mais lorsque le contrôle de la contamination est strict (noyaux aseptiques ISO 5 à 7), que les échecs de la surveillance environnementale sont fréquents ou que les ressources de validation sont limitées, les serpillières jetables pour salle blanche offrent un contrôle supérieur de la contamination et un coût total de possession inférieur malgré un prix unitaire plus élevé.
Ce guide examine les facteurs réglementaires derrière l'adoption des vadrouilles jetables, quantifie les principaux avantages (zéro contamination croisée, performances prévisibles, charge de validation réduite), compare le coût total de possession par rapport aux systèmes réutilisables, cartographie les cas d'utilisation par classification ISO et recommande les produits de vadrouille jetables MIDPOSI adaptés aux exigences des installations. À la fin, vous disposerez d’un cadre décisionnel clair pour savoir quand les vadrouilles jetables pour salles blanches justifient leur coût par un risque de contamination réduit, une conformité simplifiée et des cycles d’enquête EM évités.

Pourquoi les vadrouilles jetables se développent dans le secteur pharmaceutique
L’évolution vers des serpillères jetables pour salles blanches n’est pas une tendance motivée par le marketing des fournisseurs : elle reflète des changements fondamentaux dans les attentes réglementaires, des échecs mesurables du contrôle de la contamination imputables aux outils réutilisables et les aspects économiques de la surveillance environnementale dans la fabrication pharmaceutique moderne.
Principaux avantages des vadrouilles jetables pour salles blanches (zéro contamination croisée)
Les vadrouilles jetables pour salles blanches offrent quatre avantages mesurables par rapport aux systèmes réutilisables : garantie de zéro contamination croisée, performances particulaires et microbiennes prévisibles, charge de validation et de documentation réduite et efficacité du travail améliorée. Ces avantages s’accentuent dans les applications pharmaceutiques à haut risque, où les marges de contrôle de la contamination sont étroites et où la surveillance réglementaire est intense.
Zéro contamination croisée garantie
La contamination croisée (le transfert de contaminants d'un emplacement, d'un produit ou d'une opération à un autre) constitue le risque fondamental présenté par les outils de nettoyage réutilisables. Chaque tampon de vadrouille réutilisable accumule de la biocharge, des particules et des résidus chimiques pendant son utilisation. Le lavage réduit ces contaminants mais atteint rarement la stérilité ou l'élimination complète des résidus. Lorsque cette vadrouille rentre dans une zone classée, elle transporte la contamination des environnements antérieurs.
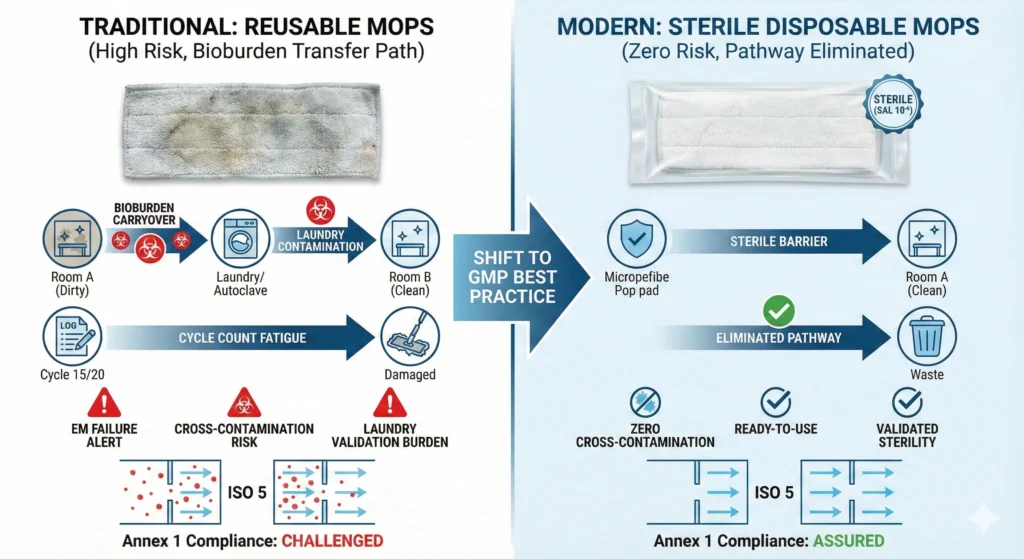
Les vadrouilles jetables pour salles blanches éliminent cette voie :
- Une vadrouille fraîche à chaque cycle: Chaque opération de nettoyage commence par un nouveau tampon de vadrouille retiré directement de son emballage stérile validé (pour les produits jetables irradiés aux rayons gamma) ou de son emballage scellé peu pelucheux (pour les produits jetables non stériles). Aucun transfert de charge microbienne provenant des pièces précédentes, aucune accumulation de particules provenant des passages de vadrouille précédents, aucun résidu de détergent à lessive.
- Pas de transfert de contamination d’une pièce à l’autre: Les installations utilisant des vadrouilles réutilisables maintiennent généralement un inventaire séparé pour différentes qualités ISO (les vadrouilles ISO 5 ne sont jamais utilisées dans les zones ISO 8). Même avec des protocoles de séparation parfaits, les erreurs d’étiquetage et les pénuries de stocks créent un risque de cession croisée. Les systèmes jetables éliminent ce mode de défaillance : les vadrouilles ne peuvent pas être réutilisées, la contamination entre zones est donc impossible.
- Aucune contamination liée au linge: Les vadrouilles réutilisables traversent les buanderies où les possibilités de contamination croisée abondent : lavage à charges mixtes, cycles de rinçage inadéquats, équipement partagé manipulant à la fois les blouses de salle blanche et le linge général des installations. Les vadrouilles jetables contournent l’ensemble du système de blanchisserie, supprimant ainsi une voie de contamination en plusieurs étapes.
Simplification de la validation grâce à l'élimination des variables de retraitement
Les protocoles de validation du nettoyage des outils réutilisables doivent tenir compte des pires scénarios de retraitement : nombre de cycles maximal (fin de vie qualifiée), défi de charge biologique maximal, efficacité de lavage minimale. Chaque variable introduit une incertitude dans les performances du contrôle de la contamination.
Les vadrouilles jetables ne présentent aucune variable de retraitement. Les tests de qualification des matériaux (génération de particules, compatibilité chimique, référence de charge microbienne) valident la vadrouille dans son état tel que reçu, jamais utilisé, le même état présenté lors de l'utilisation réelle. Cela élimine la complexité de la validation :
- Aucune étude de dégradation par comptage cyclique: La validation des vadrouilles réutilisables nécessite des tests à plusieurs points du cycle de vie (nouveau, 25 cycles, 50 cycles, 100 cycles) pour démontrer que la génération de particules reste dans les critères d'acceptation. La validation jetable teste uniquement la seule condition « neuve ».
- Aucune validation de l’efficacité du blanchiment: Les installations utilisant des vadrouilles réutilisables doivent valider les cycles de lessive, les concentrations de détergents, la réduction de la charge biologique et l'élimination des résidus. Les systèmes jetables n’ont aucune étape de lavage à valider.
- Aucun mode de défaillance du retraitement: Contamination croisée pendant la lessive, échecs de stérilisation en autoclave, erreurs de suivi affectant les vadrouilles à de mauvaises zones : aucun de ces modes d'échec n'existe lorsque les outils sont à usage unique.
Particule prévisible & Performance microbienne
Les programmes de surveillance environnementale dépendent de sources de contamination stables et prévisibles pour détecter les véritables événements de contamination. Lorsque les outils de nettoyage éliminent un nombre variable de particules et de biocharge tout au long de leur cycle de vie, ils introduisent du bruit dans les données EM qui obscurcit les véritables signaux de contamination.
Génération de particules stables (<100 Particules/m²)
Les vadrouilles jetables en polyester à bords scellés génèrent un nombre de particules cohérent dans toutes les unités :
- Performances typiques: <50 à 100 particules ≥0,5 µm par mètre carré nettoyées pour les produits jetables validés de qualité pharmaceutique
- Aucune dégradation dans le temps: Chaque vadrouille jetable fonctionne de manière identique : pas de séparation des bords, pas de rupture de fibres, pas de changements dimensionnels induits par l'autoclave. La génération de particules sur la vadrouille n°1 correspond à la vadrouille n°1 000.
- Tendances émergentes simplifiées: Lorsque le nombre de particules reste stable pendant les opérations de nettoyage, les équipes de surveillance environnementale peuvent attribuer en toute confiance les pics de particules aux événements de contamination (défaillances des tenues du personnel, contamination par transfert de matériaux, dysfonctionnements de l'équipement) plutôt qu'à la dégradation des outils de nettoyage.
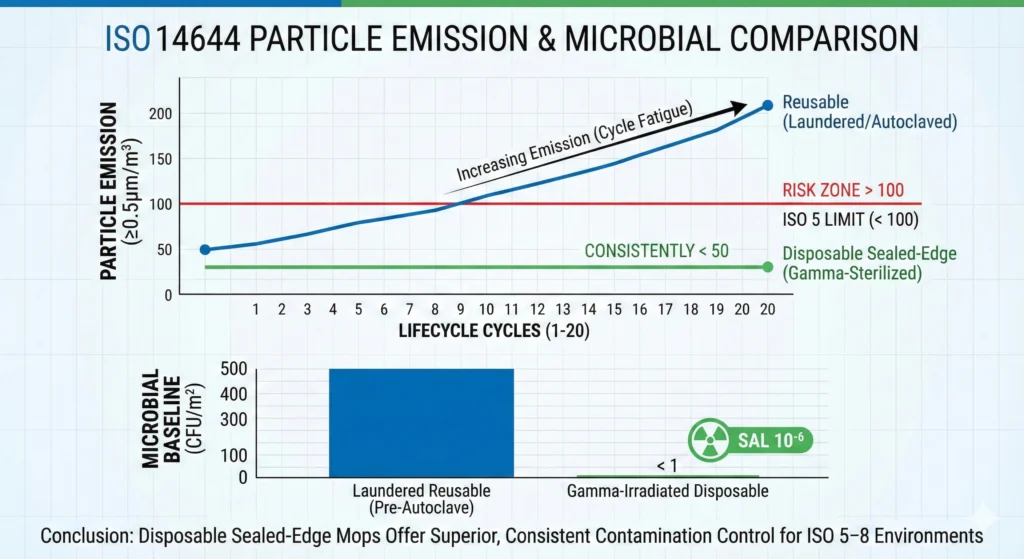
En revanche, les vadrouilles réutilisables augmentent la génération de particules tout au long de leur durée de vie. Une vadrouille réutilisable à bords scellés en polyester peut commencer à 50 particules/m² lorsqu'elle est neuve, augmenter jusqu'à 100 particules/m² au cycle 50 et atteindre 200 à 300 particules/m² vers la fin de sa durée de vie admissible (cycle 100 à 150). Cette augmentation de la génération de particules de 4 à 6 fois crée une contribution à la contamination en fonction du temps qui complique l'interprétation des données EM.
Base de référence prévisible pour la biocharge (produits jetables gamma-stériles)
Les vadrouilles jetables irradiées aux rayons gamma offrent un niveau d'assurance de stérilité (SAL) 10⁻⁶, soit une probabilité sur un million d'unités non stériles. Cette méthode de stérilisation terminale permet d'éliminer complètement la charge microbienne :
- Zéro micro-organisme viable: L'irradiation gamma (généralement une dose de 25 à 50 kGy) inactive toutes les cellules végétatives bactériennes, les spores, les champignons et les virus en endommageant l'ADN. Contrairement à l'autoclavage (qui peut laisser des spores résistantes à la chaleur viables si les paramètres du cycle dérivent) ou à la désinfection chimique (qui laisse des résidus de désinfectant et peut ne pas atteindre l'efficacité sporicide), l'irradiation gamma offre une stérilité absolue sans résidus.
- Certificats de stérilité validés: Les produits jetables stérilisés aux rayons gamma sont livrés avec des certificats de stérilisation documentant la dose délivrée, les résultats des indicateurs biologiques (BI) et l'atteinte du SAL. Les installations peuvent accepter ces certificats sous réserve de la qualification du fournisseur (conformément à la section 4.34 de l'annexe 1), évitant ainsi les tests de stérilité en interne.
- Performances émergentes prévisibles: Les zones de catégorie A/B utilisant des vadrouilles jetables gamma-stériles établissent des lignes de base stables pour la charge microbienne. Toute détection microbienne lors de la surveillance environnementale après le nettoyage représente une contamination provenant d'autres sources (personnel, traitement de l'air, transfert de matériaux) et non du transfert de charge microbienne des outils de nettoyage.
Les vadrouilles jetables non stériles (pour les applications de classe ISO 7 à 8) offrent toujours des performances prévisibles en matière de charge microbienne grâce à des contrôles de fabrication validés. Les produits jetables de qualité pharmaceutique préservent la charge biologique <10 UFC/tampon de vadrouille grâce à la fabrication en salle blanche, aux matériaux d'emballage stérilisés et au stockage validé. Cette référence reste constante dans toutes les unités, contrairement aux vadrouilles réutilisables où la variabilité de l'efficacité du lavage introduit des fluctuations de la charge biologique.
Validation inférieure & Fardeau de la documentation
La charge de travail de validation constitue un coût caché dans les programmes d’outils de nettoyage réutilisables. Les installations doivent élaborer des protocoles, exécuter des études, analyser des données et conserver une documentation pour plusieurs éléments de validation, chacun consommant du temps de spécialiste en assurance qualité, des ressources de laboratoire de microbiologie et des heures de qualification d'équipement.

Ce dont ont besoin les vadrouilles réutilisables :
- Qualification d'équipement de blanchisserie (IQ/OQ/PQ): Qualification de l'installation vérifiant les spécifications de l'équipement, qualification opérationnelle validant les paramètres du cycle (distribution de la température, concentration du détergent, efficacité du rinçage), qualification des performances démontrant la réduction de la charge microbienne dans les pires cas de charge.
- Qualification des matériaux des outils de nettoyage: Tests de génération de particules à l'état neuf et en fin de vie (nombre de cycles maximum) ; validation de la compatibilité chimique de tous les désinfectants des installations ; tests de stabilité dimensionnelle par cycles d'autoclave
- Validation du système de suivi d'inventaire tournant: Validation des systèmes de suivi par codes-barres ou RFID, test des alertes de déclenchement de mise hors service, démonstration de la traçabilité tout au long du cycle de vie des vadrouilles
- Vérification de la stérilité ou de la charge biologique (si autoclavé): Etudes de placement d'indicateurs biologiques, validation de cycles de stérilisation, démonstration de niveau d'assurance de stérilité (SAL)
- Revalidation périodique: Revalidation annuelle ou biennale après changement d'équipement, modification des paramètres de cycle ou mise à jour de la formule du détergent
Ce dont ont besoin les vadrouilles jetables :
- Qualification matérielle uniquement : Tests de génération de particules (généralement effectués par le fournisseur avec rapport de validation fourni), vérification de la compatibilité chimique avec les désinfectants spécifiques à l'installation
- Inspection à la réception: Inspection visuelle de l'intégrité des emballages, vérification des certificats de stérilité (pour les unités gamma-stériles), documentation des numéros de lot
- Qualification du fournisseur: Audit des contrôles des salles blanches du fabricant, validation du processus de stérilisation, système de gestion de la qualité – généralement satisfait grâce à l'examen du package de validation fourni par le fournisseur.
Réduction des heures de validation
Une installation pharmaceutique représentative passant des vadrouilles réutilisables aux vadrouilles jetables dans une zone de support aseptique ISO classe 7 de 500 m² pourrait réduire la charge de travail de validation en :
- Validation initiale: 120-160 heures (validation du linge réutilisable + configuration du système de suivi) vs 20-30 heures (qualification des matériaux jetables + procédure de réception)
- Revalidation annuelle: 40 à 60 heures (revalidation du linge + vérification du système de comptage cyclique) vs 0 heure (aucune revalidation requise ; l'inspection à la réception fait partie des opérations de routine)
- Aide à l'enquête: 8 à 12 heures par excursion EM (examen médico-légal de l'historique des tâches de vadrouille, journaux de lessive, décompte des cycles) contre 2 à 3 heures (simple vérification du numéro de lot jetable et examen du certificat)
Pour les équipes d'assurance qualité travaillant avec un effectif limité (ce qui est courant dans les startups de biotechnologie, les organisations de fabrication sous contrat et les installations gérant des opérations Lean), cette réduction du fardeau de validation se traduit directement par une bande passante pour des activités à plus forte valeur ajoutée : validation de nettoyage de nouveaux produits, améliorations du programme de surveillance environnementale, enquêtes sur les écarts.
Travail & Efficacité du temps
L'efficacité opérationnelle s'étend sur des centaines, voire des milliers de cycles de nettoyage par an. De petites améliorations procédurales (élimination de l'enregistrement du comptage cyclique, suppression des étapes d'inspection à la vadrouille, simplification de l'élimination) se traduisent par des économies de main-d'œuvre mesurables.
Pas de suivi du comptage cyclique
Les programmes de vadrouille réutilisables exigent que les opérateurs enregistrent chaque utilisation de vadrouille :
- Pré-utilisation : Scannez le code-barres de la vadrouille ou l'étiquette RFID, vérifiez le nombre de cycles dans la plage qualifiée, documentez l'affectation de la vadrouille à une pièce/zone spécifique.
- Post-utilisation: Remettre la serpillière à l'étape du linge sale, scanner l'inventaire, déclencher le cycle blanchisserie/autoclave si le seuil de comptage prédéterminé est atteint.
- Audits périodiques: L'assurance qualité effectue des audits mensuels ou trimestriels des journaux d'inventaire cyclique pour vérifier la conformité, identifier les lacunes de suivi et imposer le retrait des vadrouilles trop âgées.
Les systèmes jetables éliminent tout ce flux de travail. Les opérateurs retirent la vadrouille de l'emballage, l'utilisent une seule fois, la jettent dans les déchets classifiés : pas de numérisation, pas de journalisation, pas de vérification du comptage cyclique. Pour les installations nettoyant quotidiennement 200 à 500 m² sur plusieurs équipes, cette simplification des procédures permet d'économiser 10 à 15 minutes par équipe (au total pour toutes les opérations de nettoyage), soit environ 60 à 75 heures par an de temps d'opérateur récupéré.
Pas de lavage, séchage, redistribution
La logistique des vadrouilles réutilisables crée des flux de travail en plusieurs étapes :
- Collecte du linge sale: Les opérateurs transfèrent les vadrouilles usagées des zones de salle blanche vers la buanderie, en maintenant la ségrégation par qualité ISO.
- Blanchiment: Le personnel de la blanchisserie charge les vadrouilles dans les laveuses (séparées par catégorie), exécute les cycles de lavage validés, les transfère aux sécheuses
- Stérilisation (si nécessaire): Charger les vadrouilles séchées dans l'autoclave, exécuter le cycle validé, vérifier les indicateurs biologiques
- Redistribution: Transporter les vadrouilles propres/stériles vers les zones de salle blanche, réapprovisionner les stocks aux emplacements de stockage désignés
Chaque étape consomme des heures de travail et introduit du retard. Le délai d'exécution typique d'une vadrouille réutilisable est de 24 à 48 heures (plus longtemps si l'autoclavage est requis ou si la lessive est externalisée). Les installations doivent maintenir un inventaire de 2 à 3 fois pour garantir une disponibilité adéquate des vadrouilles pendant les cycles de lessive.
Les serpillères jetables décomposent cette chaîne logistique en deux étapes :
- Réception et stockage: Accepter les expéditions de vadrouilles jetables, effectuer une inspection à la réception, stocker dans les zones d'inventaire désignées pour les salles blanches.
- Élimination : Retirez les vadrouilles usagées de la salle blanche dans des conteneurs à déchets classifiés conformément aux protocoles de gestion des déchets de l'installation.
Pas de blanchiment, pas de stérilisation, pas de redistribution. Les besoins en inventaire chutent à 1 × (vadrouilles nécessaires aux opérations en cours) plus le stock de sécurité (généralement une caisse supplémentaire par SKU). Pour les petites installations disposant d'une infrastructure de blanchisserie limitée ou les startups biotechnologiques sans capacité de blanchisserie interne, les systèmes jetables éliminent le besoin de construire ou d'externaliser entièrement les opérations de blanchisserie.
Particulièrement utile pour les installations BPF composées de petites équipes
Les startups de biotechnologie, les fabricants spécialisés et les organisations de fabrication sous contrat dirigeant des équipes opérationnelles réduites bénéficient de manière disproportionnée des systèmes de vadrouille jetables :
- Pas de personnel de blanchisserie dédié: Installations avec <20 personnels de salle blanche ne peuvent souvent pas justifier des opérateurs de blanchisserie à temps plein. Les systèmes jetables éliminent cette exigence d’effectif.
- Formation simplifiée: La formation des opérateurs pour les systèmes jetables nécessite une SOP (« Retirer de l'emballage, utiliser une fois, jeter ») contre plusieurs SOP pour les systèmes réutilisables (inspection par vadrouille, enregistrement du comptage cyclique, séparation du linge, chargement de l'autoclave).
- Charge de travail CAPA réduite: Les enquêtes sur les erreurs de suivi du comptage cyclique, les échecs de ségrégation du linge et les écarts de stérilisation en autoclave disparaissent lorsque les outils sont à usage unique.
Modifications de l’annexe 1 des BPF de l’UE (2023-2025)
L’annexe 1 révisée des BPF de l’UE (entrée en vigueur le 25 août 2023) repositionne fondamentalement le contrôle de la contamination en tant que cadre stratégique à l’échelle du site. Les versions antérieures traitaient le nettoyage et la désinfection comme des exigences procédurales ; la révision de 2023 élève la stratégie de contrôle de la contamination (CCS) au rang d'un système obligatoire et documenté qui définit les points de contrôle critiques et évalue l'efficacité des mesures de conception, de procédure, techniques et de surveillance dans l'ensemble de l'installation.
Outils de nettoyage en tant qu'éléments CCS
La section 2.5 de l'annexe 1 répertorie explicitement « le nettoyage et la désinfection » parmi les éléments de base du CCS nécessitant une validation, et les sections 4.33 à 4.35 exigent que les désinfectants et les détergents utilisés dans les zones de catégorie A et B « doivent être stériles avant utilisation ». Le règlement exige en outre des processus de désinfection validés, le nettoyage précédant la désinfection pour garantir une élimination efficace des résidus. Ces exigences s'appliquent non seulement aux produits chimiques mais aussi aux outils qui les appliquent : les têtes de vadrouille, les lingettes et les instruments de nettoyage doivent maintenir la stérilité et des performances validées dans les zones aseptiques.
L'expression « outils stériles pour les manipulations » (section 8.16) étend cette logique : si les opérateurs manipulent des matériaux dans des zones de traitement aseptique à l'aide d'outils stériles, les outils de nettoyage en contact avec ces mêmes surfaces classées doivent répondre à des normes équivalentes de stérilité et de contrôle de la contamination.
Vecteurs de contamination cachés et désinfection par transfert
Les sections 4.11 à 4.12 de l'Annexe 1 identifient le transfert de matériaux et d'équipements comme « l'une des plus grandes sources potentielles de contamination », nécessitant une désinfection de transfert validée et des programmes surveillés. Les outils de nettoyage réutilisables sont constamment transférés entre les pièces et les zones : une vadrouille utilisée dans un couloir de support de niveau C un jour peut être lavée et déployée dans un environnement de niveau B lors du quart de travail suivant. Sans retraitement validé (blanchiment, désinfection, vérification de la stérilité), la vadrouille devient un « vecteur de contamination caché » transportant de la biocharge, des résidus de particules et des résidus chimiques entre les environnements classés.
L’accent mis par le règlement sur les surfaces lisses et imperméables qui minimisent les pertes et tolèrent des désinfections répétées (sections 4.5 à 4.7) s’applique également à la sélection des outils de nettoyage. Les vadrouilles jetables éliminent la voie de dégradation : pas de suivi du nombre de cycles, pas de séparation des bords induite par l'autoclave, pas de rupture de fibres induite par le lavage. Chaque vadrouille repart à neuf, répondant aux spécifications de génération de particules et de stérilité sans usure cumulative.
Risque de blanchisserie et de retraitement
La section 7.17 de l'annexe 1 signale explicitement le lavage des vêtements comme un risque de contamination et de contamination croisée, nécessitant des processus de blanchisserie qualifiés, une séparation des zones de production et des limites de cycle définies. Les mêmes voies de contamination affectent les systèmes de vadrouilles réutilisables. Les blanchisseries qui manipulent à la fois des outils d'habillage et de nettoyage introduisent des opportunités de contamination croisée : des cycles de rinçage de détergent inadéquats laissent des résidus de tensioactifs, une réduction incomplète de la charge microbienne transfère les charges microbiennes et le traitement de charges mixtes contamine les outils de qualité A/B avec des particules provenant d'articles de qualité inférieure.
Les installations sans opérations de blanchisserie internes validées doivent sous-traiter, ce qui ajoute à la complexité de la chaîne d'approvisionnement, aux retards d'exécution et au risque de contamination par des tiers. Les vadrouilles jetables contournent l'ensemble du système de blanchisserie, réduisant ainsi la logistique de retraitement en une seule étape : retirer le tampon de vadrouille de son emballage stérile, l'utiliser une seule fois, le jeter avec les déchets classés.
Cause fondamentale : des outils réutilisables à l'origine des échecs de la technologie EM
Les programmes de surveillance environnementale des installations pharmaceutiques détectent régulièrement les pics de contamination pendant et immédiatement après le nettoyage des sols. Lorsque les équipes d’enquête remontent à la cause profonde de ces écarts, les outils de nettoyage réutilisables apparaissent comme des récidivistes.
Biocharge résiduelle et transfert croisé
Les têtes de vadrouille réutilisables entrent en contact avec des surfaces de sol chargées de contamination microbienne, de résidus de désinfectant et de particules. Même après le lavage, la charge biologique et les résidus chimiques persistent :
- Réduction incomplète de la charge microbienne: Les cycles de lessive standards (lavage à l'eau chaude, détergent, séchage en machine) réduisent la charge microbienne mais n'atteignent pas la stérilité. Les cellules végétatives bactériennes survivent dans les interstices des tissus et les cellules sporulées (Bacillus, Geobacillus) tolèrent entièrement les conditions de lessive. Une vadrouille réutilisable entrant dans une zone de catégorie A/B sans stérilisation terminale (autoclavage ou irradiation gamma) introduit des micro-organismes viables directement sur les surfaces ensuite contactées par un produit stérile ou un équipement en contact avec le produit.
- Transfert croisé entre les zones: Les vadrouilles utilisées dans les zones de support ISO classe 8 accumulent une charge biologique et un nombre de particules plus élevés que les vadrouilles dédiées aux noyaux aseptiques ISO classe 5. Si la séparation du linge est inadéquate (lavage de charges mixtes, équipement de buanderie partagé, suivi inapproprié), les vadrouilles de catégorie A/B sont contaminées par des résidus de catégorie C/D. Un seul événement d'affectation croisée (utilisation d'une vadrouille ISO 8 dans une salle ISO 5 en raison d'une erreur d'étiquetage ou d'une rupture de stock) peut semer une charge biologique dans des environnements aseptiques et déclencher des cycles d'enquête de plusieurs semaines.
- Résidus de détergent à lessive: Les tensioactifs et assouplissants restant sur les fibres de la vadrouille créent des surfaces collantes qui attirent et retiennent les particules. Ces résidus interfèrent également avec l'efficacité du désinfectant : les tensioactifs cationiques contenus dans les assouplissants neutralisent les désinfectants anioniques (composés d'ammonium quaternaire), réduisant ainsi les taux de destruction microbienne lors du nettoyage et laissant des organismes viables sur les surfaces traitées.
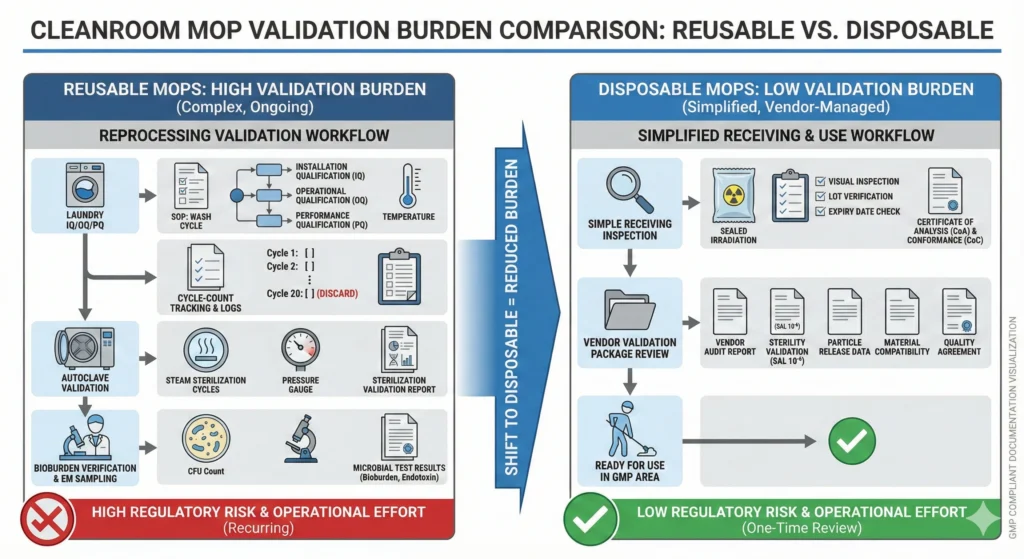
Retraitement des charges de documentation et de validation
Les programmes d’outils de nettoyage réutilisables imposent des exigences étendues en matière de validation et de documentation :
- Validation du blanchiment (IQ/OQ/PQ): Les installations doivent qualifier les équipements de blanchisserie (laveuses, sécheuses, autoclaves), valider les paramètres du cycle (durée, température, concentration de détergent) et démontrer une réduction de la charge microbienne à des limites acceptables. Cela nécessite des études de provocation microbiologique (inoculation des têtes de vadrouille avec des organismes cibles, traitement tout au long du cycle de lavage complet, récupération et quantification des survivants) et une revalidation périodique lorsque les paramètres du cycle changent ou que l'équipement est entretenu.
- Suivi de l'inventaire cyclique et critères de mise hors service: Chaque tête de vadrouille réutilisable a une durée de vie qualifiée (par exemple 50 cycles d'autoclave pour les vadrouilles à bords scellés en polyester). Les installations doivent mettre en œuvre des systèmes de suivi (codes-barres, journaux manuels ou étiquettes RFID) pour enregistrer l'historique d'utilisation et imposer la mise hors service en fin de vie admissible. Les échecs de suivi introduisent des risques : les vadrouilles trop âgées éliminent les particules et la charge microbienne, mais leur retrait prématuré gaspille les stocks et augmente les coûts.
- Vérification de la stérilité ou de la charge biologique: Si les vadrouilles réutilisables sont autoclavées pour être utilisées dans des zones de catégorie A/B, le cycle de stérilisation doit être validé selon la norme ISO 11137 ou équivalent, avec des indicateurs de stérilité placés dans des configurations de charge représentatives. Les installations sans capacité d'autoclave doivent soit envoyer des vadrouilles à des fournisseurs de stérilisation externes (ce qui augmente les délais d'exécution et les coûts), soit accepter un risque élevé de charge biologique.
- Documents d'enquête: Lorsque des excursions EM se produisent, les équipes d'enquête doivent examiner l'historique des outils de nettoyage : quelle vadrouille a été utilisée, quand a-t-elle été lavée pour la dernière fois, quel a été son nombre de cycles, dans quelles zones a-t-elle été utilisée précédemment. Cette analyse médico-légale nécessite des enregistrements de traçabilité complets. Des lacunes dans la documentation (journaux de blanchisserie manquants, tâches de vadrouille non enregistrées) prolongent les enquêtes et compliquent la clôture du CAPA.
Les vadrouilles jetables éliminent la majeure partie de cette infrastructure de validation. Les outils à usage unique nécessitent uniquement une inspection de réception (vérification des certificats de stérilité, inspection visuelle de l'intégrité de l'emballage) et une qualification des matériaux (tests de génération de particules, validation de compatibilité chimique) : pas de validation de blanchisserie, pas de suivi d'inventaire cyclique, pas de documentation de retraitement.
Adoption croissante dans le domaine du remplissage-finition & Biotechnologie
Les données du marché montrent une adoption accélérée de consommables de nettoyage à usage unique validés dans la fabrication pharmaceutique et biotechnologique, motivée par les pressions de conformité réglementaire et les aspects économiques opérationnels.
Lignes de remplissage-finition et traitement aseptique
Les opérations de remplissage-finition (remplissage stérile, chargement de lyophilisation, bouchage des flacons) s'effectuent sous un flux d'air unidirectionnel de classe ISO 5 (grade A) avec des fonds ISO de classe 7 (grade B). Les limites de particules sont extrêmes : 3 520 particules ≥0,5 µm par mètre cube pour ISO 5, contre 352 000 particules/m³ pour ISO 7. Tout outil de nettoyage générant une contribution mesurable en particules risque de dévier de la classification.
Serpillères jetables pour salles blanches validées pour la génération de particules (<50 particules/m² pour le chant scellé en polyester ; <10 particules/m² pour les conceptions à filament continu haut de gamme) offrent des performances prévisibles et constantes dans toutes les utilisations. Les vadrouilles réutilisables se dégradent avec le temps (les bords se séparent, les fibres se cassent, la génération de particules augmente), créant une contribution variable à la contamination qui complique l'analyse des tendances en matière de surveillance environnementale.
Fabrication de biotechnologies et de thérapies cellulaires
La fabrication de médicaments biologiques et de thérapies cellulaires fonctionne selon des paradigmes de lots plus petits et de puissance plus élevée que les produits pharmaceutiques traditionnels à petites molécules. Les événements de contamination qui pourraient être tolérables dans un lot de comprimés de 10 000 doses deviennent catastrophiques dans un produit CAR-T personnalisé de 50 doses. Les installations de biotechnologie adoptent des outils de nettoyage jetables dans le cadre de stratégies plus larges de systèmes à usage unique :
- Bioréacteurs à usage unique et parcours fluidiques: Les systèmes basés sur des sacs jetables éliminent la validation du nettoyage des récipients et réduisent le risque de contamination croisée entre les lots. L’extension de cette logique au nettoyage des sols maintient la philosophie de contrôle de la contamination à usage unique à l’échelle du système.
- Fabrication sous contrat et installations multi-produits: Les CDMO manipulant plusieurs produits clients dans les mêmes salles blanches sont confrontés à des exigences strictes en matière de validation du nettoyage et de prévention de la contamination entre produits. Les vadrouilles jetables simplifient le changement : chaque nouvelle campagne commence avec de nouveaux outils de nettoyage, éliminant ainsi le risque de transfert des produits précédents sans études approfondies de validation du nettoyage.
- Modèles opérationnels Lean: Les startups biotechnologiques et les petits fabricants manquent souvent d’infrastructure de blanchisserie interne. L'externalisation du lavage des vadrouilles réutilisables augmente les coûts, les délais d'exécution et le risque de contamination par des tiers. Les vadrouilles jetables réduisent la chaîne d'approvisionnement en livraison directe par le fournisseur de consommables pré-stérilisés et prêts à l'emploi.
L’analyse de l’industrie confirme que l’Annexe 1 des BPF de l’UE « oblige les producteurs pharmaceutiques à passer à des vêtements et lingettes stériles à usage unique », favorisant l’adoption de consommables jetables validés dans toutes les catégories de nettoyage. Les lingettes stériles pré-saturées capturent déjà une part de marché substantielle dans les suites aseptiques ; Les systèmes de vadrouilles jetables suivent la même courbe d'adoption à mesure que les installations étendent les stratégies de contrôle de la contamination à usage unique au nettoyage des sols.

Comparaison des coûts : jetables ou réutilisables
Le coût unitaire plus élevé des vadrouilles jetables pour salles blanches (généralement entre 8 et 25 dollars par tampon, contre 15 à 40 dollars pour une vadrouille réutilisable avec une durée de vie de 50 à 100 cycles) crée un choc initial pour les équipes d'approvisionnement. Mais l'analyse du coût total de possession (TCO) révèle que les systèmes jetables génèrent souvent des coûts de durée de vie inférieurs dans les applications pharmaceutiques à haut risque une fois les coûts de retraitement, de validation et d'échec de contamination inclus.
Éléments de coûts directs
Systèmes de vadrouille jetables
- Coût unitaire du tampon de vadrouille: 8 à 15 $ par serviette pour les jetables non stériles en polyester à bords scellés (applications ISO 7 à 8) ; 15 à 25 $ par serviette pour les produits jetables stériles irradiés aux rayons gamma (zones ISO 5 à 6 de qualité A/B)
- Systèmes de poignée: 50-150$ par manche réutilisable en aluminium ou en acier inoxydable (compatible avec les systèmes de fixation de tampons jetables) ; les poignées ont une durée de vie de plusieurs années
- Stockage et inventaire: Minimal : les produits jetables sont expédiés dans un emballage compact, ne nécessitent aucune séparation par nombre de cycles ou par statut de stérilisation
- Élimination des déchets: Gestion des déchets pharmaceutiques classifiés (généralement entre 0,50 et 2 $ par livre) ; Les tampons de vadrouille jetables pèsent entre 50 et 150 grammes, ce qui ajoute 0,05 à 0,30 $ par vadrouille au coût d'élimination des déchets.
Systèmes de vadrouille réutilisables
- Coût initial de la tête de vadrouille: 15 à 40 $ par tête de vadrouille réutilisable en polyester ou en microfibre à bords scellés
- Coût de lavage par cycle: 2 à 5 $ par vadrouille (traitement de lessive commerciale, détergent, services publics) ; le blanchiment en interne réduit ce montant à 1 à 3 dollars par cycle mais nécessite un investissement en biens d'équipement
- Stérilisation en autoclave (si nécessaire) : 3 à 8 $ par cycle, y compris les services publics, les indicateurs biologiques, la documentation et l'amortissement de l'équipement
- Système de suivi du comptage cyclique : 5 000 à 20 000 $ pour l'infrastructure de codes-barres ou RFID (scanners, logiciels, impression d'étiquettes) plus 0,50 à 1 $ par vadrouille et par cycle pour le suivi du travail
- Coût de possession des stocks: Inventaire de 2 à 3 vadrouilles requis pour maintenir une disponibilité adéquate pendant les cycles de rotation du linge
Coûts indirects cachés (souvent négligés)
Les facteurs décisifs du TCO résident souvent dans les coûts opérationnels cachés que les équipes d'achat sous-estiment lorsqu'elles évaluent uniquement le prix unitaire.
Charge de validation et de documentation
- Validation initiale du linge: 120 à 160 heures de temps de spécialiste en assurance qualité (60 à 100 $/heure) pour IQ/OQ/PQ = 7 200 à 16 000 $
- Qualification des matériaux de vadrouille tout au long du cycle de vie: 40 à 60 heures pour les tests de particules dans des conditions neuves et de fin de vie, validation de la compatibilité chimique = 2 400 à 6 000 $
- Validation de la stérilisation en autoclave (le cas échéant): 60 à 80 heures pour le développement du cycle, études d'indicateurs biologiques, démonstration SAL = 3 600 à 8 000 $
- Revalidation annuelle: 40 à 60 heures par an = 2 400 à 6 000 $ par an
- Validation jetable par comparaison: 20 à 30 heures pour la qualification des matériaux (souvent fournies par le fournisseur) + développement de la procédure de réception = 1 200 à 3 000 $ de coût unique, sans revalidation annuelle
Coûts des enquêtes de surveillance environnementale
Les excursions EM attribuées à la contamination des outils de nettoyage déclenchent des cycles d'enquête de plusieurs semaines :
- Travail d'enquête: 20 à 40 heures par excursion (temps du microbiologiste, documentation d'assurance qualité, traitement des écarts) = 1 200 à 4 000 $ par événement
- Analyse des causes profondes: Examen médico-légal de l'historique des tâches de vadrouille, des journaux de blanchisserie, des décomptes de cycles, des enregistrements de retraitement
- Mise en œuvre du CAPA: Révisions de procédures, recyclage, surveillance améliorée – souvent 40 à 80 heures supplémentaires = 2 400 à 8 000 $
- Risque d'impact sur les lots: Dans les pires scénarios, les échecs EM lors du remplissage aseptique déclenchent des suspensions de lots, une extension des tests de stérilité ou un rejet de lots – des coûts allant de 50 000 $ (retenue de petits lots et enquête) à 500 000 $ et plus (rejet de lots et notification réglementaire).
Les installations connaissant ne serait-ce qu'une défaillance EM par an avec une charge d'enquête modérée (5 000 à 10 000 $ en main d'œuvre et documentation) compensent les coûts importants des vadrouilles jetables.
Gains d’efficacité du travail
- Élimination du suivi de l'inventaire tournant: 60 à 75 heures par an économisées sur toutes les opérations de nettoyage = valeur annuelle de 1 800 à 3 000 $ (au tarif mixte de l'opérateur de 30 $/heure)
- Élimination de la logistique de blanchisserie: 100 à 200 heures par an économisées (collecte des salissures, chargement du cycle de lavage, stérilisation, redistribution) = valeur annuelle de 3 000 à 6 000 $
- Simplification de la formation: La complexité réduite des SOP permet d'économiser 10 à 20 heures par an en matière de prestation de formation et de vérification des compétences = valeur annuelle de 600 à 2 000 $
Comparaison du coût total de possession (exemple de zone de support aseptique ISO classe 7)
Prenons l'exemple d'une zone de support de fabrication pharmaceutique ISO classe 7 de 500 m² nettoyée quotidiennement (365 jours/an), nécessitant 2 serpillères par cycle de nettoyage :
Scénario A : Vadrouilles réutilisables
- Coûts directs: 730 utilisations de vadrouille/an ÷ Durée de vie de 75 cycles de vadrouille = 10 vadrouilles achetées annuellement à 30 $ pièce = 300 $
- Blanchiment: 730 cycles × 3 $ par cycle (traitement interne) = 2 190 $
- Stérilisation en autoclave: 730 cycles × 5 $ par cycle = 3 650 $
- Travail de suivi du cycle: 730 cycles × 0,75 $ par cycle = 548 $
- Validation initiale (amorti sur 5 ans) : 12 000 $ ÷ 5 = 2 400 $ par année
- Revalidation annuelle: 4 000 $
- Fardeau des enquêtes SE (1 événement tous les 2 ans, de manière prudente) : 7 500 $ ÷ 2 = 3 750 $ en moyenne annuelle
- CTP annuel total: 16 838 $
Scénario B : Vadrouilles jetables (gamma-stériles)
- Coûts directs: 730 tampons de vadrouille × 18 $ par tampon = 13 140 $
- Gérer l'amortissement: 100$ ÷ durée de vie de 5 ans = 20$ par année
- Élimination des déchets: 730 blocs × 0,15 $ par bloc = 110 $
- Qualification matérielle initiale (amorti sur 5 ans) : 2 000 $ ÷ 5 = 400 $ par année
- Aucun frais de revalidation, de blanchisserie, de stérilisation ou de suivi
- Réduction du fardeau des enquêtes EM: Excursions proches de zéro liées aux outils de nettoyage = 0 $
- Gains d’efficacité du travail: 4 000$ par an (suivi, logistique blanchisserie, formation)
- CTP annuel total: 13 670 $ – 4 000 $ (gains d’efficacité) = Coût net de 9 670 $
Résultat: Les vadrouilles jetables livrent Un coût total de possession réduit de 42 % (9 670 $ contre 16 838 $) malgré un coût unitaire plus élevé, dû à l'élimination de l'infrastructure de retraitement, à la réduction du fardeau de validation et à l'évitement des enquêtes EM.
Seuils de décision : quand les produits jetables justifient leur coût
Les vadrouilles jetables pour salles blanches offrent un TCO avantageux dans les conditions suivantes :
- Classifications ISO à haut risque (ISO 5–7) : Les limites de particules et les marges de contrôle de la contamination sont strictes ; Le risque de défaillance EM et la charge d’enquête sont élevés
- Installations avec historique de défaillances EM: Même une excursion de contamination par an attribuée aux outils de nettoyage (coût d'enquête de 5 000 à 10 000 $) compense les dépenses substantielles liées aux vadrouilles jetables.
- Opérations de petite et moyenne taille (<1 000 m² de salle blanche) : les systèmes réutilisables nécessitent des coûts de validation et d’infrastructure fixes qui ne diminuent pas ; les coûts jetables évoluent de manière linéaire avec l'utilisation
- Installations sans blanchisserie interne: La lessive externalisée ajoute 5 à 10 $ par vadrouille et par cycle, plus les délais d'exécution ; les produits jetables éliminent la dépendance envers les tiers
- Des équipes opérationnelles réduites: Les startups de biotechnologie et les CMO avec un effectif limité en matière d'assurance qualité/blanchisserie bénéficient d'une réduction de la charge de validation et de gains d'efficacité du travail
- Installations multiproduits (CDMO): La validation du nettoyage lors du changement de produit est simplifiée lorsque les outils de nettoyage sont à usage unique ; aucun risque de report entre les campagnes
Les vadrouilles réutilisables restent rentables lorsque :
- Fabrication à grande échelle (>2 000 m² de lavage quotidien) : un volume élevé de consommation de vadrouilles (plus de 1 000 vadrouilles/an) entraîne des coûts jetables supérieurs au TCO réutilisable, même avec la charge de retraitement incluse.
- Domaines de support ISO 8 à faible risque EM: Des exigences moindres en matière de contrôle de la contamination réduisent le fardeau des enquêtes ; l’économie du réutilisable s’améliore dans les environnements de qualité inférieure
- Une infrastructure de blanchisserie interne validée existe déjà: Les installations dotées d'opérations de blanchisserie matures et qualifiées et d'un suivi robuste du comptage cyclique réduisent le différentiel de coûts de retraitement.
- Priorité à la durabilité: Certaines organisations donnent la priorité à la réduction des déchets plutôt qu’à l’optimisation du TCO ; des systèmes réutilisables validés avec un contrôle documenté de la contamination offrent des profils de risque acceptables
Meilleurs cas d'utilisation des vadrouilles jetables dans les environnements BPF
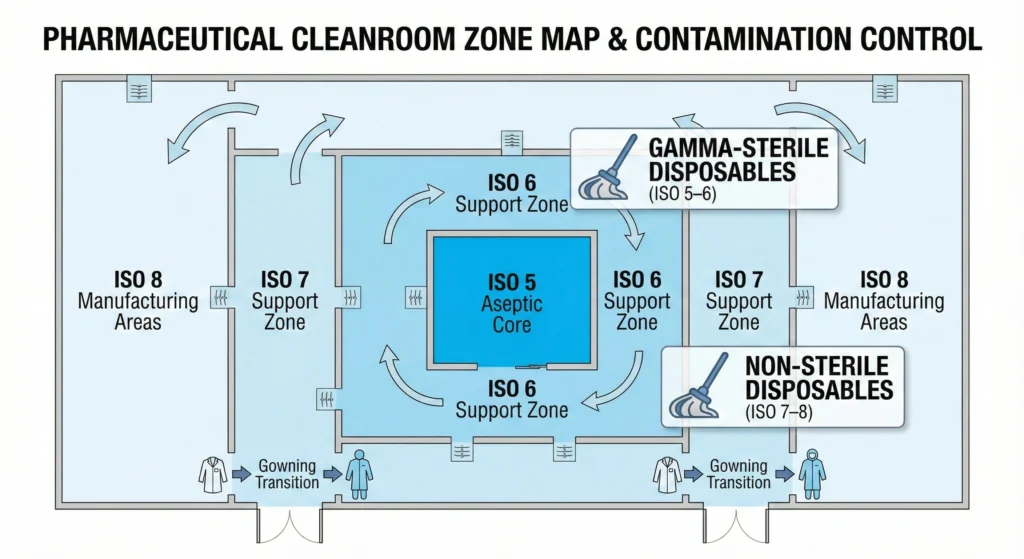
Les vadrouilles jetables pour salles blanches offrent une valeur maximale lorsque les exigences de contrôle de la contamination, les contraintes opérationnelles et les profils de risque correspondent à leurs atouts. Cette section répertorie les types d'installations spécifiques, les classifications ISO et les scénarios opérationnels dans lesquels les systèmes jetables justifient leur coût par un contrôle supérieur de la contamination et un coût total de possession réduit.
Noyaux aseptiques ISO classe 5 (grade A)
Exigences: Flux d'air unidirectionnel, limite de particules 3 520 particules ≥0,5 µm/m³, stérilisation terminale ou traitement aseptique, tolérance zéro à la charge microbienne
Pourquoi les produits jetables excellent:
- Les produits jetables gamma-stériles délivrent un SAL 10⁻⁶: Les vadrouilles réutilisables nécessitent un autoclavage pour la stérilité, ce qui entraîne une charge de validation du cycle de stérilisation, des exigences en matière d'indicateurs biologiques et des échecs potentiels de stérilisation. Les produits jetables irradiés aux rayons gamma arrivent pré-stérilisés avec des certificats, éliminant ainsi les exigences de stérilisation en interne.
- Zéro risque de contamination croisée: Les zones de catégorie A exigent un contrôle absolu de la contamination. Une seule utilisation croisée de vadrouille (utilisant une vadrouille ISO 7 de catégorie A en raison d'un manque de stock) introduit de la biocharge dans les zones aseptiques. Les produits jetables éliminent ce mode de défaillance.
- Performances prévisibles des particules: Les limites de particules sont extrêmes (3 520/m³). Les vadrouilles réutilisables éliminent de plus en plus de particules à mesure qu'elles vieillissent ; Les vadrouilles jetables en polyester à bords scellés maintiennent <50 particules/m² sur toutes les utilisations.
- Validation simplifiée: Les installations évitent la validation de l'autoclavage, la validation du suivi du comptage cyclique et les études de réduction de la charge microbienne dans la lessive, ce qui est essentiel pour les petites installations de biotechnologie disposant de ressources d'assurance qualité limitées.
Applications typiques:
- Lignes de remplissage aseptique (remplissage de flacons, remplissage de seringues, chargement pour lyophilisation)
- Suites de préparation stériles (pharmacies hospitalières, installations de préparation)
- Fabrication de thérapies cellulaires (traitement CAR-T, production de médicaments personnalisés)
- Nettoyage des enceintes de sécurité biologique et des isolateurs
Recommandation MIDPOSI: Serpillères jetables en polyester à bords scellés irradiés aux rayons gamma et validées <Performance 50 particules/m² et certificats de stérilité SAL 10⁻⁶
Zones de support aseptique ISO classe 6-7 (grade B/C)
Exigences: Limites de particules 35 200/m³ (ISO 6) à 352 000/m³ (ISO 7), charge biologique contrôlée, contrôle de la contamination par transfert de matière
Pourquoi les produits jetables excellent:
- Prévention de la contamination par transfert de matériaux: Les zones de grade B/C servent de sas et de zones de transfert de matériaux entre les zones de grade inférieur et les noyaux de grade A. Les vadrouilles réutilisables utilisées dans plusieurs zones deviennent des vecteurs de contamination. Les produits jetables garantissent que chaque cycle de nettoyage commence par un outil validé et sans contamination.
- Réduction du fardeau des enquêtes EM: Les zones de grade B/C font l'objet d'une surveillance électromagnétique élevée : toute excursion de particule ou de charge biologique déclenche une enquête. Les vadrouilles jetables aux performances prévisibles simplifient les tendances EM et réduisent les excursions liées aux outils de nettoyage.
- Efficacité du travail dans les installations multi-pièces: Les suites aseptiques comprennent souvent 5 à 10 salles de support interconnectées de grade B/C. Les systèmes jetables éliminent le suivi des vadrouilles dans les pièces, la vérification du décompte des cycles à chaque utilisation et la logistique de séparation du linge.
Facteurs de décision:
- Les établissements qui effectuent de fréquentes excursions d'EM en bénéficient le plus : même une enquête par an (coût de 5 000 à 10 000 $) compense les dépenses substantielles liées aux vadrouilles jetables.
- Opérations de petite et moyenne taille (<500 m² de surface totale de catégorie B/C) voir TCO jetable avantageux
- Les installations sans blanchisserie interne validée éliminent la dépendance à la blanchisserie de tiers
Applications typiques:
- Fonds de lignes de remplissage-arrivée et couloirs de support
- Sas de transfert de matériel entre les zones de grade C et de grade A
- Salles d'habillage desservant des noyaux aseptiques
- Zones de nettoyage et de préparation des équipements
Recommandation MIDPOSI: Produits jetables irradiés aux rayons gamma pour les zones critiques de grade B adjacentes aux zones de grade A ; jetables non stériles en polyester à bords scellés acceptables pour les zones de support de catégorie C avec validation <Performance 100 particules/m²
Fabrication ISO classe 8 (grade D) & Zones de support — Utilisation sélective
Exigences: Limite de particules 3 520 000/m³, surveillance de routine de la charge microbienne, risque de contrôle de contamination réduit
Quand les produits jetables ont du sens:
- Installations multi-produits (CMO/CDMO): Le nettoyage par changement de produit nécessite une élimination validée de la contamination croisée des produits. Les vadrouilles jetables simplifient le changement : aucun risque de résidus de produit antérieurs provenant des vadrouilles réutilisables.
- Fabrication de médicaments à haute puissance: Les composés très puissants (cytotoxiques, hormones) nécessitent une validation de nettoyage rigoureuse pour éviter l'exposition de l'opérateur et la contamination croisée. Les outils de nettoyage jetables éliminent le risque de transfert sans études approfondies de validation du nettoyage.
- Installations avec une infrastructure de blanchisserie limitée: Les startups de biotechnologie et les petits fabricants ne disposant pas de blanchisserie interne évitent de créer ou d'externaliser leurs opérations de blanchisserie en utilisant des produits jetables dans toutes les qualités ISO.
- Réponse à un événement de contamination: Après des excursions EM ou des événements de contamination, les installations peuvent temporairement passer aux produits jetables dans les zones touchées pendant l'enquête sur les causes profondes et la mise en œuvre du CAPA, garantissant ainsi que les outils de nettoyage ne contribuent pas à une contamination continue.
Quand les réutilisables restent optimaux:
- Zones de support ISO 8 à grande échelle (>Entrepôt de 1 000 m², systèmes de couloirs, fabrication générale) où le risque de contamination est faible et le volume de consommation de vadrouille est élevé
- Installations dotées d'une blanchisserie interne validée et de systèmes robustes de suivi du comptage des cycles déjà opérationnels
- Organisations donnant la priorité à la réduction des déchets et à la durabilité lorsque le profil de risque de contamination est acceptable
Applications typiques des produits jetables:
- Suites de fabrication d'API multi-produits (scénarios de changement de CMO)
- Zones de fabrication de substances médicamenteuses à haute puissance
- Aires de préparation pour le nettoyage des équipements desservant les zones à qualité supérieure
- Zones d’isolement pour les enquêtes de contamination
Recommandation MIDPOSI: Consommables jetables non stériles en polyester à bord scellé avec validation <Performance 100 particules/m² ; rentable pour un déploiement sélectif tout en conservant des systèmes réutilisables pour les zones de support à faible risque
Startups biotechnologiques & Installations BPF à petite échelle
Profil opérationnel: <20 personnes en salle blanche, ressources d'assurance qualité/validation limitées, pas d'infrastructure de blanchisserie interne, modèle opérationnel allégé, fabrication agile (petits lots, changements de produits fréquents)
Pourquoi les produits jetables sont stratégiques:
- Aucun investissement dans l’infrastructure de blanchisserie: Élimine un investissement en capital de 50 000 à 200 000 $ dans la construction de laveuses, sécheuses, autoclaves et buanderies industrielles
- Réduction du fardeau de la validation: Les équipes d'assurance qualité réparties sur plusieurs activités de validation (qualification des équipements, validation du nettoyage, validation des processus) bénéficient de l'élimination de la validation du linge, de la validation du suivi de l'inventaire tournant et de la validation de la stérilisation.
- Formation simplifiée des opérateurs: Une SOP unique (« Retirer de l'emballage, utiliser une fois, jeter ») réduit le temps de formation et le fardeau de la vérification des compétences.
- Coûts évolutifs: Les coûts jetables évoluent de manière linéaire avec le volume de production, idéal pour les startups en phase de fabrication précoce avec une fréquence de lots variable
- Démarrage rapide des installations: Les nouvelles suites GMP deviennent opérationnelles plus rapidement sans qualification des équipements de blanchisserie, sans développement de procédures de retraitement et sans validation du système de suivi.
Profils typiques:
- Startups biotechnologiques en fabrication clinique de phase I/II (1 à 5 lots par mois)
- Fabricants de thérapies cellulaires et géniques (médecine personnalisée, petits lots)
- Centres médicaux universitaires dotés de suites de préparation GMP
- Fabricants d'API spécialisés avec <Surface totale de salle blanche de 500 m²
Recommandation MIDPOSI: Programme complet de vadrouilles jetables pour toutes les qualités ISO : produits jetables gamma-stériles pour les noyaux aseptiques de qualité A/B, produits jetables non stériles pour les zones de support de qualité C/D, associé à un package de validation (données sur les particules, certificats de stérilité, rapports de compatibilité des matériaux) pour accélérer la préparation réglementaire.
Organisations de fabrication sous contrat (CMO/CDMO)
Défi opérationnel: Produits clients multiples fabriqués dans des salles blanches partagées ; des exigences strictes en matière de validation du nettoyage et de prévention de la contamination croisée des produits ; changements de produits fréquents
Pourquoi les produits jetables simplifient les opérations:
- Aucun risque de transfert de produit: Les études de validation du nettoyage doivent démontrer <10 ppm de résidu du produit précédent. Les outils de nettoyage jetables éliminent entièrement une voie de transfert : aucun risque de résidus de produits antérieurs incrustés dans les fibres de vadrouille réutilisables.
- Documentation de changement simplifiée: Les listes de contrôle de changement de produit incluent la vérification des outils de nettoyage. Les produits jetables éliminent le suivi médico-légal (« Cette serpillère a-t-elle été utilisée lors d'une campagne précédente ? Quel était son nombre de cycles ? Quand a-t-elle été lavée pour la dernière fois ? ») : les opérateurs utilisent simplement des produits jetables neufs.
- Confiance des clients: Les clients pharmaceutiques effectuant des audits et des due diligences évaluent les contrôles de contamination croisée. Les systèmes de nettoyage jetables démontrent une prévention proactive de la contamination et une complexité de validation réduite.
- Capacité flexible: Les CMO connaissent des calendriers de production variables. Les coûts jetables évoluent avec l'activité de fabrication réelle, évitant ainsi les coûts fixes d'exploitation de la blanchisserie pendant les périodes de faible utilisation.
Applications typiques:
- CMO de remplissage et de finition stériles traitant plusieurs produits clients
- CMO de fabrication d'API avec des suites multi-produits
- CDMO à petites molécules et substances médicamenteuses biologiques
- Fabrication spécialisée (API à haute puissance, substances contrôlées)
Recommandation MIDPOSI: Programmes de vadrouilles jetables pour les noyaux aseptiques (zones ISO 5 à 7) où s'effectue le changement de produit ; déploiement sélectif réutilisable dans des zones de support ISO 8 dédiées au service de campagnes mono-produit

Gamme de vadrouilles jetables pour salle blanche MIDPOSI (sélecteur de produits)
MIDPOSI fabrique des vadrouilles jetables pour salles blanches de qualité pharmaceutique, conçues spécifiquement pour les applications de contrôle de la contamination BPF. Tous les produits sont livrés avec des packages complets de documentation de validation (données de test de génération de particules, certificats de stérilité (pour les produits irradiés aux rayons gamma), rapports de compatibilité des matériaux et certificats d'analyse) permettant une qualification réglementaire et un démarrage rapide des installations.
Vadrouille jetable gamma-stérile MDCR-GS100 (ISO 5-6 Grade A/B)
Spécifications clés:
- Matériel: Tricot à filaments continus 100 % polyester à bords scellés, fabriqué en salle blanche pharmaceutique
- Stérilisation: Irradiation gamma (dose de 25 à 50 kGy) atteignant le niveau d'assurance de stérilité (SAL) 10⁻⁶
- Génération de particules: <50 particules ≥0,5 µm par mètre carré nettoyées (validées selon les méthodes de test ISO 14644-1)
- Base de référence pour la biocharge: Zéro micro-organisme viable (stérilisation terminale)
- Dimensions: Tête de balai 40 cm × 15 cm (compatible avec les systèmes de manche aluminium/inox MIDPOSI)
- Conditionnement: Emballage stérile en double emballage avec fermetures pelables ; sac intérieur adapté au transfert dans les zones de catégorie A/B
- Documentation: Certificat de stérilisation (dose délivrée, résultats des indicateurs biologiques, validation SAL), données de tests de particules, rapport de compatibilité des matériaux (IPA, peroxyde d'hydrogène, désinfectants à base d'ammonium quaternaire)
Candidatures validées:
- Lignes de remplissage aseptique (remplissage de flacons, montage de seringues, lyophilisation)
- Salles de préparation stériles (pharmacies hospitalières, établissements 503B)
- Salles blanches de fabrication de thérapies cellulaires et géniques
- Postes de sécurité biologique, isolateurs et systèmes de barrières à accès restreint (RABS)
Coût: 18 à 22 $ par vadrouille (tarif au volume disponible pour les installations utilisant >500 tampons par an)
Prise en charge des validations: Package de validation complet inclus avec la commande initiale : rapport de test de génération de particules selon la norme ISO 14644-1, certificat de stérilisation avec cartographie des doses et résultats des indicateurs biologiques, étude des extractibles démontrant <10 ppm de substances lixiviables après contact avec un désinfectant
Vadrouille jetable non stérile MDCR-NS200 (ISO 7–8 Grade C/D)
Spécifications clés:
- Matériel: Mélange de microfibres de polyester à bords scellés, fabriqué en salle blanche avec des performances validées à faible peluche
- Base de référence pour la biocharge: <10 UFC par tampon de vadrouille (contrôles de fabrication validés, tests de routine de la charge microbienne)
- Génération de particules: <100 particules ≥0,5 µm par mètre carré nettoyées
- Compatibilité chimique: Validé pour l'isopropanol, le peroxyde d'hydrogène (3 à 6 %), les composés d'ammonium quaternaire, le dioxyde de chlore et les désinfectants phénoliques
- Dimensions: Tête de vadrouille 40 cm × 15 cm (système de fixation universel compatible avec la plupart des manches de vadrouille salle blanche)
- Conditionnement: Emballage scellé peu pelucheux avec fermeture refermable (50 tampons de vadrouille par sac)
- Documentation: Données de tests de particules, rapport de base sur la charge microbienne, rapport de validation de compatibilité des matériaux
Candidatures validées:
- Zones de support aseptiques ISO classe 7 (fonds de remplissage-finition, vestiaires)
- Zones de fabrication pharmaceutique ISO classe 8 (production d'API, fabrication de comprimés, suites de conditionnement)
- Installations multi-produits nécessitant un nettoyage de changement (opérations CMO/CDMO)
- Zones d’isolement pour les enquêtes de contamination
Coût : 8 à 12 $ par tampon de vadrouille (remises sur volume pour >1 000 tampons par an)
Prise en charge des validations: Kit de validation du fournisseur fourni : rapport de test de génération de particules, documentation de base sur la charge microbienne (valeurs moyennes des UFC et du 95e centile), matrice de compatibilité chimique montrant la compatibilité avec les principaux désinfectants pharmaceutiques.
Vadrouille jetable pré-saturée MDCR-PSAT (prête à l'emploi avec IPA ou désinfectant)
Spécifications clés:
- Matériel: Polyester à bords scellés avec capacité d'absorption et rétention de désinfectant validées
- Options de saturation: 70 % isopropanol/30 % eau (qualité USP) ; 3 % de peroxyde d'hydrogène ; ou désinfectant spécifié par l'établissement (saturation personnalisée disponible)
- Stérilisation: Irradiation gamma post-saturation atteignant SAL 10⁻⁶ (désinfectant stérile et vadrouille stérile)
- Génération de particules: <50 particules/m² (comparable au MDCR-GS100)
- Expiration: Durée de conservation de 24 mois (l'emballage en aluminium scellé empêche l'évaporation)
- Conditionnement: Sachets individuels en aluminium (prêts à transférer dans les zones de catégorie A/B) ou paquets de 25 vadrouilles pour une utilisation de catégorie C/D
Candidatures validées:
- Nettoyage ponctuel et intervention en cas de déversement dans les zones aseptiques
- Nettoyage de petites surfaces (<Pièces de 50 m²) où la préparation du désinfectant n'est pas pratique
- Nettoyage d'urgence pendant la production (pas d'interruption pour le mélange du désinfectant)
- Installations cherchant à éliminer la préparation de désinfectants et l’exposition par contact des opérateurs
Coût: 22-28 $ par vadrouille (coût plus élevé en raison de la saturation du désinfectant et de la stérilisation après saturation)
Prise en charge des validations: Ensemble complet de validation comprenant des tests d'efficacité du désinfectant (log de réduction contre les organismes cibles), des données de génération de particules après saturation, un certificat de stérilité et des tests de compatibilité démontrant l'absence de résidus de surface ou de dégradation des matériaux.
Systèmes de poignée MIDPOSI (réutilisables, compatibles avec tous les tampons de vadrouille jetables)
Poignée en aluminium MDH-AL100 (Applications ISO 7-8) :
- Construction légère en aluminium anodisé (150 grammes)
- Autoclavable à 134°C (validé pour 100 cycles de stérilisation)
- Clip de fixation universel compatible avec les tampons de vadrouille MDCR-GS100, MDCR-NS200 et MDCR-PSAT
- Coût : 85 $ par poignée
Poignée en acier inoxydable MDH-SS200 (Applications ISO 5-6 grade A/B) :
- Construction en acier inoxydable 316L (résistant à la corrosion, génération de particules nulles)
- Autoclavable à 134°C (validé pour plus de 200 cycles de stérilisation)
- Finition de surface lisse, sans crevasses (désinfection facile, sans abri de charge microbienne)
- Système de fixation universel
- Coût : 140 $ par poignée
Comment commander et demander des packages de validation
MIDPOSI fournit un support technique et réglementaire complet aux installations évaluant ou mettant en œuvre des programmes de vadrouilles jetables pour salles blanches :
Kits d’échantillons pour les tests pilotes:
- Demandez 10 à 20 échantillons de tampons de vadrouille (MDCR-GS100 ou MDCR-NS200) pour une évaluation en interne
- Comprend : package de validation (données sur les particules, rapports de stérilité/microcharge, matrice de compatibilité), instructions d'utilisation et fiche technique
- Les tests pilotes permettent aux installations de valider les performances dans des conditions opérationnelles réelles avant l'approvisionnement complet.
Contenu du package de validation (Fourni avec toutes les commandes) :
- Rapport de test de génération de particules: Tests conformes à la norme ISO 14644-1 documentant les particules ≥0,5 µm par m² nettoyé
- Certificat de stérilité (pour les produits irradiés gamma) : Dose délivrée, résultats des indicateurs biologiques, validation SAL 10⁻⁶
- Rapport de référence sur la biocharge (pour les produits non stériles) : unités formant colonies (UFC) par tampon de vadrouille, testées selon USP <61> et <62>
- Validation de compatibilité des matériaux: Matrice de compatibilité ne montrant aucune dégradation ni augmentation de la génération de particules après un contact avec des désinfectants spécifiés par l'installation (IPA, peroxyde d'hydrogène, composés d'ammonium quaternaire, dioxyde de chlore)
- Etude des matières extractibles et lixiviables: Démonstration <10 ppm de substances lixiviables après contact avec un désinfectant (analyse GC-MS selon ICH Q3C)
- Certificat de conformité: Vérification de la conformité spécifique d'un lot aux spécifications relatives aux particules, à la charge biologique et à la stérilité
Consultation technique:
- Les spécialistes du contrôle de la contamination de MIDPOSI fournissent des recommandations spécifiques à l'installation basées sur la classification ISO, l'historique des défaillances EM, l'échelle opérationnelle et l'optimisation du TCO.
- Prise en charge des soumissions réglementaires : résumés de validation formatés pour les dépôts réglementaires FDA, EMA ou PMDA
- Études de validation personnalisées disponibles (tests de résistance de contact, compatibilité avec des désinfectants spécifiques, études étendues de génération de particules)
Contact pour les prix, les échantillons et l'assistance technique:
- E-mail: [email protected]
- Temps de réponse: Devis et packages de validation livrés dans les 12 heures suivant la demande
- Délai de mise en œuvre: Les articles en stock sont expédiés sous 48 heures ; configurations personnalisées (dimensions spécifiques, saturation de désinfectant personnalisée) expédiées sous 2 semaines









