クリーンルーム消耗品のバッチトレーサビリティは、単なる文書化作業ではありません。これは、製造業者、滅菌処理チーム、規制対象施設が原材料、生産、滅菌、流通、最終用途を 1 つの検証可能な証拠チェーンに結び付けることを可能にする運用のバックボーンです。
製薬、バイオテクノロジー、半導体、医療機器の環境では、トレーサビリティが不完全であると、書類上のギャップをはるかに超えたリスクが生じます。それは調査を遅らせ、リコールへの対応を弱め、監査を複雑にし、汚染管理プログラムに対する信頼を損ないます。堅牢なシステムは、品質チームが事後的な記録収集から予防的な管理に移行するのに役立ちます。
クリーンルーム消耗品のバッチトレーサビリティとは、材料の入荷から製造、滅菌、流通、最終使用に至るまでの各バッチの完全な検索可能な記録を維持することを意味します。実際には、効果的なシステムでは、何が製造され、どの原材料から、どのようなプロセス条件で、どこで出荷され、逸脱やリコールが発生した場合にどの顧客または内部ユーザーが影響を受けるかを特定する必要があります。
規制対象施設の場合、最良のシステムは単に紙の上で準拠しているだけではありません。これらは検索が速く、検証が簡単で、監査に対応しており、目標を絞ったリコールを数日ではなく数時間以内にサポートできます。
強力なバッチトレーサビリティにより、原材料のロット、生産バッチ、滅菌記録、出荷データ、エンドユーザーの消費が単一の証拠チェーンにリンクされます。
監査対応システムは、切断された記録を受動的に保存するだけでなく、迅速な調査と対象を絞ったリコールをサポートする必要があります。
明確なバッチ番号付けロジックにより、オペレーターの混乱が軽減され、下流のレポート、ラベル付け、リリース、苦情処理が改善されます。
前方トレーサビリティ、後方トレーサビリティ、およびリコール シミュレーションを定期的にテストして、システムが圧力下で実際に動作することを証明する必要があります。
多くの施設では、すでにバッチ番号をカートン、ラベル、または滅菌文書に記録しています。問題は、これらの記録が購買、倉庫、生産、滅菌、物流、エンドユーザーのログにわたって断片化されていることが多いことです。苦情、汚染イベント、または監査要求が発生すると、チームは履歴を手動で再構築する必要があります。
このアプローチは時間がかかり、エラーが発生しやすく、コストがかかります。成熟したトレーサビリティ プログラムは、調査時間を短縮し、リリースの信頼性を向上させ、リコール措置の範囲を制限します。また、傾向分析、サプライヤー管理、CAPA、顧客コミュニケーションもサポートします。

クリーンルームの消耗品トレーサビリティ システムは、規制対象組織が逸脱を調査し、管理を証明する方法を中心に設計する必要があります。多くのユーザーにとって最も関連性の高い参考資料には、EU GMP Annex 1、FDA cGMP 記録管理の期待事項、医療機器関連の品質システムに関する ISO 13485 トレーサビリティ要件などがあります。
| 規制・規格 | 重点領域 | 運用上の意味 |
|---|---|---|
| ME GMP Annex 1 | トレーサビリティ、バッチ記録、リコール機能 | 施設は、調査や市場活動中に、影響を受ける材料と完成品を迅速に特定できる必要があります。 |
| FDA 21 CFR 211.180 / 211.198 | 配布記録、苦情ファイル、保存 | 記録は、苦情の評価、ロットの影響レビュー、および管理されたリコールの実行をサポートする必要があります。 |
| ISO 13485 セクション 7.5.8 | 一意の識別と検索 | 組織は、文書化されたトレーサビリティ手順を維持し、必要に応じてリンクされた記録を取得できるようにする必要があります。 |
これは、バイヤーと QA チームにとって、トレーサビリティを倉庫のみの機能として扱うべきではないことを意味します。これは、サプライヤーの管理、生産文書、滅菌リリース、出荷履歴、エンドユーザーの説明責任に関わる部門横断的な品質要件です。
バッチのトレーサビリティを構築する有効な方法は、システムを原材料、製造、滅菌、流通、消費という 5 つの接続された層に分割することです。このフレームワークは、チームがエンドツーエンドの可視性を失うことなく、所有権、データ フィールド、検証チェックポイントを定義するのに役立ちます。
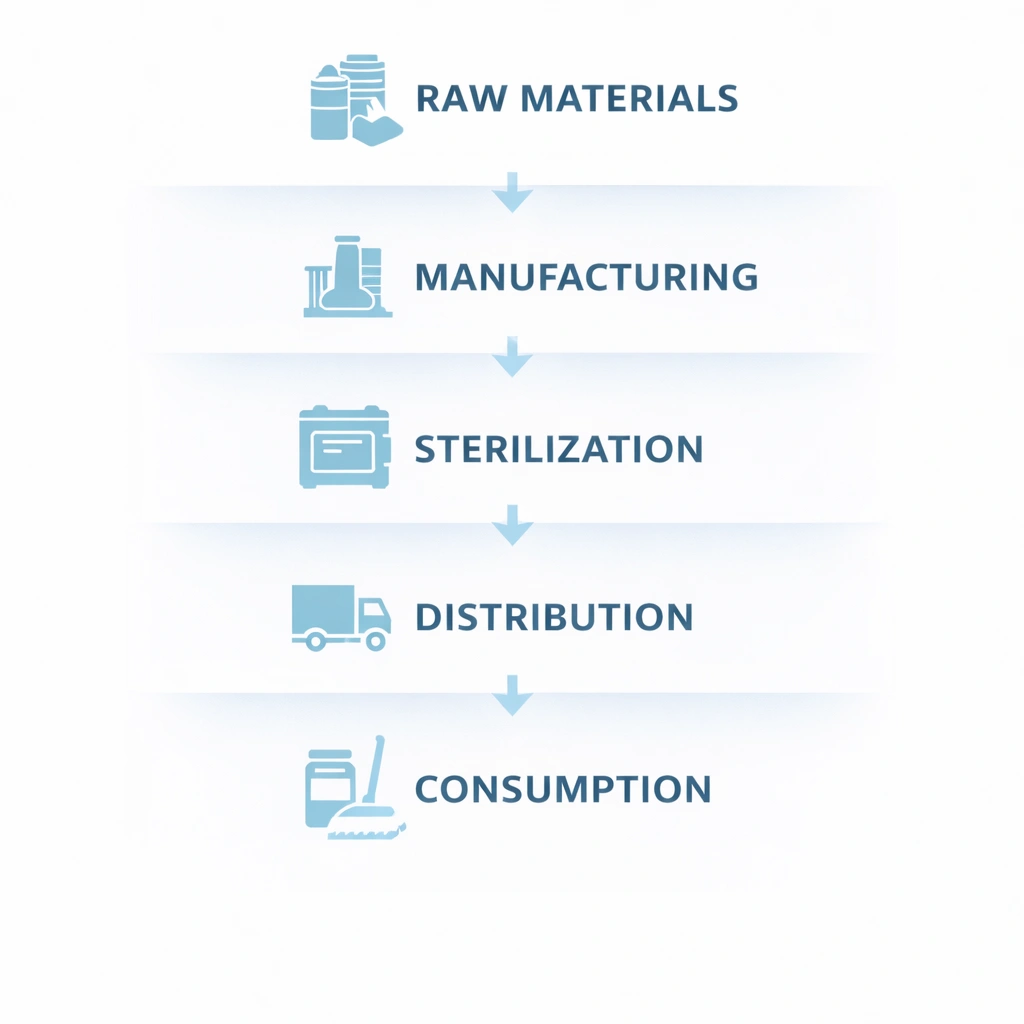
サプライヤーの ID、サプライヤーのロット番号、受領日、受入検査ステータス、COA や CoC などの関連証明書を取得します。これが上流制御の開始点です。
どの材料が使用されたか、どのラインでバッチが製造されたか、誰がプロセスを操作またはリリースしたか、どの工程内チェックまたは最終 QC チェックが実行されたかを記録します。
滅菌消耗品の場合は、生産バッチを滅菌バッチ、サイクルパラメータ、滅菌方法、リリースステータス、および検証証拠にリンクします。
バッチ番号を顧客、出荷数量、出荷日、配送業者情報、および宛先の詳細にリンクします。これは苦情のトリアージとリコールの封じ込めに不可欠です。
使用モデルで必要な場合は、バッチ番号、使用日、場所、廃棄ルートのユーザー側の記録を維持してください。これは、リスクの高い GMP 環境では特に価値があります。
バッチ番号はシリアルスタンプ以上である必要があります。迅速な解釈、正確な保管、きれいなラベルの表示、およびエラーの少ない手動処理をサポートする必要があります。構造化フォーマットにより、デジタル検索とレポートの信頼性も高まります。

| バッチ要素 | 例 | なぜそれが重要なのか |
|---|---|---|
| サプライヤー/メーカーコード | ミドポシ | 製造元を特定し、ブランド、サイト、または供給の流れを分離します。 |
| 日付セグメント | 2026-04-06 | オペレーターが生産年表と保持ロジックを迅速に特定できるようにします。 |
| シリアルナンバー | 001 | 同じ日またはサイクルウィンドウ内で生産された複数のバッチを区別します。 |
| サフィックス/プロセスマーカー | A / B / C | 生産、滅菌、再滅菌、または QA ワークフローの区別に役立ちます。 |
裏付けとなる記録が不完全であれば、強力な物理的ラベル付けでも十分ではありません。防御可能なトレーサビリティ ファイルにより、レビュー担当者は完成バッチから原材料に戻り、原材料から影響を受けるすべての完成バッチおよび顧客出荷に進むことができる必要があります。
仕入先ロット、入荷数量、検査結果、書類チェック、リリース状況。
バッチ番号、オペレーター、ライン、プロセス日付、材料使用量、QC チェックポイント、偏差。
滅菌ロット、サイクルデータ、リリース決定、顧客出荷数量、仕向地、クレーム連携。
また、ドキュメント セットは、サプライヤーの監査、顧客の認定、苦情処理、CAPA レビューの際に簡単に取得できる必要があります。適切なファイルを見つけるのに時間がかかりすぎる場合は、システムの機能が机上の見た目よりも弱いことになります。
トレーサビリティ システムは想定されるものではなく、テストされるべきです。最も現実的なアプローチは、前方トレーサビリティ、後方トレーサビリティ、リコール シミュレーションの 3 種類の演習を実行することです。これらのテストにより、データ フィールドが本当にリンクされているかどうか、チームがどこを見ればよいかを知っているか、応答時間が内部の期待を満たしているかどうかが明らかになります。
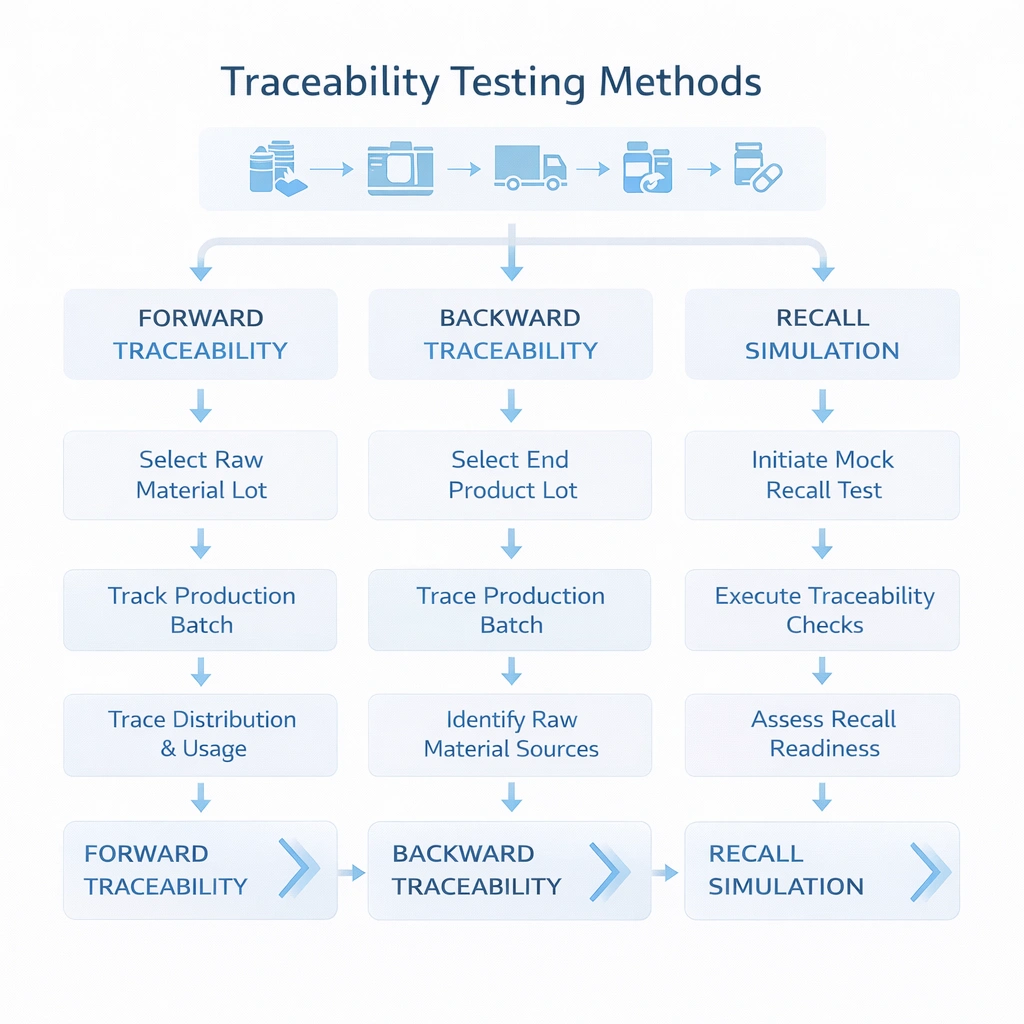
入荷する材料ロットから始めて、どの生産バッチ、滅菌サイクル、および顧客への出荷が影響を受けたかを特定します。
苦情や顧客が使用したバッチから始めて、原材料、プロセス記録、リリース ステータスまで遡ります。
バッチを選択し、対象となるリコールをシミュレーションします。影響を受けるすべての顧客、数量、出荷ルートを特定し、所有者に連絡します。必要な合計時間と見つかったデータのギャップを記録します。高度に管理された環境では、この演習は、システムが本当にリコール対応であるかどうかを評価するための最も迅速な方法の 1 つです。
| テストの種類 | 主な質問 | 期待される出力 |
|---|---|---|
| フォワードトレーサビリティ | この入力はどこへ行ったのでしょうか? | 生産、滅菌、出荷記録に影響 |
| 過去のトレーサビリティ | 何がこの結果を生み出したのでしょうか? | ソース資料、プロセス履歴、リリース証拠 |
| リコールシミュレーション | 迅速かつ正確に行動できるでしょうか? | 顧客リスト、数量マップ、応答タイミング、データギャップログ |
リコールのワークフローは、即興で作るのではなく、事前に決めておく必要があります。品質上の問題が発生した場合、チームは問題を分類し、影響を受けるバッチを特定し、関係者に通知し、さらなる配布を停止し、根本原因と是正措置を文書化する方法をすでに知っている必要があります。
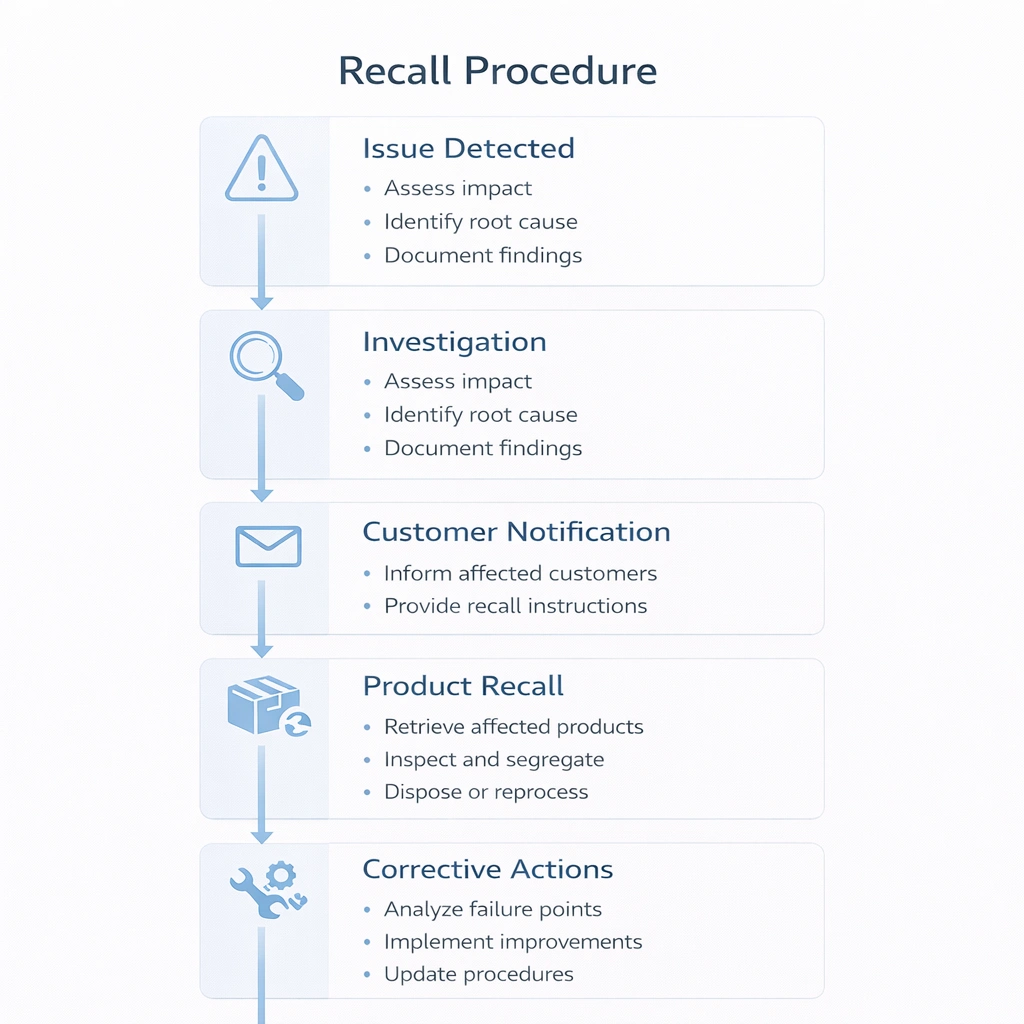
スプレッドシートベースのシステムはそれほど複雑ではありませんが、製品範囲、顧客数、無菌ワークフローが拡大するにつれて、通常は電子トレーサビリティがより実用的になります。バーコードまたは RFID をサポートするシステムは、手動入力のリスクを軽減し、リコール シミュレーションをより迅速かつ再現可能にします。

データフィールド、所有権、バッチコードロジック、保持ルール、滅菌ラインと非滅菌ラインのトレーサビリティ範囲を定義します。
フォーム、サプライヤーのロットキャプチャ、生産記録、滅菌連携、出荷記録を標準化します。
順方向トレーサビリティ、逆方向トレーサビリティ、リコール シミュレーション テストを実行し、見つかったギャップを文書化します。
少なくとも、システムは、入荷する材料ロット、生産バッチ、リリースまたは滅菌記録(該当する場合)、出荷履歴、および調査中に影響を受ける顧客またはユーザーを特定する機能を接続する必要があります。
バッチラベル付けにより製品グループが識別されます。上流の材料、プロセス記録、リリース決定、および下流の流通または使用記録にラベルを付ける完全なトレーサビリティ リンク。
多くの品質チームは少なくとも年に一度テストを実行しますが、高リスクまたはより複雑な運用では、特にシステム変更、サプライヤーの変更、または大規模な CAPA アクションの後、より頻繁にテストする場合があります。
はい、少量の操作の場合は可能です。しかし、製品のバリエーション、無菌管理、または顧客の複雑さが増すと、通常はデジタル システムの方が検索速度が向上し、エラーが軽減され、監査制御が提供されます。
無菌製品では、苦情、無菌性に関する懸念、またはリコールの決定が生じた場合に、バッチ履歴、滅菌連携、放出証拠、および下流の可視性をより厳密に管理する必要があるためです。
Midposi は、認定、無菌ステータスのレビュー、バッチのトレーサビリティに関する議論のための文書指向のコミュニケーションなど、管理された環境向けに設計されたクリーンルーム用消耗品で規制対象のバイヤーをサポートします。


1営業日以内にご連絡いたします。末尾が次のメールに注意してください 「*@midposi.com」.