Отслеживание партий расходных материалов для чистых помещений — это не просто процедура документирования. Это операционная основа, которая позволяет производителям, командам по стерильной обработке и регулируемым предприятиям связывать сырье, производство, стерилизацию, распространение и конечное использование в одну поддающуюся проверке цепочку доказательств.
В фармацевтической, биотехнологической, полупроводниковой и медицинской промышленности неполная прослеживаемость создает риски, выходящие далеко за рамки пробелов в документации. Это задерживает расследования, ослабляет реакцию на отзыв, усложняет проверки и подрывает доверие к программам контроля загрязнения. Надежная система должна помочь командам по обеспечению качества перейти от реактивного сбора записей к упреждающему контролю.
Отслеживание партий расходных материалов для чистых помещений означает ведение полной и восстанавливаемой записи каждой партии от входящего материала до производства, стерилизации, распределения и конечного использования. На практике эффективная система должна идентифицировать, что было произведено, из каких исходных материалов, при каких условиях процесса, куда это было отправлено и какие клиенты или внутренние пользователи пострадали в случае отклонения или отзыва.
Для регулируемых объектов лучшие системы соответствуют требованиям не только на бумаге. Их можно быстро найти, легко проверить, они готовы к аудиту и способны обеспечить целенаправленный отзыв в течение нескольких часов, а не дней.
Надежная отслеживаемость партий связывает партии сырья, производственные партии, записи о стерилизации, данные об отправке и потреблении конечными пользователями в единую цепочку доказательств.
Системы, готовые к аудиту, должны поддерживать быстрое расследование и целенаправленный отзыв, а не просто пассивное хранение разрозненных записей.
Четкая логика нумерации партий уменьшает путаницу операторов и улучшает последующую отчетность, маркировку, выпуск продукции и обработку рекламаций.
Прямая и обратная отслеживаемость и моделирование отзыва должны периодически проверяться, чтобы доказать, что система действительно работает под давлением.
Многие учреждения уже записывают номера партий на картонных коробках, этикетках или документах о стерилизации. Проблема в том, что эти записи часто фрагментированы по журналам закупок, склада, производства, стерилизации, логистики и конечных пользователей. Когда возникает жалоба, событие загрязнения или запрос на аудит, команде приходится восстанавливать историю вручную.
Такой подход медленный, подвержен ошибкам и дорог. Развитая программа отслеживания сокращает время расследования, повышает надежность выпуска и ограничивает объем действий по отзыву. Он также поддерживает анализ тенденций, управление поставщиками, CAPA и общение с клиентами.

Система отслеживания расходных материалов для чистых помещений должна быть построена таким образом, чтобы регулируемые организации расследовали отклонения и доказывали наличие контроля. Для многих пользователей наиболее актуальными ссылками являются Приложение 1 к GMP ЕС, требования FDA к ведению документации cGMP и требования к прослеживаемости ISO 13485 для систем качества, связанных с медицинскими изделиями.
| Регламент/Стандарт | Область фокуса | Операционное значение |
|---|---|---|
| Приложение 1 GMP ЕС | Прослеживаемость, учет партий, возможность отзыва | Предприятия должны иметь возможность быстро идентифицировать затронутые материалы и готовую продукцию во время расследований или рыночных действий. |
| FDA 21 CFR 211.180/211.198 | Записи о распределении, файлы жалоб, хранение | Записи должны поддерживать оценку жалоб, анализ влияния партии и контролируемое выполнение отзыва. |
| ISO 13485, раздел 7.5.8. | Уникальная идентификация и поиск | Организация должна поддерживать документированные процедуры отслеживания и иметь возможность извлекать связанные записи, когда это необходимо. |
Для покупателей и команд контроля качества это означает, что отслеживаемость не должна рассматриваться как функция только склада. Это межфункциональное требование к качеству, касающееся контроля поставщиков, производственной документации, разрешения на стерилизацию, истории поставок и ответственности конечного пользователя.
Полезный способ структурировать отслеживание партий — разделить систему на пять взаимосвязанных уровней: сырье, производство, стерилизация, распределение и потребление. Эта платформа помогает командам определять права собственности, поля данных и контрольные точки проверки без потери сквозной прозрачности.
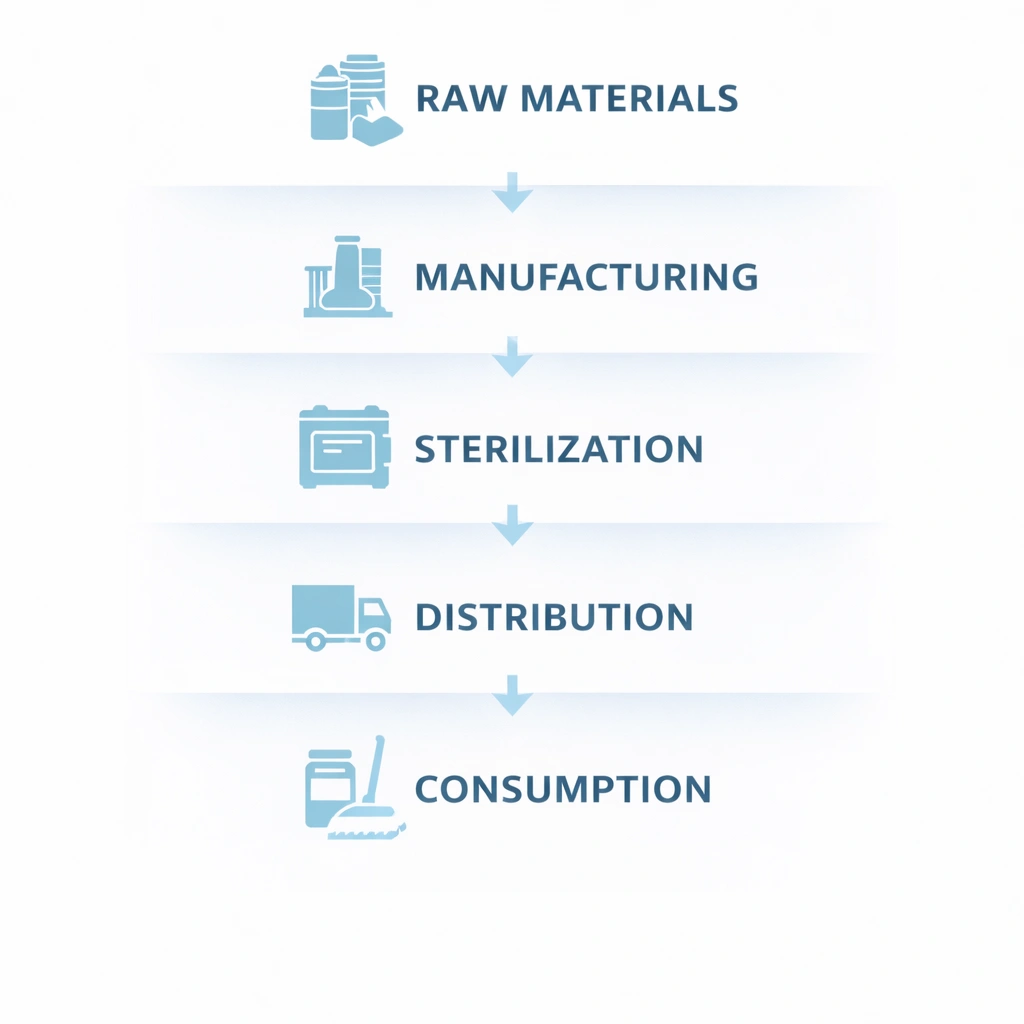
Зарегистрируйте данные поставщика, номер партии поставщика, дату поступления, статус входного контроля и соответствующие сертификаты, такие как сертификат подлинности или сертификат соответствия. Это отправная точка для восходящего контроля.
Запишите, какие материалы использовались, на какой линии производилась партия, кто управлял или запускал процесс, а также какие внутрипроизводственные или окончательные проверки качества выполнялись.
Для стерильных расходных материалов свяжите производственную партию с стерилизуемой партией, параметрами цикла, методом стерилизации, статусом выпуска и любыми подтверждающими данными.
Свяжите номера партий с клиентами, объемами поставок, датами отгрузки, информацией о перевозчике и деталями пункта назначения. Это важно для сортировки жалоб и сдерживания отзыва.
Если этого требует модель использования, ведите записи на стороне пользователя о номере партии, дате использования, местоположении и маршруте утилизации. Это особенно ценно в условиях GMP с высоким уровнем риска.
Номер партии должен быть больше, чем серийный штамп. Он должен обеспечивать быструю интерпретацию, точное хранение, представление чистой этикетки и ручную обработку с низким уровнем ошибок. Структурированный формат также делает цифровой поиск и отчетность более надежными.

| Пакетный элемент | Пример | Почему это важно |
|---|---|---|
| Код поставщика/производителя | МИДПОСИ | Определяет происхождение производства и разделяет бренды, площадки или потоки поставок. |
| Сегмент даты | 2026-04-06 | Помогает операторам быстро определить хронологию производства и логику хранения. |
| Серийный номер | 001 | Дифференцирует несколько партий, произведенных в течение одного дня или цикла. |
| Суффикс/маркер процесса | А/Б/С | Полезно для разграничения рабочих процессов производства, стерилизации, повторной стерилизации или контроля качества. |
Даже надежной физической маркировки недостаточно, если подтверждающие записи неполны. Защищенный файл отслеживания должен позволять рецензенту переходить от готовой партии обратно к исходным материалам и от исходного материала к каждой затронутой готовой партии и поставке клиенту.
Партия поставщика, полученное количество, результат проверки, проверка документов, статус выпуска.
Номер партии, оператор, линия, дата процесса, использование материала, контрольные точки контроля качества, отклонения.
Партия стерилизации, данные цикла, решение о выпуске, отгруженное клиенту количество, пункт назначения, связь с рекламациями.
Комплект документации также должен быть легко доступным во время аудита поставщиков, оценки клиентов, рассмотрения жалоб и проверок CAPA. Если поиск нужного файла занимает слишком много времени, система функционально слабее, чем кажется на бумаге.
Систему прослеживаемости следует тестировать, а не предполагать. Наиболее практичным подходом является проведение трех типов упражнений: прямая прослеживаемость, обратная прослеживаемость и моделирование отзыва. Эти тесты показывают, действительно ли поля данных связаны между собой, знают ли команды, где искать, и соответствует ли время ответа внутренним ожиданиям.
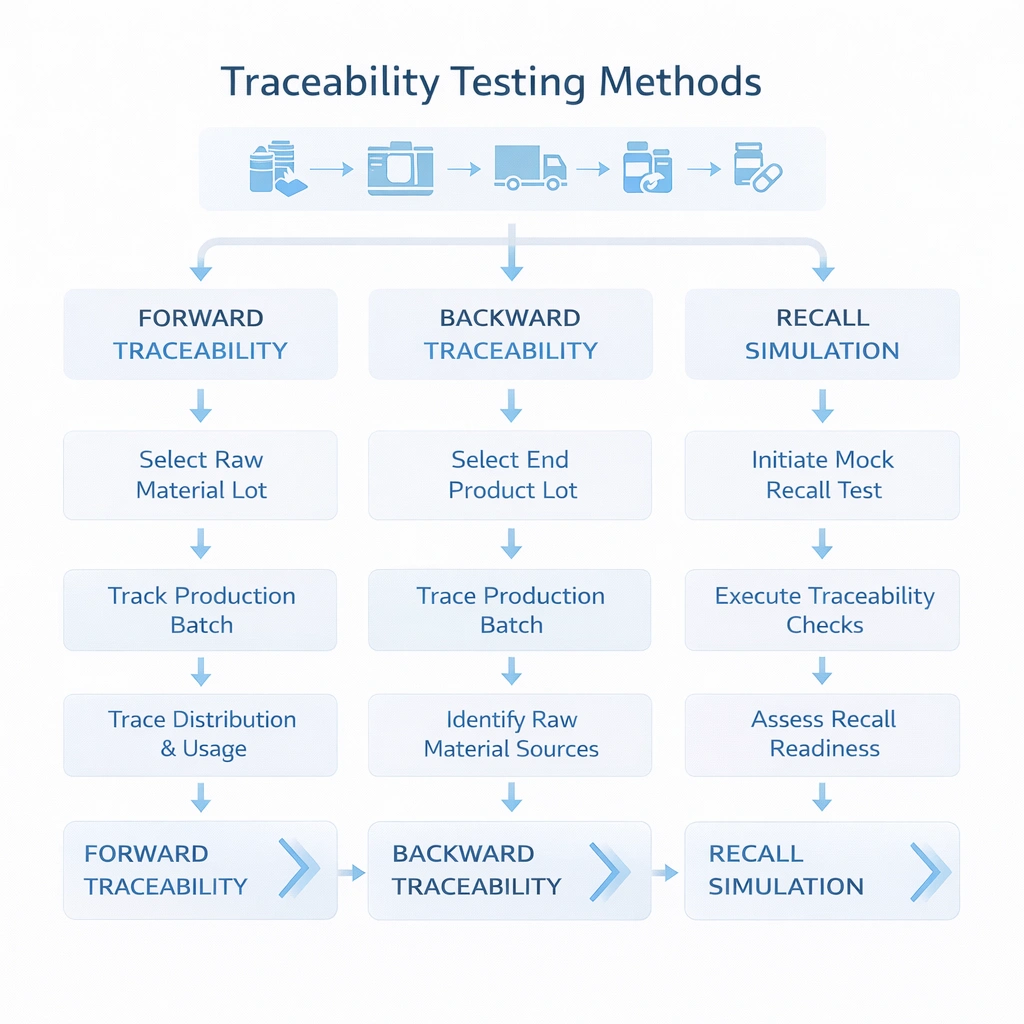
Начните с входящей партии материала и определите, какие производственные партии, циклы стерилизации и поставки клиентам были затронуты.
Начните с жалобы или партии, использованной клиентом, и проследите исходные материалы, записи процесса и статус выпуска.
Выберите партию и смоделируйте целевой отзыв: определите каждого затронутого клиента, количество, маршрут доставки и свяжитесь с владельцем. Запишите общее необходимое время и обнаруженные пробелы в данных. В средах с высоким уровнем контроля это упражнение является одним из самых быстрых способов оценить, действительно ли система готова к отзыву.
| Тип теста | Главный вопрос | Ожидаемый результат |
|---|---|---|
| Прямая отслеживаемость | Куда пропал этот ввод? | Затронутые записи о производстве, стерилизации и отгрузке. |
| Обратная прослеживаемость | Что привело к такому результату? | Исходный материал, история процесса, доказательства выпуска |
| Вспомнить моделирование | Можем ли мы действовать быстро и точно? | Список клиентов, карта количества, время ответа, журнал пробелов в данных |
Рабочий процесс отзыва должен быть заранее определен, а не импровизирован. При возникновении проблемы с качеством команды уже должны знать, как классифицировать проблему, идентифицировать затронутые партии, уведомлять заинтересованные стороны, останавливать дальнейшее распространение и документировать первопричину и корректирующие действия.
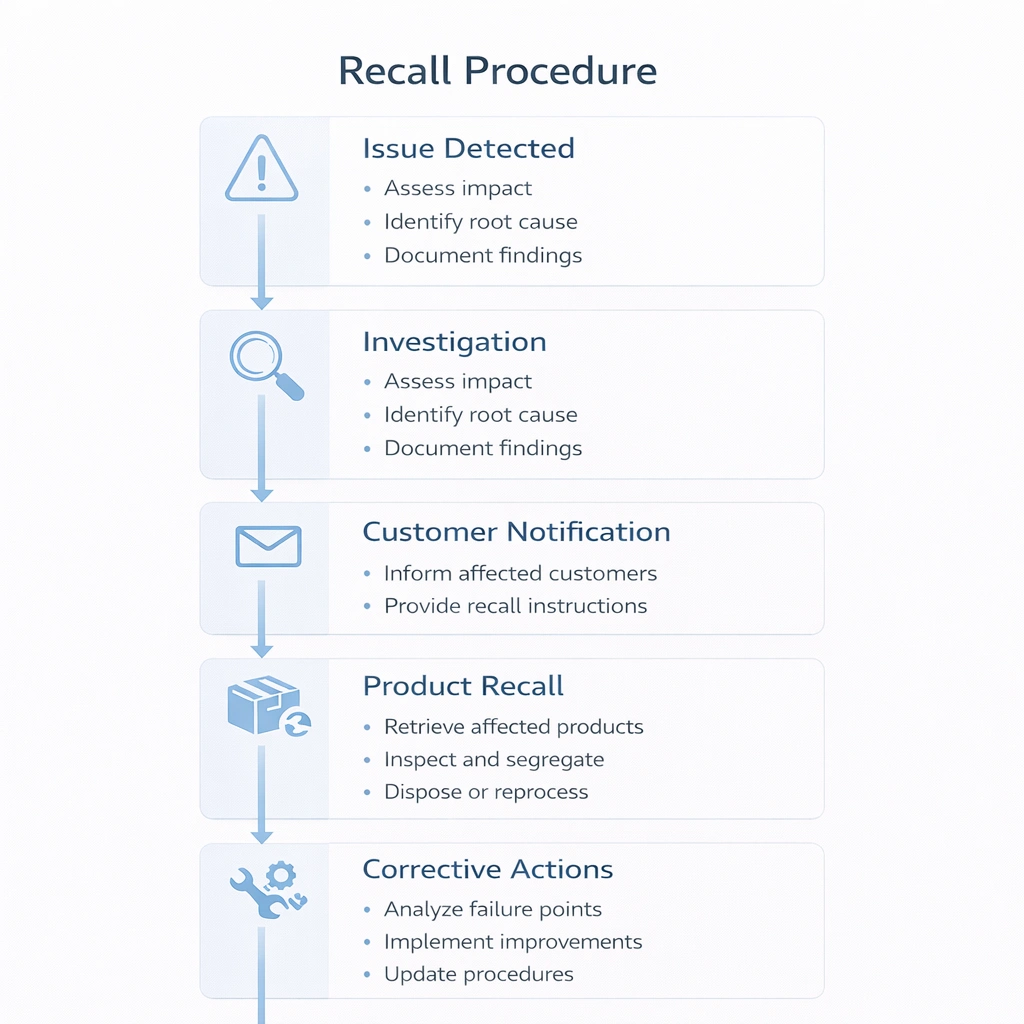
Системы на основе электронных таблиц могут работать с низкой сложностью, но по мере расширения ассортимента продукции, количества клиентов и рабочих процессов по стерильности электронное отслеживание обычно становится более практичным. Системы с поддержкой штрих-кодов или RFID снижают риск ручного ввода и делают моделирование отзыва более быстрым и повторяемым.

Определите поля данных, право собственности, логику кода партии, правила хранения и область отслеживания для стерильных и нестерильных линий.
Стандартизируйте формы, учет партий поставщика, производственные записи, привязку стерилизации и записи об отправке.
Выполните прямую и обратную отслеживаемость, а также вызовите симуляционные тесты и задокументируйте обнаруженные пробелы.
Как минимум, система должна связывать входящие партии материалов, производственные партии, записи о выпуске или стерилизации, где это применимо, историю поставок и возможность идентифицировать затронутых клиентов или пользователей во время расследования.
Маркировка партии идентифицирует группу продуктов. Полная прослеживаемость, которая маркирует исходные материалы, записи процессов, решения о выпуске и последующие записи о распространении или использовании.
Многие команды по обеспечению качества проводят тестирование не реже одного раза в год, в то время как операции с более высоким риском или более сложные операции могут проводиться чаще, особенно после изменений в системе, смены поставщиков или крупных действий CAPA.
Да, для небольших объемов операций. Но как только увеличивается разнообразие продуктов, контроль стерильности или сложность клиентов, цифровые системы обычно обеспечивают лучшую скорость поиска, снижение ошибок и контроль аудита.
Потому что стерильные продукты требуют более жесткого контроля за историей партий, привязкой к стерилизации, доказательствами выпуска и прозрачностью на последующих этапах в случае возникновения жалоб, проблем со стерильностью или решения об отзыве.
Midposi поддерживает регулируемых покупателей расходными материалами для чистых помещений, предназначенными для контролируемых сред, включая ориентированную на документацию коммуникацию для квалификации, проверку статуса стерильности и обсуждение отслеживания партии.


Мы свяжемся с вами в течение 1 рабочего дня, обратите внимание на письмо с суффиксом «*@midposi.com».