QA مينيجرز ۽ تصديق ڪندڙ انجنيئرن لاءِ هڪ ٽيڪنيڪل حوالو سائيٽ جي آلودگي ڪنٽرول حڪمت عملي (CCS) ۾ استعمال جي قابل سراغ جي انضمام تي.

جي ايم پي جي ريگيوليٽري ماحول ۾، ڪلين روم ايم او پي کي هاڻي عام افاديت جي طور تي نه ڏٺو ويو آهي پر هڪ نازڪ ڪنٽرول ان پٽ جي طور تي. بيچ ٽريس ايبلٽي صاف ڪرڻ وارو ڪمرو ايم پي سسٽم ٽن بنيادي ڪمن جي خدمت ڪن ٿا:
Product-level traceability identifies a SKU; batch-level traceability identifies the specific manufacturing event. For cleanroom mops, this requires a "genealogy" that links the finished product back to the specific lot of polyester yarn or microfiber fabric used, the cleanroom laundry shift, and the specific sterilization cycle.
جڏهن موپس کي ڪنٽرول ٿيل ان پٽ طور علاج ڪيو وڃي ٿو، هر انفرادي پيڪيج هڪ ڊيٽا پوائنٽ آهي. هي ڊيٽا QA ٽيمن کي اها تصديق ڪرڻ جي اجازت ڏئي ٿي ته انهن جي هٿ ۾ موجود پراڊڪٽ ڪارڪردگي ۽ پاڪيزگي ۾ هڪجهڙائي آهي پراڊڪٽ جي تصديق ٿيل ابتدائي سهولت جي شروعات يا PQ (ڪارڪردگي جي قابليت) دوران.
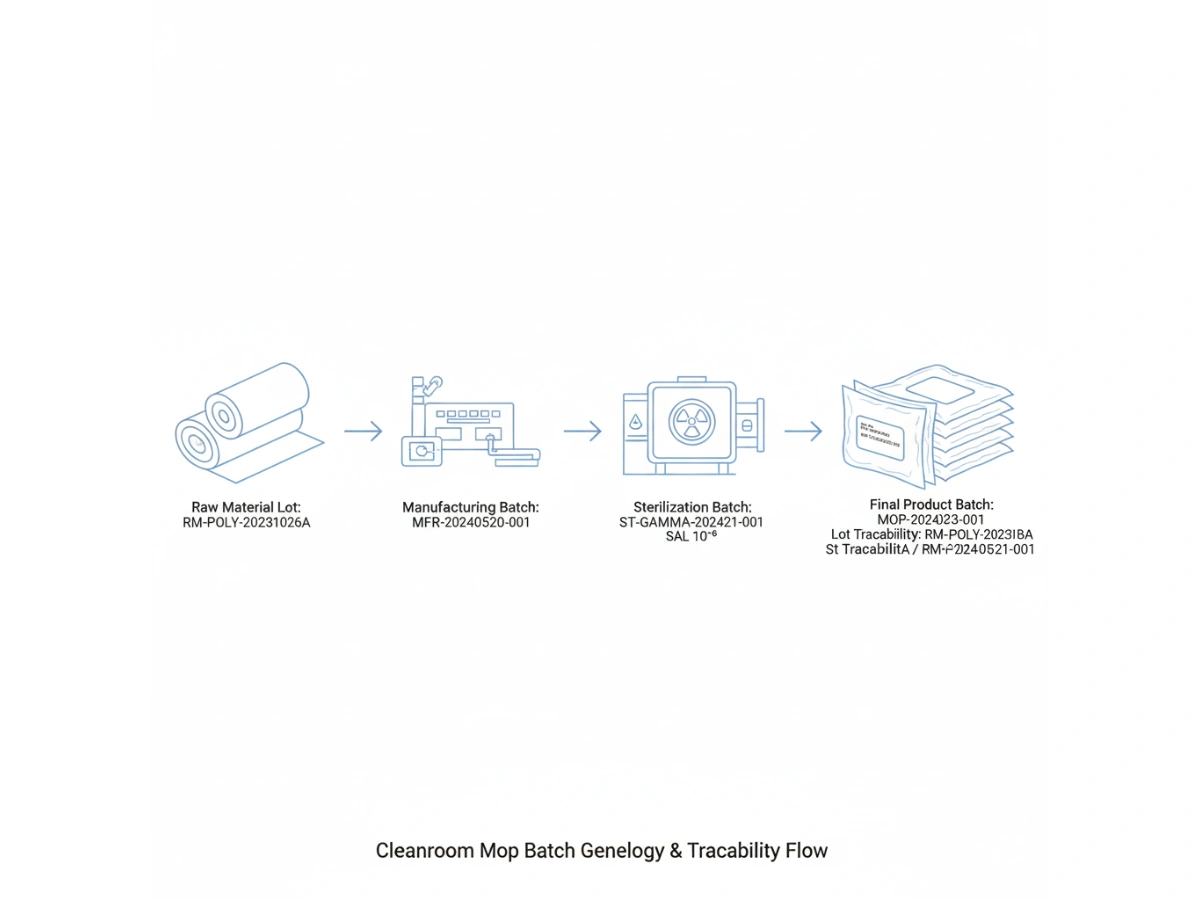
جديد GMP اصولن جي ضرورت آهي ته حساس سطحن سان رابطي ۾ اچڻ واري سڀني مواد کي مڪمل طور تي حساب ڪيو وڃي. هڪ معائنو دوران، هڪ آڊيٽر پيداوار جي تاريخ چونڊي سگهي ٿو ۽ پڇي سگھي ٿو تمام گهڻو traceability ان ڏينهن تي استعمال ٿيل صفائي واري مواد جو.
Expectations focus on the "Linkage of Records." An auditor will look for a seamless transition from the facility's cleaning logs to the بيچ-سطح دستاويز فراهم ڪندڙ طرفان فراهم ڪيل. جيڪڏهن هڪ ايم پي بيچ تجزيو جي سرٽيفڪيٽ (COA) يا نسبندي رڪارڊ سان ڳنڍيل نه ٿي سگهي، پوري صاف روم سوٽ جي جراثيم ۽ صفائي کي سوال ۾ سڏيو وڃي ٿو.

لاء هڪ مضبوط traceability نظام صاف ڪمرو استعمال ٿيندڙ GMP تعميل ۾ شامل هجڻ گهرجي:
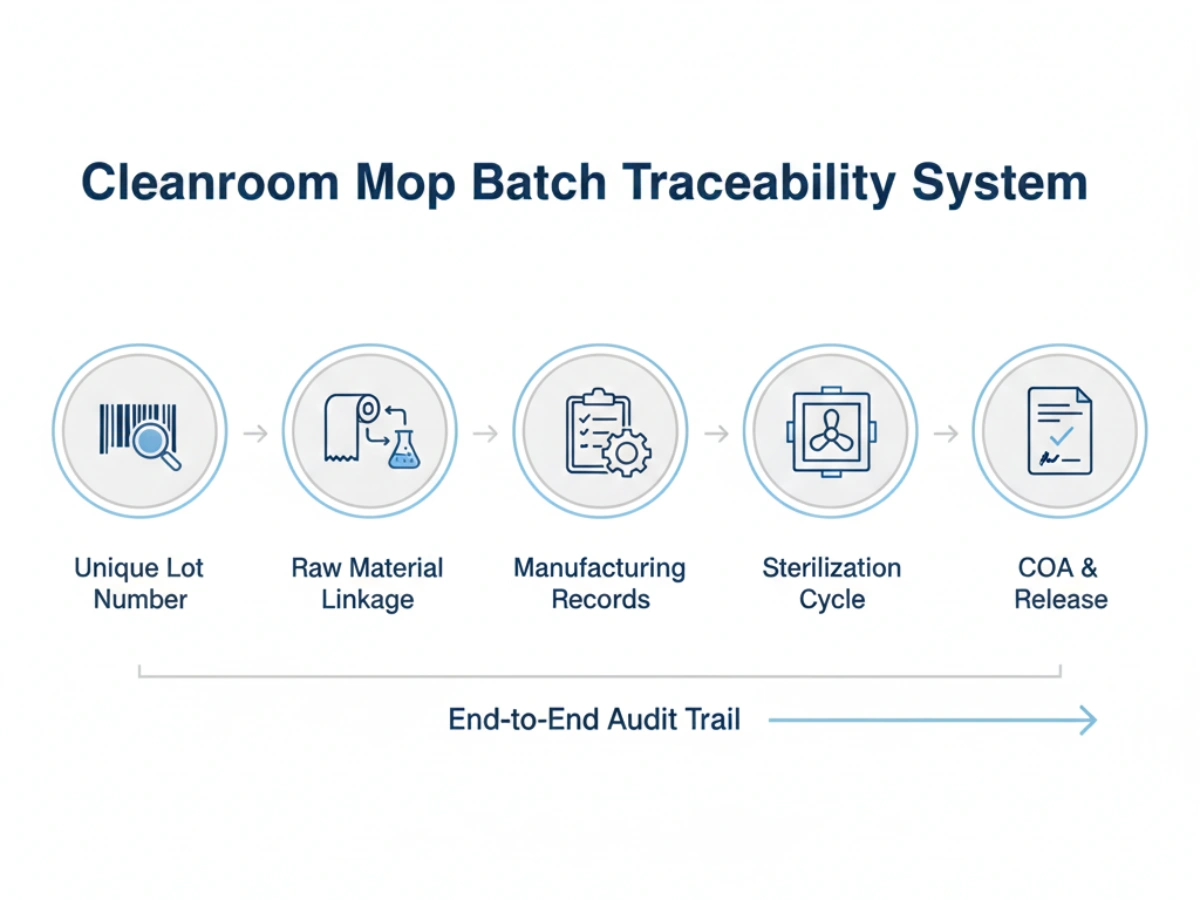
Supply stability is often threatened by "drift"—small, undocumented changes in manufacturing that accumulate over years. Batch traceability prevents this by establishing a baseline for گهڻي کان گهڻي مطابقت.
CAPA (اصلاحي ۽ بچاءُ واري عمل) جي صورت ۾ جنهن ۾ ماحولياتي نگراني (EM) اسپيڪس شامل آهن، سراغ رسي قابليت QA کي اهو طئي ڪرڻ جي اجازت ڏئي ٿي ته ڇا موپس جي هڪ مخصوص بيچ واقعي ۾ حصو ورتو آهي. انهي جي بغير، سهولت کي مجبور ڪيو وڃي ته سڀني انوینٽري کي رد ڪري ۽ پيداوار کي روڪيو، هڪ وڏي آپريشنل خطري کي وڌايو. Traceability هڪ امڪاني سهولت جي وسيع بحران کي مقامي مواد قرنطين ۾ تبديل ڪري ٿو.

اي pharmaceutical mop manufacturer / OEM acts as an extension of the pharma site’s quality system. Their responsibilities include:
For a qualified manufacturer, the ability to produce these records on demand is the hallmark of GMP maturity.
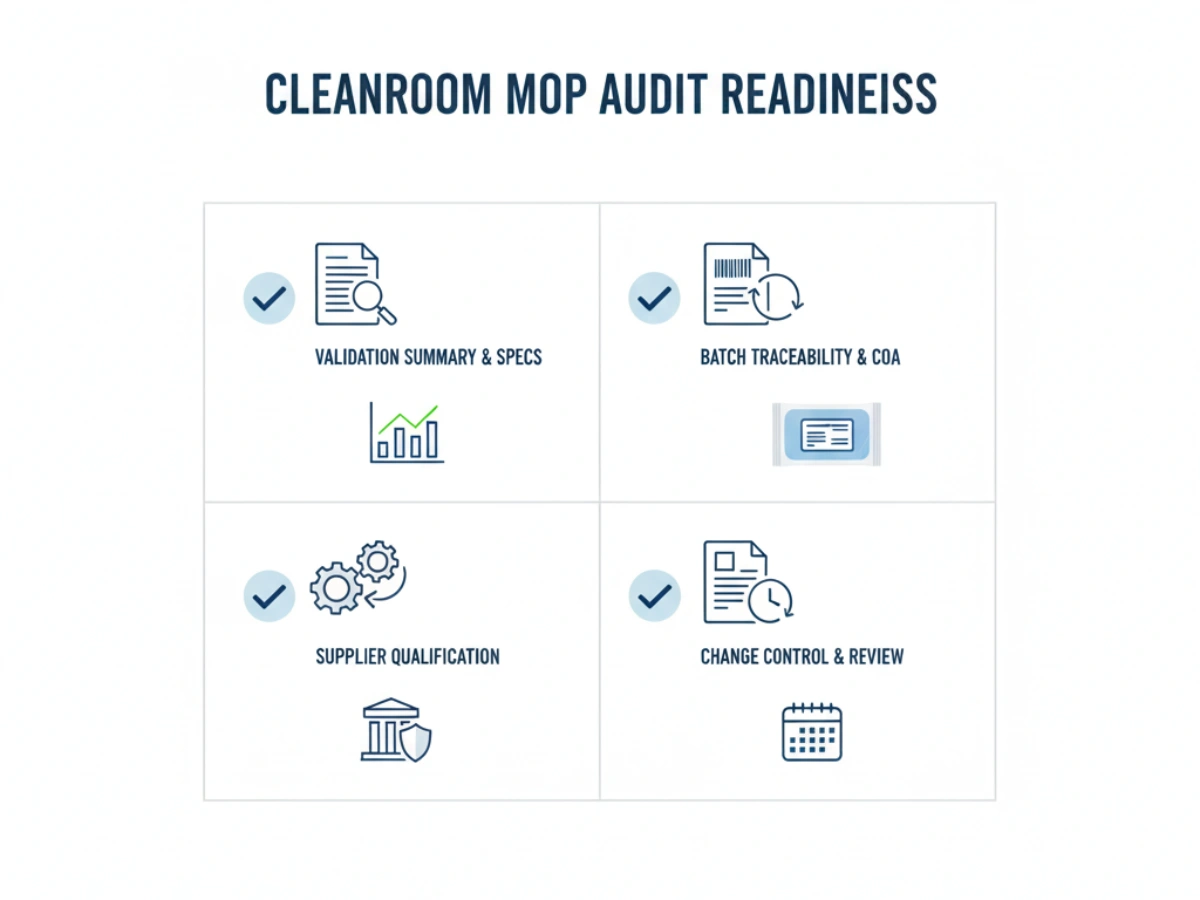
دوران OEM supplier qualification, QA teams should utilize the following checklist:
| Checkpoint | گهرج |
|---|---|
| Batch Definition | Is the batch size clearly defined and manageable? |
| Sample Retention | Does the supplier keep retain samples for every lot? |
| Audit Access | Can the supplier provide full raw material logs within 48 hours? |
| Physical Labeling | Is the batch number resistant to cleanroom disinfectants (IPA)? |
Batch traceability is not merely a documentation exercise; it is the backbone of a defensible quality system. In the context of Grade A and B environments, the ability to track every fiber and sterilization cycle ensures that the cleaning process remains a controlled variable rather than an unknown risk.
Mature pharmaceutical QA teams prioritize suppliers who demonstrate total transparency in their batch records, viewing them as long-term partners in patient safety and regulatory compliance.
Ask for lot genealogy, batch-specific COAs, sterilization linkage, and change-control readiness to strengthen your audit narrative.
Request Documentation Package

اسان توهان سان 1 ڪم ڪندڙ ڏينهن اندر رابطو ڪنداسين، مهرباني ڪري لاتعداد سان اي ميل ڏانهن ڌيان ڏيو "*@midposi.com".