Annex 1 مطابق صفائي واري ڪمري واري ماحول لاءِ گاما شعاعن جي بمقابله آٽو ڪلو اسٽريلائيزيشن جو ٽيڪنيڪل جائزو.

EU GMP Annex 1 تحت، موپنگ سسٽم جو هڪ نازڪ حصو بڻجي ٿو آلودگي ڪنٽرول حڪمت عملي (CCS). The selected sterilization method directly affects audit exposure, validation workload, and transfer risk for pharmaceutical facilities.
As explained in our pharmaceutical cleanroom mop supplier selection guide , sterility alone is not sufficient — material stability, packaging integrity, and documentation traceability must also be demonstrated.
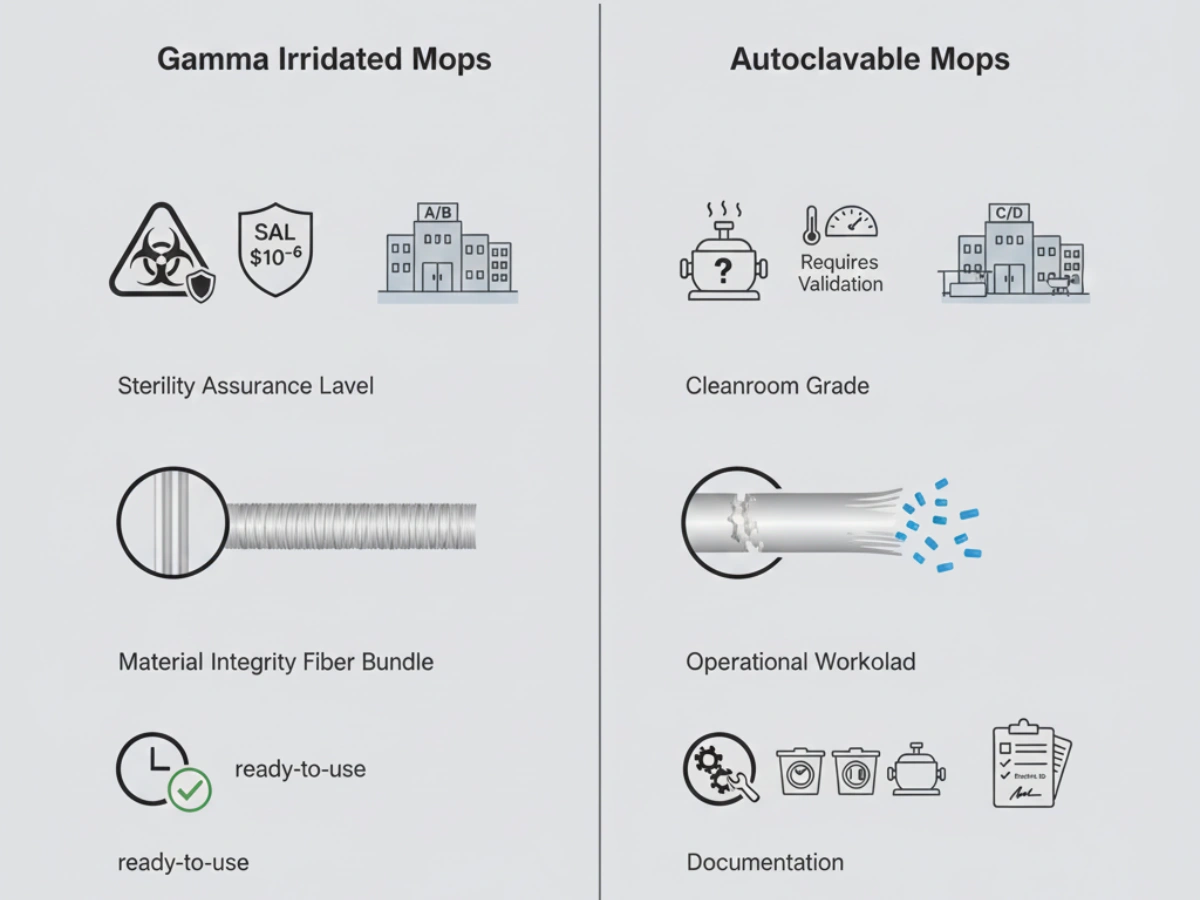
Gamma irradiation is a terminal "cold" sterilization process. Its penetrative nature ensures uniform sterilization throughout dense mop structures. Each batch is validated to SAL 10⁻⁶ and supplied with a batch-specific COI.

Autoclave sterilization relies on saturated steam (121 °C). Effective autoclaving requires dense mop heads to undergo validated vacuum cycles to eliminate trapped air and prevent cold spots.

ذرڙن جي شيڊنگ جي GMP حدن کان وڌي وڃڻ کان اڳ سهولتن کي وڌ ۾ وڌ قابل اجازت چڪرن جي تصديق ڪرڻ گھرجي.
| خاضري گهر | گاما Irradiated Mop | خودڪشي لائق Mop |
|---|---|---|
| جراثيم جي ضمانت | تصديق ٿيل SAL 10⁻⁶ في بيچ | سائيڪل تي منحصر؛ اندر جي تصديق |
| درجي جي مناسبت | گريڊ A/B لاءِ بهتر | عام طور تي گريڊ C/D |
| مواد جي سالميت | هاء (اڪيلو استعمال، نه پائڻ) | هر چڪر سان خراب ٿئي ٿو |
This risk is most visible during material transfer into Grade A/B areas. For a detailed explanation, refer to our dedicated guide on ڊبل بيگ ٿيل جراثيم ڪش صاف روم ايم او پي پيڪنگنگ ۽ منتقلي منطق .
From a QA and operations perspective, sterilization method selection should align with cleanroom grade, internal validation capability, and supplier documentation maturity.
For validation-driven facilities, we support technical review with batch documentation, sterilization summaries, and evaluation samples.
درخواست ٽيڪنيڪل ڊيٽا يا نموني

اسان توهان سان 1 ڪم ڪندڙ ڏينهن اندر رابطو ڪنداسين، مهرباني ڪري لاتعداد سان اي ميل ڏانهن ڌيان ڏيو "*@midposi.com".