سائٹ کنٹیمینیشن کنٹرول اسٹریٹجی (CCS) میں قابل استعمال ٹریس ایبلٹی کے انضمام پر QA مینیجرز اور توثیق انجینئرز کے لیے ایک تکنیکی حوالہ۔

جی ایم پی ریگولیٹڈ ماحول میں، کلین روم ایم او پی کو اب ایک عام افادیت کے طور پر نہیں دیکھا جاتا بلکہ ایک اہم کنٹرول شدہ ان پٹ کے طور پر دیکھا جاتا ہے۔ بیچ ٹریس ایبلٹی کلین روم ایم او پی نظام تین بنیادی کام انجام دیتا ہے:
Product-level traceability identifies a SKU; batch-level traceability identifies the specific manufacturing event. For cleanroom mops, this requires a "genealogy" that links the finished product back to the specific lot of polyester yarn or microfiber fabric used, the cleanroom laundry shift, and the specific sterilization cycle.
جب mops کو کنٹرول شدہ ان پٹ کے طور پر سمجھا جاتا ہے، تو ہر انفرادی پیکج ڈیٹا پوائنٹ ہوتا ہے۔ یہ ڈیٹا QA ٹیموں کو اس بات کی تصدیق کرنے کی اجازت دیتا ہے کہ ان کے ہاتھ میں موجود پروڈکٹ کارکردگی اور پاکیزگی کے لحاظ سے ایک جیسی ہے جس کی توثیق ابتدائی سہولت کے آغاز یا PQ (کارکردگی کی اہلیت) کے دوران کی گئی تھی۔
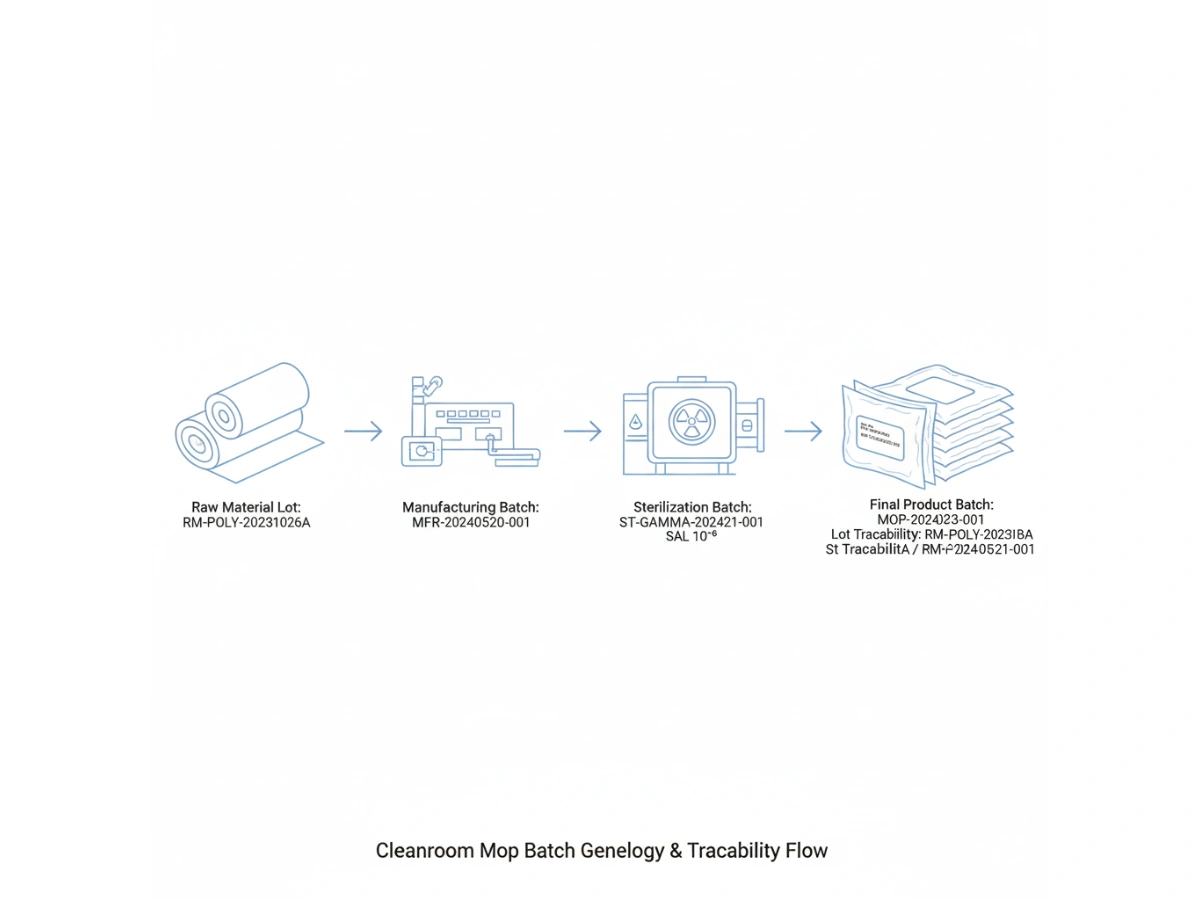
جدید GMP اصولوں کا تقاضا ہے کہ حساس سطحوں کے ساتھ رابطے میں آنے والے تمام مواد کا مکمل حساب کتاب کیا جائے۔ معائنہ کے دوران، ایک آڈیٹر پیداوار کی تاریخ کا انتخاب کر سکتا ہے اور پوچھ سکتا ہے۔ بہت ٹریسیبلٹی of the cleaning materials used on that day.
Expectations focus on the "Linkage of Records." An auditor will look for a seamless transition from the facility's cleaning logs to the batch-level documentation provided by the supplier. If a mop batch cannot be linked to a Certificate of Analysis (COA) or a sterilization record, the sterility and cleanliness of the entire cleanroom suite may be called into question.

A robust traceability system for cleanroom consumables GMP compliance must include:
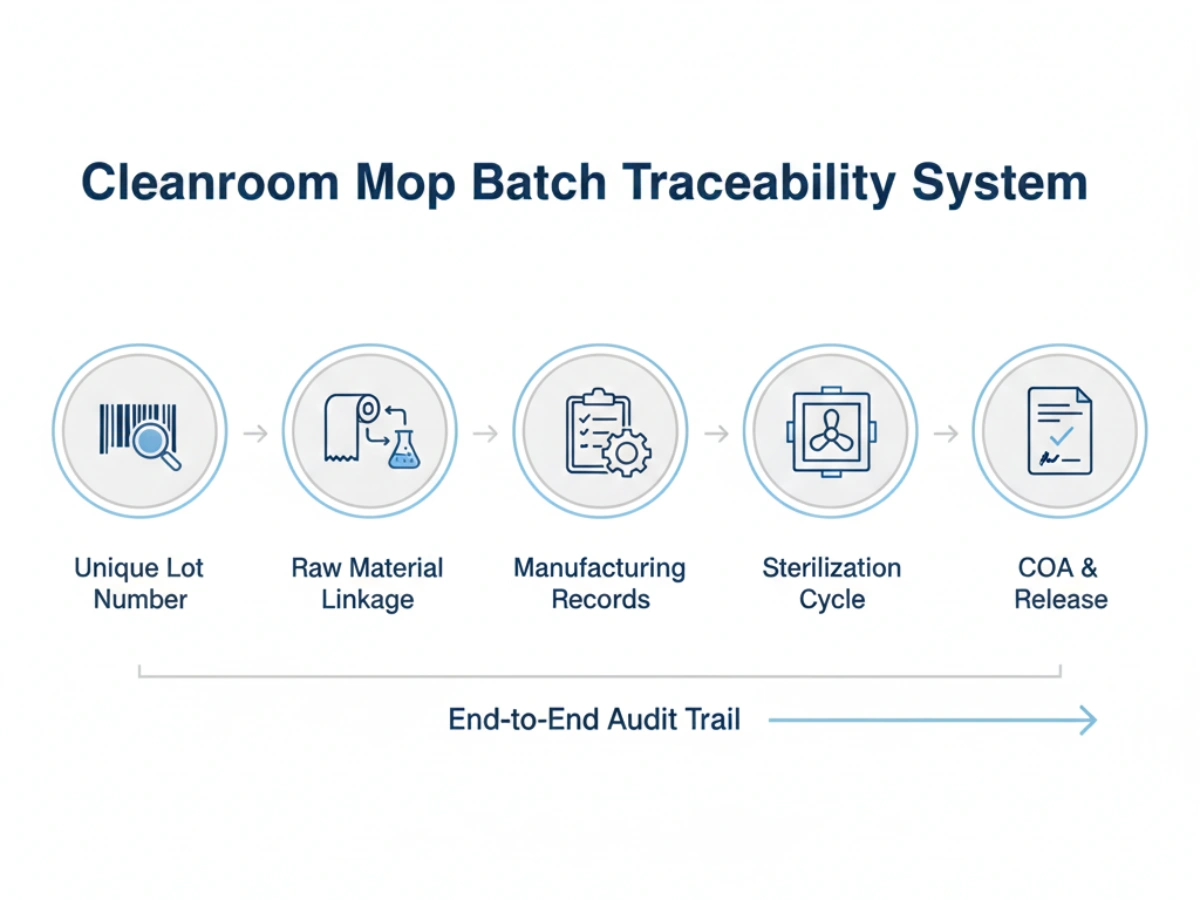
Supply stability is often threatened by "drift"—small, undocumented changes in manufacturing that accumulate over years. Batch traceability prevents this by establishing a baseline for lot-to-lot consistency.
In the event of a CAPA (Corrective and Preventive Action) involving environmental monitoring (EM) spikes, traceability allows QA to determine if a specific batch of mops contributed to the event. Without this, the facility may be forced to discard all inventory and halt production, posing a massive operational risk. Traceability transforms a potential facility-wide crisis into a localized material quarantine.

A pharmaceutical mop manufacturer / OEM acts as an extension of the pharma site’s quality system. Their responsibilities include:
For a qualified manufacturer, the ability to produce these records on demand is the hallmark of GMP maturity.
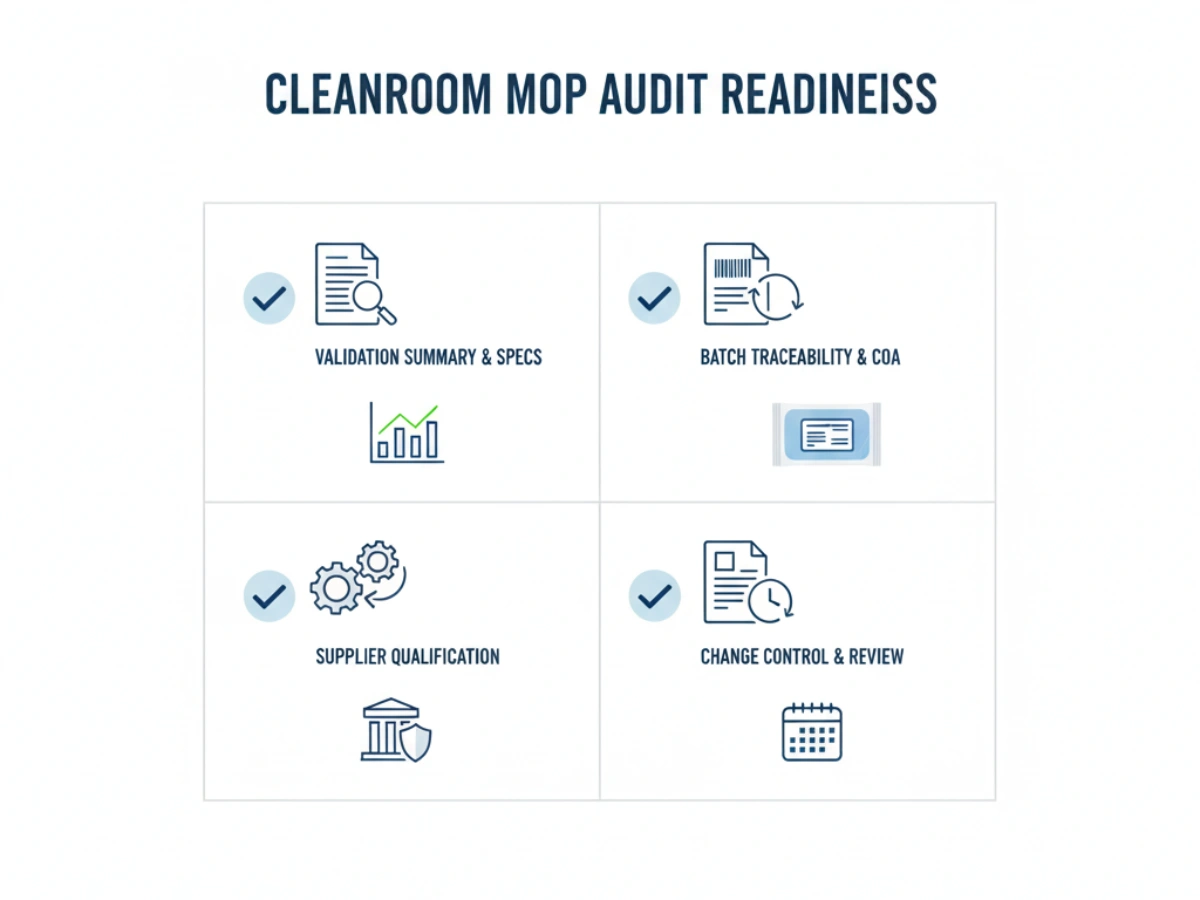
During OEM supplier qualification, QA teams should utilize the following checklist:
| Checkpoint | ضرورت |
|---|---|
| Batch Definition | Is the batch size clearly defined and manageable? |
| Sample Retention | Does the supplier keep retain samples for every lot? |
| Audit Access | Can the supplier provide full raw material logs within 48 hours? |
| Physical Labeling | Is the batch number resistant to cleanroom disinfectants (IPA)? |
Batch traceability is not merely a documentation exercise; it is the backbone of a defensible quality system. In the context of Grade A and B environments, the ability to track every fiber and sterilization cycle ensures that the cleaning process remains a controlled variable rather than an unknown risk.
Mature pharmaceutical QA teams prioritize suppliers who demonstrate total transparency in their batch records, viewing them as long-term partners in patient safety and regulatory compliance.
Ask for lot genealogy, batch-specific COAs, sterilization linkage, and change-control readiness to strengthen your audit narrative.
Request Documentation Package

ہم 1 کام کے دن کے اندر آپ سے رابطہ کریں گے، براہ کرم لاحقہ کے ساتھ ای میل پر توجہ دیں۔ "*@midposi.com".