نظام SOP للغرف النظيفة & إدارة الامتثال
إجراءات التشغيل القياسية الخاصة بتنظيف غرف الأبحاث: دليل التوثيق والتدريب والتحقق والامتثال الكامل
A complete guide to building a cleanroom cleaning SOP system for pharmaceutical and controlled environments, including documentation structure, training control, cleaning frequency logic, validation planning, audit readiness, and contamination control governance.
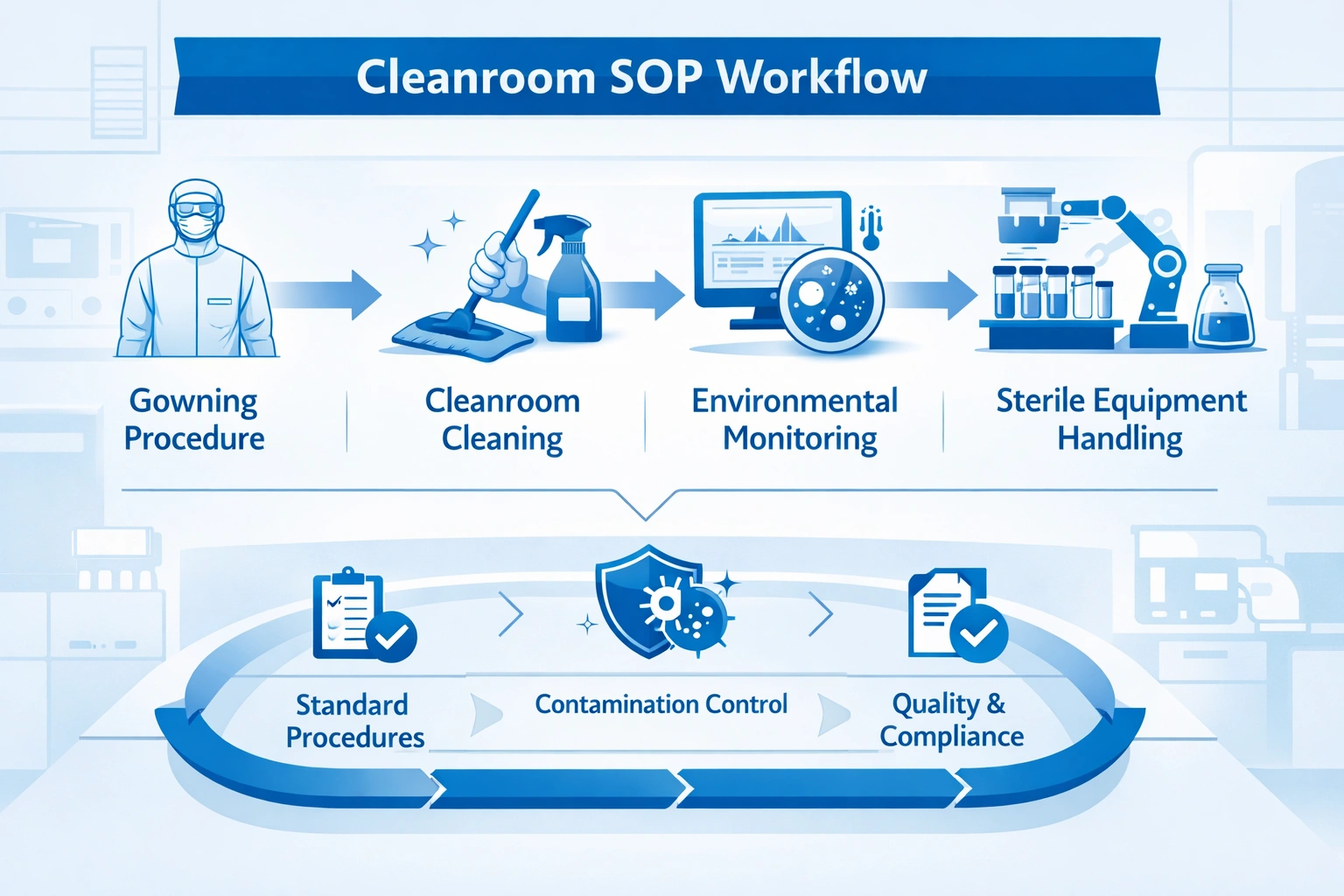
ما هو الإجراء التشغيلي الموحد (SOP) لتنظيف غرف الأبحاث؟
A cleanroom cleaning SOP is a controlled document that defines how cleaning and disinfection activities are planned, executed, recorded, reviewed, and improved in controlled environments. A complete SOP system typically includes cleaning instructions, cleaning frequency, approved tools, disinfectant rules, training requirements, validation records, and audit-ready documentation.
لماذا يجب أن يكون الإجراء التشغيلي الموحد لتنظيف غرف الأبحاث أكثر من مجرد تعليمات تنظيف
Many facilities treat a cleanroom cleaning SOP as a simple work instruction. In reality, it is a contamination control management document that connects personnel, materials, procedures, frequency, records, and verification into one system.
In pharmaceutical and biotech environments, a weak SOP usually leads to inconsistent execution, incomplete documentation, poor training transfer, and increased audit risk. A strong نظام توثيق SOP للغرف النظيفة يساعد على توحيد التنظيف اليومي مع دعم الامتثال لممارسات التصنيع الجيدة وإمكانية التتبع.
ما الذي يجب أن يتضمنه نظام SOP الكامل لتنظيف غرف الأبحاث
نطاق الوثيقة والغرض منها
تحديد درجة غرف الأبحاث ونوع الغرفة ونطاق العملية وهدف التحكم في التلوث.
الأدوات والمواد الاستهلاكية المعتمدة
قم بإدراج أنظمة الممسحة والمناديل المبللة والدلاء والملابس ونوعية المياه والمطهرات المؤهلة.
تعليمات التنظيف
حدد ما يتم تنظيفه، وبأي ترتيب، وبأي طريقة، وتحت أي احتياطات.
تردد التنظيف
حدد عدد المرات التي يجب فيها تنظيف الأسطح والأرضيات والجدران ونقاط الاتصال الحرجة.
التدريب والتأهيل
اشرح من يمكنه القيام بالتنظيف، وما هو التدريب المطلوب، وكيفية التحقق من الكفاءة.
التوثيق والمراجعة
تحديد السجلات وقواعد تسجيل الخروج ومعالجة الانحراف ودورات مراجعة إجراءات التشغيل المعيارية (SOP) الدورية.
Facilities needing a more technical execution workflow for critical-grade environments should also review the dedicated دليل إجراءات تنظيف غرف الأبحاث ISO 5.
كيفية تحديد تكرار التنظيف في إجراءات التشغيل القياسية الخاصة بغرفة الأبحاث
One of the most common SOP weaknesses is using generic cleaning frequency language such as “clean regularly” or “clean as needed.” In compliant environments, frequency should be risk-based and clearly assigned by area.
يجب أن يميز SOP بين:
- مناطق الإنتاج الحرجة
- مناطق الدعم والغرف الهوائية
- الأرضيات والجدران والأسقف والأسطح الملامسة
- التنظيف الروتيني مقابل دوران المطهر مقابل تدخل مبيد الجراثيم
إذا كان فريقك يقوم ببناء برنامج ترددي مرتبط بنتائج أخذ العينات، فيجب أن يتماشى ذلك مع المراقبة البيئية للغرف النظيفة على أساس المخاطر ومراجعة اتجاه التلوث بدلاً من الروتين الثابت وحده.
التدريب ومراقبة التنفيذ
A cleaning SOP only works when operators perform the same action the same way every time. That is why training is not a support activity. It is part of the SOP system itself.
يجب أن تشمل مراقبة التدريب ما يلي:
- التدريب الأولي للمشغل
- عرض سير العمل المرئي
- المؤهلات المرصودة والتوقيع
- إعادة التدريب الدوري
- إعادة التأهيل على أساس الانحراف

التحقق من صحة التنظيف وجاهزية التدقيق
A mature SOP system should not stop at execution. It should support validation and audit readiness. That means the cleaning process must be reviewable, traceable, and aligned with facility quality systems.
قد تتضمن وثائق الدعم المتعلقة بالتحقق ما يلي:
- سجلات التنظيف وأوراق التوقيع
- سجلات تحضير المطهر
- إمكانية تتبع الكثير لرؤوس الممسحة والمناديل
- بيانات مراجعة الرصد البيئي
- الانحراف وسجلات CAPA
- المراجعة الدورية لفعالية إجراءات التشغيل القياسية (SOP).
بالنسبة للمرافق التي تقوم بإعداد حزم الوثائق، تشمل موارد الدعم المفيدة قوائم التحقق من صحة غرف الأبحاث FDA cGMP و تأهيل غرف الأبحاث والتحقق من صحة قوالب SOP.
الأخطاء الشائعة في نظام SOP
كتابة المهمة فقط، وليس النظام
يشرح إجراء التشغيل المعياري (SOP) حركة التنظيف ولكنه يتجاهل التردد والسجلات والتدريب ومراقبة المراجعة.
موافقة غير واضحة على الأداة
يستخدم المشغلون مناديل أو رؤوس ممسحة أو مطهرات مختلفة لأن الوثيقة عامة جدًا.
- ربط التدريب ضعيف
إن إجراءات التشغيل القياسية موجودة، ولكن لا يوجد فحص رسمي للكفاءة لإثبات أن المشغلين يتبعونها بشكل صحيح.
لا يوجد تكرار للتنظيف على أساس المخاطر
خطة التنظيف عامة ولا تتماشى مع تصنيف الغرفة أو اتجاهات التلوث.
تصميم سجل سيء
تلتقط السجلات النشاط ولكن لا توجد معلومات كافية لإمكانية التتبع أو المراجعة أو الدفاع عن التفتيش.
لا يوجد اتصال للتحقق من الصحة
يتم استخدام إجراء التشغيل المعياري (SOP) تشغيليًا، ولكن لا يتم دمجه في التأهيل أو الاستعداد للتدقيق أو أنظمة CAPA.
ممسحة غرف الأبحاث الموصى بها واستراتيجية المواد الاستهلاكية
Even the best SOP will fail if the cleaning tools are inconsistent or poorly matched to the target cleanroom. Pharmaceutical teams should define approved consumables in the SOP and keep them aligned with contamination risk, sterilization method, and validation burden.

الموارد ذات الصلة: متطلبات ممسحة غرف الأبحاث الصيدلانيةو يمكن التخلص منها مقابل ممسحات غرف الأبحاث القابلة لإعادة الاستخدام, and كيفية تأهيل مورد ممسحة غرف الأبحاث الصيدلانية.
أسئلة مكررة
ما الذي تم تضمينه في الإجراء التشغيلي الموحد (SOP) لتنظيف غرف الأبحاث؟
A complete cleanroom cleaning SOP usually includes cleaning scope, approved tools, disinfectants, cleaning sequence, frequency, documentation requirements, training controls, and review procedures.
كيف يختلف الإجراء التشغيلي الموحد (SOP) الخاص بتنظيف غرف الأبحاث عن تعليمات العمل؟
A work instruction explains how to perform a task. A full SOP system also defines control logic, documentation, accountability, review, and compliance expectations.
كيف ينبغي تحديد وتيرة التنظيف؟
Cleaning frequency should be based on room classification, process risk, surface type, contamination trends, and the facility’s overall contamination control strategy.
لماذا يعد التدريب مهمًا في نظام SOP الخاص بغرف الأبحاث؟
Training ensures different operators follow the same validated method consistently, reducing execution variation and helping protect audit readiness.
هل يمكن لإجراءات التشغيل القياسية الخاصة بتنظيف غرف الأبحاث أن تدعم الاستعداد للتدقيق؟
Yes. A well-built SOP system improves traceability, record consistency, training proof, and validation alignment, all of which support inspection and audit performance.
هل تحتاج إلى حل أفضل لممسحة غرف الأبحاث الجاهزة لإجراءات التشغيل القياسية (SOP)؟
Midposi supports pharmaceutical and controlled-environment teams with sterile mop systems, contamination control consumables, and qualification-oriented cleaning solutions.



