فئات SOP النموذجية
- العباءات ودخول الأفراد
- التنظيف والتطهير
- المراقبة البيئية
- نقل المواد والمعدات
- تطهير منطقة الدفعة
- الانحراف والاستجابة للحوادث
دليل SOP لغرفة الأبحاث الصيدلانية
A practical guide to cleanroom standard operating procedures, contamination control, sterile cleaning workflows, environmental monitoring, GMP documentation, and future AI-driven quality systems.

In pharmaceutical and biotechnology manufacturing, cleanroom standard operating procedures are not just compliance documents. They are the operational backbone for contamination control, sterile behavior, validated cleaning, material transfer, and environmental consistency.
The strongest cleanroom SOP systems help manufacturers reduce deviation risk, improve audit readiness, standardize operator behavior, and protect product quality in ISO 5, ISO 7, and GMP-controlled spaces.
If you are building or upgrading a pharmaceutical cleaning program, it is also useful to review related guidance on cleanroom mopping SOPsو pharmaceutical cleanroom mop cleaning SOPs, and EU GMP Annex 1 cleanroom SOP documentation.
A cleanroom SOP is a documented procedure that defines how a specific activity must be performed inside a controlled environment. These activities usually include gowning, room entry, equipment handling, cleaning and disinfection, material transfer, line clearance, and environmental monitoring.
In pharmaceutical manufacturing, a well-written SOP does more than describe a task. It defines sequence, frequency, materials, approved tools, operator responsibilities, escalation rules, and documentation requirements.
Teams that are still structuring their documentation framework may also find it helpful to review تأهيل غرف الأبحاث والتحقق من صحة قوالب SOPو قوائم التحقق من صحة غرف الأبحاث FDA cGMP, and risk-based cleanroom environmental monitoring SOP guidance.
Most contamination issues do not begin with dramatic equipment failure. They begin with inconsistency: an incomplete wipe-down, an incorrect mop path, poor gown discipline, unverified transfer steps, or environmental data that was not acted on in time.
That is why cleanroom SOPs matter. They turn contamination control from individual habit into repeatable system behavior.
بالنسبة للفرق التي تركز على جاهزية الملحق 1، والمناطق المعقمة، ومراقبة التوثيق، تتضمن القراءة ذات الصلة التحكم في التلوث الميكروبي في غرف الأبحاث لأنظمة العزلو التحكم في التلوث الميكروبي في أنظمة عزل غرف الأبحاث, and إجراءات التشغيل القياسية الخاصة بتطهير غرف الأبحاث وتعقيمها لمعالجة الدفعات.
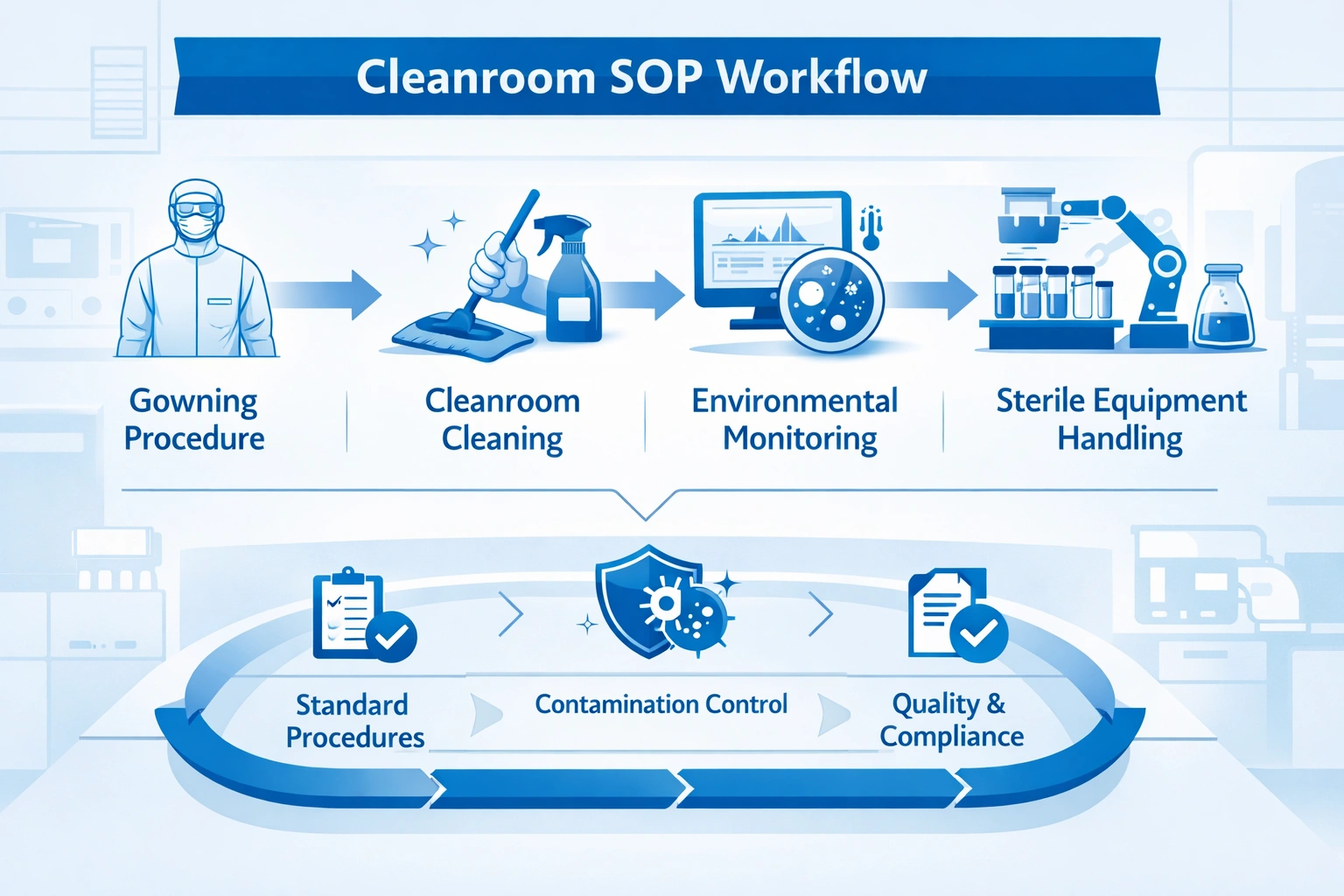
A practical cleanroom SOP framework usually follows a defined operational chain. Although every facility has its own validation requirements, the core structure is often similar.
This workflow becomes much stronger when paired with a validated product system. For example, many pharmaceutical teams compare يمكن التخلص منها مقابل ممسحات غرف الأبحاث القابلة لإعادة الاستخدام, evaluate المماسح المشععة بأشعة غاما مقابل ممسحات غرف الأبحاث القابلة للتعقيم, and study low-lint cleanroom mop material comparisons before finalizing SOP-approved tools.
Cleaning is one of the most critical parts of any cleanroom SOP program. The procedure must specify not only what to clean, but how to clean it, with what material, at what frequency, and with what documented method.

يتطلب مناديل تم التحقق منها، ونمط مسح محدد، ووقت اتصال مناسب للمطهر.
يتطلب مسار ممسحة يمكن التحكم فيه، ورأس ممسحة معتمد، ومنطق واضح للاتجاه من الأوساخ إلى التنظيف.
تدعم المماسح المعقمة والمناديل ذات الوبر المنخفض وأنظمة الدلاء المتوافقة التحكم المتكرر في التلوث.
إذا كان فريقك يقوم باختيار أدوات التنظيف أو ترقيتها، فستتضمن المراجع الداخلية المفيدة متطلبات ممسحة غرف الأبحاث الصيدلانيةو أدلة تنفيذ ممسحة غرف الأبحاثو أنظمة دلو ممسحة غرف الأبحاث, and مماسح غرف الأبحاث الصيدلانية لبيئات الملحق 1 لممارسات التصنيع الجيدة.
مؤهلات المورد مهم أيضا. يرى كيفية تأهيل مورد ممسحة غرف الأبحاث الصيدلانيةو وثائق التحقق من صحة ممسحة غرف الأبحاث وشهادة توثيق البرامج, and إمكانية تتبع الدفعات لمماسح غرف الأبحاث الصيدلانية.
Contamination does not come from one single source. It usually develops through an interaction between personnel, surfaces, airflow, tools, transferred materials, and incomplete execution.

وينبغي أيضًا مراجعة استراتيجية مكافحة التلوث في بناء المرافق منع مخاطر تلوث غرف الأبحاثو مناديل غرف الأبحاث خالية من الوبر لتنظيف المناطق الحرجة, and تطبيقات ممسحة غرف الأبحاث في مجال التكنولوجيا الحيوية.
The next stage of cleanroom SOP development is not less documentation. It is smarter control. More pharmaceutical manufacturers are now exploring digital tools that connect SOP execution with real-time data, contamination analytics, and predictive monitoring.

Even in advanced facilities, the foundation still remains the same: a clear SOP, trained personnel, validated materials, and a repeatable contamination control method.
يجب أن تكون إجراءات التشغيل القياسية الخاصة بغرف الأبحاث دقيقة من الناحية التشغيلية، وليست غامضة أو عامة.
استخدم المناديل المبللة والمماسح المعقمة والأنظمة المتوافقة التي تدعم التكرار.
وينبغي للنتائج البيئية أن تؤدي إلى اتخاذ إجراءات، وليس مجرد حفظ السجلات.
يعد اتساق المشغل أحد أقوى متغيرات التحكم في التلوث.
تحدد إجراءات التشغيل المعيارية (SOP) الخاصة بالغرفة النظيفة كيفية تنفيذ المهام الخاضعة للرقابة للحفاظ على الاتساق وتقليل مخاطر التلوث ودعم الامتثال في إنتاج الأدوية أو التكنولوجيا الحيوية.
ويجب أن تتضمن المواد المعتمدة، وتسلسل التنظيف، وتكرار المنطقة، ونوع المطهر، ووقت الاتصال، واختيار الأداة، وخطوات التوثيق، والمسؤوليات.
تساعد المماسح المعقمة على تقليل مخاطر التلوث في عمليات التنظيف الحرجة من خلال دعم طرق التنظيف المعتمدة والأداء المتسق منخفض الوبر.
يجب مراجعة إجراءات التشغيل القياسية (SOPs) على أساس مجدول وتحديثها أيضًا عندما تتطلب تغييرات العملية أو الانحرافات أو نتائج التدقيق أو مخاطر التلوث الجديدة المراجعة.
لا، يمكن للذكاء الاصطناعي تحسين المراقبة ودعم القرار، لكنه لا يحل محل الحاجة إلى إجراءات مكتوبة واضحة، ومواد تم التحقق من صحتها، وتنفيذ بشري مدرب.
Midposi supports pharmaceutical and cleanroom teams with sterile mops, low-lint wipes, and contamination control consumables designed for controlled environments.


سوف نتصل بك في غضون يوم عمل واحد ، يرجى الانتباه إلى البريد الإلكتروني الذي يحتوي على اللاحقة "*@midposi.com".