A QA-focused technical guide for GMP material entry into Grade A/B zones—covering peel-and-pass logic, packaging integrity risks, and audit-defensible controls aligned with EU GMP Annex 1 expectations.

Sterilität wird während der Herstellung erreicht, die meisten Kontaminationsereignisse treten jedoch während der Herstellung auf aseptischer Transfer—when materials move from uncontrolled areas to Grade C, then B, and finally A. Without redundant barriers, the mop packaging surface can act as a carrier for particulates and bioburden.
In der Praxis, sterile Moppverpackung functions as a controlled boundary: the outer bag is stripped at the interface, while the inner bag remains sterile until the point of use. This is the operational basis of Peel-and-Pass.
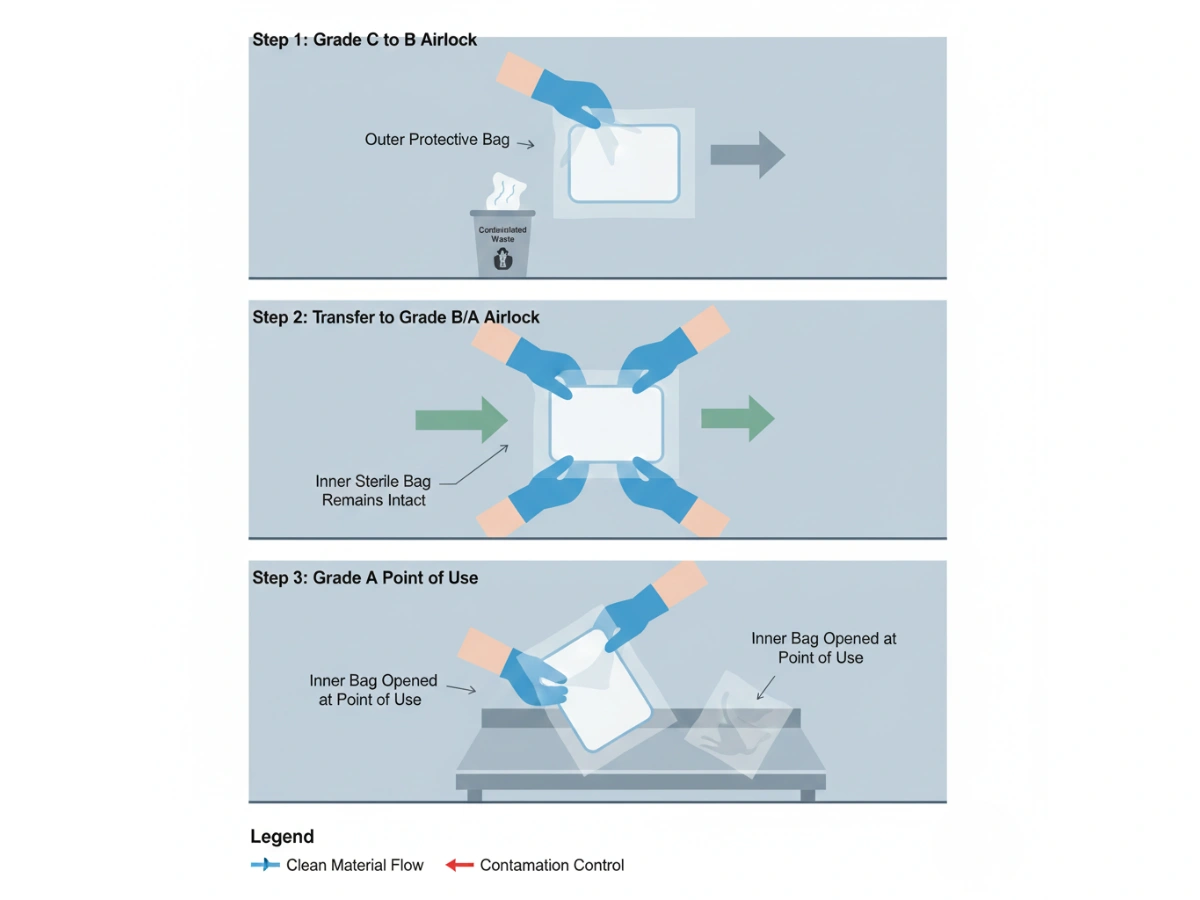

For Grade A/B operations, the core question is not “sterile at release,” but “sterile at point-of-use.” Double-bagging reduces transfer variability by removing the external surface at the boundary rather than relying on wipe-down success every time.

Use this simplified logic to align packaging selection with grade, transfer method, and validation burden. For Grade A/B, an engineered barrier is typically preferred over manual disinfection dependence.
| Entscheidungsfaktor | Einzelbeutelverpackung | Doppelbeutelverpackung |
|---|---|---|
| Übertragungskontrolle | Erfordert validiertes Abwischen und Disziplin | Peel-and-Pass entfernt Verunreinigungen an der Grenze |
| Fehlermodus | Single Point of Failure | Redundante sterile Barriereschichten |
| Audit-Vertretbarkeit | Stark abhängig von Beweisen zur SOP-Ausführung | Stärkere technische Kontrollerzählung für CCS |
| Operative Arbeitsbelastung | Höher (Desinfektion, Überwachung, Abweichungen) | Unterer (standardisierter Strip-at-Boundary-Prozess) |



Wir werden uns innerhalb eines Werktages mit Ihnen in Verbindung setzen. Bitte beachten Sie die E-Mail mit dem Suffix „*@midposi.com“.