Ein QS-orientierter Vergleich von Endlosfilament-Polyester mit geteilter Mikrofaser – mit Schwerpunkt auf Ausfallrisiko, Sterilisationsstress und Validierungsnachweisen für GMP-Umgebungen.
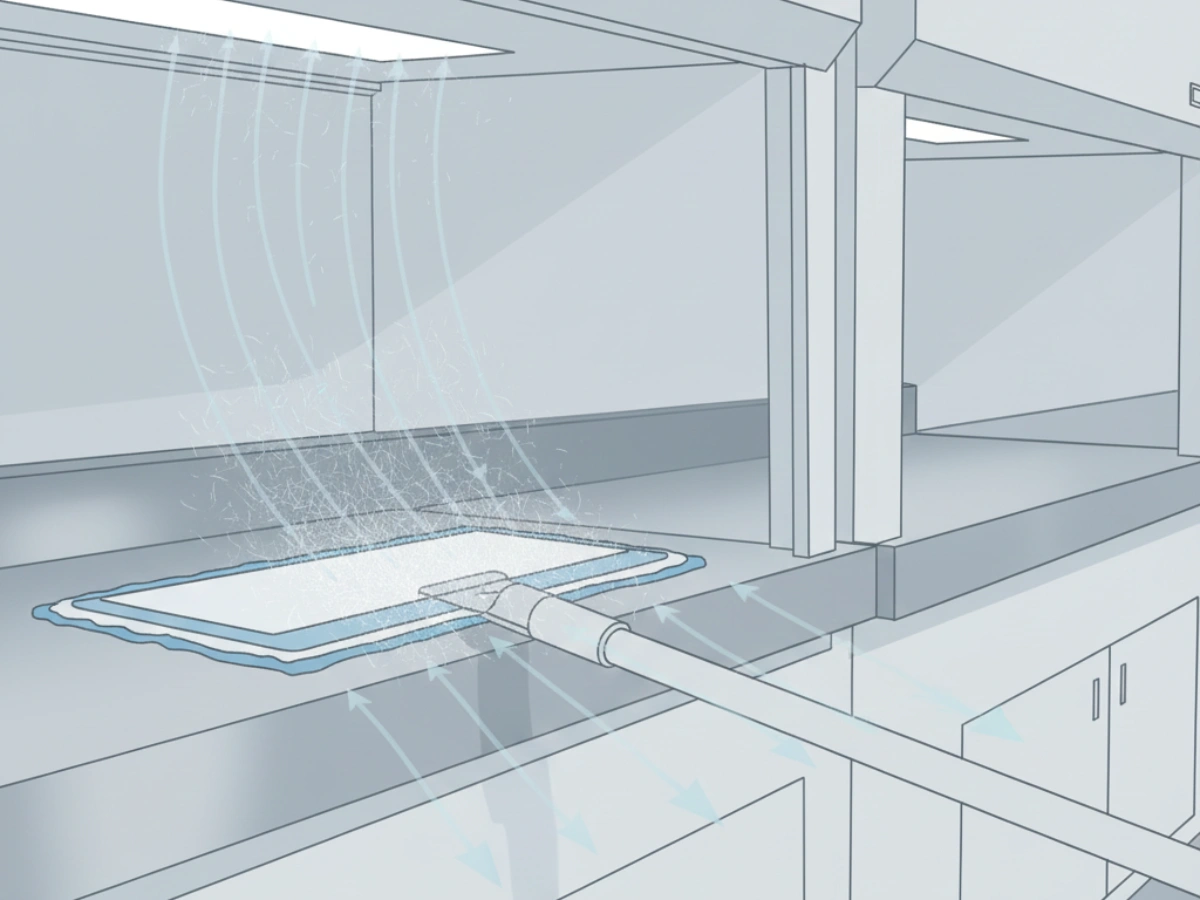
Bei der sterilen Herstellung werden aus Reinigungswerkzeugen freigesetzte Fasern als Fehler bei der Kontaminationskontrolle behandelt. In der Praxis handelt es sich bei „Low Lint“ nicht um eine Marketingphrase, sondern um eine Validierungsvariable, die sich auf die CCS-Wirksamkeit und das Abweichungsrisiko auswirkt.
Für QA-Teams ist die Schlüsselfrage die Wiederholbarkeit: Behält der Mopp sein Abwurfprofil nach den maximal zulässigen Sterilisations- und Handhabungszyklen bei? Wenn Sie ein Framework auf Beschaffungsebene benötigen, beginnen Sie mit dem Säulenleitfaden: Lieferant von pharmazeutischen Reinraummopps.
Das Flusenrisiko wird durch die Faserarchitektur (kontinuierlich vs. geteilt), die Kantenkonstruktion und das Belastungsprofil durch Sterilisation und Verwendung bestimmt. „Mikrofaser“ ist nicht automatisch sicherer; Gespaltene Filamente können zu mehr Bruchstellen führen.

Selbst wenn ein Mopp als „autoklavierbar“ gekennzeichnet ist, kann die wiederholte Dampfeinwirkung mit der Zeit die Faserintegrität verändern. Bei geteilten Mikrofaserstrukturen können Dampfzyklen den Filamentbruch und die Kantenermüdung beschleunigen.

Das größte Risiko für Haarausfall besteht häufig an Kanten – insbesondere nach wiederholtem Abrieb. Laserschneiden und Ultraschallversiegeln sind gängige Ansätze zur Reduzierung von Makroflusen. Eine detaillierte technische Übersicht darüber, wie diese Schritte gesteuert werden, finden Sie unter: Herstellungsprozess für Reinraum-Moppköpfe.
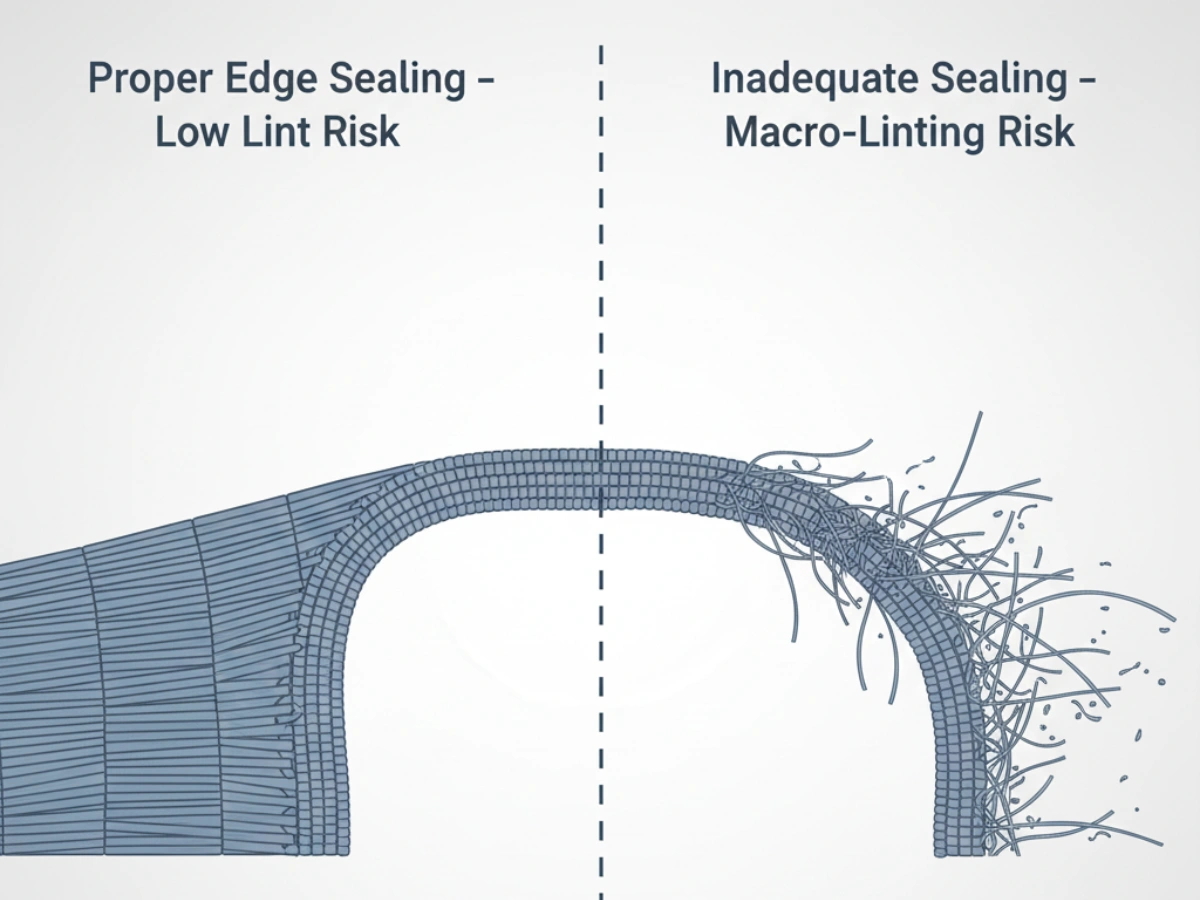
Die geteilte Struktur der Mikrofaser verbessert die Aufnahmeeffizienz, führt jedoch zu mehr Mikroenden und Bruchstellen. Wenn das Produkt wiederholt verarbeitet wird (Dampfzyklen) oder die Kanten nicht richtig verschmolzen werden, steigt das Risiko der Flusenbildung – weshalb für die Verwendung der Klasse A in der Regel stärkere Nachweise und strengere Grenzwerte erforderlich sind.
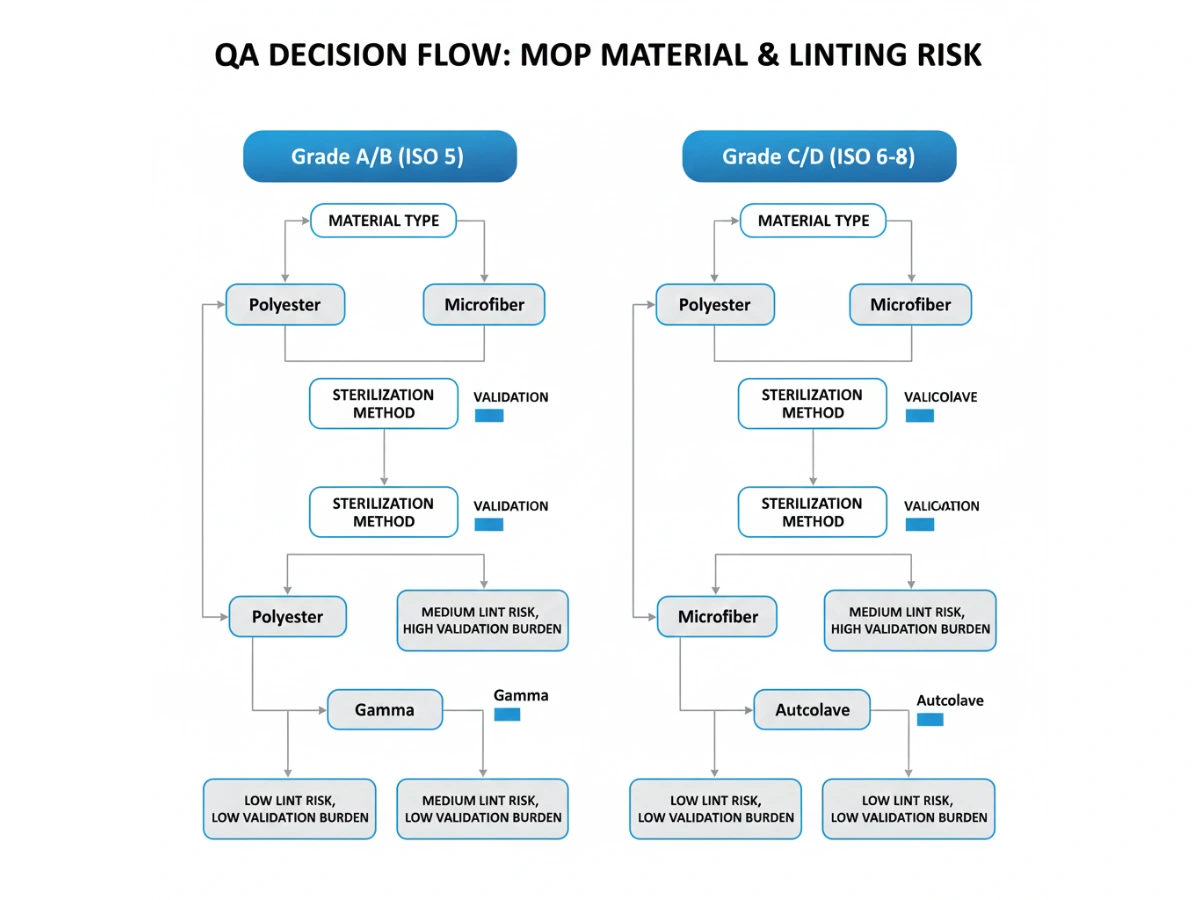
Verwenden Sie einen Entscheidungsbaum, der die Qualitätsanforderungen, die Sterilisationsmethode und die Verfügbarkeit von Nachweisen (Abwurftests, Kantenversiegelungsmethode, Zyklenhaltbarkeit) aufeinander abstimmt. Wenn Sie ein vollständiges Paket zur Lieferantenqualifizierung erstellen, finden Sie hier Querverweise zum Beschaffungsrahmen: Lieferant von pharmazeutischen Reinraummopps.


Wir werden uns innerhalb eines Werktages mit Ihnen in Verbindung setzen. Bitte beachten Sie die E-Mail mit dem Suffix „*@midposi.com“.