Typische SOP-Kategorien
- Umkleide- und Personaleintritt
- Reinigung und Desinfektion
- Umweltüberwachung
- Material- und Gerätetransfer
- Freigabe des Chargenbereichs
- Reaktion auf Abweichungen und Vorfälle
SOP-Leitfaden für pharmazeutische Reinräume
A practical guide to cleanroom standard operating procedures, contamination control, sterile cleaning workflows, environmental monitoring, GMP documentation, and future AI-driven quality systems.

In pharmaceutical and biotechnology manufacturing, cleanroom standard operating procedures are not just compliance documents. They are the operational backbone for contamination control, sterile behavior, validated cleaning, material transfer, and environmental consistency.
The strongest cleanroom SOP systems help manufacturers reduce deviation risk, improve audit readiness, standardize operator behavior, and protect product quality in ISO 5, ISO 7, and GMP-controlled spaces.
If you are building or upgrading a pharmaceutical cleaning program, it is also useful to review related guidance on SOPs zum Wischen im Reinraum, SOPs für die Reinigung von pharmazeutischen Reinraummopps, and EU GMP Annex 1 Reinraum-SOP-Dokumentation.
A cleanroom SOP is a documented procedure that defines how a specific activity must be performed inside a controlled environment. These activities usually include gowning, room entry, equipment handling, cleaning and disinfection, material transfer, line clearance, and environmental monitoring.
In pharmaceutical manufacturing, a well-written SOP does more than describe a task. It defines sequence, frequency, materials, approved tools, operator responsibilities, escalation rules, and documentation requirements.
Für Teams, die ihr Dokumentationsgerüst noch strukturieren, kann es ebenfalls hilfreich sein, es zu überprüfen SOP-Vorlagen für die Reinraumqualifizierung und -validierung, Checklisten für die cGMP-Reinraumvalidierung der FDA, and SOP-Anleitung zur risikobasierten Überwachung der Reinraumumgebung.
Most contamination issues do not begin with dramatic equipment failure. They begin with inconsistency: an incomplete wipe-down, an incorrect mop path, poor gown discipline, unverified transfer steps, or environmental data that was not acted on in time.
Deshalb sind Reinraum-SOPs wichtig. Sie verwandeln die Kontaminationskontrolle von der individuellen Gewohnheit in wiederholbares Systemverhalten.
Für Teams, die sich auf die Anhang-1-Bereitschaft, aseptische Zonen und Dokumentationskontrolle konzentrieren, umfasst die entsprechende Lektüre Folgendes Kontrolle der mikrobiellen Kontamination im Reinraum für Isolatorsysteme, Mikrobielle Kontaminationskontrolle in Reinraum-Isolatorsystemen, and SOPs zur Dekontamination und Sterilisation von Reinräumen für die Chargenverarbeitung.
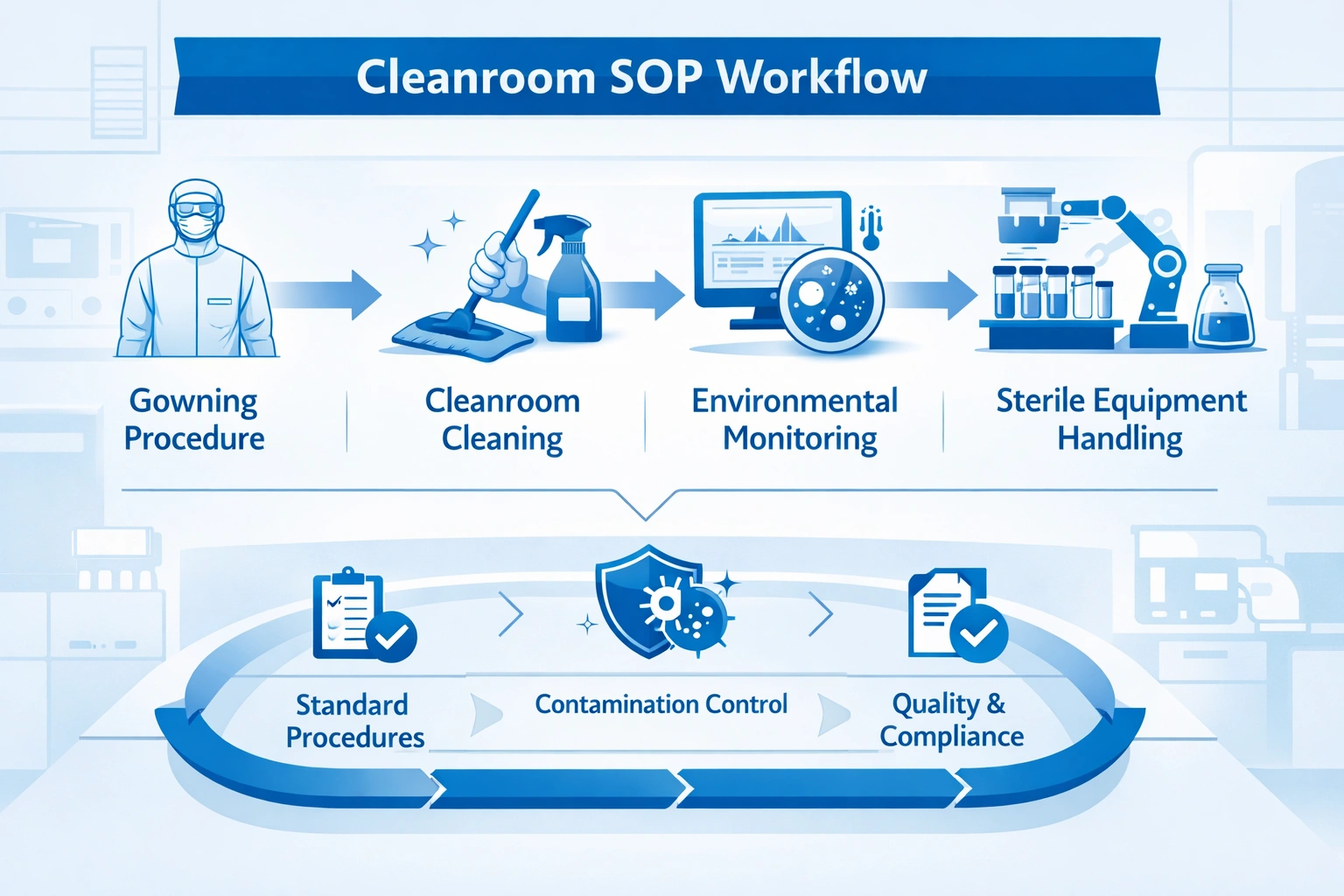
A practical cleanroom SOP framework usually follows a defined operational chain. Although every facility has its own validation requirements, the core structure is often similar.
This workflow becomes much stronger when paired with a validated product system. For example, many pharmaceutical teams compare Einweg-Reinraum-Mopps vs. wiederverwendbare Reinraum-Mopps, evaluate gammabestrahlte vs. autoklavierbare Reinraummopps, and study Materialvergleiche für fusselarme Reinraummopps bevor SOP-zugelassene Werkzeuge fertiggestellt werden.
Cleaning is one of the most critical parts of any cleanroom SOP program. The procedure must specify not only what to clean, but how to clean it, with what material, at what frequency, and with what documented method.

Erfordert validierte Tücher, ein definiertes Wischmuster und eine angemessene Einwirkzeit des Desinfektionsmittels.
Erfordert einen kontrollierten Wischweg, einen zugelassenen Wischkopf und eine klare Richtungslogik von Schmutz zu Reinigung.
Sterile Mopps, fusselarme Tücher und kompatible Eimersysteme unterstützen eine wiederholbare Kontaminationskontrolle.
Wenn Ihr Team Reinigungswerkzeuge auswählt oder aktualisiert, sind nützliche interne Referenzen enthalten Anforderungen an pharmazeutische Reinraummopps, Anleitungen zur Implementierung von Reinraum-Mopps, Reinraum-Moppeimersysteme, and pharmazeutische Reinraummopps für GMP Annex 1-Umgebungen.
Auch die Qualifikation der Lieferanten spielt eine Rolle. Sehen So qualifizieren Sie einen Lieferanten für pharmazeutische Reinraummopps, Reinraum-Mopp-Validierungsdokumente und COA, and Chargenrückverfolgbarkeit für pharmazeutische Reinraummopps.
Contamination does not come from one single source. It usually develops through an interaction between personnel, surfaces, airflow, tools, transferred materials, and incomplete execution.

Auch die Strategie zur Kontaminationskontrolle von Gebäuden sollte überprüft werden Vermeidung von Kontaminationsrisiken im Reinraum, fusselfreie Reinraumtücher für die Reinigung kritischer Zonen, and Biotech-Reinraum-Moppanwendungen.
The next stage of cleanroom SOP development is not less documentation. It is smarter control. More pharmaceutical manufacturers are now exploring digital tools that connect SOP execution with real-time data, contamination analytics, and predictive monitoring.

Even in advanced facilities, the foundation still remains the same: a clear SOP, trained personnel, validated materials, and a repeatable contamination control method.
Reinraum-SOPs sollten betrieblich präzise und nicht vage oder allgemein sein.
Verwenden Sie validierte Tücher, sterile Mopps und kompatible Systeme, die die Wiederholbarkeit unterstützen.
Umweltergebnisse sollten Maßnahmen auslösen und nicht nur das Führen von Aufzeichnungen.
Die Bedienerkonsistenz ist eine der stärksten Variablen zur Kontaminationskontrolle.
Eine Reinraum-SOP definiert, wie kontrollierte Aufgaben durchgeführt werden müssen, um die Konsistenz aufrechtzuerhalten, das Kontaminationsrisiko zu reduzieren und die Compliance in der pharmazeutischen oder biotechnologischen Produktion zu unterstützen.
Es sollte zugelassene Materialien, Reinigungsreihenfolge, Bereichshäufigkeit, Desinfektionsmitteltyp, Kontaktzeit, Werkzeugauswahl, Dokumentationsschritte und Verantwortlichkeiten umfassen.
Sterile Mopps tragen dazu bei, das Kontaminationsrisiko bei kritischen Reinigungsprozessen zu reduzieren, indem sie validierte Reinigungsmethoden und eine gleichbleibend fusselarme Leistung unterstützen.
SOPs sollten regelmäßig überprüft und auch aktualisiert werden, wenn Prozessänderungen, Abweichungen, Auditergebnisse oder neue Kontaminationsrisiken eine Überarbeitung erfordern.
Nein. KI kann die Überwachung und Entscheidungsunterstützung verbessern, ersetzt jedoch nicht die Notwendigkeit klarer schriftlicher Verfahren, validierter Materialien und geschulter menschlicher Ausführung.
Midposi supports pharmaceutical and cleanroom teams with sterile mops, low-lint wipes, and contamination control consumables designed for controlled environments.


Wir werden uns innerhalb eines Werktages mit Ihnen in Verbindung setzen. Bitte beachten Sie die E-Mail mit dem Suffix „*@midposi.com“.